Основи біоорганічної хімії (навчальний посібник) - Г. О. Сирова - 2018
Тема
Кислотно-основні властивості органічних сполук
Актуальність теми. Кислотність та основність є однією з найбільш важливих властивостей речовин, які часто визначають їхню поведінку в організмі.
Загальна мета: вивчити кислотність органічних сполук як найважливіші властивості, що обумовлюють багато хімічних процесів у живих організмах.
Конкретні цілі
1. Уміти прогнозувати кислотні та основні властивості речовин залежно від їх будови.
2. На основі електронної будови функціональніх груп уміти пояснити кислотні властивості спиртів, фенолів і карбонових кислот, їхню залежність від числа функціональних груп і наявність замісників при радикалі.
3. Усвідомити, у чому полягає С-Н кислотність і як вона впливає на властивості сполуки.
4. На основі електронної будови атома нітрогену пояснити основні властивості аліфатичних і ароматичних амінів, а також нітрогеновмісних гетероциклів.
5. Знати, які класи органічніх сполук мають амфотерні властивості.
Теоретичні питання
1. Кислотні властивості органічних сполук. Типи кислотності.
2. Основні властивості органічних сполук.
1. Відповідно до протолітичної теорії Бренстеда кислоти - це нейтральні молекули або іони, здатні віддавати протон (донори протонів). Основи - нейтральні молекули або іони, здатні приєднувати протон (акцептори протонів).
Кислотність і основність не є абсолютними, а є відносними властивостями сполук: кислотні властивості проявляються лише в присутності основ, а основні - у присутності кислот.
Кислотами можуть бути органічні сполуки, що містять атоми гідрогену, з'єднані з більш електронегативним атомом (оксиген, сульфур, нітроген, карбон).
Залежно від того, з яким атомом зв'язаний гідроген, розрізняють:
- ОН-кислоти (спирти, феноли, карбонові кислоти);
- SH-кислоти (меркаптани);
- NH-кислоти (аміни, аміди);
- CH-кислоти (вуглеводні та їх похідні).
Для елементів одного періоду здатність віддавати протон зростає зі збільшенням електронегативності. Тому кислоти Бренстеда з однаковими радикалами розташовуються за зростанням кислотності в такому порядку:
![]()
З ОН-кислот розглянемо кислотні властивості спиртів, фенолів, карбонових кислот.
Полярність ОН-зв'язку в гідроксильній групі спирту обумовлює її здатність до гетероциклічного розриву. Такий тип розриву зв'язку має місце при взаємодії з активними металами, при цьому утворюються тверді, розчинні в спирті сполуки - алкоголяти з іонним зв'язком оксиген-метал:
![]()
Позитивний індуктивний ефект (+I) карбонового радикалу спричиняє зменшення полярності О-Н зв’язку та ослаблює кислотні властивості спиртів:
![]()
Тому спирти є слабшими кислотами, ніж вода. З цієї ж причини кислотність спиртів зменшується зі збільшенням числа карбонових атомів радикала.
Кислотність багатоатомних спиртів вища, ніж одноатомних, завдяки -І-ефекту гідроксильних груп. Особливо легко атоми гідрогену багатоатомних спиртів заміщуються деякими важкими металами внаслідок утворення хелатних внутрішньокомплексних сполук:
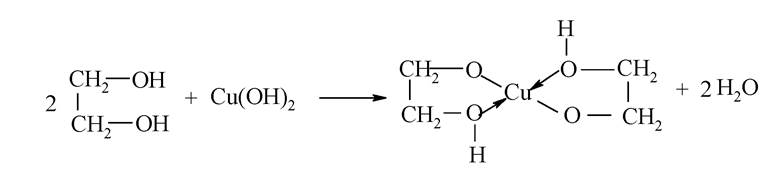
Хелати мають яскраве забарвлення, і їх утворення використовується для якісного визначення багатоатомних спиртів.
Кислотні властивості тіолів виражені сильніше, ніж у спиртів. Це пов'язано з більшою поляризованістю атома сульфуру порівняно з оксигеном. Тому тіоли утворюють солі (тіоли або меркаптани) з водними розчинами лугів:
![]()
Кислотність фенолів виражена сильніше, ніж у спиртів. Це пояснюється тим, що спарені електрони атома оксигену зміщені до ароматичого ядра (+М-ефект), що спричняє збільшення поляризації О-Н зв’язку.
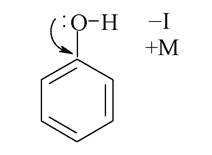
На відміну від аліфатичних спиртів, фенол легко взаємодіє із лугами, утворюючи солі-феноляти:
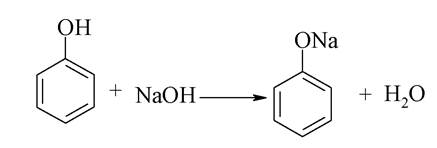
Феноли реагують також з металами, солями, проявляючи всі хімічні властивості кислот. Якісною реакцією на фенольний гідроксил є взаємодія із солями трьохвалентного феруму:
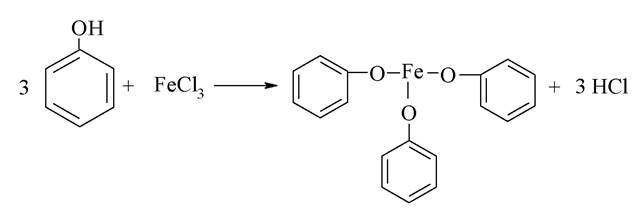
Введення електроноакцепторних замісників в ароматичне ядро підвищує кислотність фенолів, а електронодонорних - знижує її. Найбільш яскраво кислотні властивості виражені в ряду карбонових кислот - сполук, що містять карбоксильні групи -СООН. Наявність сусідньої з гідроксилом карбонільної групи обумовлює спряження спарених електронів оксигену гідроксильної групи з електронами п-зв'язку карбонілу:
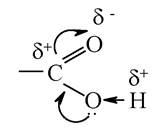
У результаті електронегативність атома кисню зростає, що призводить до посилення поляризації О-Н зв'язку і полегшує можливість відщеплення протона. У водному розчині нижчі карбонові кислоти помітно дисоціюють з утворенням протонів:
![]()
Карбоксилат-аніон являє собою делокалізовану трьохцентрову систему, у якій зв’язки атома карбону з обома атомами оксигену вирівняні:
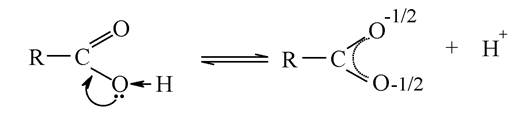
Карбонові кислоти - слабкі електроліти. Чим більш стабільний аніон, який утворюється при дисоціації, тим сильніше рівновага процесу дисоціації зміщена вправо. Отже, чим аніон стабільніший, тим сильніша кислота. Стабільність аніона, своєю чергою, визначається ступенем делокалізації негативного заряду. Тому чинники, що сприяють делокалізації заряду, посилюють кислотність, а чинники, які перешкоджають делокалізації, знижують її.
Це однаковою мірою справедливо і для інших класів сполук, які проявляють кислотні властивості. Зокрема, дикарбонові кислоти є більш сильними кислотами, ніж одноосновні з тим самим числом атомів карбону, унаслідок -І-ефекту другої карбоксильної групи:
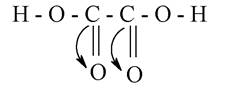
Карбонові кислоти змінюють забарвлення індикаторів і проявляють усі властивості кислот, взаємодіючи з металами, основами, основними оксидами, солями. Розглянемо це на прикладі двоосновних кислот, менш відомих з курсу середньої школи і таких, що відіграють важливу роль у біохімічних перетвореннях. Як і всі двохосновні кислоти, вони можуть утворювати середні і кислі солі:
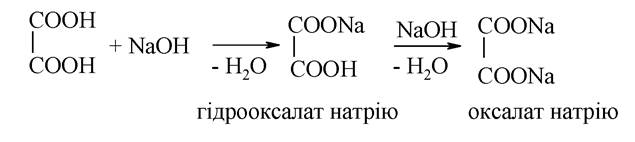
Полярність С-Н зв'язку у вуглеводнях незначна, і тому їхні кислотні властивості виражені вкрай слабко. Наявність електроноакцепторних замісників помітно збільшує С-Н кислотність. При цьому протон відділяється від атома карбону, що знаходиться в a-положенні відносно замісника. Прикладом прояву С-Н кислотності є альдольна конденсація - взаємодія молекул альдегідів між собою в присутності водного розчину лугу (див. тему «Будова і властивості альдегідів і кетонів»).
Особливо чітко С-Н кислотність проявляється у сполук, що містять метиленову групу між двома електроноакцепторними замісниками: Р- оксикислот, Р-амінокислот та ін. У цьому випадку протон у карбонового атома досить легко відщеплюється і молекула перетворюється на карбаніони:
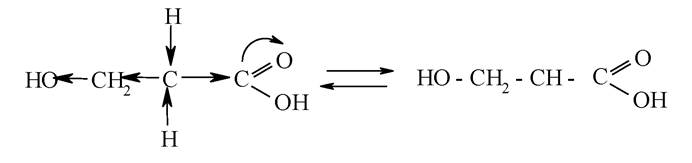
Цим обумовлюються специфічні реакції таких сполук. До основ, відповідно до протолітичної теорії Бренстеда, відносять сполуки - акцептори протонів. Зв'язування протонів органічними сполуками може здійснюватися або за рахунок неподіленої пари електронів, або за рахунок електронів п-зв'язку.
2. Найбільш чітко основні властивості виражені в ряду амінів - сполук, що містять замісники -NH2; -NHR або R1-N-R2. Хімічні властивості амінів багато в чому визначаються наявністю в атома нітрогену неподіленої пари електронів, що надає схожості з амоніаком. Так, при розчиненні у воді відбувається приєднання протона, а надлишкові гідроксильні групи обумовлюють лужну реакцію розчинів:
![]()
Іон [R-NH3]+ слід розглядати як комплексний іон, центральним атомом в якому є нітроген з координаційним числом, що дорівнює 4, а атоми гідрогену або алкіли розташовані у внутрішній координаційній сфері.
Основні властивості амінів проявляються також в їхній здатності взаємодіяти з кислотами з утворенням солей:
![]()
Солі амінів - тверді кристалічні речовини, добре розчинні у воді. Луги, як більш сильні основани, витісняють аміни з цих солей:
![]()
Унаслідок +І ефекту вуглеводневих радикалів аміни є сильнішими основами, ніж амоніак. Введення третьої алкільної групи викликає зменшення основності, що пояснюється просторовим утрудненням через екрануючий вплив трьох алкільних груп.
Основні властивості мають четвертинні амонієві основи, які за силою можна порівняти з лугами.
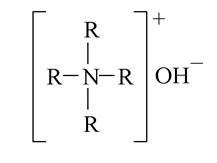
Основні властивості ароматичних амінів виражені набагато слабкіше, ніж в аліфатичних. Це обумовлено спряженням неподіленої пари електронів атома нітрогену з електронною системою ядра:
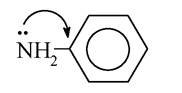
У результаті електронна густина в атомі нітрогену виявляється зниженою, і його здатність приєднувати протон послаблюється.
Водний розчин ароматичних амінів не змінює забарвлення індикаторів, вони не утворюють солі зі слабкими кислотами. При взаємодії із сильними кислотами відбувається утворення солей:
![]()
Електроноакцепторні замісники зменшують основність ароматичних амінів, а електронодонорні - збільшують її.
Основні властивості притаманні також нітрогеновмісним гетероциклічним сполукам. При цьому основність значною мірою залежить від того, чи вступає неподілена пара електронів нітрогену в спряження з електронами вуглецевих атомів циклу або ні. Так, у піролу основні властивості виражені вкрай слабо, оскільки спарені електрони нітрогену беруть участь у спряженні, унаслідок чого утворюється ароматичний характер кільця і ускладнюється приєднання протона до атома нітрогену:
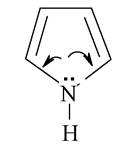
У молекулі піридину спряжена система утворена без участі неподіленої пари нітрогену, тому піридин поводить себе аналогічно до аліфатичних амінів.
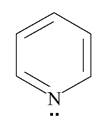
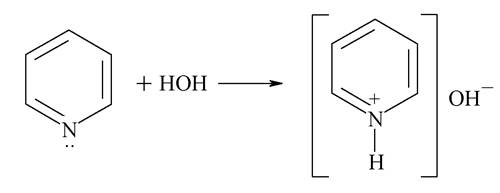
Водний розчин піридину має лужну реакцію:
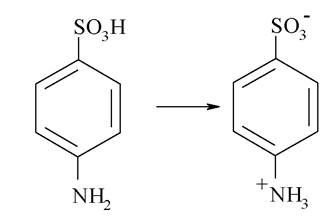
Для сполук, які містять групу основного і кислотного характеру, є характерним утворення внутрішніх солей, у яких протони, що утворюються при дисоциації кислотного угруповання, зв’язуються основною групою:
Внутрішні солі утворюють також гетерофункціональні сполуки, що мають кислотні та основні групи, які будуть розглянуті нижче.
Протон може приєднуватися неподіленою парою електронів оксигенового атома спиртів, альдегідів, ефірів і т. ін. При цьому утворюються оксонієві основи - алкільні похідні іона гідроксонію:
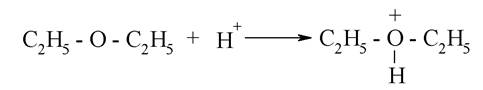
Так само, як іон гідроксонію, оксонієві основи нестійкі: вони є проміжними продуктами в багатьох реакціях, особливо при кислотному каталізі. Прикладом прояву основних властивостей за рахунок приєднання протона електронами п-зв'язку слугує розглянута раніше реакція гідратації алкенів, нуклеофільного заміщення і елімінування спирту.
Виконайте завдання і перевірте правильність їхнього розв’язання за еталонами відповідей
Завдання № 1
1. Яка зі сполук: пірол або піридин є більш сильною основою?
А. Пірол. В. Піридин. С. Пірол, піридин. D. Немає відповіді.
2. Яка кислота є більш сильною: оцтова чи хлороцтова?
А. Оцтова. В. Хлороцтова. С. Одаковою мірою. D. Немає відповіді.
3. Яка зі сполук - амоніак, метиламін чи диметиламін - є більш сильною основою?
А. Амоніак. В. Метиламін. С. Диметиламін. D. Немає відповіді.
Еталони відповідей: 1-В, 2-В, 3-С.
Завдання № 2
1. Яка зі сполук проявляє слабковиражені кислотні властивості: етанол чи бутанол більшою мірою?
А. Етанол. В. Бутанол. С. Однакові. D. Немає відповіді.
2. Яке середовище у водному розчині аспарагінової кислоти?
А. Нейтральне. В. Кисле. С. Основне. D. Немає відповіді.
3. Яка сполука: етанол чи гліцерин проявляють кислотні властивості більшою мірою?
А. Етанол. В. Гліцерин. С. Не проявляють. D. Немає відповіді.
Еталони відповідей: 1-А; 2-В; 3-В.
Завдання № 3
1. Яке середовище у водному розчині лізину?
А. Кисле. В. Основне. С. Нейтральне. D. Немає відповіді.
2. Яка речовина сильніше проявляє кислотні властивості: вода чи метанол?
А. Вода. В. Метанол. С. Вода, метанол. D. Немає відповіді.
3. Яка кількість кислотних центрів у сполуки:
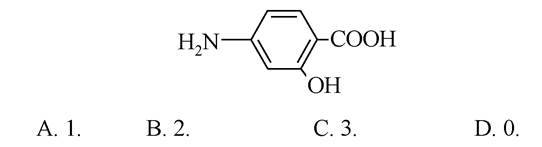
Еталони відповідей:1-В; 2-А; 3-В.