Биохимия и молекулярная биология - Белясова Н.А. 2002
Молекулярные основы и механизмы наследственности
Сохранение постоянства и изменчивость геномов
Репарация ДНК
Несмотря на высокую точность работы ферментов, осуществляющих репликацию ДНК, а также на существование механизма корректорской правки, при синтезе новых цепей ДНК все же происходят ошибки, связанные с включением в их состав некомплементарных нуклеотидов. Кроме того, молекулы ДНК подвергаются в клетках воздействию разнообразных физических и химических факторов, нарушающих их структуру. К числу наиболее часто возникающих повреждений ДНК можно отнести следующие:
— разрыв (β-N)-гликозидных связей между пурином и дезоксирибозой (депуринизация), который чаще всего является следствием повышения температуры. За сутки в клетке человека совершается от 5000 до 10 000 актов депуринизации;
— спонтанное дезаминирование остатков цитозина и аденина с образованием, соответственно, остатков урацила и гипоксантина (примерно 100 событий на геном в сутки);
— алкилирование азотистых оснований под действием химических веществ особого класса (алкилирующих агентов);
— интеркаляция (встраивание) некоторых соединений между соседними парами нуклеотидов;
— образование ковалентных сшивок между цепями ДНК под действием бифункциональных агентов;
— образование, возникающих при поглощении ультрафиолетового света (УФ) циклобутановых димеров (рис. 2.2) между соседними пиримидинами в цепи.
Большинство перечисленных повреждений нарушает процессы репликации и экспрессии генов, например, каждый тиминовый димер в ДНК E. coli задерживает репликацию на 10 с. Кроме того, эти повреждения являются источником мутаций, если их исправление не осуществится до начала репликации ДНК.
Чаще всего подобные нарушения происходят лишь в одной из нитей ДНК, при этом во второй нити напротив повреждения в большинстве случаев содержится «правильная» последовательность, которая может служить матрицей для исправления ошибок. Таким образом, двойная спираль ДНК, а также то, что в ней закодирована информация о структуре репарационных ферментов, делает возможным уникальный механизм исправления ошибок — репарацию, характерный только для одного класса молекул — ДНК.
Репарационных систем и механизмов, существующих у разных организмов, очень много, среди них есть такие, которые специфичны лишь для исправления повреждений одного рода, а есть и менее специфичные. Для удобства все известные к настоящему времени репарационные процессы можно разделить на две категории: 1) те, что не требуют участия репликации и представляют собой непосредственное исправление нарушений в ДНК; 2) более сложные процессы, в ходе которых происходит репарационная репликация. Лучше всего репарационные механизмы изучены по отношению к исправлению повреждений, вызванных УФ-облучением, — пиримидиновых димеров (рис. 2.2).
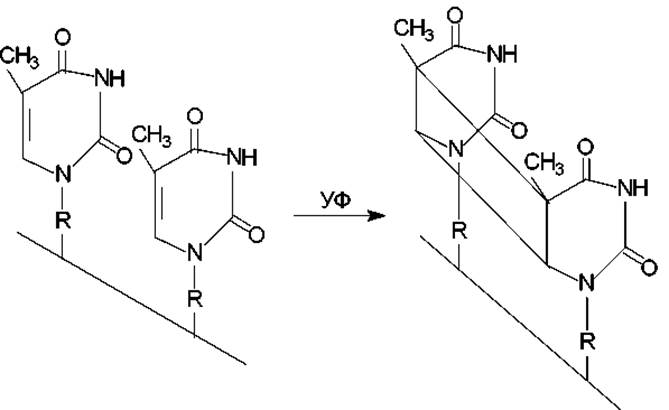
Рис. 2.2. Образование тиминовых димеров в одной из цепей ДНК включает формирование циклобутанового кольца (состоит из четырех углеродных атомов) при взаимодействии атомов соседних пиримидиновых оснований
Поскольку в наиболее известных процессах репарации последствий УФ- облучения принимают участие зависимые от УФ-света ферменты, репарационные механизмы делят также на световую (способную осуществиться лишь на видимом свету) и темновую (не требующую участия видимого света) репарацию.
К репарационным механизмам прямого исправления повреждений можно отнести дезалкилирование остатков гуанина и мономеризацию циклобутановых димеров между соседними пиримидиновыми основаниями. Дезалкилирование метилгуаниновых остатков относится к темновой репарации и происходит при участии ферментов, присутствующих в клетках бактерий и млекопитающих. О6-метилгуанин-ДНК-алкил-трансфераза катализирует перенос алкильных групп на сульфгидрильные группы цистеиновых остатков фермента (рис. 2.3).
Расщепление димеров между пиримидиновыми нуклеотидами происходит в процессе фотореактивации — восстановления структуры молекул ДНК, поврежденных УФ-излучением в результате последующего воздействия видимого света (световая репарация). Известна неферментативная коротковолновая фотореактивация, которая заключается в мономеризации димеров при действии ультрафиолетового излучения с длиной волны 240 нм, а также ферментативная фотореактивация. Последнюю обычно и подразумевают под собственно фотореактивацией. Этот процесс требует участия видимого света с длиной волны 300—600 нм и осуществляется под действием специфических фотореактивирующих ферментов (дезоксирибопиримидинфотолиазы). Субстратом фотолиазы служат димеры пиримидиновых оснований, с которыми она образует комплекс (с неповрежденной ДНК фермент не связывается). Используя энергию поглощенного света, фермент разрушает димер без разрыва цепей ДНК (рис. 2.4).
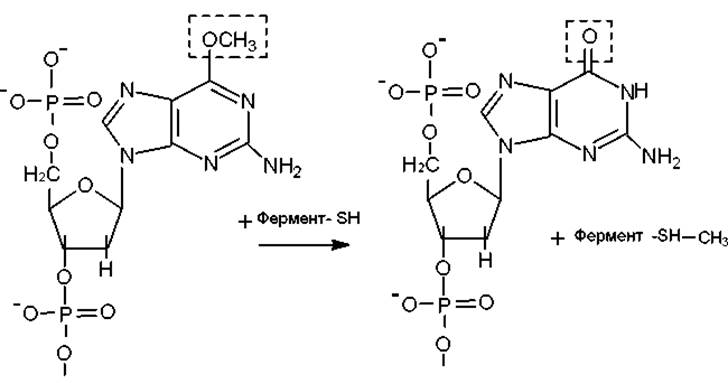
Рис. 2.3. Дезалкилирование О6-метилгуаниновых остатков катализируется специфической ДНК-алкилтрансферазой
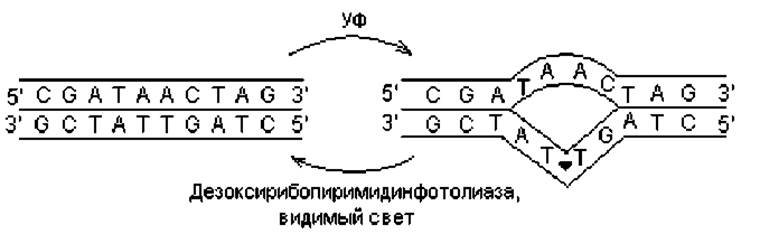
Рис. 2.4. Образование тиминовых димеров под действием УФ-света и их разрушение на свету при помощи фотореактивирующего фермента
Явление фотореактивации широко распространено в природе и обнаружено даже у таких примитивных микроорганизмов, как микоплазмы. Фотореактивирующие ферменты найдены у некоторых высших растений и животных, а также у всех изученных бактерий, за исключением Deinococcus radiodurans, который, тем не менее, чрезвычайно устойчив к действию УФ-света: эти бактерии выдерживают дозы в 1000 раз более высокие, чем те, которые убивают E. coli. При полном отсутствии способности к фотореактивации D. radiodurans обладает мощной системой эксцизионной репарации.
Репарационные события, связанные с заменой искаженных участков, не требуют участия видимого света и в них, кроме других ферментов, важную роль играют нуклеазы двух типов: экзо- и эндонуклеазы. Экзонуклеазы осуществляют расщепление ДНК, начиная с концов цепей, а эндонуклеазы атакуют цепи во внутренних частях, формируя в ДНК однонитевые разрывы. Среди многообразия разных видов репарации, связанной с репаративным синтезом ДНК, можно выделить два основных: эксцизионную и пострепликативную репарацию.
Эксцизионная репарация. Отличительной особенностью эксцизионной репарации является удаление поврежденного участка ДНК. Этот вид репарации не столь специфичен в отношении повреждений ДНК, как фотореактивация, и с его помощью могут исправляться не только пиримидиновые димеры, но и многие другие изменения структуры ДНК. Эксцизионная репарация (рис. 2.5, А) представляет собой многоэтапный процесс и включает следующие события: 1) узнавание повреждения в ДНК, которое осуществляется специфическими эндонуклеазами, выполняющими и следующую стадию; 2) надрезание одной цепи ДНК вблизи повреждения — инцизия (осуществляют эндонуклеазы); 3) удаление группы нуклеотидов вместе с повреждением — эксцизия (осуществляют экзонуклеазы); 4) ресинтез ДНК — заполнение образовавшейся бреши (ДНК-полимеразная активность); 5) восстановление непрерывности репарируемой цепи за счет образования ковалентных связей сахарофосфатного остова молекулы.
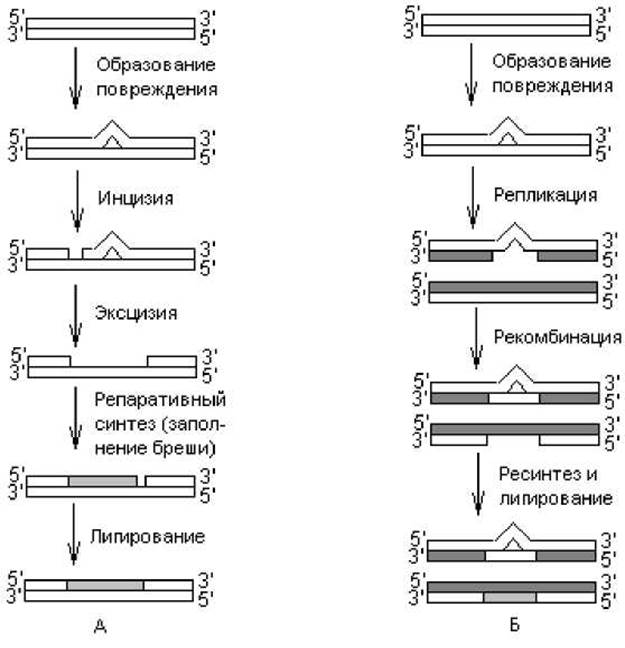
Рис. 2.5. Два типа темновой репарации: А — эксцизионная репарация, Б — пострепликативная репарация. Светлые линии — исходные цепи ДНК; темные линии — цепи ДНК, синтезированные в ходе репарационных событий
Лучше всего механизм эксцизионной репарации изучен на примере темнового удаления пиримидиновых димеров из ДНК E. coli, облученных ультрафиолетом. В клетках кишечной палочки за данный процесс отвечают гены uvrA-D (кодируют структуру ферментов, вырезающих участок цепи ДНК с димером), а также polА (определяет структуру ДНК-полимеразы I, осуществляющую репартивный синтез ДНК). Особенностью такого способа эксцизионной репарации является образование одноцепочечных надрезов по обе стороны тиминового димера.
Некоторые организмы используют для репарации повреждений, в том числе связанных с образованием тиминовых димеров, еще одну разновидность эксцизионной репарации, предусматривающую участие в процессе особого фермента — N-гликозилазы. В данном случае первым репаративным событием является расщепление гликозидной связи между поврежденным основанием (например, одним из тиминов в димере, N-алкилированным пурином и др.) и дезоксирибозой. Таким образом, имеет место локальная апуринизация, или апиримидинизация; возникает так называемый АР-сайт, узнаваемый АР-специфической эндонуклеазой, которая расщепляет фосфоди-эфирную связь рядом с АР-сайтом. Затем брешь заполняется с помощью обычного репаративного синтеза.
В бактериальных и эукариотических клетках обнаружен целый ряд различных N-гликозилаз. Например, урацил-ДНК-гликозилаза узнает неправильную пару dG/dU, возникшую в результате спонтанного дезаминирования остатка дезоксицитозина из пары dG/dC. Дезаминирование цитозина может привести при репликации к возникновению мутантной нуклеотидной пары dA/dT, поскольку с точки зрения образования водородных связей урацил ведет себя аналогично тимину. Другой, широко распространенный фермент подобного типа, представляет собой пиримидиновый димер-N-гликозилазу, которая создает апиримидиновый сайт при репарации повреждений, связанных с образованием пиримидиновых димеров.
Сайты, в которых произошла депуринизация или депиримидинизация, выщепляются ферментами АР (апуриновые и апиримидиновые)-эндонуклеазами. В клетках про- и эукариот имеется много разнообразных АР-эндонуклеаз. Некоторые из них надрезают цепь с 3'-стороны АР-сайта, а другие расщепляют диэфирную связь с 5'-стороны; в любом случае образуются 3'-гидроксильный и 5'-фосфорильный концы. Это позволяет экзонук- леазе удалить прилегающие остатки по обе стороны надреза вместе с повреждением.
Различные варианты эксцизионной репарации широко распространены у про- и эукариотических организмов, в том числе у млекопитающих. Нарушения процессов эксцизионной репарации могут приводить к драматическим последствиям. Так, у людей известно наследственное заболевание — пигментная ксеродерма, основными симптомами которого является повышенная чувствительность к солнечному свету, приводящая к развитию рака кожи. У этих больных обнаружены различные дефекты эксцизионной репарации.
Пострепликативная репарация. Этот тип репарации требует участия продуктов генов, задействованных также в рекомбинационных событиях (rec-гены), и не осуществляется в клетках rec-мутантов, поэтому его называют еще и рекомбинационной репарацией. Рекомбинционная пострепликативная репарация основана на процессах репликации и рекомбинации поврежденной ДНК, она наименее специфична из всех рассмотренных типов репарации, поскольку в ней отсутствует этап узнавания повреждения. Это довольно быстрый способ восстановления нативной структуры ДНК в дочерних (вновь синтезированных) цепях: показано, что репарация происходит уже в первые минуты после облучения. Особенностью данного процесса является сохранение повреждения в исходных (материнских) цепочках (рис. 2.5, Б).
Наряду с быстрой существует и медленная пострепликативная репарация, для которой требуется несколько часов. Ее производит система ферментов, которая отсутствует в необлученных клетках и которую индуцирует облучение. Этот механизм получил название SOS-репарации. Его удивительным отличием является значительное увеличение частоты мутаций, несмотря на то что ДНК и так уже повреждена. Это может являться следствием использования в качестве матрицы цепи ДНК, содержащей повреждения.
Пострепликативная репарация существует не только у бактерий, но и в клетках эукариот, в том числе у млекопитающих.