БИОХИМИЯ УЧЕБНИК ДЛЯ ВУЗОВ - Е. С. Северина - 2004
РАЗДЕЛ 9. ОБМЕН И ФУНКЦИИ АМИНОКИСЛОТ
III. Переваривание белков
В пищевых продуктах содержание свободных аминокислот очень мало. Подавляющее их количество входит в состав белков, которые гидролизуются в ЖКТ под действием ферментов протеаз (пептидгидролаз). Субстратная специфичность этих ферментов заключается в том, что каждый из них с наибольшей скоростью расщепляет пептидные связи, образованные определёнными аминокислотами. Протеазы, гидролизующие пептидные связи внутри белковой молекулы, относят к группе эндопептидаз. Ферменты, относящиеся к группе экзопептидаз, гидролизуют пептидную связь, образованную концевыми аминокислотами. Под действием всех протеаз ЖКТ белки пищи распадаются на отдельные аминокислоты, которые затем поступают в клетки тканей.
А. Переваривание белков в желудке
Желудочный сок — продукт нескольких типов клеток. Обкладочные (париетальные) клетки стенок желудка образуют соляную кислоту, главные клетки секретируют пепсиноген. Добавочные и другие клетки эпителия желудка выделяют муцинсодержащую слизь. Париетальные клетки секретируют в полость желудка также гликопротеин, который называют «внутренним фактором» (фактором Касла). Этот белок связывает «внешний фактор» — витамин В12, предотвращает его разрушение и способствует всасыванию.
1. Образование и роль соляной кислоты
Основная пищеварительная функция желудка заключается в том, что в нём начинается переваривание белка. Существенную роль в этом процессе играет соляная кислота. Белки, поступающие в желудок, стимулируют выделение гистамина и группы белковых гормонов — гастринов (см. раздел 11), которые, в свою очередь, вызывают секрецию НСl и профермента — пепсиногена. НСl образуется в обкладочных клетках желудочных желёз в ходе реакций, представленных на рис. 9-2.
Рис. 9-2. Секреция соляной кислоты в желудке. 1 — карбоангидраза; 2 — Н+/К+- АТФ-аза; 3 — белки-переносчики анионов; 4 — хлоридный канал.
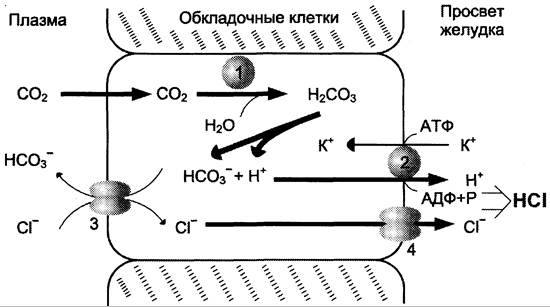
Источником Н+ является Н2СO3, которая образуется в обкладочных клетках желудка из СО2, диффундирующего из крови, и Н2O под действием фермента карбоангидразы (карбонатдегидратазы):
H2O + CO2 —> Н2СO3 —> НСO3- + H+.
Диссоциация Н2СO3 приводит к образованию бикарбоната, который с участием специальных белков выделяется в плазму в обмен на Сl-, и ионов Н+, которые поступают в просвет желудка путём активного транспорта, катализируемого мембранной Н+/К+-АТФ-азой. При этом концентрация протонов в просвете желудка увеличивается в 106 раз. Ионы Сl- поступают в просвет желудка через хлоридный канал.
Концентрация НСl в желудочном соке может достигать 0,16 М, за счёт чего значение pH снижается до 1,0 — 2,0. Приём белковой пищи часто сопровождается выделением щелочной мочи за счёт секреции большого количества бикарбоната в процессе образования НСl.
Под действием HCl происходит денатурация белков пищи, не подвергшихся термической обработке, что увеличивает доступность пептидных связей для протеаз. НСl обладает бактерицидным действием и препятствует попаданию патогенных бактерий в кишечник. Кроме того, соляная кислота активирует пепсиноген и создаёт оптимум pH для действия пепсина.
2. Механизм активации пепсина
Под действием гастринов в главных клетках желудочных желёз стимулируются синтез и секреция пепсиногена — неактивной формы пепсина. Пепсиноген — белок, состоящий из одной полипептидной цепи с молекулярной массой 40 кД. Под действием НСl он превращается в активный пепсин (молекулярная масса 32,7 кД) с оптимумом pH 1,0 — 2,5. В процессе активации в результате частичного протеолиза от N-конца молекулы пепсиногена отщепляются 42 аминокислотных остатка, которые содержат почти все положительно заряженные аминокислоты, имеющиеся в пепсиногене. Таким образом, в активном пепсине преобладающими оказываются отрицательно заряженные аминокислоты, которые участвуют в конформационных перестройках молекулы и формировании активного центра. Образовавшиеся под действием НСl активные молекулы пепсина быстро активируют остальные молекулы пепсиногена (аутокатализ). Пепсин в первую очередь гидролизует пептидные связи в белках, образованные ароматическими аминокислотами (фенилаланин, триптофан, тирозин) и несколько медленнее — образованные лейцином и дикарбоновыми аминокислотами. Пепсин — эндопептидаза, поэтому в результате его действия в желудке образуются более короткие пептиды, но не свободные аминокислоты.
3. Возрастные особенности переваривания белков в желудке
У детей грудного возраста в желудке находится фермент реннин (химозин), вызывающий свёртывание молока. Основной белок молока — казеин, представляющий смесь нескольких белков, различающихся по аминокислотному составу и электрофоретической подвижности. Реннин катализирует отщепление от казеина гликопептида, в результате чего образуется параказеин. Параказеин присоединяет ионы Са2+, образуя нерастворимый сгусток, чем предотвращает быстрый выход молока из желудка. Белки успевают расщепиться под действием пепсина. В желудке взрослых людей реннина нет, молоко у них створаживается под действием НСl и пепсина.
В слизистой оболочке желудка человека найдена ещё одна протеаза — гастриксин. Все 3 фермента (пепсин, реннин и гастриксин) сходны по первичной структуре, что указывает на их происхождение от общего гена-предшественника.
4. Нарушения переваривания белков в желудке
При различных заболеваниях ЖКТ в желудке нарушается выделение НСl и пепсиногена, при этом переваривание белков заметно снижается. Наиболее часто встречаются патологические изменения кислотности желудочного сока. Нарушение образования пепсина отмечают реже и выявляют при более значительных поражениях желудка.
Определение кислотности желудочного сока используют для диагностики различных заболеваний желудка (табл. 9-2). Повышенная кислотность желудочного сока обычно сопровождается изжогой, диареей и может быть симптомом язвы желудка и двенадцатиперстной кишки, а также гиперацидного гастрита. Пониженная кислотность бывает при некоторых видах гастритов. Полное отсутствие НСl и пепсина (желудочная ахилия) наблюдается при атрофических гастритах и часто сопровождается пернициозной анемией вследствие недостаточности выработки фактора Касла и нарушения всасывания витамина В12 (см. раздел 3). Анацидность (pH желудочного сока >6,0) свидетельствует о значительной потере слизистой оболочкой желудка обкладочных клеток, секретирующих соляную кислоту, что часто вызывает рак желудка.
Таблица 9-2. Компоненты желудочного сока в норме и при патологических состояниях
Состояние |
pH |
Кислотность (ТЕ) |
Пепсин |
Фактор Касла |
Молочная кислота |
Кровь |
||
общая |
связанная НСl |
свободная НСl |
||||||
Норма |
1,5-2,0 |
40-60 |
20-30 |
20-40 |
+ |
+ |
- |
- |
Гиперацидный гастрит |
1,0 |
80 |
40 |
+ |
+ |
- |
- |
|
Гипоацидный гастрит |
2,5 |
40 |
20 |
± |
± |
± |
- |
|
Ахилия |
7,0 |
20 |
- |
- |
- |
+ |
- |
|
Язва желудка |
1,5 |
60 |
40 |
+ |
+ |
- |
+ |
|
Рак желудка |
6,0 и > |
40-60 |
20 |
+ |
+ |
+ |
+ |
|
Кислотность желудочного сока выражается в титрационных единицах (ТЕ) — количество 0,1 М NaOH в 1 мл, затраченное на титрование 100 мл желудочного сока по определённому индикатору. При определении кислотности желудочного сока различают: общую кислотность, связанную НСl и свободную НСl.
Общая кислотность желудочного сока — совокупность всех кислотореагирующих веществ желудочного сока, представляет собой секрет желудка, собираемый в течение 1 ч. Значения общей кислотности в норме составляют 40 — 60 ТЕ.
Связанная соляная кислота — НСl, связанная с белками и продуктами их переваривания. Значения связанной НСl у здоровых людей — 20-30 ТЕ.
Свободная НСl — соляная кислота, не связанная с компонентами желудочного сока. Значения свободной НСl в норме — 20 — 40 ТЕ.
pH желудочного сока в норме — 1,5 — 2,0.
Молочная кислота в норме в желудочном соке отсутствует. Она образуется при уменьшении содержания или отсутствии свободной соляной кислоты в результате размножения молочнокислых бактерий или при злокачественных опухолях желудка, в клетках которых глюкоза окисляется анаэробным путём.
При диагностике заболеваний желудка, кроме биохимических анализов, обязательно проводят рентгенологические и эндоскопические исследования, а также биопсию.
Б. Переваривание белков в кишечнике
Желудочное содержимое (химус) в процессе переваривания поступает в двенадцатиперстную кишку. Низкое значение pH химуса вызывает в кишечнике выделение белкового гормона секретина, поступающего в кровь. Этот гормон в свою очередь стимулирует выделение из поджелудочной железы в тонкий кишечник панкреатического сока, содержащего НСO3, что приводит к нейтрализации НСl желудочного сока и ингибированию пепсина. В результате pH резко возрастает от 1,5 — 2,0 до ~7,0.
Поступление пептидов в тонкий кишечник вызывает секрецию другого белкового гормона — холецистокинина (см. раздел 11), который стимулирует выделение панкреатических ферментов с оптимумом pH 7,5 — 8,0. Под действием ферментов поджелудочной железы и клеток кишечника завершается переваривание белков.
1. Активация панкреатических ферментов
В поджелудочной железе синтезируются проферменты ряда протеаз: трипсиноген, химотрипсиноген, проэластаза, прокарбоксипептидазы А и В. В кишечнике они путём частичного протеолиза превращаются в активные ферменты трипсин, химотрипсин, эластазу и карбоксипептидазы А и В.
Активация трипсиногена происходит под действием фермента эпителия кишечника энтеропептидазы. Этот фермент отщепляет с N-конца молекулы трипсиногена гексапептид Вал-(Асп)4- Лиз. Изменение конформации оставшейся части полипептидной цепи приводит к формированию активного центра, и образуется активный трипсин. Последовательность Вал-(Асп)4-Лиз присуща большинству известных трипсиногенов разных организмов — от рыб до человека.
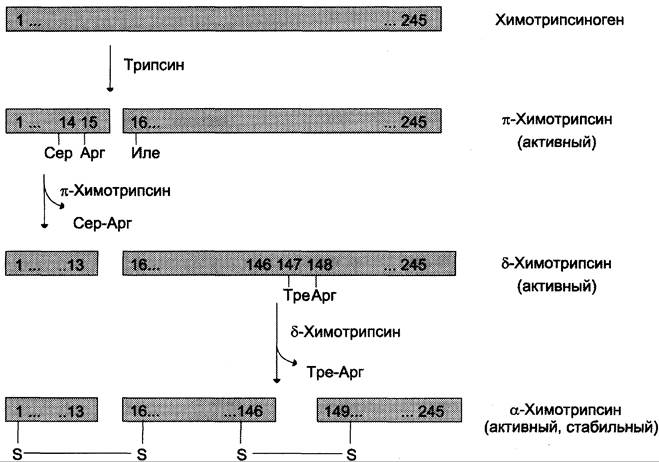
Образовавшийся трипсин активирует химотрипсиноген, из которого получается несколько активных ферментов (рис. 9-3). Химотрипсиноген состоит из одной полипептидной цепи, содержащей 245 аминокислотных остатков и пяти дисульфидных мостиков. Под действием трипсина расщепляется пептидная связь между 15-й и 16-й аминокислотами, в результате чего образуется активный π-химотрипсин. Затем под действием π-химотрипсина отщепляется дипептид сер(14)-арг(15), что приводит к образованию 5-химотрипсина. Отщепление дипептида тре(147)-арг(148) завершает образование стабильной формы активного фермента — α-химотрипсина, который состоит из трёх полипептидных цепей, соединённых дисульфидными мостиками.
Рис. 9-3. Активация химотрипсиногена. Молекула химотрипсиногена состоит из 245 аминокислотных остатков и имеет пять дисульфидных мостиков. На схеме показаны участки фермента, подвергающиеся протеолизу. α-Химотрипсин — активная стабильная форма фермента — состоит из трёх попипептидных цепей, ковалентно связанных между собой двумя дисульфидными мостиками и нековалентно — за счёт водородных связей и гидрофобных взаимодействий.
Остальные проферменты панкреатических протеаз (проэластаза и прокарбоксипептидазы А и В) также активируются трипсином путём частичного протеолиза. В результате образуются активные ферменты — эластаза и карбоксипептидазы А и В.
2. Специфичность действия протеаз
Трипсин преимущественно гидролизует пептидные связи, образованные карбоксильными группами аргинина и лизина. Химотрипсины наиболее активны в отношении пептидных связей, образованных карбоксильными группами ароматических аминокислот (Фен, Тир, Три).
Карбоксипептидазы А и В — цинксодержащие ферменты, отщепляют С-концевые остатки аминокислот. Причём карбоксипептидаза А отщепляет преимущественно аминокислоты, содержащие ароматические или гидрофобные радикалы, а карбоксипептидаза В — остатки аргинина и лизина.
Последний этап переваривания — гидролиз небольших пептидов, происходит под действием ферментов аминопептидаз и дипептидаз, которые синтезируются клетками тонкого кишечника в активной форме.
Аминопептидазы последовательно отщепляют N-концевые аминокислоты пептидной цепи. Наиболее известна лейцинаминопептидаза — Zn2+- или Мn2+-содержащий фермент, несмотря на название, обладающий широкой специфичностью по отношению к N-концевым аминокислотам.
Дипептидазы расщепляют дипептиды на аминокислоты, но не действуют на трипептиды.
В результате последовательного действия всех пищеварительных протеаз большинство пищевых белков расщепляется до свободных аминокислот.
В. Защита клеток от действия протеаз
Клетки поджелудочной железы защищены от действия пищеварительных ферментов тем, что:
✵ эти ферменты образуются в виде неактивных предшественников в клетках поджелудочной железы и активируются только после секреции в просвет кишечника. Таким образом, место синтеза и место действия этих ферментов пространственно разделены.
✵ в клетках поджелудочной железы присутствует белок-ингибитор трипсина, образующий с активной формой фермента (в случае преждевременной активации) прочный комплекс.
В полости желудка и кишечника протеазы не контактируют с белками клеток, поскольку слизистая оболочка покрыта слоем слизи, а каждая клетка содержит на наружной поверхности плазматической мембраны полисахариды, которые не расщепляются протеазами и тем самым защищают клетку от их действия.
Разрушение клеточных белков протеазами происходит при язвенной болезни желудка или двенадцатиперстной кишки. Однако начальные механизмы возникновения язвы ещё мало изучены.
Г. Транспорт аминокислот в клетки
Аминокислоты, образовавшиеся при переваривании белков, быстро всасываются в кишечнике. Транспорт их осуществляется двумя путями: через воротную систему печени, ведущую прямо в печень, и по лимфатическим сосудам, сообщающимся с кровью через грудной лимфатический проток. Максимальная концентрация аминокислот в крови достигается через 30 — 50 мин после приёма белковой пищи (углеводы и жиры замедляют всасывание аминокислот). Всасывание L-аминокислот (но не D-изомеров) — активный процесс, требующий затраты энергии. Аминокислоты переносятся через кишечную стенку от слизистой её поверхности в кровь (рис. 9-4). Перенос через щёточную кайму осуществляется целым радом переносчиков, многие из которых действуют при участии Na+-зависимых механизмов симпорта, подобно переносу глюкозы (см. раздел 7).
Рис. 9-4. Механизм всасывания аминокислот в кишечнике. L-аминокислота поступает в энтероцит путём симпорта с ионом Nа+. Далее специфическая транслоказа переносит аминокислоту через мембрану в кровь. Обмен ионов натрия между клетками осуществляется путём первично-активного транспорта с помощью Na+, К+-АТФ-азы.
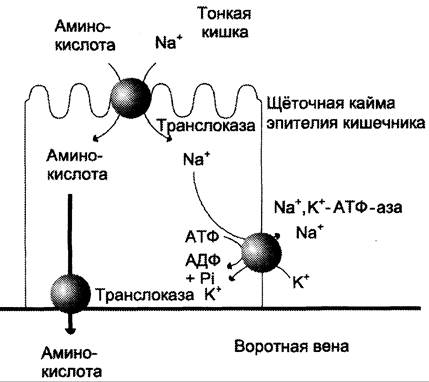
Различная скорость проникновения аминокислот через мембраны клеток указывает на наличие транспортных систем, обеспечивающих перенос аминокислот как через внешнюю плазматическую мембрану, так и через внутриклеточные мембраны. В настоящее время известно по крайней мере пять специфических транспортных систем, каждая из которых функционирует для переноса определённой группы близких по строению аминокислот:
✵ нейтральных, с короткой боковой цепью (аланин, серин, треонин);
✵ нейтральных, с длинной или разветвлённой боковой цепью (валин, лейцин, изолейцин);
✵ с катионными радикалами (лизин, аргинин);
✵ с анионными радикалами (глутаминовая и аспарагиновая кислоты);
✵ иминокислот (пролин, оксипролин).
Причём к числу Na+-зависимых относятся переносчики аминокислот, входящих в первую и пятую группы, а также переносчик метионина. Независимые от Na+ переносчики специфичны для некоторых нейтральных аминокислот (фенилаланин, лейцин) и аминокислот с катионными радикалами (лизин).
Аминокислоты конкурируют друг с другом за специфические участки связывания. Например, всасывание лейцина (если концентрация его достаточно высока) уменьшает всасывание изолейцина и валина.
Одна из специфических транспортных систем для некоторых нейтральных аминокислот функционирует в кишечнике, почках и, по-видимому, мозге. Она получила название y-глутамильного цикла (рис. 9-5).
Рис. 9-5. y-Глутамильный цикл. Система состоит из одного мембранного и пяти цитоплазматических ферментов. Перенос аминокислоты внутрь клетки осуществляется в комплексе с глутамильным остатком глутатиона под действием y-глутамилтранс- феразы. Затем аминокислота освобождается, а y-глутамильный остаток в несколько стадий превращается в глутатион, который способен присоединять следующую молекулу аминокислоты. Е1 — у-глутамилтрансфераза; Е2 — у-глутамилциклотрансфераза; Е3 — пептидаза; Е4 — оксопролиназа; Е5 — y-глутамилцистеинсинтетаза; Е6 — глутатионсинтетаза.
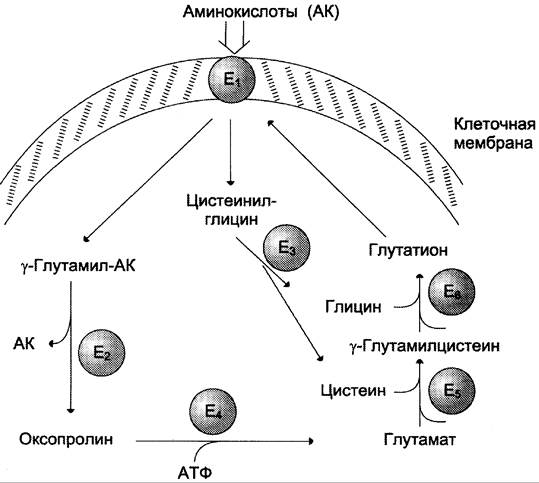
В этой системе участвуют 6 ферментов, один из которых находится в клеточной мембране, а остальные — в цитозоле. Ключевую роль в транспорте аминокислоты играет мембранно-связанный фермент y-глутамилтрансфераза. Этот фермент является гликопротеином и катализирует перенос y-глутамильной группы от глутатиона (иногда другого y-глутамильного пептида) на транспортируемую аминокислоту и последующий перенос комплекса в клетку. Глутатион представляет собой трипептид — y-глутамилцистеинилглицин, который находится во всех тканях животных. Реакция протекает следующим образом (см. схему А на с. 468).
Аминокислота, связанная с y-глутамильным остатком, оказывается внутри клетки. В следующей реакции происходит отщепление у-глутамильного остатка под действием фермента y-глутамилциклотрансферазы (см. схему Б).
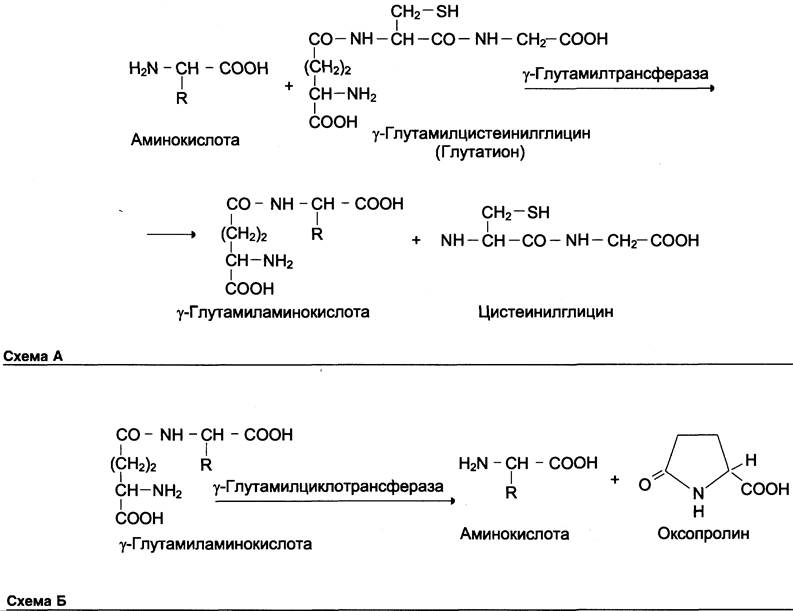
Дипептид цистеинилглицин расщепляется под действием пептидазы на 2 аминокислоты — цистеин и глицин. В результате этих 3 реакций происходит перенос одной молекулы аминокислоты в клетку (или внутриклеточную структуру). Следующие 3 реакции обеспечивают регенерацию глутатиона, благодаря чему цикл повторяется многократно. Для транспорта в клетку одной молекулы аминокислоты с участием y-глутамильного цикла затрачиваются 3 молекулы АТФ.
Д. Нарушение переваривания белков и транспорта аминокислот
Небольшую долю продуктов переваривания белка составляют негидролизованные короткие пептиды. У некоторых людей возникает иммунная реакция на приём белка, что, очевидно, связано со способностью к всасыванию таких пептидов. Продукты полностью переваренного белка (аминокислоты) лишены антигенных свойств и иммунных реакций не вызывают.
У новорождённых проницаемость слизистой оболочки кишечника выше, чем у взрослых, поэтому в кровь могут поступать антитела молозива (секрет молочных желёз, выделяющийся в первые дни после родов, обогащённый антителами и антитоксинами). Это усугубляется наличием в молозиве белка — ингибитора трипсина. Протеолитические ферменты в пищеварительных секретах новорождённых обладают низкой активностью. Всё это способствует всасыванию в кишечнике небольшого количества нативных белков, достаточного для обеспечения иммунной реакции. Очевидно, подобное усиление всасывающей способности кишечника является причиной наблюдаемой иногда непереносимости белков пищи (например, молока и яиц) у взрослых людей.
Всё больше подтверждений получает гипотеза, согласно которой при заболевании целиакии (нетропической спру) происходит нарушение клеток слизистой оболочки кишечника, где всасываются небольшие негидролизованные пептиды. Целиакия характеризуется повышенной чувствительностью к глютену — белку клейковины зёрен злаков, употребляемых с пищей человеком. Этот белок оказывает токсическое действие на слизистую оболочку тонкой кишки, что приводит к её патологическим изменениям и нарушению всасывания. Патогенез заболевания недостаточно ясен.
Такие заболевания, как цистинурия, болезнь Хартнапа и некоторые другие, возникают вследствие дефекта переносчиков нейтральных аминокислот в кишечнике и почках. Описана врождённая патология, связанная с дефектом фермента 5-оксопролиназы (рис. 9-5, реакция 4). При этом с мочой выделяется оксопролин. У этих больных нарушены транспорт аминокислот в ткани и их метаболизм в клетках.