Підручник - БІОЛОГІЧНА ХІМІЯ - Губський Ю.І. - 2000
Розділ II. ЗАГАЛЬНІ ЗАКОНОМІРНОСТІ МЕТАБОЛІЗМУ
ГЛАВА 10. ЦИКЛ ТРИКАРБОНОВИХ КИСЛОТ
10.2. ФЕРМЕНТАТИВНІ РЕАКЦІЇ ЦИКЛУ ТРИКАРБОНОВИХ КИСЛОТ
1. Утворення лимонної кислоти (цитрату) за рахунок конденсації ацетил-КоА з щавлевооцтовою кислотою (оксалоацетатом):
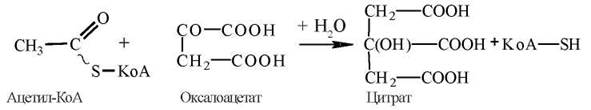
Реакція каталізується ферментом цитратсинтазою. Вона є регуляторним ферментом, активність якого гальмується АТФ, НАДН, сукциніл-КоА та довголанцюговими ацил-КоА.
2. Перетворення (ізомеризація) цитрату на ізоцитрат. Реакція каталізується ферментом аконітазою і складається з двох етапів:
2.1. Дегідратація лимонної кислоти з утворенням цис-аконітової кислоти (цис-аконітату):
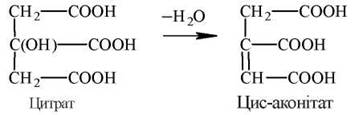
2.2. Приєднання до цис-аконітату молекули води. При приєднанні до подвійного зв’язку в складі цис-аконітату Н+ та ОН- у транс-положенні результатом реакції є утворення ізолимонної кислоти (ізоцитрату):
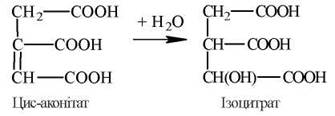
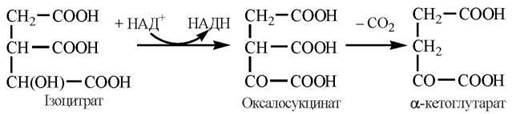
3. Дегідрування та декарбоксилювання ізоцитрату. Реакція каталізується НАД-залежною ізоцитратдегідрогеназою і призводить до утворення α-кетоглутарової кислоти (α-кетоглутарату).
Ізоцитратдегідрогеназа є регуляторним ферментом, позитивний модулятор якого — АДФ, негативний — НАДН.
Фермент має дві молекулярні форми — мономерну (молекулярна маса ізоцитратдегідрогенази з мітохондрій серця дорівнює 330 кД) та димерну. В присутності позитивного модулятора АДФ мономери агрегують між собою з утворенням димеру. Негативний модулятор НАДН протидіє індукованій АДФ агрегації мономерних форм ферменту. Обидві молекулярні форми ізоцитратдегідрогенази мають каталітичні властивості, але за умов низької концентрації АДФ димер значно більш активний.
4. Окислення α-кетоглутарату до сукцинату.
Цей процес відбувається у дві стадії:
4.1. Окислювальне декарбоксилювання α-кетоглутарату з утворенням сукциніл-КоА — стадія, що каталізується мультиензимним α-кетоглутаратдегідрогеназним комплексом. Кінцевий продукт — високоенергетичний тіоефір сукциніл-КоА, в макроергічному зв’язку якого акумульовано хімічну енергію окислювально-відновлювальною реакцією, що мала місце:
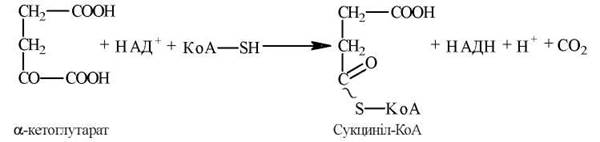
НАДН, що утворився в цій реакції, окислюється в дихальному ланцюзі мітохондрій із генерацією 3 молекул АТФ.
За механізмом реакції цей процес нагадує окислювальне декарбоксилювання пірувату до ацетил-КоА (див. главу 11); як і піруватдегідрогеназний, α-кетоглутаратдегідрогеназний комплекс має у своєму складі коферменти тіаміндифосфат (ТДФ), ліпоєву кислоту (ЛК), КоА, НАД+ та ФАД. Молекулярна маса цього комплексу з клітин E. Coli дорівнює 2,1 · 106.
4.2. Деацилювання сукциніл-КоА (перетворення на янтарну кислоту (сукцинат).
Реакція каталізується ферментом сукцинілтіокіназою. У результаті розщеплюється макроергічний зв’язок у молекулі сукциніл-КоА, та за рахунок цієї енергії утворюється нова макроергічна сполука нуклеозидтрифосфат ГТФ:
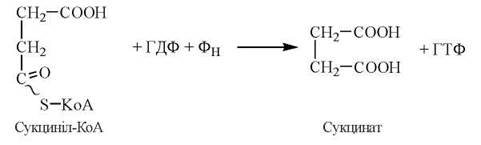
Потім ГТФ передає свою кінцеву фосфатну групу на АДФ у нуклеозидфосфокіназній реакції з утворенням АТФ:
![]()
5. Окислення янтарної кислоти до фумарової кислоти (фумарату). Реакція каталізується ФАД-залежним ферментом сукцинатдегідрогеназою:
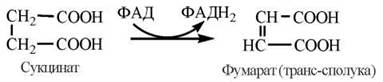
Окислення відновленого коферменту (ФАДН2) за допомогою коензиму Q дихального ланцюга мітохондрій призводить до синтезу за рахунок окисного фосфорилювання 2 молекул АТФ.
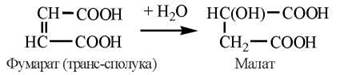
6. Перетворення фумарової кислоти на яблучну кислоту (малат) внаслідок приєднання до фумарату молекули води.
Реакція каталізується ферментом фумарат-гідратазою (фумаразою):
7. Окислення малату до оксалоацетату (щавлевооцтової кислоти).
Реакція каталізується НАД-залежним ферментом — малатдегідрогеназою мітохондрій:
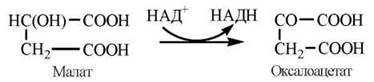
Окислення НАДН, що утворився, в дихальному ланцюзі мітохондрій призводить до генерації 3 молекул АТФ.
Малатдегідрогеназна реакція завершує цикл трикарбонових кислот. Оксалоацетат, який є продуктом даної реакції, здатний до взаємодії з новими молекулами ацетил-КоА.
Загальну метаболічну карту циклу трикарбонових кислот подано на рис. 10.2
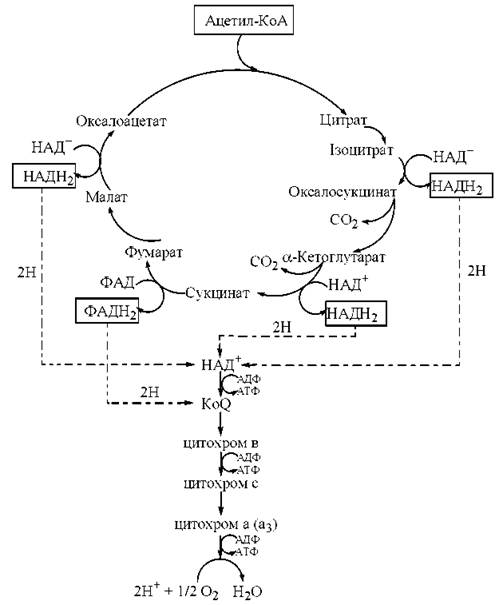
Рис. 10.2. Метаболічна карта циклу трикарбованих кислот та зв’язок ЦТК з дихальним ланцюгом мітохондрій.