СТРУКТУРА И СВОЙСТВА БИОМОЛЕКУЛ - А. Е. Земляков - 2017
07. БИОРЕГУЛЯТОРЫ: ПРОСТАГЛАНДИНЫ И ИХ АНАЛОГИ
Простагландины и ряд близких им эндогенных биологически активных соединений липидной природы, обладающих свойствами гормонов, имеют общего биосинтетического предшественника - арахидоновую кислоту. Для ряда простагландинов исходным материалом служат аналоги арахидоновой кислоты, содержащие три или пять двойных связей, соответственно, 20:3 ω6 и 20:5 ω3.
Арахидоновая кислота входит в состав фосфолипидов, из которых она выделяется под действием фермента фосфолипазы. С помощью циклооксигеназы из неё образуются первичные простагландины, которые в дальнейшем способны превращаться во вторичные простагландины и тромбоксаны. Действие на арахидоновую кислоту липоксигеназ приводит к синтезу лейкотриенов и их аналогов липоксинов.
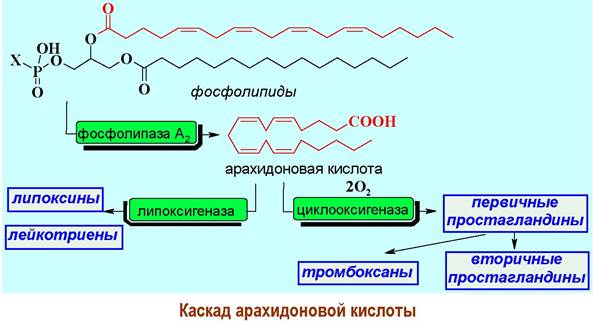
Эти группы биорегуляторов отличаются повсеместным распространением в тканях млекопитающих. Присутствуют они в очень малых концентрациях (~10-10 г на 1 г ткани), так как не существует специальных органов их получения и накопления, а происходит их синтез внутриклеточными ферментами в ответ на соответствующий биологический сигнал. Кроме того, простагландины быстро биотрансформируются. Время их полужизни около 30 сек.
Обычно они оказывают свое физиологическое действие непосредственно у места образования. В отдельных тканях присутствуют не все ферменты каскада арахидоновой кислоты. Поэтому с одной стороны осуществляется выработка биорегуляторов определенного типа, которые оказывают свое специфическое действие, а с другой стороны лекарственные препараты типа аспирина, влияющие на отдельные пути этого каскада, оказывают многогранное действие на организм. Так, тот же аспирин наряду с противовоспалительным эффектом обладает противотромботической активностью (см. ниже).
Ряд лекарственных препаратов влияет на образование этих классов биорегуляторов, изменяя не только их общее количество, но и соотношение между отдельными типами и сериями. Например, нестероидные противовоспалительные лекарственные средства ингибируют циклооксигеназу, что приводит к уменьшению образования простагландинов и тромбоксанов, повышению выхода лейкотриенов. В то же время некоторые флавоноиды (например, рутин) подавляют биосинтез лейкотриенов. Противовоспалительное действие глюкокортикостероидов также во многом объясняется их способностью ингибировать процесс биосинтеза простагландинов.
Существенная роль в выявлении этой группы биологически активных соединений принадлежит шведским ученым. В 1935 г. Ульф фон Эйлер впервые выделил и выявил активность простагландинов. В 1982 г. Нобелевская премия по физиологии и медицине за исследование простагландинов и его аналогов была присуждена профессору С. Бергстрёму, который в 1957 г. выделил простагландины в чистом виде, и профессору Б. Самуэльсону, установившему образование простагландинов, тромбоксанов и лейкотриенов в результате метаболических превращений арахидоновой кислоты.

❖ Простагландины. В основе структуры простагландинов лежит простаноевая кислота, содержащая циклопентановый фрагмент. Название данного класса соединений произошло от латинского названия предстательной железы (Glandula prostatica) - в начале исследований ошибочно считалось, что этот орган вырабатывает простагландины.
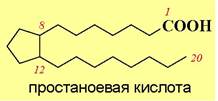
В настоящее время известно более 20 простагландинов (сокращенное обозначение PG), которые в зависимости от природы и расположения заместителей подразделяют на группы, обозначаемые латинскими буквами (А-J). Внутри групп выделяют подгруппы по количеству двойных связей, которое указывается цифровыми индексами. Для подгруппы PGF в индексе греческими буквами α и β показывают конфигурацию гидроксила у С9 в циклопентановом кольце.
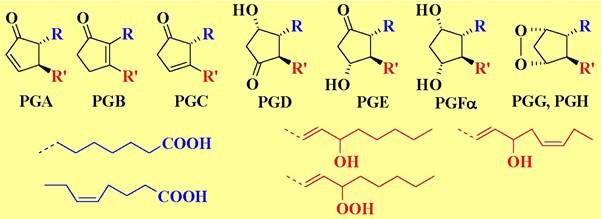
✵ Биосинтез простагландинов. Ключевой момент биосинтеза - окисление арахидоновой кислотой циклооксигеназой в результате чего образуются первичные простагландины PGG2 и PGH2. Последний далее подвергается циклизации в простациклин (PGI2), восстановлению до PGF2a или изомеризации до PGD2 и PGE2.
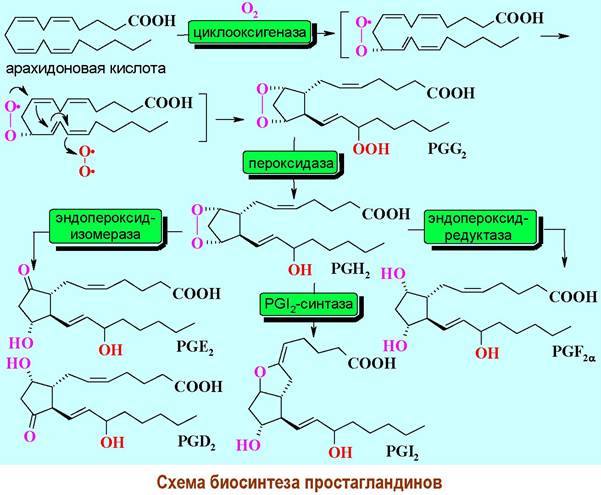
Далее могут происходить процессы дегидратации PGE2 до соответствующих производных PGA2 и PGB2.
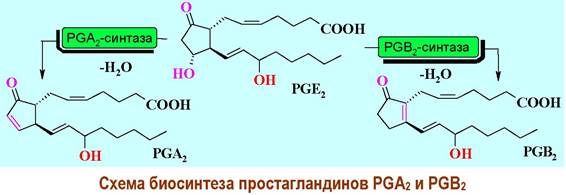
Эйкозатриеновая (20:3 ω6) и эйкозапентаеновая (20:5 ω3) кислоты начинают ряды, соответственно, моноеновых и триеновых простагландинов, например, PGЕ1 и PGЕ3. Соответствующие производные отличаются по биологической активности от простагландинов ряда арахидоновой кислоты.
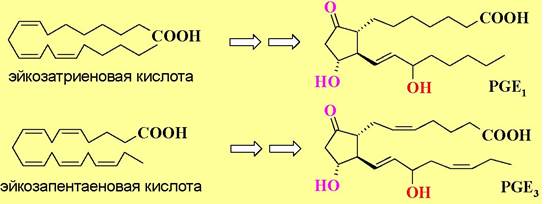
✵ Циклооксигеназа. Фермент циклооксигеназа относится к мембранным хромопротеинам и состоит из двух субъединиц с молекулярной массой по 72 кДа.
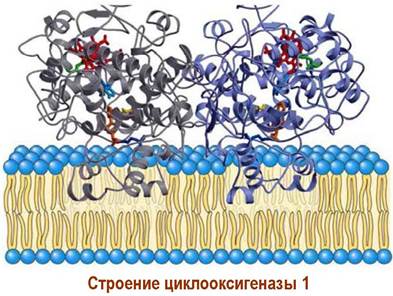
Существуют две изоформы этого фермента - циклооксигеназа-1 (СОХ-1) и циклооксигеназа-2 (СОХ-2). Первая реализуется в клетках в нормальном состоянии, а вторая в воспалительных клетках. Строение их очень близко - около 65% аминокислотной последовательности совпадает.
Фермент обеспечивает катализ двух реакций: окисление арахидоновой кислоты до PGG2 и расщепление гидропероксидной группы до гидроксильной с образованием PGH2.
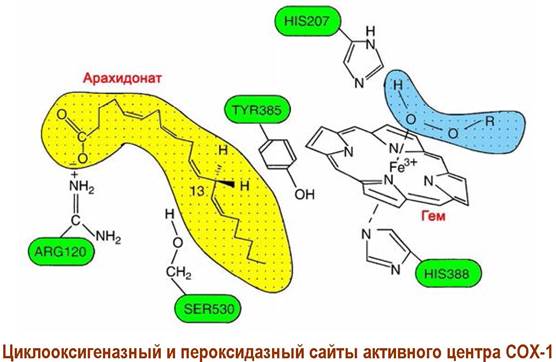
Для инициирования ферментативного процесса предварительно происходит окисление гема гидропероксидом. Восстановление гема происходит за счет переноса электрона от остатка тирозина. Образующийся при этом радикал тирозина оттягивает атом водорода у арахидоновой кислот, облегчая ее окисление.
✵ Биологическое действие простагландинов многообразно. Наиболее характерно действие этих соединений на гладкую мускулатуру, секреторную функцию желудка, кровообращение, иммунную систему. В частности, PGЕ1 и PGЕ2 расширяют сосуды бронхов, а PGF1 и PGD2 наоборот вызывают сокращение бронхов, PGЕ1 уменьшает выделение желудочного сока и сопутствующих ему веществ, PGЕ2, PGА1 и PGА2 снижают артериальное давление и облегчают кровепоток, PGЕ1 и PGF2 стимулируют родовую деятельность. Простациклин существенно уменьшает агрегацию тромбоцитов, усиливает антикоагулянтное действие гепарина, расширяет кровеносные сосуды.
Значительная часть биологических эффектов простагландинов связана с взаимодействием со специфическими рецепторами. Например, активация рецептора ЕР1 (связан с Gq-белками) приводит к бронхоспазму и сокращению гладких мышц желудочно-кишечного тракта, а взаимодействие PGЕ с рецептора ЕР2 (связан с Gs-белками) наоборот вызывает расширение бронхов и расслабление гладкой мускулатуры.
Простагландины также выступают в качестве медиаторов воспаления и аллергических реакций (например, бронхиальной астмы), влияют на ряд протекающих в организме негативных процессов, в том числе, метастазирование.
В качестве лекарственных средств простагландины используют для возбуждения и стимуляции родовой деятельности. Первоначально в медицинской практике использовали простагландины, получаемые на основе метилового эфира ацетил-PGА2, извлекаемого из некоторых видов кораллов. В настоящее время, несмотря на многостадийность и сложность, простагландины получают синтетическим путем.
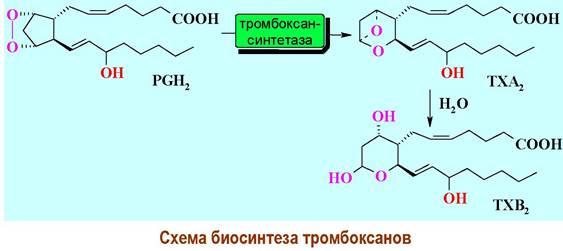
❖ Тромбоксаны - липидные биорегуляторы, близкие по структуре и происхождению к простагландинам, образующиеся в тромбоцитах. В отличие от простагландинов содержат в своей структуре тетрагидропирановый цикл. Различают две группы тромбоксанов ТХА и ТХВ.
Биосинтетическим предшественником тромбоксанов является PGН2, который под действием тромбоксансинтетазы дает ТХА2, а тот в свою очередь способен гидролизоваться до ТХВ2.
Тромбоксаны по своим свойствам во многом противоположны простагландинам. В отличие от PGI2 ТХА2 сокращает кровеносные сосуды и вызывает сильную агрегацию тромбоцитов. Все это может привести к образованию тромбов и атеросклерозу сосудов.
Кроверазжижающее действие аспирина связано с подавлением синтеза тромбоксанов (см. ниже). Тромбоциты, являющиеся безъядерными клетками, неспособны синтезировать новые молекулы этого фермента, поэтому образование тромбоксана подавляется резко и на весь срок жизни этих клеток.
❖ Лейкотриены. Название этой группы соединений связано с лейкоцитами, где они были вначале обнаружены, и наличием системы трех сопряженных двойных связей.
Еще в первой половине ХХ в. в легких было выявлено вещество, проявляющее бронхоконстрикторное действие. Этот вариант бронхоспазма отличался от вызванного гистамином более медленным развитием и большей продолжительностью. Структура этих соединений была установлена в конце 1970-х годов под руководством Бенгта Самуэльсона.
В зависимости от строения лейкотриены подразделяются на несколько подгрупп, обозначаемых латинскими буквами. Цифровой индекс, как и в случае простагландинов, обозначает количество двойных связей. Лейкотриены ряда подгрупп содержат остатки аминокислоты цистеина (LTE) или цистеинсодержащих ди- (LTD и LTF) и трипептидов (LTC).
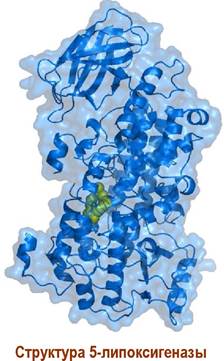
Биосинтетически лейкотриены происходят от арахидоновой кислоты, которая под действием 5-липоксигеназы превращается в малостабильный интермедиат LTA4. Дальнейшая биотрансформация приводит к LTB4. Альтернативно эпоксидный цикл в LTA4 раскрывается в результате присоединения трипептида глутатиона и образуется LTC4.
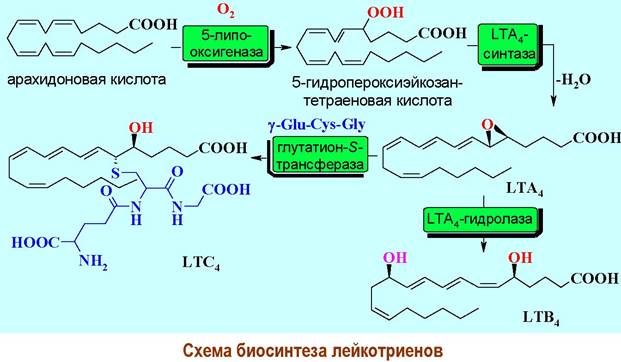
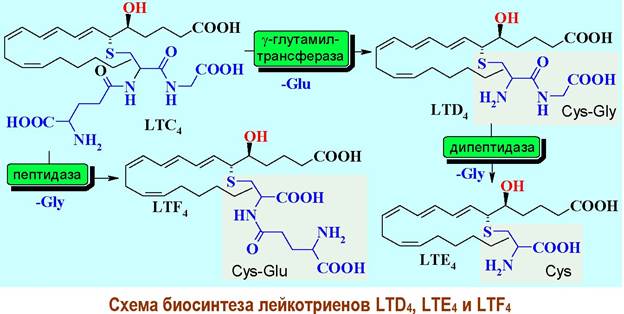
Лейкотриен LTC4 в свою очередь в результате отщепления глицина или глутаминовой кислоты дает LTD4 и LTF4, а при гидролизе с удалением дипептидного фрагмента образуется LTЕ4.
Наиболее широко распространены лейкотриены типов LTА и LTВ, найденные не только в клетках животных, но и в ряде растений, например, картофеле. Эти соединения не накапливаются в тканях, а синтезируются в ответ на определенные сигналы.
✵ Биологические эффекты. Лейкотриены играют существенную роль в развитии бронхиальной астмы. Они активируют воспалительные процессы и бронхоспазм. В частности, так называемый аспириновый бронхоспазм связан с блокированием аспирином продукции простагландинов за счет ингибирования циклооксигеназы (см. ниже), что может вызвать активацию 5- липоксигеназы и как следствие сужение бронхов в результате увеличения биосинтеза лейкотриенов.
С действием соединений этой группы биорегуляторов связывают и анафилактический эффект - быстрое и очень опасное для жизни развитие аллергической реакции.
Выявлены специфические рецепторы на лейкотриены, взаимодействием с которыми связан ряд их физиологических эффектов. Так содержащие аминокислоты лейкотриены LTC4 - LTF4 при действии на рецепторы CysLT1 вызывают бронхоспазм, а их связывание с рецепторами СуsLT1 изменяет тонус и проницаемость кровеносных сосудов. Активация лейкотриенами LTВ4 индуцирует хемотаксис и иммунные реакции.
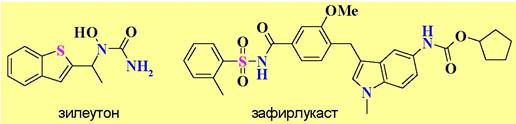
С целью лечения бронхиальной астмы были разработаны лекарственные средства, блокирующие синтез лейкотриенов путем ингибирования или фермента 5-липоксигеназы (зилеутон), или лейкотриеновых рецепторов (зафир- лукаст).
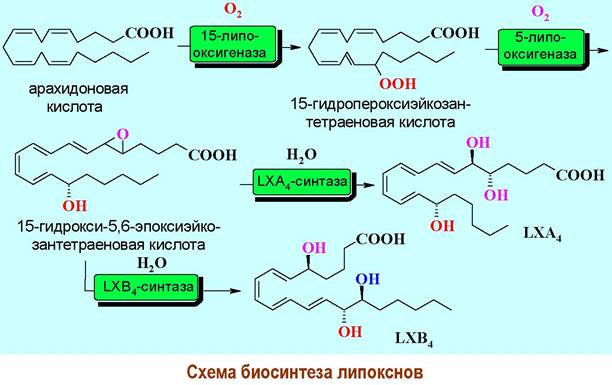
❖ Липоксины. Наряду с лейкотриенами в лейкоцитах обнаружены (1984 г., Бенгт Самуэльсон) другие биорегуляторные метаболиты арахидоновой кислоты - липоксины (LХА и LХВ), имеющие в своей структуре четыре сопряженные двойные связи и три гидроксильные группы.
Ключевыми стадиями их биосинтеза является последовательное окисление арахидоновой кислоты 15-липоксигеназой и 5-липоксигеназой.
Выявлено, что взаимодействие LХА4 с рецепторами LХА4R приводит к ингибированию хемотаксиса (направленное движение) лейкоцитов. С другой стороны, эти липоксины способны блокировать лейкотриеновые рецепторы CysLT1 и тем самым препятствуют развитию бронхоспазма и процесса воспаления.
❖ Нестероидные противовоспалительные препараты. В эту группу лекарственных средств включают ряд веществ, проявляющих наряду с противовоспалительной активностью также анальгетическое, жаропонижающее действие и ряд других физиологических эффектов. Механизмы действия этих препаратов сложны и многокомпонентны. Однако значительный вклад в их комплексное лечебное воздействие НСПВП вносит ингибирование продукции простагландинов и тромбоксанов, в первую очередь путем блокирования действия циклооксигеназы - фермента, катализирующего первый этап их биосинтеза. Впервые блокирование циклооксигеназы аспирином было показано британским профессором Джоном Вейном (Нобелевская премия по физиологии и медицине 1982 г.).


✵ Аспирин. В народной медицине давно известно противовоспалительное действие коры ивы белой (Salix alba).

В 30-х годах XIX в. несколько групп ученых выделили из коры ивы гликозид салицин. В 1838 г. итальянский химик Раффаэле Пириа окислением салицина получил салициловую кислоту. В 80-х годах этого же века была установлена высокая противовоспалительная активность этого соединения.
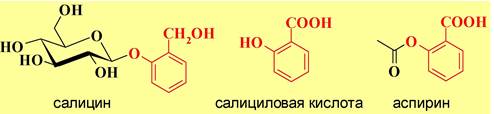
Впервые ацетилсалициловая кислота была синтезирована в 1853 г. французским химиком Шарлем Жераром, но эта работа не получила дальнейшего развития. В 1897 г. немецкий химик Феликс Хоффманн, работавший в фирме «Байер», предложил способ практического синтеза ацетилсалициловой кислоты, которая в меньшей степени раздражала стенки желудка, и внедрил ее в медицинскую практику под названием «аспирин».

Ацетилсалициловая кислота - лекарственный препарат широкого диапазона действия. Она проявляет противовоспалительную, анальгетическую, жаропонижающую активность. Эти эффекты связаны со способностью аспирина комплексно воздействовать на очаг воспаления - уменьшается проницаемость капилляров, тормозится биосинтез медиаторов воспаления (брадикинина, гистамина, простагландинов), ингибируется синтез АТР и тем самым уменьшается энергетическое обеспечение биохимических реакций.
В последние десятилетия аспирин широко используется как антиагрегационное средство, препятствующее образованию тромбов у больных инфарктом миокарда и других сердечно-сосудистых заболеваний, что также связано с ингибированием биосинтеза тромбоксана ТХА2.
Для предотвращения негативного воздействия ацетилсалициловой кислоты на желудок необходимо применять этот препарат после еды в измельченном виде, запивая большим количеством жидкости. В медицинской практике широко используются специальные лекарственные формы аспирина, уменьшающие раздражающее действие на слизистую оболочку желудка, - покрытые нерастворимой в желудке оболочкой таблетки, «шипучие» композиции, обычно содержащие гидрокарбонат натрия и лимонную кислоту, обеспечивающие хорошую растворимость в воде.
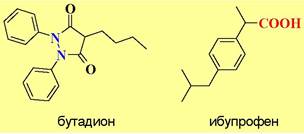
✵ Другие нестероидные противовоспалительные препараты. Бутадион - препарат анальгетического, жаропонижающего и противовоспалительного действия. Как ингибитор биосинтеза простагландинов превосходит аспирин. С 1949 г. использовался при лечении ревматизма и полиартритов.
Аналогичным лечебным действием обладает ибупрофен. Этот препарат был получен в 1961 г. британским химиком С. Адамсом. В настоящее время это один из самых распространенных антипиретиков. Также имеются данные, что он стимулирует выработку интерферона.

Еще более активны ортофен (диклофенак натрия) и индометацин. Все эти препараты неспецифически ингибируют изомерные формы фермента циклооксигеназы, катализирующего образование всего пула простагландинов, как медиаторов воспалительных реакций, так и PGЕ1, который тормозит выделение желудочного сока. Поэтому эти лекарственные средства раздражающе действуют на слизистую желудка.
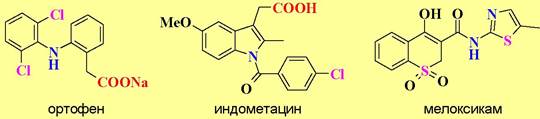
✵ Избирательные ингибиторы циклооксигеназы-2. Описанного выше недостатка в существенной степени лишен препарат мелоксикам, который избирательно блокирует только циклооксигеназу-2, обеспечивающую синтез простагландиновых медиаторов воспаления.