Биотехнология - Ю.О. Сазыкин 2006
Общая биотехнология
Биобъекты: способы их создания и совершенствования
Совершенствование биообъектов методами мутагенеза и селекции
Как правило, работающий с биообъектом биотехнолог крайне заинтересован в его совершенствовании независимо от того, на какой ступени «лестницы живых существ» находится этот биообъект. Если организм, выделенный из природной среды («дичок») не будет подвергнут совершенствованию, то производственный процесс образования целевого продукта или экономически нецелесообразен, или технически трудно осуществим. Наиболее четко эта тенденция прослеживается в случае биообъектов, принадлежащих к микроорганизмам. Изменение биообъекта, благоприятное для его использования в производстве, должно передаваться по наследству и, соответственно, вызываться мутацией. На биохимическом уровне мутация — изменение первичной структуры ДНК в конкретном ее участке, что, в конечном счете, приводит к изменению фенотипа биообъекта. Меняется биосинтетическая способность биообъекта: изменяется либо набор его ферментов, либо активность некоторых из них.
Подчеркнем, что мутации — это первоисточник изменчивости организмов, создающий основу для эволюции. Однако во второй половине XIX в. для микроорганизмов был открыт еще один источник изменчивости — перенос чужеродных генов — своего рода «генная инженерия природы».
Долгое время понятие мутации относили только к хромосомам у прокариот и хромосомам (ядру) У эукариот. В настоящее время кроме хромосомных мутаций появилось также понятие мутаций цитоплазматических (плазмидных — у прокариот, митохондриальных и плазмидных — у эукариот).
Мутации могут быть обусловлены как перестройкой репликона (изменением в нем числа и порядка расположения генов), так и изменениями внутри индивидуального гена.
Применительно к любым биообъектам, но особенно часто в случае микроорганизмов, выявляются так называемые спонтанные мутации, обнаруживаемые в популяции клеток без специального воздействия на нее. По выраженности почти любого признака клетки в микробной популяции составляют вариационный ряд. Большинство клеток имеют среднюю выраженность признака. Отклонения «+» и «-» от среднего значения встречаются в популяции тем реже, чем больше величина отклонения в любую сторону (рис. 1). Первоначальный, самый простой подход к совершенствованию биообъекта заключался в отборе отклонений «+» (предполагая, что именно эти отклонения соответствуют интересам производства). В новом клоне (генетически однородное потомство одной клетки; на твердой среде — колония), полученном из клетки с отклонением «+» вновь проводился отбор по тому же принципу. Однако такая процедура при ее неоднократном повторении довольно быстро теряет эффективность, т. е. отклонения «+» становятся в новых клонах все меньше и меньше по величине.
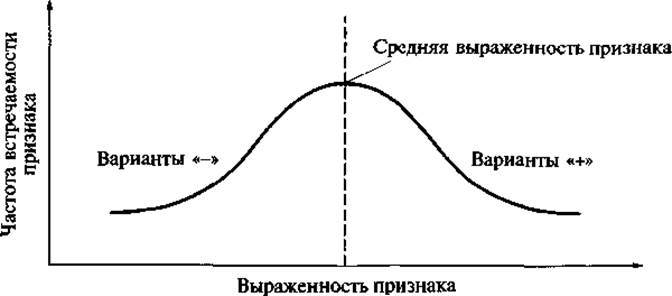
Рис. 1. Вариационный ряд
Спонтанные мутации встречаются, как правило, довольно редко. Разброс по степени выраженности признаков обычно невелик.
Совершенствование биообъектов путем предварительного мутагенеза и последующей селекции оказалось гораздо более действенным. В этом случае разброс мутантов по выраженности признаков (как «+», так и «-») резко увеличивается. Среди них оказываются мутанты с пониженной способностью к реверсии, т.е. со стабильно измененным признаком. Мутагенез осуществляется при обработке биообъекта физическими или химическими мутагенами. В первом случае, как правило, это ультрафиолетовые, гамма-, рентгеновские лучи; во втором — нитрозометилмочевина, нитрозогуанидин, акридиновые красители, некоторые природные вещества (например, из ДНК-тропных антибиотиков вследствие их токсичности не применяемых в клинике инфекционных заболеваний). Механизм активности как физических, так и химических мутагенов связан с их непосредственным действием на ДНК (прежде всего на азотистые основания ДНК, что выражается в сшивках, димеризации, алкилировании последних, интеркаляции между ними).
Подразумевается, естественно, что повреждения не приводят к летальному исходу. Таким образом, после обработки биообъекта мутагенами (физическими или химическими) их воздействие на ДНК приводит к частому наследственному изменению уже на уровне фенотипа (тех или иных его свойств). Последующей задачей является отбор и оценка именно нужных биотехнологу мутаций. Для их выявления обработанную культуру высеивают на твердые питательные среды разных составов, предварительно разведя ее с таким расчетом, чтобы на твердой среде не было сплошного роста, а формировались отдельные колонии, образуемые при размножении именно отдельных клеток. Затем каждую колонию пересеивают и полученную культуру (клон) проверяют по тем или иным признакам в сравнении с исходной. Эта селекционная часть работы в целом весьма трудоемка, хотя приемы, позволяющие повысить ее эффективность, постоянно совершенствуются.
Так, изменяя состав твердых питательных сред, на которых вырастают колонии, можно сразу получить первоначальные сведения о свойствах клеток этой колонии в сравнении с клетками исходной культуры. Для высеивания клонов с разными особенностями метаболизма используют так называемый «метод отпечатков», разработанный Дж. Ледербергом и Э. Ледерберг. Популяцию микробных клеток разводят так, чтобы на чашке Петри с питательной средой вырастало около ста колоний и они были бы четко разделены. На металлический цилиндр диаметром, близким к диаметру чашки Петри, надевают бархат; затем все стерилизуют, создавая, таким образом, «стерильное бархатное дно» цилиндра. Далее прикладывают это дно к поверхности среды в чашке с выросшими на ней колониями. При этом колонии как бы «отпечатываются» на бархате. Затем этот бархат прикладывают к поверхности сред разного состава. Таким образом можно установить: какая из колоний в исходной чашке (на бархате расположение колоний отражает их расположение на поверхности твердой среды в исходной чашке) соответствует, например, мутанту, нуждающемуся в конкретном витамине, или конкретной аминокислоте; или какая колония состоит из мутантных клеток, способных к образованию фермента, окисляющего определенный субстрат; или какая колония состоит из клеток, получивших резистентность к тому или иному антибиотику и т.п.
В первую очередь биотехнолога интересуют мутантные культуры, обладающие повышенной способностью к образованию целевого продукта. Продуцент целевого вещества, наиболее перспективный в практическом отношении, может многократно обрабатываться разными мутагенами. Новые мутантные штаммы, получаемые в научных лабораториях разных стран мира, служат предметом обмена при творческом сотрудничестве, лицензионной продажи и т. п.
Потенциальные возможности мутагенеза (с последующей селекцией) обусловлены зависимостью биосинтеза целевого продукта от многих метаболических процессов в организме продуцента. Например, повышенную активность организма, образующего целевой продукт, можно ожидать, если мутация привела к дупликации (удвоению) или амплификации (умножению) структурных генов, включенных в систему синтеза целевого продукта. Далее активность можно повысить, если за счет разных типов мутаций будут подавлены функции репрессорных генов, регулирующих синтез целевого продукта. Весьма эффективный путь увеличения образования целевого продукта — нарушение системы ретроингибирования. Повысить активность продуцента можно также, изменив (за счет мутаций) систему транспорта предшественников целевого продукта в клетку. Наконец, иногда целевой продукт при резком увеличении его образования отрицательно влияет на жизнеспособность собственного продуцента (так называемый суицидный эффект). Повышение резистентности продуцента к образуемому им же веществу часто необходимо для получения, например, суперпродуцентов антибиотиков.
Помимо дупликации и амплификации структурных генов мутации могут носить характер делеции — «стирания», т.е. «выпадения» части генетического материала. Мутации могут быть обусловлены транспозицией (вставкой участка хромосомы в новое место) или инверсией (изменением порядка расположения генов в хромосоме). При этом геном мутантного организма претерпевает изменения, ведущие в одних случаях к потере мутантом определенного признака, а в других — к возникновению у него нового признака. Гены на новых местах оказываются под контролем иных регуляторных систем. Кроме того, в клетках мутанта могут появиться несвойственные исходному организму гибридные белки за счет того, что под контролем одного промотора оказываются полинуклеотидные цепи двух (или более) структурных генов, ранее отдаленных один от другого.
Немалое значение для биотехнологического производства могут иметь и так называемые «точечные» мутации. В этом случае изменения происходят в пределах только одного гена. Например, выпадение или вставка одного или нескольких оснований. К «точечным» мутациям относятся трансверсия (когда происходит замена пурина на пиримидин) и транзиция (замена одного пурина на другой пурин или одного пиримидина на другой пиримидин). Замены в одной паре нуклеотидов (минимальные замены) при передаче генетического кода на стадии трансляции ведут к появлению в кодируемом белке вместо одной аминокислоты другой. Это может резко изменить конформацию данного белка и, соответственно, его функциональную активность, особенно в случае замены аминокислотного остатка в активном или аллостерическом центре.
Одним из самых блестящих примеров эффективности мутагенеза с последующей селекцией по признаку увеличения образования целевого продукта является история создания современных суперпродуцентов пенициллина. Работа с исходными биообъектами — штаммами (штамм — клоновая культура, однородность которой по определенным признакам поддерживается отбором) гриба Penicillium chrysogenum, выделенными из природных источников, велась с 1940-х гг. в течение нескольких десятилетий во многих лабораториях. Вначале некоторый успех был достигнут при отборе мутантов, появившихся в результате спонтанных мутаций. Затем перешли к индуцированию мутаций физическими и химическими мутагенами. В результате ряда удачных мутаций и ступенчатого отбора все более продуктивных мутантов активность штаммов Penicillium chrysogenum, используемых в промышленности стран, где производят пенициллин, сейчас в 100 тыс. раз выше, чем у обнаруженного А. Флемингом исходного штамма, с которого и началась история открытия пенициллина.
Производственные штаммы (применительно к биотехнологическому производству) с такой высокой продуктивностью (это относится не только к пенициллину, но и к другим целевым продуктам) крайне нестабильны вследствие того, что многочисленные искусственные изменения в геноме клеток штамма сами по себе для жизнеспособности этих клеток положительного значения не имеют. Поэтому мутантные штаммы требуют постоянного контроля при хранении: популяцию клеток высеивают на твердую среду и полученные из отдельных колоний культуры проверяют на продуктивность. При этом ревертанты — культуры с пониженной активностью отбрасывают. Реверсия объясняется обратными спонтанными мутациями, ведущими к возврашению участка генома (конкретного фрагмента ДНК) в его первоначальное состояние. Специальные ферментные системы репарации участвуют в реверсии к норме — в эволюционном механизме поддержания постоянства вида.
Совершенствование биообъектов применительно к производству не исчерпывается только повышением их продуктивности. Хотя это направление, несомненно, является главным, но оно не может быть единственным: успешная работа биотехнологического производства определяется многими факторами. С экономической точки зрения весьма важно получение мутантов, способных использовать более дешевые и менее дефицитные питательные среды. Если для работы в исследовательской лаборатории дорогие среды не создают особых финансовых проблем, то при крупно-тоннажном производстве понижение их стоимости (хотя и без увеличения уровня активности продуцента) крайне важно.
Другой пример: в случае некоторых биообъектов культуральная жидкость после окончания ферментации имеет неблагоприятные в технологическом отношении реологические свойства. Поэтому в цехе выделения и очистки целевого продукта, работая с культуральной жидкостью повышенной вязкости, сталкиваются с трудностями при использовании сепараторов, фильтр-прессов и т.д. Мутации, соответствующим образом меняющие метаболизм биообъекта, в значительной мере снимают эти трудности.
Большое значение в отношении гарантии надежности производства приобретает получение фагоустойчивых биообъектов. Соблюдение асептических условий при проведении ферментации прежде всего касается предотвращения попадания в посевной материал (а также в ферментационный аппарат) клеток и спор посторонних бактерий и грибов (в более редких случаях водорослей и простейших). Предотвратить проникновение в ферментер фагов вместе с технологическим воздухом, стерилизуемым путем фильтрации, крайне трудно. Не случайно вирусы в первые годы после их открытия именовали «фильтрующимися». Поэтому основной путь борьбы с бактериофагами, актинофагами и фагами, поражающими грибы, — получение устойчивых к ним мутантных форм биообъектов.
Не касаясь специальных случаев работы с биообъектами-патогенами, следует подчеркнуть, что иногда задача совершенствования биообъектов исходит из требований промышленной гигиены. Например, выделенный из природного источника продуцент одного из важных беталактамных антибиотиков в значительном количестве образовывал летучие вещества с неприятным запахом гниющих овощей.
Мутации, ведущие к удалению генов, кодирующих ферменты, участвующие в синтезе этих летучих веществ, приобрели в данном случае практическое значение для производства.
Из всего изложенного следует, что современный биообъект, используемый в биотехнологической промышленности, — это суперпродуцент, отличающийся от исходного природного штамма не по одному, а, как правило, по нескольким показателям. Хранение таких штаммов-суперпродуцентов представляет серьезную самостоятельную проблему. При всех способах хранения их необходимо периодически пересеивать и проверять как на продуктивность, так и на другие важные для производства свойства.
В случае применения высших растений и животных в качестве биообъектов для получения лекарственных средств возможности использования мутагенеза и селекции для их совершенствования ограничены. Однако в принципе мутагенез и селекция здесь не исключены. Особенно это относится к растениям, образующим вторичные метаболиты, которые используются как лекарственные вещества.