Биотехнология - Ю.О. Сазыкин 2006
Частная биотехнология
Проблемы поиска, создания и применения антибиотиков в медицинской практике
Механизмы действия антибиотиков - Ингибиторы синтеза нуклеиновых кислот
К этой группе антибиотиков (антрациклины, блеомицин, оливомицин и др.) относится ряд ДНК-тропных противоопухолевых веществ. Они подавляют синтез РНК, а некоторые из них — синтез и ДНК, и РНК, поскольку связываются с ДНК (последняя играет роль матрицы как при репликации ДНК, так и при транскрипции, т.е. синтезе РНК).
Такие антибиотики всегда заметно токсичны, потому что связываются с ДНК любого происхождения — бактериального, вирусного, растительного, животного. Возможность их применения как цитостатиков в онкологической практике обусловлена тем, что клетки опухолей растут (размножаются) быстрее клеток нормальной ткани, и антибиотический эффект на опухоли выражается сильнее.
В инфекционной клинике ДНК-тропные препараты не принято употреблять ввиду их токсичности и наличия в распоряжении лечащего врача ряда более избирательно действующих антимикробных антибиотиков.
Ингибиторами синтеза нуклеиновых кислот могут быть не только ДНК-тропные антибиотики. Антибиотик рифампицин — ингибитор синтеза РНК, связывается не с ДНК-матрицей, а с ферментом — РНК-полимеразой, причем связывается избирательно: только с ферментом из бактерий, а не из животных клеток. Рифампицин применяется для лечения ряда инфекций, в том числе туберкулеза, так как может длительно вводиться человеку без проявления токсичности.
К числу ингибиторов ферментов, участвующих в синтезе и превращениях нуклеиновых кислот, относятся и новые синтетические антибактериальные вещества — фторхинолоны, внедряемые в настоящее время в лечебную практику.
Эти препараты обладают широким антибактериальным спектром действия. В качестве примера можно привести пефлоксацин (абактал):
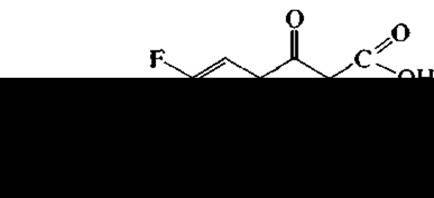
преимущественно влияющий на грамотрицательные бактерии и норфлоксацин (нолицин):
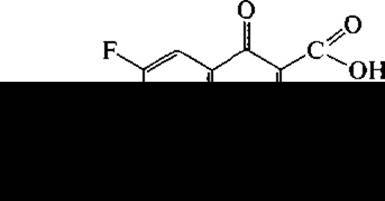
отличающийся от первого отсутствием метильной группы в пиперазинильном ядре и более высокой антибактериальной активностью.
Отметим, что есть данные о влиянии фторхинолонов на развитие хрящевой ткани (в связи с этим применение фторхинолонов в детской клинике не рекомендуется). Они не являются продуктами биотехнологического производства. Вместе с тем, учитывая их практическую важность, а также возможность получения ковалентно связанных цефалоспоринов с фторхинолонами, целесообразно кратко рассмотреть механизм их действия.
Фторхинолоны являются ингибиторами фермента ДНК-гиразы. Функция этого фермента — введение в кольцевую ДНК «супервитков» или «скручивание» ее молекулы. Молекула ДНК становится более компактной, а также приобретает «внутреннее напряжение»: при разрезании ее рестриктазами комплементарные нити быстро расходятся, чем облегчается действие ДНК- и РНК- полимераз при репликации ДНК или транскрипции (синтезе РНК на ДНК-матрице). Фермент ДНК-гираза состоит из нескольких субъединиц и катализирует несколько реакций, в том числе требующих энергии при введении в ДНК супервитков. Фторхинолоны подавляют функции так называемой субъединицы А. Бактериальная ДНК-гираза относится по классификации ферментов к ДНК-топоизомеразам. В реакции с ДНК-топоизомеразами животной клетки фторхинолоны не вступают.