ЕКОЛОГІЧНА БІОХІМІЯ - Навчальний посібник - В. М. Ісаєнко 2005
Розділ. 11 ЕКОЛОГІЧНА БІОХІМІЯ І БІОТЕХНОЛОГІЯ
11.4.Хімічна біотехнологія
Виробництво хімічних речовин з відновлюваної біомаси — один з істотних напрямів біотехнології. Серед багатьох методів, які використовуються в хімічній біотехнології, є бродіння. До важливих бродильних процесів належать виробництво етанолу — розчинника, харчового продукту, проміжної речовини в реакціях хімічного синтезу, палива тощо.
Етанол — екологічно чисте паливо, яке утворює під час згорання лише СО2 і Н2O з високою теплотою згорання (1370 кДж/моль). Отримання етанолу методом бродіння почалося в глибокій давнині (виготовлення пива). Спиртове бродіння здійснюється дріжджами родів Saccharomyces, Schizosaccharomyces, Candida, Kluyveromyces, мезофільними (Zymomonas mobilis, Sarcina ventriculii, Erwimia amy- lovora) і термофільними (Thermoanaerobaster brockii, Thermoanaerobісum ethanolicus, Clostridium thermocellum та ін.) бактеріями, за деяких умов — рослинними і грибними (Trichoderma sp., Aspergillus oryzae) клітинами.
Спиртове бродіння відповідає рівнянню:
![]()
За декарбоксилювання пірувату утворюється ацетальдегід:
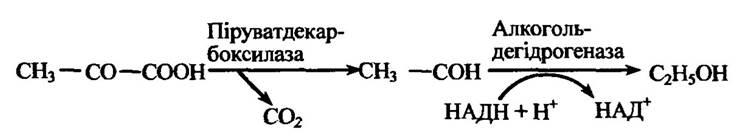
Ацетальдегід може бути зв’язаний біосульфатом:
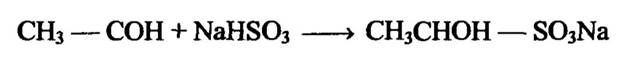
При цьому НАДН може відновлювати проміжний продукт гліколізу — діоксиацетонфосфат, який перетворюється в гліцерол, цінну речовину для хімічної та харчової промисловості:
![]()
Отже, гліцерол стає продуктом бродіння тоді, коли стимулюється перетворення ацетальдегіду в етанол і ацетат.
Гліцерол може утворюватися з діоксиацетонфосфату також на початковій стадії бродіння, поки в клітинах не відбулося нагромадження ацетальдегіду, який є основним викорисговувачем НАДН за його перетворення в етанол.
У процесі спиртового бродіння утворюються другорядні продукти — сивушні масла — суміш одноатомних спиртів жирного ряду (ізобутанол, пантанол, ізопетанол та інші спирти). Під час перетворення продуктів метаболізму вуглеводів теж можуть утворюватися другорядні продукти, зоїфема ізобутанол — за взаємодії пірувату з ацетальдегідом. Крім сивушних масел другорядними продуктами також є відновлені сполуки сульфуру (H2S, метил- і етилмеркаптани, сульфіди та ін.).
Клостридії (Clostridium thermollum та ін.), ентеробактерії (Enterobacter aerogenes та ін.) та молочнокислі бактерії (Leuconostoc mesenteroides та ін.) не містять піруватдекарбоксилазу, але вони здатні утворювати етанол. Клостридії та ентеробактерії відновлюють ацетил-КоА, а молочнокислі бактерії — ацетилсульфат:
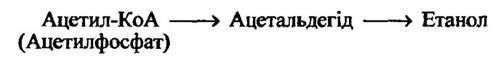
Сировина для виготовлення етанолу має містити шести- або п’ятикарбонові цукри у вигляді мономерів, які гідролізуються ферментами самих продуцентів або доданими хімічними агентами. Такі джерела сировини, як цукровий буряк, цукрова тростина, фрукти, містять моноцукри та олігоцукри, здатні утилізуватися мікроорганізмами.
Інша група сировини містить крохмаль (кукурудза, сорго, картопля та ін.) або інулін (топінамбур, батат). Целюлозовмісні продукти (деревина, відходи рослин — кукурудзяний качан, картопляне, бурякове або інше бадилля, стебла бавовнику, макуха тощо) теж є сировиною для отримання етанолу.
Традиційними виробниками етанолу є дріжджі Sacchoromyces (S.arevisiae, S.uvarum). Вони містять ферменти, необхідні для утворення етанолу з глюкози, манози, фруктози, сахарози. Клітини S.diastaticus перетворюють декстрин. Субстрати, які не характерні для Sacchoromyces, можуть підлягати бродінню іншими дріжджами, зокрема Schizosacchoromyces, Hansenula, Kluyveromyces, Candida. Бактерії мають певні переваги (швидкий ріст і використання субстрату, здатність до росту на концентрованих вуглеводами середовищах тощо) порівняно з дріжджами — продуцентами етанолу. Промислове значення мають бактерії Zymomonas mobilis, ряд термофільних бактерій (Thermoanaerobium brockii, Clostridium thermocellum, Bacillus stearothermophilus та ін.).
Ацетон і бутанол — продукти бродіння, характерні для бактерій роду Clostridium (C.beijerinckii, C.aurantibutylicum, C.acetobutylicum та ін.), що утворюють також ізопропанол. Ці речовини — ефективне біопаливо, особливо бутанол, який за фізико-хімічними властивостями значно ближчий до бензину, ніж етанол. Ацетон і бутанол використовують у хімічній промисловості як розчинники та сировину для отримання ряду сполук. Ацетон також традиційно застосовують для виробництва вибухівки.
Сировиною для отримання ацетону та бутанолу є, як правило, кукурудзяне борошно, картопля, рис, кінські каштани, меляса, молочна сироватка, гідролізати деревини і т. ін.
Однією з проблем молочної промисловості є утилізація сироватки. Водночас вона може бути джерелом отримання бутиленгліколю бактеріями Klebsiella pneumoniae та Enterobacter aerogenes, який потім перетворюється в сировину для виготовлення штучного каучуку.
Процеси, що ґрунтуються на мікробіологічній ферментації, розроблені для отримання ряду органічних кислот. Харчову оцтову кислоту отримують мікробіологічним окисненням етанолу. Проте цей процес з економічних міркувань малопридатний для виробництва оцтової кислоти у промислових масштабах. У цьому разі використовують здатність бактерій родин Acetobacter і Clostridium синтезувати оцтову кислоту з гідрогену та вуглекислого газу. Застосовують також термофільні бактерії, здатні перетворювати целюлозу в оцтову кислоту.
Молочну кислоту здатні утворювати молочнокислі бактерії роду Lactobacillus (L.delbrueckii, L.leichmannii, L.bulgaricus).
Для промислового виробництва цитринової кислоти в основному використовують гриби Aspergillus niger і Aspergillus wentii, глюко- нової кислоти з глюкози — Aspergillus niger, виннокам’яної кислоти — мутанти Acetobacter і Gluconobacter. Яблучну кислоту можна отримати з фумарової ферментацією за участю видів Paracolobactrum. Ітаконову кислоту отримують ферментацією глюкози за участю грибів роду Aspergillus, а саліцилову — багатьох видів бактерій Achromobacter, Corynebacterium.
Наведені приклади виробництва органічних кислот біотехнологічними методами далеко не вичерпують усі способи їх утворення.
Широко застосовують мікробіологічний ферментативний синтез також для отримання амінокислот. Так, виробництво таких амінокислот, як L-глутамат, L-валін, L-аланін, L-глутамін і L-пролін можна провести за участю багатьох родів бактерій, наприклад, Corynebacterium, Brevibactrium, Bacillus, Aerobacter, Microbacter, Esherichia та ін. Ауксотрофні мутанти можуть використовуватися тоді, коли необхідно синтезувати сполуки, які є кінцевими продуктами розгалужених ланцюгів метаболічних процесів. Так, L-аспартат є загальним попередником для L-лізину, L-треоніну, L-метіоніну і L-ізолейцину.
Для синтезу амінокислот застосовують також як чисті, так і не- очищені ферменти (безклітинні екстракти). Останні добуваються під час оброблення клітин поверхнево активними речовинами, що викликають порушення проникності клітинних мембран. Так, наприклад, утворення L-аспартату з фумарату амонію може відбуватися за
участю аспартази або L-аспартат-аміак-ліази. Фермент L-тирозин- фенол-ліазу використовують для синтезу L-тирозину, L-триптофаніндол-ліазу — L-триптофану. Застосовуючи безклітинний екстракт пекарських дріжджів і глутамінсинтетазу Gluconobacter subxydas з глюкози, глутамату та іонів амонію, як субстратів, отримують глутамін.
Рослини є найпоширенішим джерелом хімічних сполук для цілого ряду галузей промисловості, фармакології тощо. Нині інтенсивно розвивається отримання культури рослинних тканин. Її можна одержати з будь-якого виду рослин. Культуру рослинних тканин використовують не тільки як джерело необхідних хімічних сполук, а також і для проведення біотрансформації. Так, наприклад, може відбуватись утворення стимулятора роботи серця дигоксину гідро- ксилюванням дигитоксину в суспензійних культурах або {мобілізованих клітинах наперстянки Digitalis lanata.
Методи культури рослинних клітин широко застосовують для поліпшення сортів сільськогосподарських культур.
У біотехнологічних процесах можуть утворюватися не тільки органічні, а й неорганічні сполуки. Таким прикладом є утворення гідрогену.
Отримання гідрогену як палива є одним із перспективних напрямів енергетики. Ця сполука є екологічно чистим паливом, яка, згораючи в повітрі, утворює Н2О і незначну кількість окисів нітрогену. За енергоємністю (теплота згорання — 143 кДж/г) Н2 у 2,5 раза переважає природний газ і в 3 рази — бензин. Гідроген може бути використаним для синтезу інших видів газоподібного палива, зокрема метану. Найрізноманітніше використання гідрогену в хімічній промисловості — рафінірування нафти, отримання аміаку й метанолу, відновлення солей металів тощо.
Утворення Н2 мікроорганізмами відбувається за участю ферментів. Цей процес може бути спряженим з бродінням, функціонуванням фотосинтетичних або дихальних електрон-транспортних ланцюгів. Світлозалежне виділення Н2 характерне для пурпурних і зелених бактерій, ціанобактерій, зелених водоростей. Ця сполука продукується в процесі різних варіантів бродіння або дихання багатьма анаеробами (Clostridium, Desulfovibri, Alcaligenes, Pseudomonas та ін.), а також аеробними бактеріями (Azospirillum, Azotobacter, Rhizo- bium та ін.). Деякі фототрофні мікроорганізми здатні утворювати Н2 не тільки на світлі, а й у темряві за рахунок процесів бродіння.
За участю мікроорганізмів відбувається також утворення біогазу, який використовується як паливо. Він крім метану (СН4) містить до 15 — 50% СО2 (за об’ємом), невеликі кількості інших газів (N2, Н2, C2Ht, С3Н8, H2S) і водяну пару.
Змішана популяція мікроорганізмів із різних видів (метаногенна асоціація) використовує широке коло органічних субстратів для виробництва біогазу — полі- і моноцукри, білки, амінокислоти, органічні кислоти, спирти, ароматичні сполуки (катехол, бензойну кислоту, фенілоцгову кислоту) та інші речовини. Сировиною для отримання біогазу є промислові, сільськогосподарські та побутові відходи.
Утворення біогазу (метаногенез) складається з кількох етапів. На першій стадії в анаеробних умовах відбувається гідроліз біополімерів різними мікроорганізмами: целюлози — представниками Clostridium, Ruminococcus, Butyrovibrio, Bacteroides, Cellobacterium та ін., крохмалю — Bacteroides, Succinomonas, Selenomonas тощо, пектину — Bacteroides, Butyrovibrio, Lachnospira, Clostridium та ін., білків — Bacteroides, Clostridium, Peptococcus, Selenomonas, Megasphaera тощо. Ці мікроорганізми виконують не тільки гідроліз субстратів, а й наступні підготовчі етапи метаногенезу.
У подальшому відбуваються ацидо- і сольвентогенез — перетворення продуктів гідролізу в суміш летких жирних кислот (бутират, пропіонат, лактат, ацетат, форміат та ін.) і нейтральних розчинників (метанол, етанол, пропанол, бутанол, ацетон та ін.) з виділенням Н2, СОз, NH3, H2S. Ці процеси становлять собою поєднання різних видів бродіння — спиртового, маслянокислого, ацетонобутилового, пропіонового та ін.
Наступний етап — утворення ацетату з продуктів ацидо- та сольвентогенезу. Так, наприклад, перетворення бутирату в ацетат відбувається за участю бактерії Syntromonas wolfii. До ацетогенної мікрофлори належить також Clostridium thermoaceticum.
Ацетогенна стадія тісно взаємодіє з метаногенною — перетворення в СН4 і СО2 ацетату, форміату, метанолу, метиламінів, СО, суміші СО2 і Н2 тощо. Нині відомо приблизно 50 видів метаногенних бактерій 13 родин. Одні із них (Methanobrevibacter, Methano- thermus) використовують тільки суміш СO2 і Н2 і деколи форміат, інші — лише ацетат (Methanothrics), або обидва субстрати (Methanosarcina). У Methanolobus субстратом є метанол і метиламіни.
Зауважимо, що хімічна біотехнологія далеко не вичерпує тих питань, які розглянуто в цьому розділі. Крім цього, як правило, субстратами для процесів є відходи. Зважаючи на актуальність проблеми утилізації відходів, більшість процесів хімічної біотехнології варто розглядати як природоохоронну технологію.