Гликопротеины - Хьюз Р. 1985
Строение
Определение последовательности
Только в редких случаях к полипептидному остову глнкопротеина прикрепляется лишь одна определенная углеводная цепь. Обычно гликозилируется несколько аминокислотных остатков, и к каждому из таких гликозилированных остатков может присоединяться несколько очень сходных гликанов. С помощью протеолиза можно отделить эти гликаны, прикрепленные к связующим аминокислотам или небольшим пептидам. Затем полученные гликопептиды разделяют и определяют их моносахаридный состав, причем часто удается установить полную последовательность углеводов [7] сочетанием различных химических, ферментативных и физических методов (табл. 2.2).
Таблица 2.2. Этапы определения последовательности сахаров гликанов
|
1. |
Протеолиз: пролаза, трипсин, химотрипсин, коллагеназа и т. п. |
|
2. |
Разделение гликопептидов: гель-фильтрация, ионнообменная хроматография, электрофорез и хроматография на бумаге |
|
3. |
Состав: газово-жидкостная хроматография (моносахариды), ионообменная хроматография (аминокислоты) |
|
4. |
Определение последовательности сахаров: а) химически: метилирование, окисление йодной кислотой б) ферментативно: экзо- и эндогликозидазы в) физически: масс-спектрометрия, ядерный магнитный резонанс |
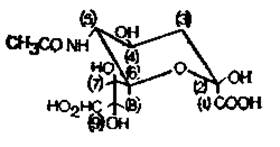
Рис. 2.3. Строение N-ацетилнейраминовой кислоти и других сиаловых кислот.
|
Название |
Место замещения |
Замещающая группа |
Типичный источник |
|
N-ацетилнейраминовая кислота |
С-5 |
CH3CONH— |
Обычный |
|
N-гликолилнейраминовая кислота |
С-5 |
HOCH3CONH— |
Ткани свиньи (>90%) |
|
О-ацетилпроизводные |
С-9 С-7 |
СН3СО— СР3СО— |
Подчелюстная железа быка (редко) |
|
С-4 |
СН3СО— |
Ткани лошади |
Идентификация таловых кислот, входящих в состав гликопротеинов, представляет собой особую проблему для анализа, поскольку основная кольцевая структура нейраминовой кислоты обнаруживается во многих вариантах, различающихся по положению замещающих групп. Наиболее часто встречающимся производным является N-ацетинейраминовая кислота (рис. 2.3); кроме того, известно еще около 20 других производных сиаловой кислоты. N-гликолилнейраминовая кислота, например, часто встречается в гликопротеинах или гликолипидах; известны также несколько О-ацильных производных этой и N-ацетилнейраминовой кислот. В образовании гликозидной связи принимает участие гидроксильная группа при С-2.