Основы биохимии Том 1 - А. Ленинджер 1985
Биомолекулы
Витамины и микроэлементы: их роль в функционировании ферментов
Фолиевая кислота служит предшественником кофермента тетрагидрофолиевой кислоты
Фолиевая кислота (от лат. «folium»-лист) впервые была выделена из листьев шпината. Она широко распространена в биологических системах. Молекула фолиевой кислоты состоит из трех основных компонентов; глутаминовой кислоты, n-аминобензоqной кислоты и гетероциклического конденсированного соединения птеридина (рис. 10-12). Недостаток фолиевой кислоты, известной также под названием птероилглутаминовой кислоты, приводит к развитию анемии. Сама по себе фолиевая кислота не обладает коферментной активностью; однако она ферментативно восстанавливается в тканях в тетрагидрофолиевую кислоту (FH4), которая и является активным коферментом. Тетрагидрофолат играет роль промежуточного переносчика одноуглеродных групп во многих сложных ферментативных реакциях. К таким группам, переносимым от одной (рис. 10-12). Характерный пример такой реакции приведен на рис. 10-13.
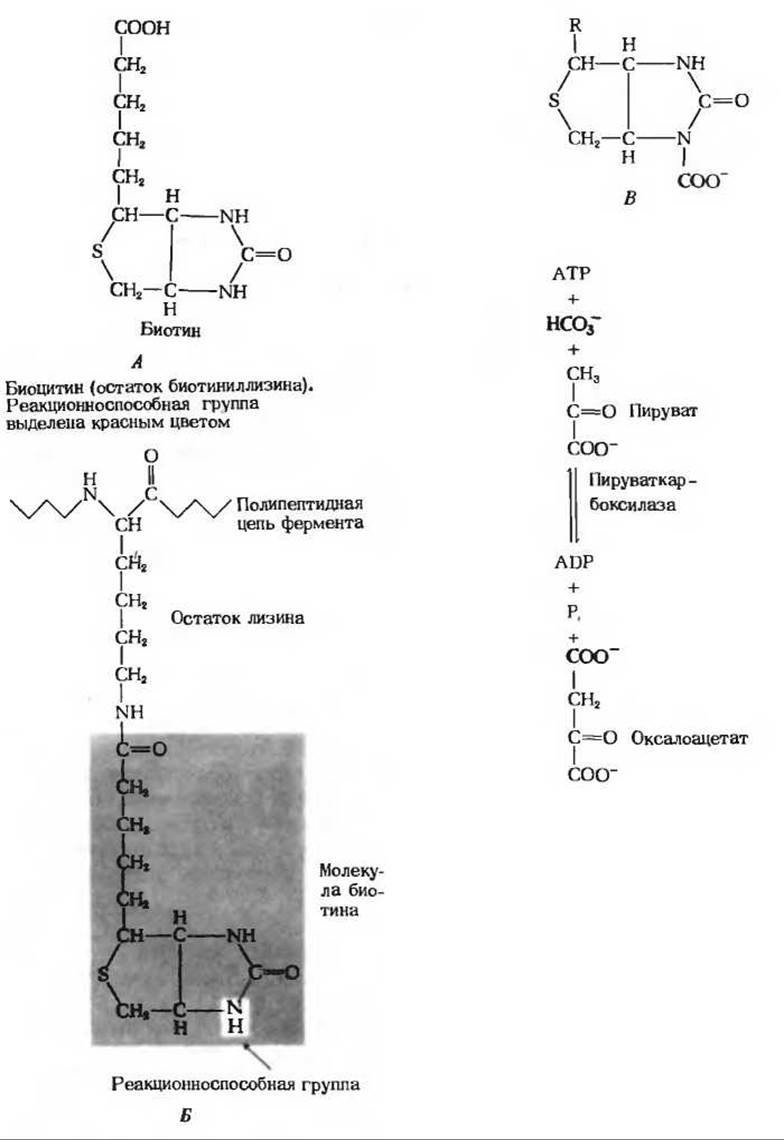
Рис. 10-11. Биотин (А) и его активная форма - биоцитин (Б), играющий роль простетической группы некоторых ферментов, катализирующих реакции карбоксилирования. В. В биотин-зависимых реакциях карбоксилирования в качестве промежуточного соединения образуется N-карбоксипроизводное биоцитина. Показана только циклическая система биоцитина. Г. Карбоксилирование пирувата с образованием оксалоацетата - важная стадия биосинтеза глюкозы из пирувата. Реакцию катализирует биотин-зависимый фермент пируваткарбоксилаза.
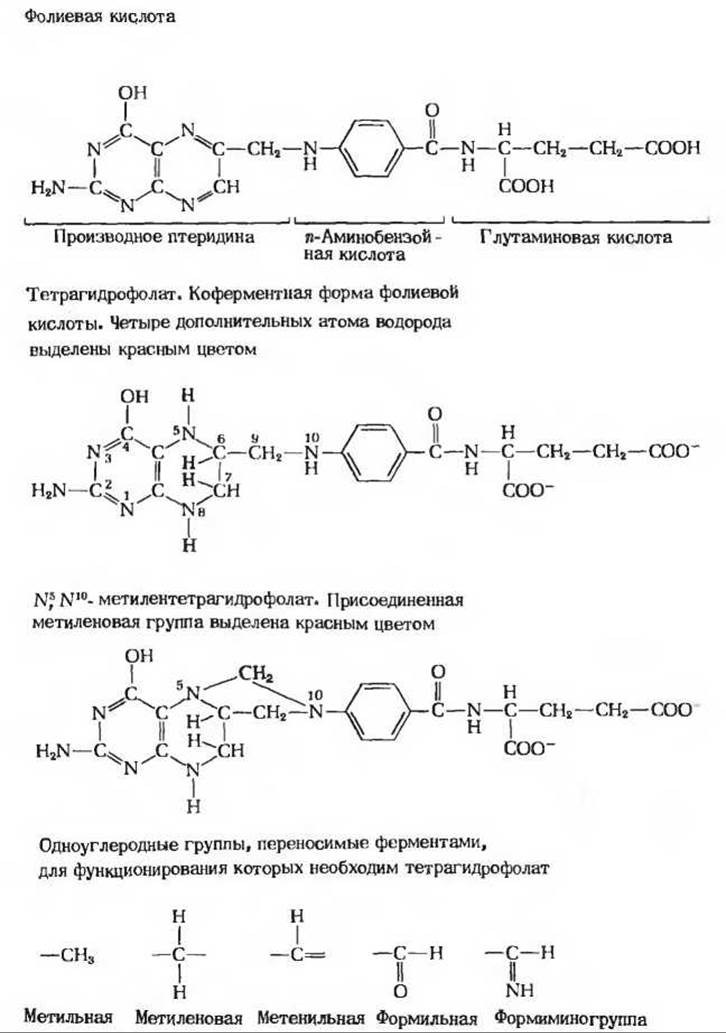
Рис. 10-12. Фолиевая кислота, ее коферментная форма тетрагидрофолат и метилентетрагидрофолат. Метиленовая группа одна из пяти различных одноуглеродных групп, которые могут переноситься посредством тетрагидрофолата. молекулы к другой, относятся метильная (—СН3), метиленовая (—СН2—), метенильная (—СН=), формильная (—CHO) и формиминогруппа (—CH=NH)
Восстановление фолиевой кислоты до ее активной формы - тетрагидрофолата - происходит в два этапа путем последовательного присоединения к молекуле двух пар водородных атомов. Второй этап - реакция, катализируемая дигидрофолатредуктазой,- эффективно ингибируется лекарственными препаратами, используемыми при терапии некоторых форм рака. Поскольку гидрофолат необходим при биосинтезе тимидиловой кислоты (одного из строительных блоков ДНК), эти лекарственные препараты ингибируют процесс репликации ДНК в быстро растущих раковых клетках.
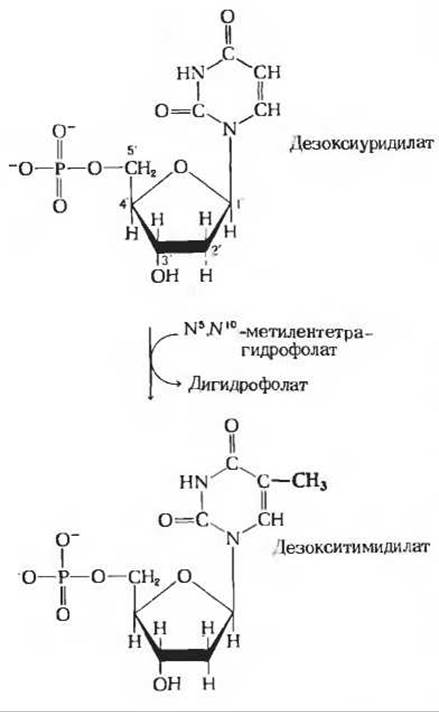
Рис. 10-13. Роль N5, N10-метилентетрагидрофолата (рис. 10-12) как донора метильной группы в ферментативном синтезе тимидиловой кислоты строительного блока ДНК. Вновь встроенная метальная группа выделена красным цветом.
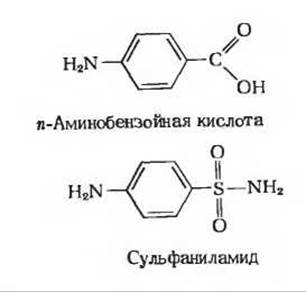
Рис. 10-14. Сходство в строении n-аминобензойной кислоты и сульфаниламида - конкурентного ингибитора ферментной системы, включающей n-аминобензоат в фолиевую кислоту.
Некоторые бактерии не нуждаются в экзогенной фолиевой кислоте как факторе роста, так как они сами могут ее синтезировать из n-аминобензойной кислоты - одного из компонентов фолиевой кислоты. Следовательно, n-аминобензойная кислота играет роль витамина для таких бактерий. Это открытие оказалось очень ценным, потому что оно позволило понять механизм действия сульфаниламида - важного лекарственного препарата, ингибирующего рост патогенных бактерий, нуждающихся в n-аминобензойной кислоте. На рис. 10-14 показано, что n-аминобензойная кислота и сульфаниламид очень сходны по своей структуре. Благодаря такому сходству сульфаниламид может конкурировать с n-аминобензоатом в процессе ферментативного синтеза фолиевой кислоты.