Основы биохимии Том 1 - А. Ленинджер 1985
Биомолекулы
Вода
Пептиды - это цепочки аминокислот
Две молекулы одной и той же или разных аминокислот могут ковалентно связываться друг с другом при помощи замещенной амидной связи (см. табл. 3-4), называемой пептидной связью, с образованием молекулы дипептида. Пептидная связь образуется путем отщепления компонентов молекулы воды от карбоксильной группы одной аминокислоты и a-аминогруппы другой аминокислоты под действием сильных конденсирующих агентов (рис. 5-18). Три аминокислоты могут соединиться аналогичным образом при помощи двух пептидных связей и образовать трипептид; точно так же можно получить тетрапептиды и пентапептиды. Если таким способом соединить большое число аминокислот, то возникает структура, называемая полипептидом. Пептиды различной длины образуются при частичном гидролизе очень длинных полипептидных цепей белков, которые могут содержать сотни аминокислотных звеньев.
На рис. 5-19 изображена структура пентапептида. Аминокислотные звенья, входящие в состав пептида, обычно называют остатками (они уже не являются аминокислотами, так как у них не хватает одного атома водорода в каждой аминогруппе и двух атомов - кислорода и водорода - в каждой карбоксильной группе). Аминокислотный остаток, находящийся на том конце пептида, где имеется свободная a-аминогруппа, называется аминоконцевым (или N-концевым) остатком, а остаток на противоположном конце, несущем свободную карбоксильную группу,- карбоксиконцевым, или С-концевым остатком. Названия пептидов образуют из названий входящих в них аминокислотных остатков в соответствии с их последовательностью, начиная с N-концевого остатка, как показано на рис. 5-19.
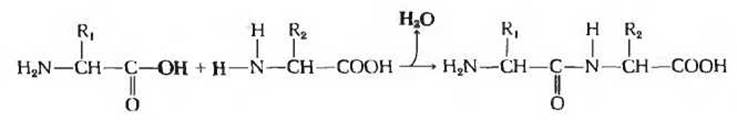
Рис. 5-18. Образование дипептида.
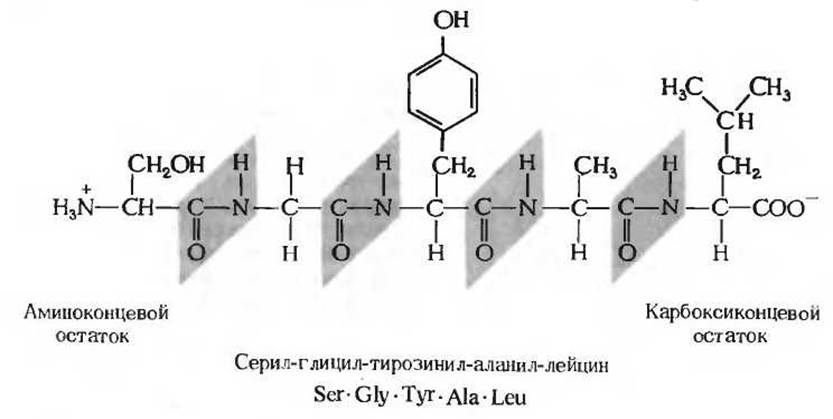
Рис. 5-19. Структура пентапептида серил-глицил-тирозинил-аланил-лейцина. Названия пептидов образуют из названий аминокислот, начиная с аминоконцевого остатка. Пептидные связи затенены, а R-группы выделены красным цветом.