Основы биохимии Том 3 - А. Ленинджер 1985
Молекулярные механизмы передачи генетической информации
ДНК: структура хромосом и генов
Некоторые физические свойства двухцепочечных ДНК отражают соотношение в их Составе пар G=C и А=Т
Если медленно нагревать растворы вирусной или бактериальной ДНК, то их молекулы денатурируют при вполне определенных температурах (рис. 27-16). Переход от нативного дуплекса ДНК к расплетенной беспорядочно скрученной денатурированной форме можно обнаружить по увеличению поглощения ультрафиолетового света или по уменьшению вязкости раствора ДНК. Для каждого вида ДНК характерна своя температура денатурации, называемая “точкой плавления”. Чем выше содержание в ДНК пар G≡C, тем выше точка плавления этой ДНК. Это объясняется тем, что пары G≡C более стабильны и на их диссоциацию требуется больше энергии, чем на разрушение пар А=Т; отчасти это обусловлено тем, что пары G≡C соединены тремя водородными связями, а пары А=Т-лишь двумя. Тщательное определение точки плавления препарата ДНК при фиксированных условиях pH и ионной силы может дать, следовательно, информацию о соотношении пар А=Т и G≡C в ДНК.
Второе физическое свойство ДНК, обусловленное соотношением пар G≡C и А=Т, -это плавучая плотность. Препарат ДНК с более высоким содержанием G≡C-пap обладает чуть большей плотностью, чем ДНК с повышенным содержанием А=Т-пар. Препараты ДНК центрифугируют при высоких скоростях в концентрированном растворе хлористого цезия (CsCl), плотность которого лежит в том же диапазоне, что и плотность ДНК. При центрифугировании в центрифужной пробирке формируется градиент плотности CsCl с наибольшей плотностью у дна пробирки. Если поместить в нее ДНК, то она сначала будет перемещаться по направлению ко дну пробирки, но затем в определенном положении остановится и будет держаться на плаву. В этом положении она не может ни всплыть, ни осесть, поскольку плотность раствора CsCl здесь равна ее плотности. С помощью этого метода, более подробно описанного в гл. 28, можно отделить друг от друга молекулы ДНК, различающиеся по содержанию G≡C-пар, поскольку они обладают разной плавучей плотностью. Исходя из плавучей плотности данной ДНК, можно подсчитать соотношение в ней пар G≡C и А=Т.
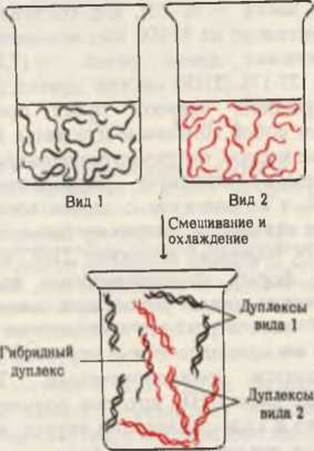
Рис. 27-15. Принцип гибридизационного теста. Два препарата ДНК, выделенной из организмов разных видов, нагревают так, что они полностью денатурируют и их цепи расходятся. При смешивании этих препаратов и медленном охлаждении комплементарные цепи ДНК каждого вида найдут друг друга и будут ренатурировать с образованием нормальных дуплексов. Если между двумя ДНК существует значительная гомология по последовательности, то возможно образование гибридных молекул, представляющих собой частичные дуплексы. Чем выше степень гомологии, тем больше вероятность образования гибридов. Содержание гибридов в смеси можно измерить разными способами, в частности с помощью хроматографии или центрифугирования в градиенте плотности. Обычно, чтобы упростить процедуру измерения, одну из ДНК метят радиоактивным изотопом.
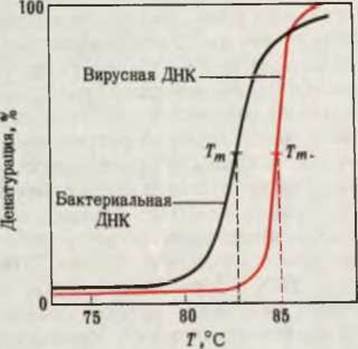
Рис. 27-16. Кривая денатурации (плавления) двух препаратов ДНК. Температура, соответствующая средней точке перехода (Tm), называется точкой плавления. Поскольку величина Тm зависит от pH и концентрации соли, всегда надо конкретизировать условия ее измерения.