Биохимия человека Том 1 - Марри Р. 1993
Биоэнергетика и метаболизм углеводов и липидов
Биоэнергетика
Роль высокоэнергетических фосфатов в биоэнергетике и в процессах улавливания энергии
Для поддержания процессов жизнедеятельности все организмы должны получать свободную энергию из внешней среды. У автотрофных организмов метаболизм сопряжен с простым экзергоническим процессом, протекающим в их окружении: зеленые растения используют энергию солнечного света; некоторые автотрофные бактерии существуют за счет реакции Fe2+ → Fe3+. Гетеротрофные же организмы получают энергию в результате сопряжения метаболизма с процессом распада сложных органических молекул, поступающих извне. Во всех этих процессах центральную роль играет АТР, обеспечивающий передачу свободной энергии от экзергонических процессов к эндергоническим (рис. 11.3 и 11.4). Как видно из рис. 11.5, АТР — это нуклеотид, содержащий аденин, рибозу и три фосфатные группы. В реакциях, протекающих внутри клетки, АТР участвует в виде Mg2+-комплекса (рис. 11.6).
Важная роль фосфатов в процессах метаболизма стала ясна после того, как были выяснены химические детали гликолиза и установлено, какую роль в этом процессе играют АТР, аденозиндифосфат (ADP) и неорганический фосфат (Рi). Вначале АТР рассматривали как переносчик фосфатных радикалов в процессе фосфорилирования. Роль АТР в биохимической энергетике была установлена в экспериментах, показывающих, что в процессе мышечного сокращения происходит распад АТР и креатинфосфата и что их ресинтез осуществляется за счет энергии, поступающей от протекающих в мышце окислительных процессов. Окончательную ясность внес Липман, который ввел представление о «богатых энергией фосфатах» и «богатой энергией фосфатной связи» и указал на их роль в биоэнергетике.
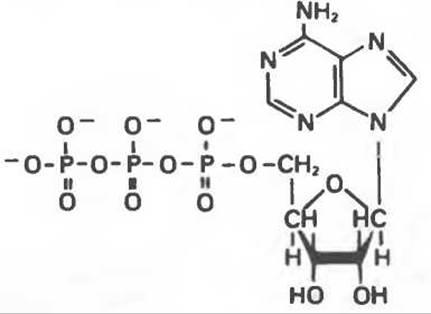
Рис. 11.5. Аденозинтрифосфат (АТР).
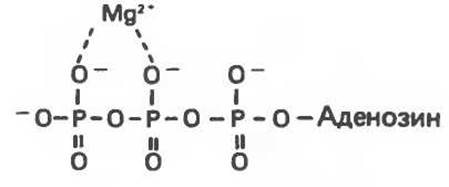
Рис. 11.6. Магниевый комплекс ЛТР (подобное строение имеет Mg-ADP).
Свободная энергия гидролиза АТР и других органических фосфатов
Стандартная свободная энергия гидролиза ряда биохимически важных органических фосфатов приведена в табл. 11.1. Сравнительную способность каждой из фосфатных групп к переходу на подходящий акцептор можно оценить по величине ∆G°' гидролиза (измеряемой при 37° С). Как видно из таблицы, значение ∆G°' для гидролиза концевого фосфата АТР, равное -30,5 кДж/моль, разделяет приведенные соединения на две группы. Одна группа — низкоэнергетические фосфаты; она представлена фосфорными эфирами, образующимися на промежуточных стадиях гликолиза, — их ∆G°' меньше, чем у АТР. Другая группа соединений — «богатые энергией фосфаты» — имеет ∆G°' больше, чем у АТР. Соединения этой группы, включая также АТР и ADP, — это обычно ангидриды (например, фосфатная группа в положении 11,3-бисфосфоглицерата), енолфосфаты (например, фосфоенолпируват) и фосфогуанидины (креатинфосфат, аргининфосфат). Другими биологически важными соединениями, которые классифицируются как «богатые энергией», являются тиоловые эфиры, образуемые коферментом А (в частности, ацетил-СоА), ацилпереносящий белок, эфиры аминокислот, участвующие в синтезе белков, S-аденозилметионин (активный метионин) и UDPGlc (уридиндифосфатглюкоза).
Таблица 11.1. Стандартная свободная энергия гидролиза некоторых биохимически важных органических фосфатов1
|
Соединение |
∆G°' |
|
|
кДж/моль |
ккал/моль |
|
|
Фосфоенолпируват |
-61,9 |
-14,8 |
|
Карбамоилфосфат |
-51,4 |
-12,3 |
|
1,3-Бисфосфоглицерат (продукт: 3-фосфоглицерат) |
-49,3 |
-11,8 |
|
Креатинфосфат |
-43,1 |
-10,3 |
|
АТР → ADP + Рі |
-30,5 |
-7,3 |
|
ADP → АМР + Pi |
-27,6 |
-6,6 |
|
Пирофосфат |
-27,6 |
-6,6 |
|
Глюкозо-1-фосфат |
-20,9 |
-5,0 |
|
Фруктозо-6-фосфат |
-15,9 |
-3,8 |
|
АМР |
-14,2 |
-3,4 |
|
Глюкозо-6-фосфат |
-13,8 |
-3,3 |
|
Глицерол-3-фосфат |
-9,2 |
-2,2 |
1) Значения ∆G для АТР и большинства других соединений взяты из работы Krebs, Komberg, 1957. [Имеется перевод: Кребс Г., Корнберг Г. Превращение энергии в живых системах.— М.: Мир, 1959.] Рi — неорганический ортофосфат.
Высокоэнергетические фосфаты
Чтобы указать на присутствие высокоэнергетической фосфатной группы, Липман ввел символ ![]() , означающий наличие высокоэнергетической (макроэргической) фосфатной связи. Символ ~ означает, что перенос группы, присоединенной указанной связью, на подходящий акцептор сопровождается выделением большого количества свободной энергии. Иногда предпочитают вместо термина «высокоэнергетическая связь» использовать термин «потенциал переноса группы». АТР содержит две высокоэнергетические фосфатные группы, ADP — одну, тогда как фосфатная связь в АМР является низкоэнергетической связью (рис. 11.7).
, означающий наличие высокоэнергетической (макроэргической) фосфатной связи. Символ ~ означает, что перенос группы, присоединенной указанной связью, на подходящий акцептор сопровождается выделением большого количества свободной энергии. Иногда предпочитают вместо термина «высокоэнергетическая связь» использовать термин «потенциал переноса группы». АТР содержит две высокоэнергетические фосфатные группы, ADP — одну, тогда как фосфатная связь в АМР является низкоэнергетической связью (рис. 11.7).
Роль высокоэнергетических фосфатов как «энергетической валюты» клетки
Среднее положение АТР в таблице величин стандартной свободной энергии гидролиза (табл. 11.1) позволяет этому соединению служить донором высокоэнергетического фосфата для тех соединений, которые в таблице находятся ниже АТР. При наличии соответствующих ферментных систем ADP может акцептировать высокоэнергетический фосфат (с образованием АТР) от тех соединений, которые находятся в таблице выше АТР. Таким образом, цикл ATP/ADP связывает процессы, генерирующие ![]() , с процессами, потребляющими
, с процессами, потребляющими ![]() (рис. 11.8).
(рис. 11.8).
Имеются три главных источника ![]() , обеспечивающие улавливание и запасание энергии. 1. Окислительное фосфорилирование. Это наиболее важный в количественном отношении источник
, обеспечивающие улавливание и запасание энергии. 1. Окислительное фосфорилирование. Это наиболее важный в количественном отношении источник ![]() у аэробных организмов. Свободная энергия, необходимая для образования
у аэробных организмов. Свободная энергия, необходимая для образования ![]() , генерируется в дыхательной окислительной цепи, функционирующей в митохондриях (с. 129). 2. Гликолиз. Суммарным результатом превращения одной молекулы глюкозы в лактат является образование двух
, генерируется в дыхательной окислительной цепи, функционирующей в митохондриях (с. 129). 2. Гликолиз. Суммарным результатом превращения одной молекулы глюкозы в лактат является образование двух ![]() (см. рис. 18.2) в ходе реакций, катализируемых фосфоглицераткиназой и пируваткиназой (рис. 11.9). 3. Цикл лимонной кислоты. Одна
(см. рис. 18.2) в ходе реакций, катализируемых фосфоглицераткиназой и пируваткиназой (рис. 11.9). 3. Цикл лимонной кислоты. Одна ![]() генерируется непосредственно в ходе цикла на стадии, катализируемой сукцинилтиокиназой (см. рис. 17.3).
генерируется непосредственно в ходе цикла на стадии, катализируемой сукцинилтиокиназой (см. рис. 17.3).
Другая группа соединений, фосфагены, выступает в качестве резервуара высокоэнергетических фосфатов; к их числу относятся креатинфосфат, содержащийся в мышцах и в мозге позвоночных, и аргининфосфат, находящийся в мышцах беспозвоночных (табл. 11.1).
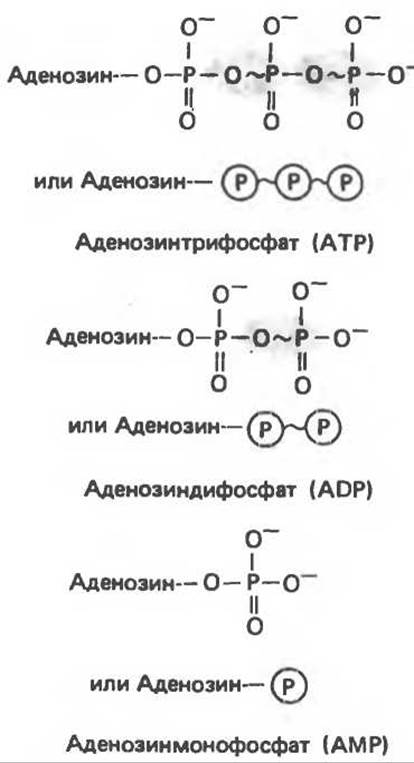
Рис. 11.7. Структура ATP, ADP и АМР с указанием положения и числа высокоэнергетических связей (~).
При физиологических условиях фосфагены поддерживают в мышцах необходимую концентрацию АТР в период его быстрого расходования как источника энергии для мышечного сокращения. С другой стороны, когда накапливается достаточно много АТР, реакция идет в направлении образования креатинфосфата, концентрация последнего повышается, и он выступает как форма хранения высокоэнергетического фосфата (рис. 11.10). Если же АТР служит донором фосфата при образовании соединений, имеющих более низкую свободную энергию гидролиза (табл. 11.1), то фосфатная группа становится низкоэнергетической, например:

Биоэнергетика сопряженных реакций
Рассмотрим подробнее энергетику сопряженных реакций (рис. 11.1 и 11.3). Первую стадию гликолиза можно рассматривать как сопряженную реакцию (см. рис. 18.2). Фосфорилирование глюкозы свободным фосфатом с образованием глюкозо-6-фосфата — сильноэндергоническая реакция:
(1) Глюкоза + Pі→ Глюкозо-6-фосфат + Н2О
(∆G°' = +13,8 кДж/моль).
Необходимо ее сопряжение с другой реакцией, экзергоничность которой больше, чем эндергоничность фосфорилирования глюкозы свободным ферментом. Такой реакцией является гидролиз АТР с отщеплением концевого фосфата:
(2) АТР → ADP + Рі (∆G°' = -30,5 кДж/моль).
При сопряжении процессов (1) и (2) в реакции, катализируемой ферментом гексокиназой, фосфорилирование глюкозы легко протекает в физиологических условиях: равновесие реакции сильно сдвинуто вправо, и она практически необратима.
![]()
Подобный механизм лежит в основе многих реакций «активации».
Взаимопревращение адениннуклеотидов
В большинстве клеток имеется фермент аденилаткиназа (миокиназа). Она катализирует обратимое превращение ATP и АМР в ADP:

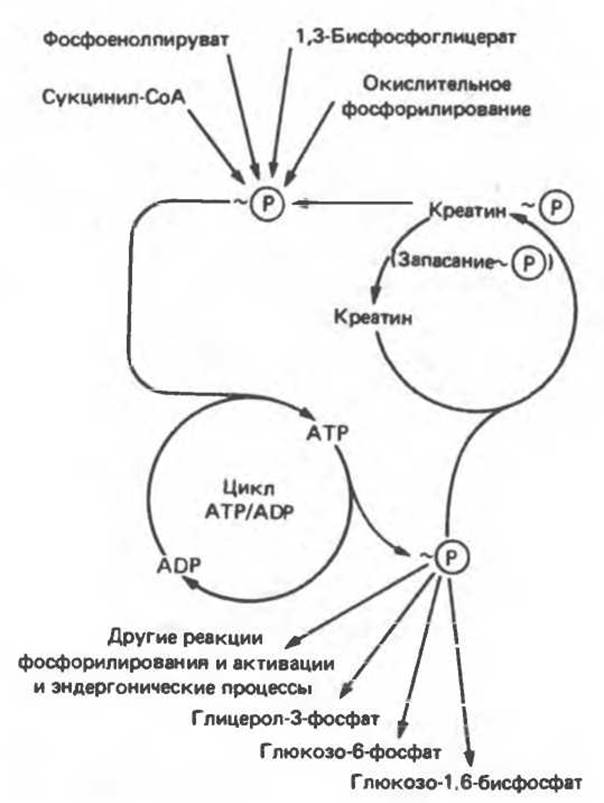
Рис. 11.8. Роль цикла АТР/ADP в системе переноса высокоэнергетического фосфата. Обратите внимание, что ![]() никогда не находится в свободном состоянии, а только переносится с одного соединения на другое.
никогда не находится в свободном состоянии, а только переносится с одного соединения на другое.
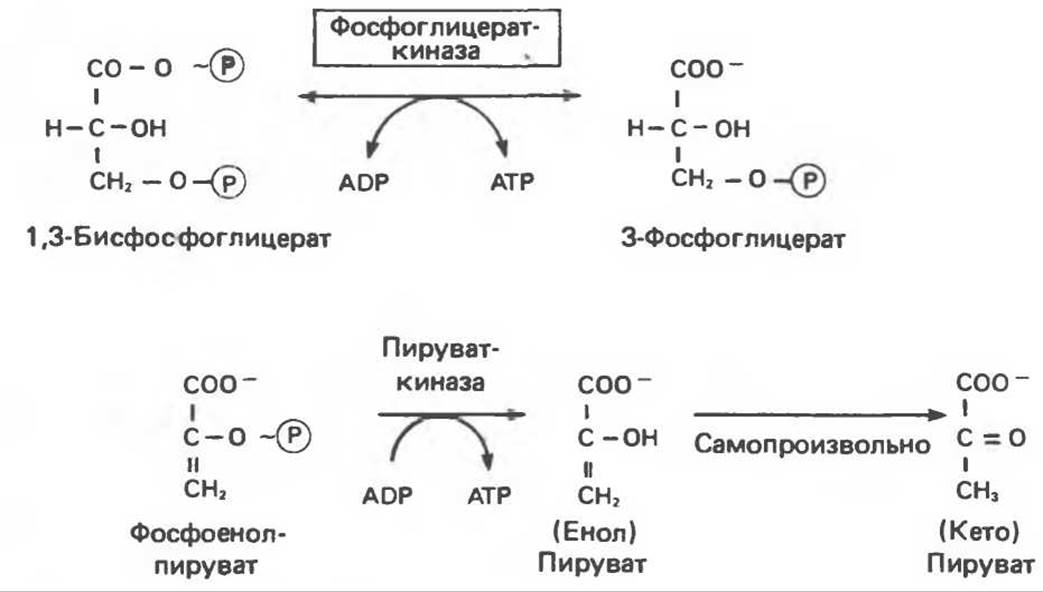
Рис. 11.9. Перенос высокоэнергетического фосфата от промежуточных продуктов гликолиза на ADP.
Эта реакция выполняет три функции: 1) позволяет использовать высокоэнергетический фосфат ADP для синтеза АТР; 2) позволяет превратить АМР, образующийся в ряде реакций активации, идущих с участием АТР, в ADP путем рефосфорилирования; 3) приводит к повышению концентрации АМР в условиях снижения содержания АТР и служит метаболическим (аллостерическим) сигналом к повышению скорости катаболических реакций, что в свою очередь приводит к увеличению генерации АТР (с. 217).
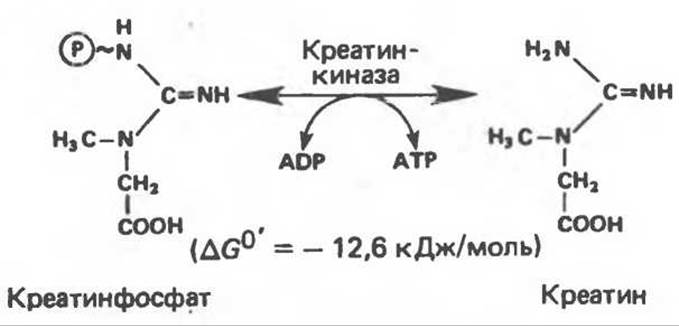
Рис. 11.10. Перенос высокоэнергетического фосфата между АТР и креатином.