Биохимия человека Том 2 - Марри Р. 1993
Биохимия внутри- и межклеточных коммуникаций
Гормоны коры надпочечников
Регуляция синтеза стероидных гормонов надпочечников
Глюкокортикоидные гормоны
Секреция кортизола зависит от АКТГ, выделение которого в свою очередь регулируется кортикотропин-рилизинг-гормоном (КРГ; кортиколиберин). Эти гормоны связаны между собой классической петлей отрицательной обратной связи (рис. 48.5). Повышение уровня свободного кортизола тормозит секрецию КРГ. Падение уровня свободного кортизола ниже нормы активирует систему, стимулируя высвобождение КРГ гипоталамусом. Этот пептид, состоящий из 41 аминокислотного остатка, усиливает синтез и высвобождение АКТГ (из молекулы предшественника проопиомеланокортина [ПОМК], см. гл. 45). В коре надпочечников АКТГ повышает скорость отщепления боковой цепи от холестерола — реакции, лимитирующей скорость стероидогенеза в целом. Указанные процессы составляют одну сторону петли отрицательной обратной связи. По мере нормализации уровня свободного кортизола в крови происходит снижение секреции КРГ гипоталамусом, что ведет к снижению выработки АКТГ гипофизом, а соответственно и кортизола — надпочечниками; таким образом выполняется вторая половина петли обратной связи. Этот сложный механизм обеспечивает быструю регуляцию уровня кортизола в крови.
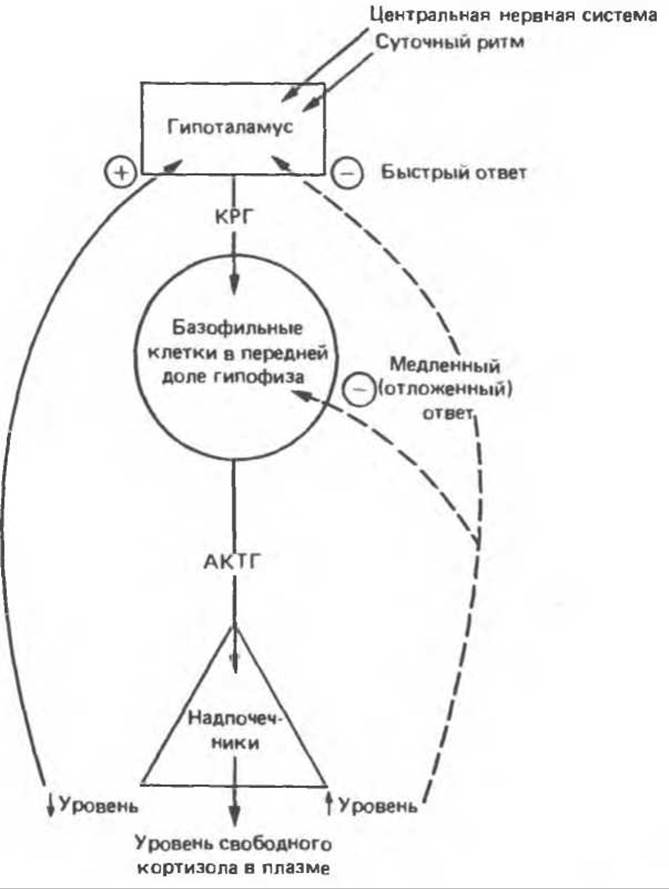
Рис. 48.5. Регуляция биосинтеза кортизола по механизму обратной связи. Сплошные линии - стимуляция; штриховые линии — ингибирование.
Высвобождение АКТГ (и секреция кортизола) регулируется нервными импульсами, поступающими из различных отделов нервной системы. Существует эндогенный ритм, определяющий секрецию КРГ, а следовательно, и АКТГ. Этот циркадианный ритм в норме настроен так, чтобы обеспечивать увеличение кортизола в крови вскоре после засыпания. Во время сна уровень кортизола продолжает возрастать, достигая пика вскоре после просыпания, затем постепенно падает до минимальных величин к концу дня и в ранее вечерние часы. Эта общая динамика возникает в результате последовательных эпизодов импульсного выброса кортизола, которым предшествует импульсная секреция АКТГ (см. гл. 45). Все вместе эти события составляют сложный цикл, зависящий от светового периода и циклов питания — голодания и сна — бодрствования. Исчезновение суточной периодичности секреции стероидов обычно связано с патологией гипофизарно-адреналовой системы, некоторыми видами депрессивных состояний, а также с дальними перелетами через несколько часовых поясов.
На секрецию кортизола влияют также физический и эмоциональные стрессы, состояние тревоги, страха, волнения и боль. Эти реакции могут нивелировать воздействия системы отрицательной обратной связи и суточного ритма.
Минералокортикоидные гормоны
Продукция альдостерони клетками клубочковой зоны регулируется совершенно иначе: основными регуляторами в этом случае служат система ренин — ангиотензин и калий, но участвуют в этом процессе также натрий, АКТГ и нейрональные механизмы.
А. Система ренин — ангиотензин. Эта система участвует в регуляции кровяного давления и электролитного обмена. Основным гормоном при этом является ангиотензин П — октапептид, образующийся из ангиотензиногена (рис. 48.6). Ангиотензиноген — это а2-глобулин, синтезируемый печенью; он служит субстратом для ренина — фермента, продуцируемого юкстагломерулярными клетками почечных афферентных артериол. Локализация этих клеток делает их особенно чувствительными к изменениям кровяного давления; многие физиологические регуляторы высвобождения ренина (табл. 48.3) действуют через почечные барорецепторы. Юкстагломерулярные клетки чувствительны также к изменениям концентрации Na+ и К+ в жидкости, протекающей через почечные канальцы; вследствие этого любая комбинация факторов, вызывающая снижение объема жидкости (обезвоживание, снижение кровяного давления, потеря жидкости или крови) либо снижение концентрации NaCl, стимулирует высвобождение ренина. На высвобождение ренина оказывают влияние центральная нервная система, а также изменения положения тела. Соответствующие сигналы передаются по симпатическим нервам к юкстагломерулярным клеткам, действуя по механизму, не зависящему от барорецепторов и солевого эффекта, а опосредованному ß-адренергическим рецептором.
Таблица 48.3. Факторы, влияющие на высвобождение ренина
|
Стимулирующие |
Ингибирующие |
|
Пониженное кровяное давление |
Повышенное кровяное давление |
|
Перемена положения тела: от горизонтального к вертикальному |
Перемена положения тела: от вертикального к горизонтальному |
|
Потеря соли организмом |
Солевая нагрузка |
|
ß-Аренергические агенты |
ß-Адренергические антагонисты |
|
Простагландины |
Ингибиторы простагландинов |
|
Калий |
|
|
Вазопрессин |
|
|
Ангиотензин II |
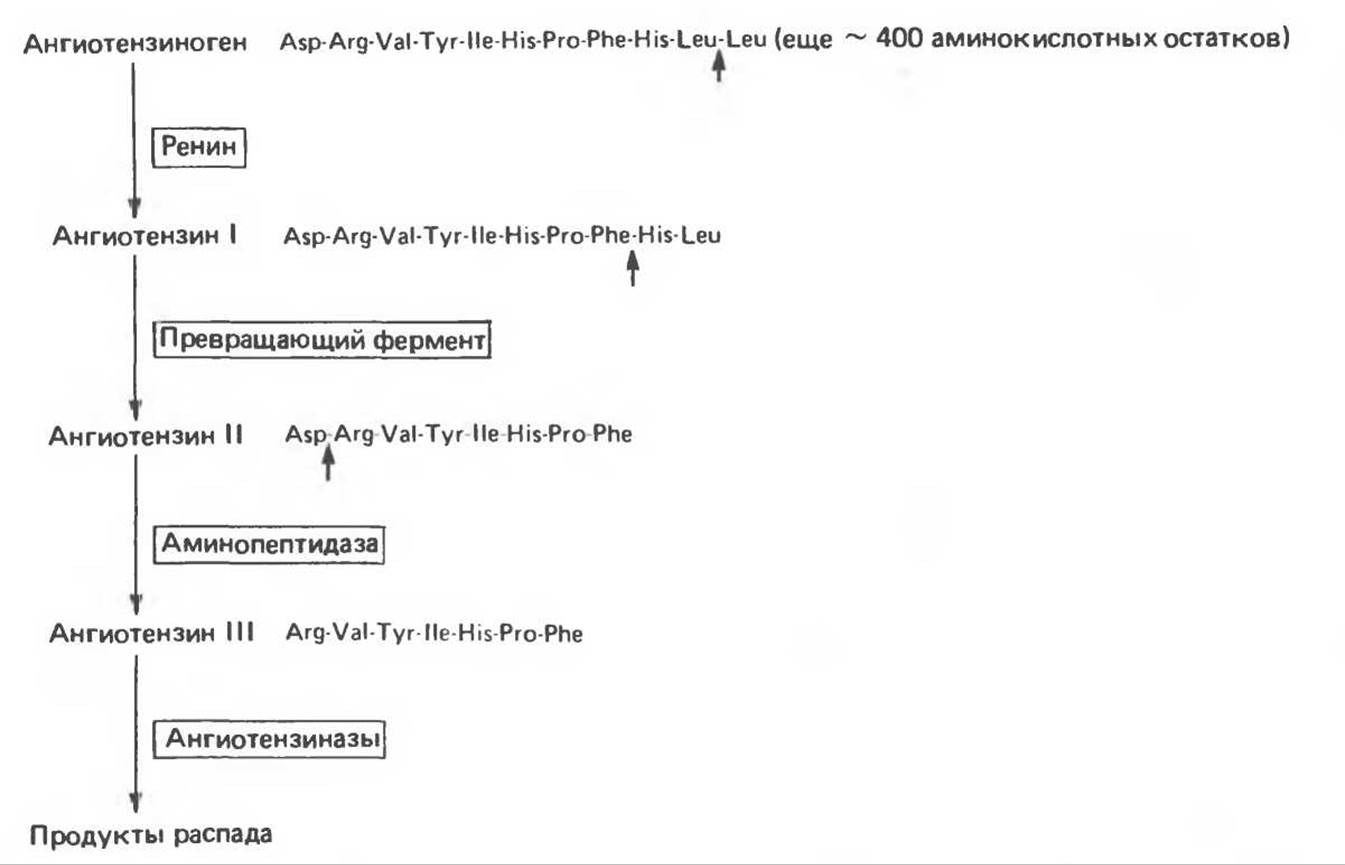
Рис. 48.6. Образование и метаболизм ангиотензинов. Участки расщепления показаны маленькими стрелками
Ренин, воздействуя на свой субстрат — ангиотензиноген, превращает его в декапептид ангиотензин I. Глюкокортикоиды и эстрогены активируют синтез ангиотензиногена в печени. Вызываемая этими гормонами гипертензия может быть частично обусловлена повышением уровня ангиотензиногена в плазме крови. Поскольку концентрация этого белка в плазме близка к Км, его воздействия с ренином, небольшие изменения этой концентрации могут сильно сказаться на образовании ангиотензина II.
Ангиотензин-превращающий фермент — гликопротеин, выявленный в легких, эндотелиальных клетках и в плазме крови, отщепляет от ангиотензина I два С-концевых аминокислотных остатка, превращая его в ангиотензин II. Эта реакция, видимо, не является скорость-лимитирующей. Различные нонапептиды — аналоги ангиотензина І — способны ингибировать превращающий фермент и потому используются для лечения ренин-зависимой гипертензии. Превращающий фермент расщепляет также брадикинин, мощное сосудорасширяющее средство. Таким образом, этот фермент повышает кровяное давление двумя различными путями.
Ангиотензин II увеличивает кровяное давление, вызывая сужение артериол, и является самым сильнодействующим из известных вазоактивных агентов. Кроме того, он тормозит высвобождение ренина юкстагломерулярными клетками и оказывает сильное стимулирующее действие на выработку альдостерона. Несмотря на то что этот эффект на надпочечники является прямым, на продукцию кортизола ангиотензин II не влияет. У некоторых видов животных ангиотензин II превращается в гептапептид ангиотензин III (рис. 48.6) в результате отщепления остатка Asp1. Стимулирующее действие на продукцию альдостерона у обоих ангиотензинов примерно одинаково. У человека уровень ангиотензина II в плазме крови в 4 раза выше, чем ангиотензина III, так что именно октапептид оказывает основной эффект. Ангиотензины II и III быстро инактивируются под действием антиотензиназ.
Ангиотензин II связывается со специфическими рецепторами клубочковых клеток. Содержание этих рецепторов зависит от «повышающей регуляции» со стороны ионов калия и самого гормона, а также «понижающей регуляции» низкими концентрациями калия; таким образом, этот ион играет центральную роль в действии ангиотензина II на надпочечники. При данном гормон-рецепторном взаимодействии не происходит активации аденилатциклазы, так что сАМР, по-видимому, не участвует в механизме действия ангиотензина II.
Действие этого гормона, стимулирующего превращение холестерола в прегненолон и кортикостерона в 18-гидроксикортикостерон и альдостерон, может быть опосредовано изменениями концентрации внутриклеточного кальция и метаболитов фосфолипидов по механизму, сходному с описанным в гл. 44. Определенную роль может играть и биосинтез простагландинов, судя по тому, что простагландины Е1 и Е2 стимулируют высвобождение альдостерона, a F1a и F2a — тормозят; в целом это типично для опосредованных простагландинами реакций. Ингибитор биосинтеза простагландинов индометацин тормозит как базальное, так и стимулированное ангиотензином II высвобождение альдостерона.
Б. Калий. Секреция альдостерона зависит от изменений уровня калия в плазме: увеличение калия всего лишь на 0,1 м∙экв/л стимулирует секрецию, а снижение на ту же величину тормозит синтез и секрецию гормона. Эффект К+ не зависит от уровней Na+ и ангиотензина II в плазме крови. Продолжительная гиперкалиемия приводит к гипертрофии клубочковой зоны и повышению чувствительности ее клеток к ионам калия. К+ воздействует на те же ферментативные этапы, что и ангиотензин II, но механизм его эффекта не известен. Подобно ангиотензину II, К+ не влияет на биосинтез кортизола.
В. АКТГ. У человека быстрое, краткосрочное снижение уровня АКТГ (например, в результате гипофизэктомии или подавления секреции глюкокортикоидами) мало сказывается на продукции альдостерона, но хроническая недостаточность АКТГ может ослаблять действие других регуляторов (ангиотензина II, Na+, К+) на содержание альдостерона в крови. У других видов (например, у крыс) АКТГ играет более важную роль в выработке альдостерона: на изолированных клетках клубочковой зоны показано, что он стимулирует синтез сАМР и начальные этапы стероидогенеза.
Г. Натрий. Недостаточность Na+ усиливает продукцию альдостерона, а нагрузка ионами натрия снижает ее, однако эти эффекты большей частью опосредованы системой ренин — ангиотензин. Возможно и прямое воздействие Na+ на синтез альдостерона, но этот эффект слаб, кратковременен и требует высоких концентраций Na+.