Биохимия человека Том 2 - Марри Р. 1993
Структура, функция и репликация информационных макромолекул
Технология рекомбинантных ДНК
Основные понятия генной инженерии
В основе методологии генной инженерии лежит выделение ДНК и проведение различных манипуляций с ее молекулами, включая получение химер (например, молекулы ДНК, построенной из фрагментов ДНК человека и бактерий).
Ферменты рестрикции
Один из важнейших инструментов генной инженерии — эндонуклеазы, ферменты, расщепляющие ДНК по специфическим последовательностям нуклеотидов внутри цепи (в противоположность экзонуклеазам, которые расщепляют ДНК с концов молекулы). Эти ферменты получили название рестриктаз, поскольку их присутствие в бактериальной клетке ограничивает рост определенных бактериальных вирусов, называемых бактериофагами. Рестриктазы расщепляют ДНК на относительно небольшие фрагменты в участках последовательности строго определенной структуры. Этим их воздействие отличается от большинства других ферментативных, химических или физических воздействий, приводящих к случайным разрывам цепей ДНК. Рестриктазы (уже открыто более 200 типов ферментов этого класса) являются частью защитной системы бактерий, охраняющей собственный геном от чужеродной, главным образом вирусной, ДНК. Рестриктазы присутствуют только в таких клетках, которые содержат и специфические метилазы. Роль этих ферментов — метилирование собственной (хозяйской) ДНК клетки и защита ее таким образом от действия рестриктаз. Сайт-специфические метилазы и рестриктазы всегда присутствуют в бактериях одновременно.
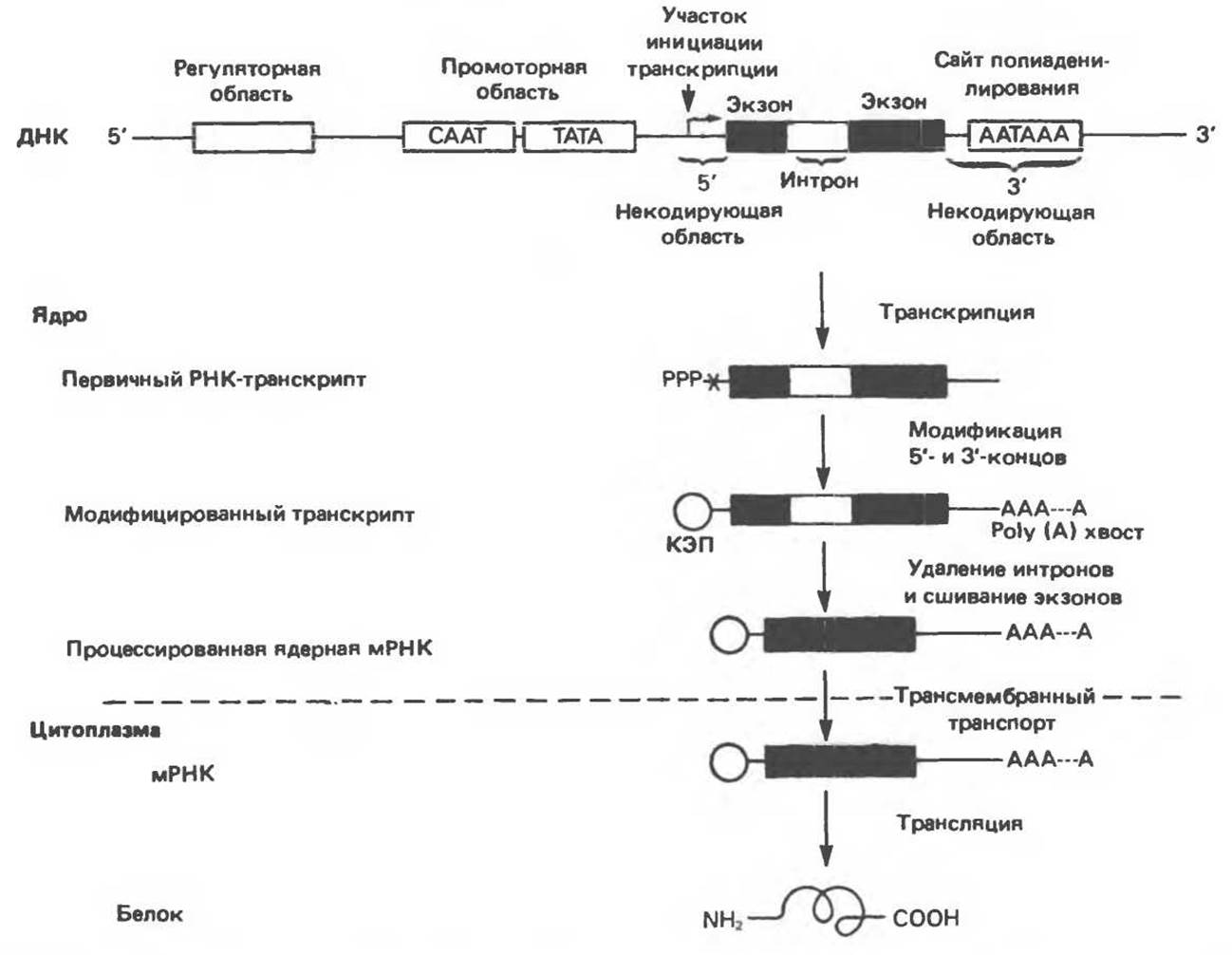
Рис. 36.1. Организация транскрипционной единицы и этапы экспрессии эукариотических генов. Эукариотические гены состоят из структурной и регуляторной областей. Структурная область представлена кодирующей ДНК и некодирующими 5'- и 3'-последовательностями. Кодирующая ДНК включает экзоны — участки ДНК, транскрипты которых остаются в составе зрелой мРНК, и интроны (транскрипты этих последовательностей удаляются из РНК в ходе процессинга). Структурная область гена ограничена с 5'-конца сайтом инициации транскрипции, а с 3'-конца — полиаденилатным сайтом или сайтом терминации. Промоторная область, содержащая специфические последовательности, взаимодействующие с белковыми факторами, рассмотрена в гл. 39 и 41. Первичный транскрипт имеет на 5'-конце специфическую структуру — КЭП и участок, богатый «А» на 3'-конце. После удаления интронов из первичного транскрипта образовавшаяся зрелая мРНК транспортируется в цитоплазму, где и транслируется с образованием белковой молекулы.
Рестриктазы принято именовать по названию бактерий, из которых их выделяют (табл. 36.1). Так, название ЕcoRI свидетельствует о том, что этот фермент выделен из Escherichia coli, BamHІ — из Bacillus amiloliquefaciens. Первая из трех букв аббревиатуры соответствует первой букве названия рода (Е). Последующие две буквы являются начальными буквами видового названия (со). Буква R говорит о том, из какого штамма выделен фермент. Римская цифра соответствует порядковому номеру рестриктазы в ряду аналогичных ферментов, выделенных из этого микроорганизма (например, ЕcoRI, ЕcoRII). Каждый фермент узнает определенную 4—7-членную последовательность в двухцепочечной ДНК. Разрезание ДНК по этим сайтам приводит к образованию либо «тупых» (например, при действии рестриктазы HpaІ), либо «липких», т. е. перекрывающихся (например, ВаmHI), концов (рис. 36.2). Для конструирования гибридных молекул особенно удобны липкие концы (см. ниже). Если допустить, что нуклеотиды распределены по молекуле ДНК совершенно случайным образом, можно рассчитать частоту встречаемости участка узнавания для данной рестриктазы. В каждой нуклеотидной позиции молекулы ДНК с одинаковой вероятностью может оказаться один из 4-х нуклеотидов (A, G, С, Т). Поэтому фермент, узнающий четырехзвенную последовательность, будет находить одну мишень на 256 пар оснований (44). В то же время фермент, различающий шестизвенную последовательность, будет находить специфический участок узнавания 1 раз на 4096 пар оснований (46). Любой фрагмент ДНК обладает характерным расположением сайтов узнавания различных рестриктаз, что позволяет строить так называемые рестриктазные карты. При расщеплении ДНК какой- либо одной рестриктазой получают смесь фрагментов, каждый из которых имеет одни и те же концевые участки. Такие фрагменты можно разделить методом электрофореза в агарозном или полиакриламидном геле (о методах блоттинга см. ниже). Эта процедура, основанная на применении рестриктаз, представляет собой важнейший этап клонирования генов.
Таблица 36.1. Некоторые рестриктазы и расщепляемые ими последовательности
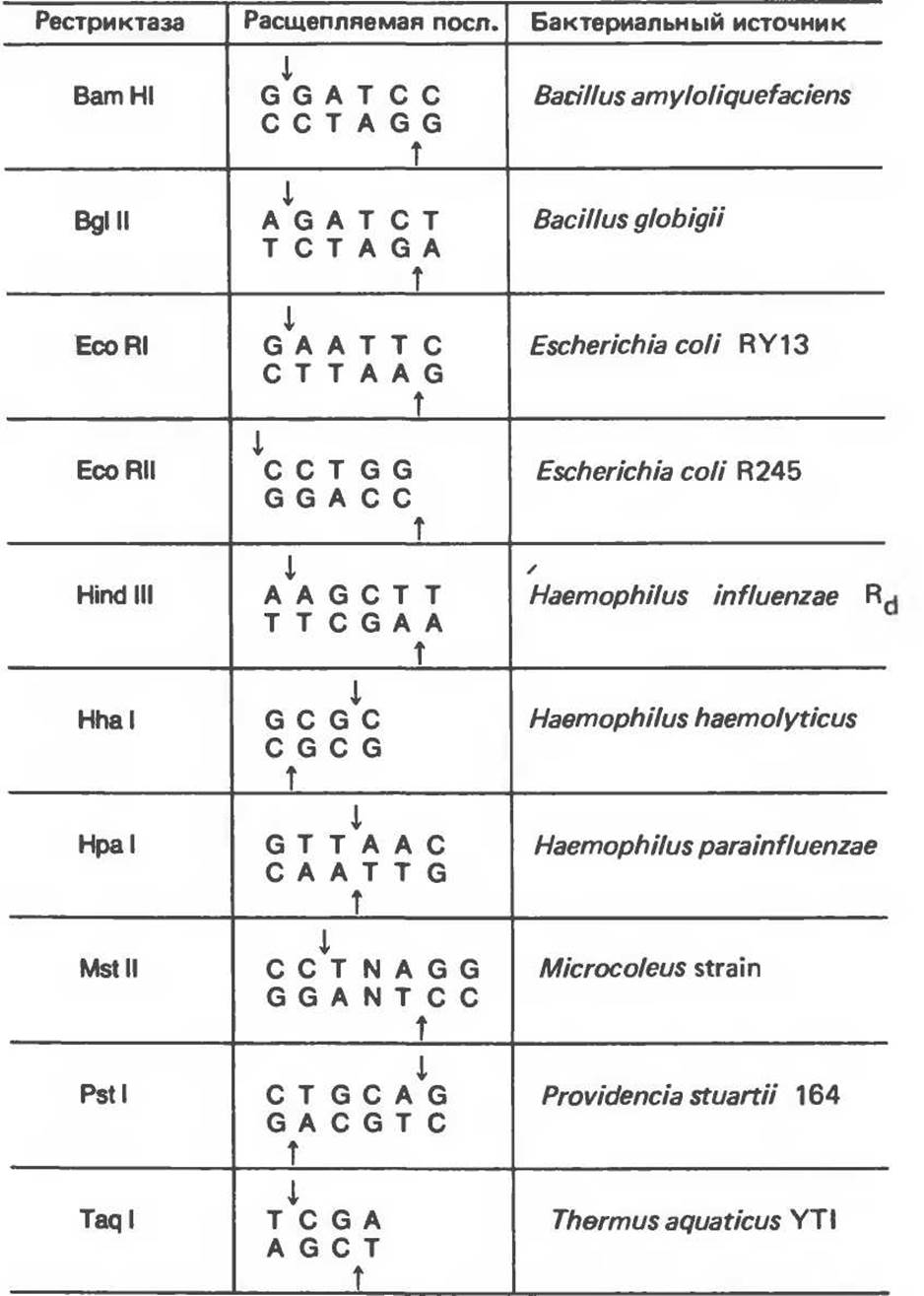
А — аденин; С — цитозин; G — гуанин, гимин. Стрелки указывают на сайты расщепления. В результате рестрикции могут формироваться «липкие» (ВаmHI) или «тупые» (Нра I) концы. Длина узнаваемой последовательности варьирует и составляет 4 п. н. для Taq I, 5 п. н. для EcoRII, 6 п. н. для EcoRI и 7 п. н. для Mst II. Согласно принятым правилам, верхняя цепь последовательности-мишени представлена в ориентации 5'→3', а нижняя — в ориентации 3'→5'. Обратите внимание, что большинство последовательностей является палиндромами (т. е. читаются одинаково в противоположных направлениях по разным цепям). Остаток, обозначенный N, означает любой нуклеотид.
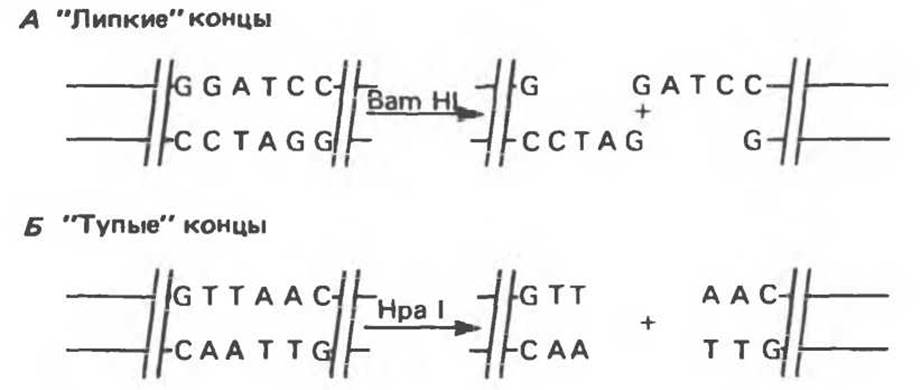
Рис. 36.2. Расщепление ДНК рестрицирующими эндонуклеазами (рестриктазами). В результате рестрикции образуются фрагменты (рестрикты) либо с «липкими» (А), либо с «тупыми» (Б) концами.
Другие ферменты
Ряд других ферментов, использующих ДНК в качестве субстрата, также имеет важное значение для генной инженерии. На некоторых из них мы остановимся в этой и последующих главах (табл. 36.2).
Конструирование химерных молекул ДНК
Ковалентное соединение (в дальнейшем мы будем пользоваться термином «лигирование») липких концов фрагментов ДНК — процедура технически не сложная, однако при этом могут возникать определенные проблемы. Так, липкие концы вектора могут лигироваться сами на себя без включения клонируемого фрагмента. Кроме того, может произойти отжиг липких концов двух различных фрагментов, что приведет к образованию гетерогенной вставки. Не все интересующие исследователя участки ДНК содержат удобно расположенные сайты узнавания для рестриктаз, дающих липкие концы. Для преодоления этих трудностей иногда используют рестриктазы, образующие тупые концы, после чего с помощью специфического фермента (терминальной трансферазы) генерируют новые концы. Так, присоединение к 3'-концам вектора гомополимерной цепочки, состоящей из dG, а к 3'-концам клонируемого фрагмента ДНК — цепочки polyd(C) — обеспечивает исключительно межмолекулярный отжиг. В ходе этой процедуры, получившей название «присоединение гомополимерного хвоста», образуется также сайт для рестриктазы Smal, что обеспечивает возможность последующего вырезания клонированного фрагмента. Иногда к тупоконечной ДНК присоединяют синтетические олигонуклеотидные линкеры, содержащие участки узнавания для определенной рестриктазы. С использованием ДНК-лигазы бактериофага Т4 может проводиться и непосредственное лигирование фрагментов с тупыми концами. Этот метод, менее эффективный, чем лигирование по липким концам, имеет однако то преимущество, что с его помощью возможно сшивание любых пар фрагментов. К недостаткам его следует отнести невозможность легко проконтролировать ориентацию вставки и число встроенных фрагментов, а также «вырезать» клонированный фрагмент из рекомбинантной молекулы ДНК.
Таблица 36.2. Ферменты, используемые в работе с рекомбинантными ДНК. (Adapted and reproduced, with permission, from Emery A. E. H. Page 41 in: An introduction to Recombinant DNA, Wiley, 1984.)
|
Фермент |
Реакция |
Область приложения |
|
Щелочная фосфатаза |
Дефосфорилирует 5'-концы РНК и ДНК |
Удаление 5'-РO4 групп перед введением метки методом кинирования, а также для предотвращения лигирования молекул вектора по типу «сам на себя» |
|
BAL-31 нуклеаза |
Деградация как 5'-, так и 3'-концов ДНК |
Введение концевых делеций в молекулы ДНК |
|
ДНК-лигаза |
Катализирует образование связей между молекулами ДНК |
«Сшивание» молекул ДНК |
|
ДНК-полимераза І |
Синтез двухцепочечной ДНК по ДНК-матрице |
Синтез двухцепочечной кДНК; ник-трансляция |
|
ДНКаза I |
В соответствующих условиях вносит одноцепочечные разрывы в ДНК |
Ник-трансляция, картирование гиперчувствительных участков в ДНК |
|
Экзонуклеаза III |
Удаляет нуклеотиды с 3'-концов ДНК |
Секвенирование ДНК, картирование ДНК-белковых взаимодействий |
|
λ-Экзонуклеаза |
Удаляет нуклеотиды с 5'-концов ДНК |
Секвенирование ДНК |
|
Полинуклеотидкиназа |
Переносит терминальный (в у-положении) фосфат АТР на 5'-ОН-группы ДНК и РНК |
Введение 32Р в ДНК и РНК |
|
Обратная транскриптаза |
Синтезирует ДНК по РНК-матрице |
Синтез кДНК по мРНК; картирование РНК (с 5'-конца) |
|
Нуклеаза S1 |
Деградирует одноцепочечную ДНК |
Удаление шпильки при синтезе кДНК; РНК-картирование (как с 5'-, так и с 3'-конца) |
|
Терминальная транс-фераза |
Добавляет нуклеотиды к 3'-концу ДНК |
Создание гомополимерных «хвостов» |
Клонирование
Понятие «клон» определяется как большая популяция идентичных молекул, бактерий или клеток — потомков одного предка. Клонирование позволяет получать большое количество идентичных молекул ДНК, которые можно охарактеризовать и использовать в каких-то целях. Метод клонирования основан на том факте, что химерные или гибридные молекулы ДНК могут быть сконструированы в составе векторов для клонирования, к которым относятся бактериальные плазмиды, фаги или космиды, способные к репликации в хозяйских клетках под контролем своих собственных регуляторных элементов. Таким путем добиваются амплификации химерной ДНК. Общая схема процесса клонирования представлена на рис. 36.3.
Бактериальные плазмиды — это небольшие кольцевые молекулы двухцепочечной ДНК, в функции которых входит, например, обеспечение устойчивости к антибиотикам для несущих их хозяйских клеток. Плазмиды обладают несколькими свойствами, которые делают их чрезвычайно удобными для использования в качестве векторов для клонирования: 1) в бактериальной клетке они могут существовать в одной или множестве копий; 2) реплицируются плазмиды независимо от хозяйской ДНК. В настоящее время для многих плазмид уже известна полная нуклеотидная последовательность. Это делает возможным точную локализацию сайтов рестрикции для клонирования фрагментов ДНК. Плазмиды значительно меньше хозяйской хромосомной ДНК и поэтому могут быть легко отделены от нее. Клонированный фрагмент легко выделяется из рекомбинантной плазмиды посредством ее расщепления той же рестриктазой, по сайту которой проводили лигирование.
Фаги обычно содержат линейную ДНК, в которую могут быть встроены фрагменты чужеродной ДНК по какому-либо из доступных сайтов рестрикции. Химерную ДНК выделяют обычно после завершения рекомбинантным фагом литического цикла и выхода зрелых инфекционных фаговых частиц. Основным преимуществом фаговых векторов перед плазмидными является то, что в отличие от плазмид, способных нести фрагменты ДНК до 6—10 т. п. н., в фаговые частицы удается встраивать фрагменты размером до 10—20 т. п. н. Величина клонируемого фрагмента определяется общим количеством ДНК, способным упаковываться в головку фага.
Фрагменты еще большего размера могут быть клонированы в космидах — векторах, объединяющих преимущества плазмид и фагов. Космиды — это плазмиды, содержащие специфические участки, называемые cos-сайтами, которые необходимы для упаковки ДНК фага λ в капсид. Эти вектора могут поддерживаться в бактериальной клетке в плазмидной форме, но так как большая часть ДНК фага из космиды удалена, то соответственно увеличивается и возможная длина клонируемого фрагмента. Довольно обычными для космид являются вставки размером 30—50 т. п. н. Свойства векторов трех типов сравниваются в табл. 36.3.
Когда решается вопрос о том, в какую область вектора ввести клонируемый фрагмент, необходимо учитывать, что вставка в функционально важную последовательность неизбежно нарушит какое-либо из свойств вектора. Впрочем, такое нарушение может быть использовано в целях селекции рекомбинантных молекул. Например, широко распространенный плазмидный вектор pBR322 несет гены устойчивости к двум антибиотикам — ампициллину и тетрациклину. Для клонирования часто используется уникальный Pstl-сайт в гене устойчивости к ампициллину. Встраивание чужеродного фрагмента ДНК приводит к инактивации гена ампициллинустойчивости, и бактерии, несущие такую рекомбинантную плазмиду, становятся чувствительными к этому антибиотику (рис. 36.4). Это позволяет легко отличить исходную плазмиду, обеспечивающую устойчивость бактерии-хозяина к обоим антибиотикам, от рекомбинантной формы. Чтобы получить еще более четкие доказательства того, что плазмидная ДНК действительно является химерной (несет вставку), можно сравнить размеры сконструированной плазмиды с исходной методом гель-электрофореза. Рекомбинантная плазмида, естественно, будет иметь больший молекулярный вес.
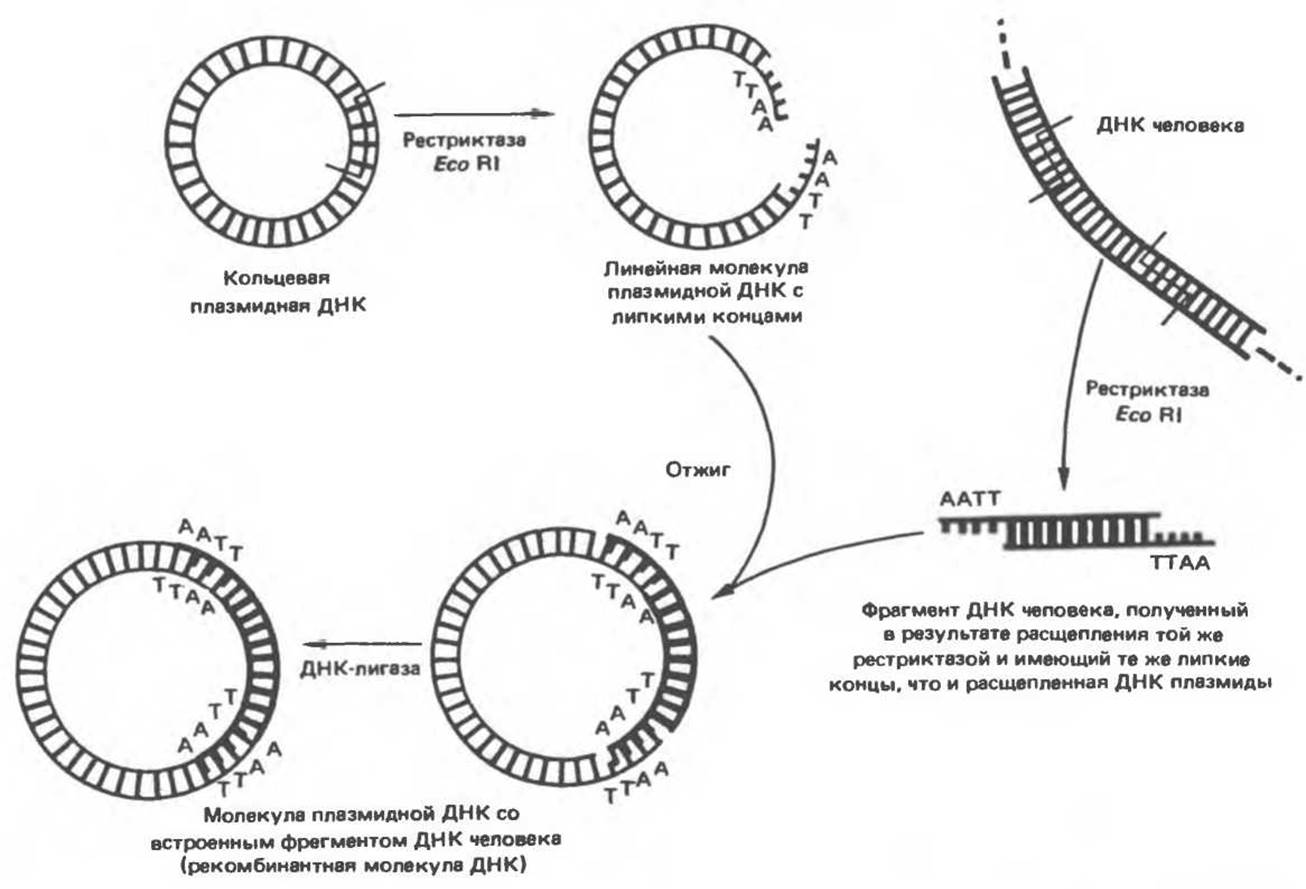
Рис. 36.3. Использование рестриктаз для конструирования рекомбинантных или химерных молекул ДНК. Введенная обратно в бактериальную клетку (при трансформации) плазмида реплицируется, а вместе с ней реплицируется и последовательность-вставка. Поскольку воссоединение липких концов реконструирует сайт узнавания рестриктазы, клонированный фрагмент может быть легко выделен из рекомбинантной плазмиды при помощи той же рестриктазы. Если при этом использовать смесь всех фрагментов, образованных в результате расщепления тотальной ДНК человека одной и той же эндонуклеазой, то при помощи клонирующих плазмид можно получить около миллиона различных рекомбинантных молекул ДНК, каждая из которых дает начало индивидуальному бактериальному клону. (Modified and reproduced with permission, from Cohen SN: The manipulation of genes. Sсi. Am. [July] 1975; 233: 34.)
Таблица 36.3. Широко распространенные векторы для клонирования
|
Вектор |
Размер клонируемого фрагмента ДНК (вставки) |
|
Плазмида pBR322 |
0,01—10 т. п. н. |
|
Лямбда Харон 4А |
10—20 т. п. н. |
|
Космиды |
35—50 т. п. н. |
Геномные библиотеки и их конструирование
Подобрав соответствующие условия клонирования, можно добиться того, что в наборе клонированных фрагментов будут содержаться практически все гены данного генома. Такие коллекции клонов, полученные для конкретного генома, называют геномными библиотеками. Геномная библиотека готовится из тотальной ДНК клеточной линии или ткани. В отличие от геномной библиотеки библиотека кДНК представляет популяцию мРНК в ткани. Геномная библиотека готовится методом частичного расщепления тотальной ДНК какой-либо «мелкощепящей» рестриктазой (например, SаuIIIА). Смысл такой обработки заключается в том, чтобы получить популяцию больших фрагментов ДНК, содержащих полноразмерные гены. Для конструирования геномных библиотек предпочтительно использовать фаговые векторы, так как они позволяют клонировать очень протяженные фрагменты ДНК (до 20 т. п. н.). Число независимо полученных фаговых клонов, требуемых для создания представительной библиотеки, обратно пропорционально размеру клонируемых фрагментов, но прямо пропорционально размеру генома (табл. 36.4). Библиотека генома человека, состоящая из 106 клонов со встроенными достаточно протяженными фрагментами, с вероятностью около 99% содержит любой уникальный ген. Получение такой библиотеки обеспечивает высокую вероятность выявления интересующего гена.
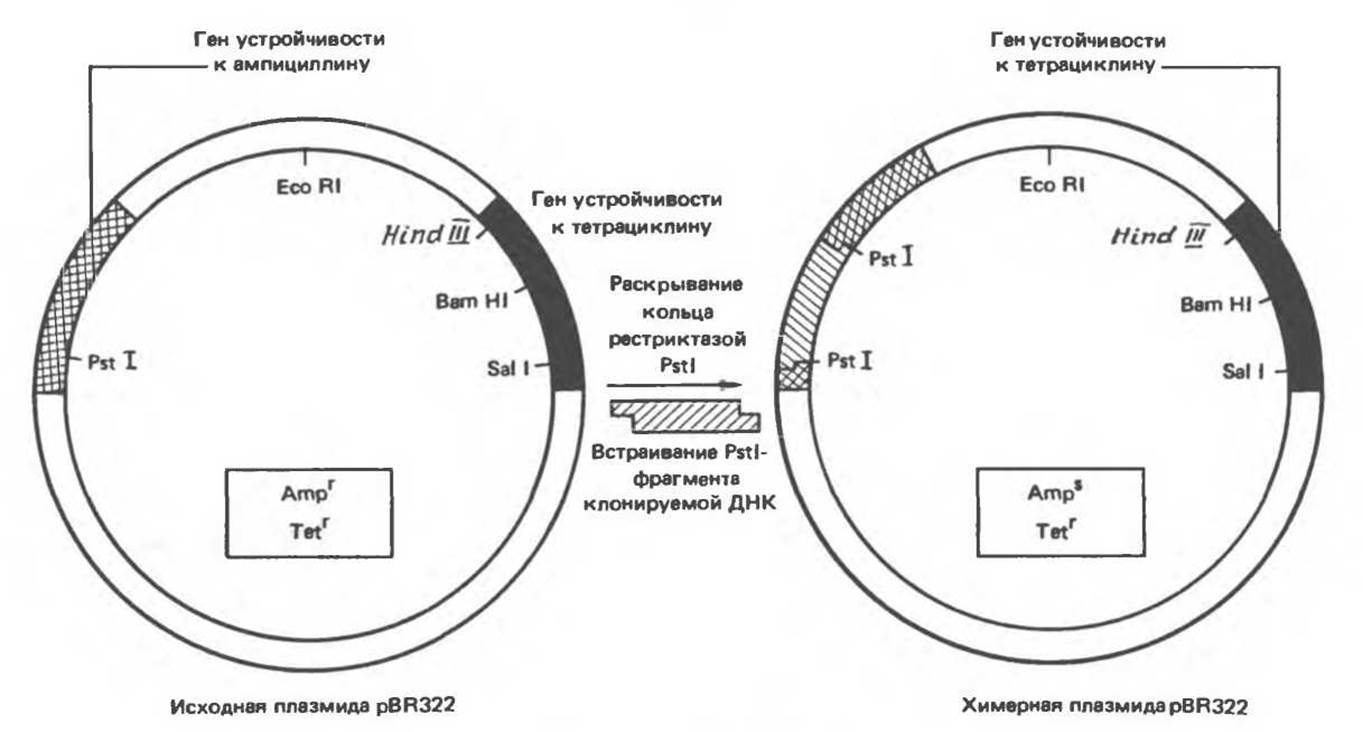
Рис. 36.4. Метод выявления рекомбинантных молекул ДНК. Фрагмент ДНК встроен в уникальный Pst 1-сайт плазмиды pBR322. «Вставка» инактивирует ген, кодирующий белок, который обеспечивает устойчивость бактерии-хозяина к ампициллину. Следовательно, бактериальные клетки, несущие рекомбинантную ДНК, не способны формировать колонии на среде, содержащей этот антибиотик. Используя для анализа трансформантов среды с тетрациклином и ампициллином, можно отобрать клоны, несущие рекомбинантные плазмиды.
Библиотека кДНК готовится в несколько этапов. Сначала выделяют тотальную мРНК ткани, а затем с помощью обратной транскриптазы и ДНК-полимеразы проводят обратную транскрипцию мРНК в двухцепочечную ДНК. По техническим причинам редко удается получить полноразмерную копию мРНК (кДНК). Как правило, клонируются более короткие ее фрагменты. Для этой работы обычно используют плазмиды, так как работать с ними легче, чем с фаговыми и космидными векторами. Впрочем, существует целый класс векторов — лямб-доидные фаги, — специально предназначенных для клонирования кДНК (см. ниже).
Векторы, обеспечивающие синтез белка, кодируемого клонированным геном, называют экспрессирующими. Такие векторы широко используют для выявления специфических кДНК молекул в кДНК-библиотеке, а также для наработки генноинженерных белков. Специально сконструированные экспрессирующие векторы имеют, как правило, сильный индуцибельный промотор, кодоны инициации трансляции для всех возможных рамок считывания, терминаторы транскрипции и трансляции и, если необходимо, определенные сигналы процессинга белка. Некоторые экспрессирующие векторы содержат гены ингибиторов протеаз, что увеличивает выход продукта экспрессируемого гена. Для конструирования библиотек кДНК весьма часто используется вектор λgt 11. Этот вектор позволяет клонировать достаточно длинные фрагменты кДНК и вместе с тем обеспечивает транскрипцию и трансляцию клонированных генов. Для скрининга кДНК-библиотек, полученных на основе вектора λgt 11, пригодны как кДНК-зонды, так и специфические антитела.
Таблица 36.4. Состав представительных геномных библиотек 11
|
Источник |
Представительная геномная библиотека |
|
Е. coli |
1500 фрагментов |
|
Дрожжи |
4500 фрагментов |
|
Дрозофила |
50000 фрагментов |
|
Млекопитающие |
800000 фрагментов |
1) Число фрагментов (независимых клонов), необходимое для создания библиотеки, гарантированно представляющей все уникальные гены, обратно пропорционально среднему размеру клонируемых фрагментов и прямо пропорционально общему количеству генов данного организма. Числа, приведенные выше, даны для библиотек с 99%-ной вероятностью представляющих полный геном при размере клонируемых фрагментов 2∙104 пар нуклеотидов. Различия в необходимом числе индивидуальных клонов отражают различную степень сложности геномов соответствующих организмов.
Число необходимых клонов рассчитывается по формуле
![]()
где Р — желаемая вероятность, a f — доля тотального генома в индивидуальном клоне. Для млекопитающих, характеризующихся сложностью гаплоидного генома 3∙109, это уравнение будет выглядеть следующим образом:
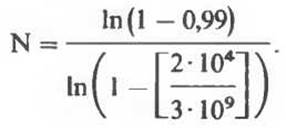
Преимущество библиотек, сконструированных на основе «вставок» большого размера, становится очевидным, если произвести соответствующие вычисления для гипотетической вставки со средним размером 5∙103 вместо 2∙104.
Зонды
Для выявления специфического клона в составе геномных или кДНК-библиотек, а также при количественном определении ДНК или РНК используются различные типы молекулярных зондов. Как правило, зонды (пробы) — это фрагменты ДНК или РНК, содержащие меченые 32Р-нуклеотиды. Работа с зондами основана на способности последних «узнавать» комплементарные последовательности в молекулах ДНК или РНК. кДНК, синтезированная на матрице специфической мРНК, может быть использована в качестве зонда при скринировании библиотеки кДНК и геномной библиотеки. Один из наиболее распространенных методов поиска специфических последовательностей основан на применении синтетических олигонуклеотидов, последовательность нуклеотидов в которых подбирается по аминокислотной последовательности небольшого участка искомого белка с учетом вырожденности кода. При условии точного совпадения последовательности, длины олигонуклеотидного зонда в 15—20 звеньев оказывается достаточно для достоверной гибридизации и обнаружения уникального гена. кДНК-зонды используются также для выявления после электрофореза специфических фрагментов ДНК или РНК и переноса их на нитроцеллюлозный фильтр (методы «Саузерн-блоттинга» и «Нозерн-блоттинга» соответственно).
Блоттинг и техника гибридизации
Для визуализации специфического фрагмента ДНК или РНК среди тысяч других «примесных» молекул используется комбинация целого ряда экспериментальных приемов, которые в совокупности получили название «блоттинг». На рис. 36.5 показаны схемы проведения Саузери-блоттинга (для визуализации фрагментов ДНК), Нозерн-блоттинга (для РНК) и Вестерн-блоттинга (для белков). Первая процедура названа по имени автора методики, остальные возникли как лабораторный жаргон, но со временем стали общепринятыми терминами. Первая методика полезна при определении количества копий гена (копийности) в данной ткани или при выявлении значительных структурных изменений в генах (делеции, вставки или перегруппировки). Иногда даже удается выявить точковую мутацию, если она затрагивает сайт рестрикции. Нозерн- и Вестернразновидности блоттинга используются для определения молекулярных размеров и количества специфических РНК и белковых молекул.
Для идентификации и выделения интересующих исследователя клонов разработан метод гибридизации в бактериальных колониях или фаговых бляшках. На колонии бактерий, выращенные на твердой среде, сначала накладывают нитроцеллюлозный фильтр. Бактерии прилипают к фильтру. После лизиса и денатурации под действием NaOH и фиксирования денатурированной ДНК прогреванием фильтр инкубируют в растворе с радиоактивно меченным зондом. По окончании гибридизации фильтр отмывают от избытка зонда и выявляют образовавшийся меченый гибридный комплекс путем контакта с рентгеновской пленкой. Сравнивая положение пятна на радиоавтографе с положением колоний на чашке, выбирают ту из них, которая дала положительный сигнал. Аналогичным образом поступают и при идентификации клонов на основе фаговых векторов. Результатом этих манипуляций является выделение искомых индивидуальных клонов (бактериальные колонии или фаговые бляшки).
Все разновидности методов гибридизации, рассмотренные в этой главе, базируются на вышеупомянутых специфических взаимодействиях пар оснований комплементарных цепей нуклеиновых кислот. Точное соответствие последовательностей гибридизующихся фрагментов приводит к быстрому образованию прочного комплекса, устойчивого к высокой температуре в ходе гибридизации и отмывки. Такие комплексы устойчивы также и при низкой концентрации соли. Комплексы, образующиеся при относительно более слабом соответствии структуры цепей, в «жестких» условиях (высокая температура или низкая концентрация соли) менее устойчивы. При этом гибридизация либо не происходит вовсе, либо гибридный комплекс разрушается при отмывке. Генные семейства, у которых наблюдается некоторая степень гомологии, можно выявить варьированием условий гибридизации и отмывки. Этот же подход применяется и при сравнении аналогичных генов разного видового происхождения.
Определение последовательности ДНК (секвенирование)
В настоящее время разработаны методы определения полной нуклеотидной последовательности ДНК (рис. 36.6). При решении этой задачи необходимо иметь большое количество идентичных молекул ДНК. Наработку интересующей последовательности можно осуществить клонированием соответствующего фрагмента. Проиллюстрированный на рис. 36.6 метод секвенирования по Максаму-Гилберту основан на химическом расщеплении ДНК по определенному основанию. Другой ферментативный метод — метод Сэнгера — базируется на применении аналогов нуклеотидов, прерывающих синтез комплементарной цепи ДНК по одноцепочечной матрице в месте встраивания в цепь соответствующего аналога.
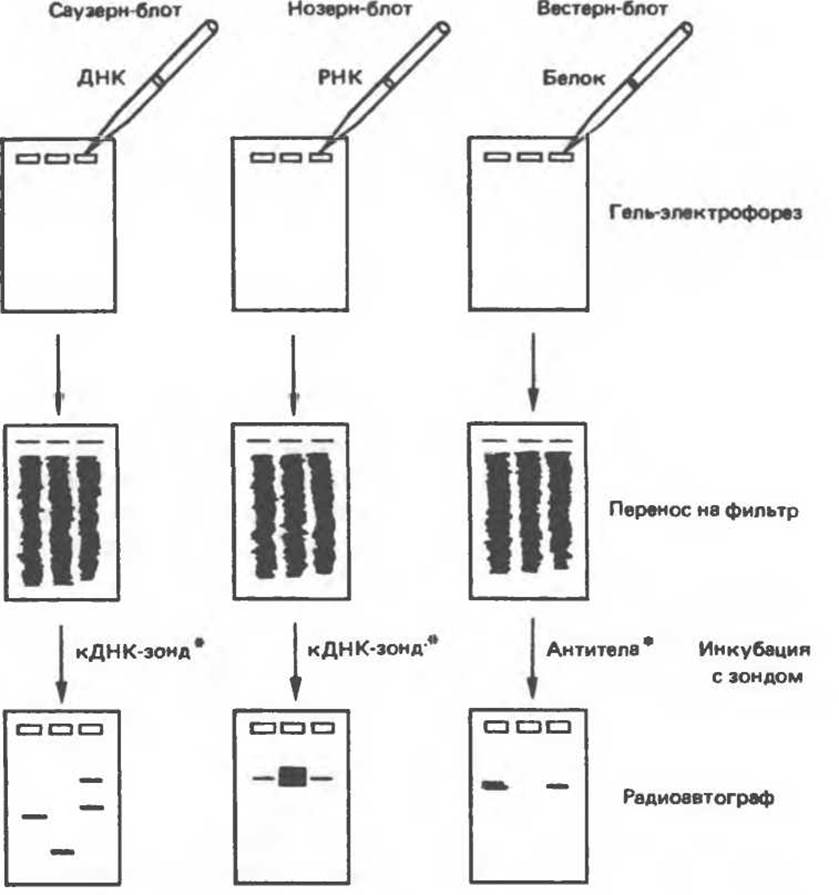
Рис. 36.5. Блоттинг-перенос. По методу Саузерна тотальную ДНК, выделенную из культуры клеток или ткани, обрабатывают одной или несколькими рестриктазами и полученную смесь фрагментов подвергают электрофорезу в агарозном или полиакриламидном геле. ДНК, несущая отрицательный заряд, мигрирует к аноду. Небольшие фрагменты двигаются быстрее крупных. После окончания электрофореза разделенные фрагменты ДНК подвергают мягкой денатурации, инкубируя гель в растворе щелочи. На следующем этапе гель накладывают на нитроцеллюлозный фильтр. Фрагменты ДНК переносят на нитроцеллюлозу с помощью методических приемов, разработанных Саузерном, и фиксируют полученную нитроцеллюлозную реплику тепловой обработкой. Далее реплику инкубируют с меченым кДНК-зондом, гибридизующимся с соответствующим комплементарным фрагментом ДНК на нитроцеллюлозном фильтре. После интенсивной промывки фильтр помещают на рентгеновскую пленку. Фиксируемые на радиоавтографе сигналы соответствуют расположению фрагментов ДНК, комплементарных последовательности зонда. Метод Нозерн-блот (для анализа РНК) принципиально не отличается от метода переноса по Саузерну (Саузерн-блот анализа). Тотальную РНК подвергают электрофорезу. Сама процедура переноса РНК из геля на фильтр несколько отличается от метода Саузерна, поскольку молекулы РНК менее стабильны, чем молекулы ДНК. Метод Вестерн-блот применяется для выявления определенных белков с помощью специфических антител или других молекулярных зондов.