Биохимия - Химические реакции в живой клетке Том 2 - Д. Мецлер 1980
Ферменты: белковые катализаторы клеток
Основы ферментативной кинетики
Для того чтобы измерить скорость химической реакции, необходимо прежде всего «запустить» эту реакцию в определенное время (например, быстро смешав реагенты), а затем при строго фиксированных значениях температуры и pH (что очень важно) измерить концентрацию реагента или продукта через определенный промежуток (или промежутки) времени. Исследователи проявили чудеса изобретательности, создав огромное число разнообразных способов регистрации кинетических кривых для отдельных ферментов. Какой бы метод ни использовал экспериментатор, его интересует скорость, с которой изменяется во времени концентрация некоторого вещества. Весьма часто исследователь строит кинетическую кривую, представляющую собой временную зависимость концентрации реагента (субстрата) [S] или продукта [Р] (рис. 6-1).
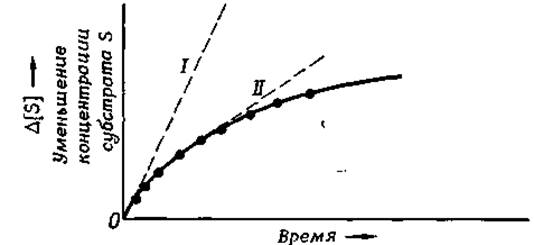
РИС. 6-1. Кинетическая кривая для ферментативной реакции, в ходе которой субстрат S превращается в продукты. І — касательная, наклон которой соответствует начальной скорости реакции; II — касательная к кривой в точке, соответствующей ненулевому моменту времени; наклон этой прямой меньше наклона касательной, проведенной в точке t = 0.
Скорость ферментативной реакции v определяется следующим образом:
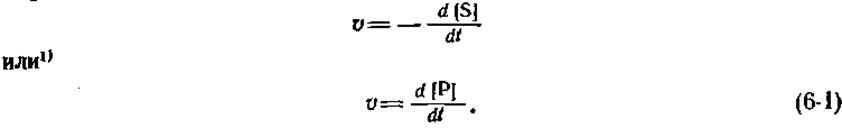
Скорость химической реакции выражают обычно в моль∙(л∙с)-1 (или М∙с-1), а энзимологии чаще пользуются размерностью моль∙(л∙мин)-12). Мгновенная скорость, которая обычно интересует исследователя, определяется наклоном касательной к кинетической кривой в данной точке (рис. 6-1).
Начальная скорость реакции — это скорость в нулевой момент времени. В некоторых случаях (например, для кривой, представленной на рис. 6-1) найти начальную скорость с достаточной точностью довольно сложно.
Для ряда химических реакций, например для процессов первого порядка, график кинетической кривой в полулогарифмическом масштабе (т. е. график зависимости lg[S] от l) представляет собой прямую, поэтому необходимость в определении наклона касательной в нулевой момент времени отпадает. Однако в большинстве случаев определение активности проводят таким образом, чтобы получить приблизительно линейную кинетическую кривую (по крайней мере для коротких временных интервалов). Зачастую при этом возникает необходимость в использовании очень чувствительных методов определения содержания продукта. Вот почему в опытах такого рода весьма широко применяют радиоактивные субстраты.
1) Следует отметить, что равенство скоростей расходования субстрата и накопления продукта справедливо лишь при стационарных условиях (разд. А,5).
2) Для выражения скорости следует всегда использовать интенсивные параметры (например, M∙c-1), а не экстенсивные (например, мкмоль∙с-1 без указания объема раствора).
Заметим, что, когда кинетическая кривая не является прямой с самого начала и когда за меру скорости принимают количество соединения, прореагировавшего за определенный промежуток времени, можно получить неверные оценки. Иногда используют интегральную форму уравнения скорости, описывающую накопление продукта во времени. Существуют и другие приемы для сопоставления относительных скоростей, пригодные даже для кинетической кривой, приведенной на рис. 6-1.