Биохимия - Химические реакции в живой клетке Том 2 - Д. Мецлер 1980
Биосинтез; как образуются новые молекулы
Полипренильные (изопреноидные) соединения
Каротины и их производные
Хотя до сих пор окончательно не доказано, что каротины синтезируются из фитоена, но, по-видимому, дело должно обстоять именно таким образом. На рис. 12-14 показаны пути образования ликопена, красного пигмента томатов, ß-каротина и других веществ, производных этих соединений. Обратите внимание, что структура ликопена представляет собой целиком транс-форму и процесс десатурации осуществляется путем потери атомов водорода, находящихся в транс-положении. Десатурация протекает в несколько этапов, причем известны многие промежуточные продукты с меньшим числом двойных связей. Замыкание колец на концах молекулы ликопена легче всего себе представить [уравнение (12-29)] по механизму кислотного катализа с промежуточным образованием карбоний-иона. Потеря одного или другого из двух протонов, примыкающих к положительно заряженному атому, приводит к образованию соответственно ß-кольца ß-каротина или a-кольца а-каротина [88] г
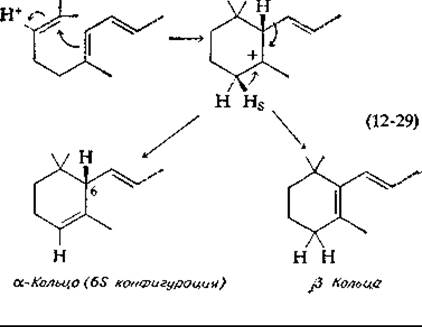
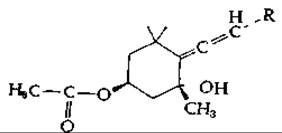
В ходе различных реакций каротины могут подвергаться гидроксилированию и другим модификациям. Структура одного из образующихся при этом ксантофиллов — зеаксантина — приведена на рис. 12-14. Читатель найдет там же структуру бурого пигмента диатомовых водорослей — фукоксантина. Обратите внимание, что один конец молекулы фукоксантина содержит эпоксид, образовавшийся под действием кислорода; другой конец несет редко встречающуюся в природе структуру — аллен. (При этом в количественном отношении фукоксантин является, вероятно, самым распространенным каротиноидом [88].) Ниже мы приводим структуру алленсодержащего конца молекулы фукоксантина (в перевернутом виде по сравнению с изображением на рис. 12-14). Обратите внимание, что на рис. 12-14 стереохимия алленовой группировки изображена не совсем правильно, а именно присоединенная к ней каротиноидная цепь R1должна выступать позади кольца, как это показано ниже:
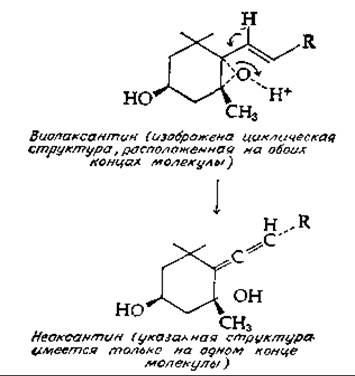
Другой каротиноид из водорослей — виолаксантин — содержит эпоксидные группы в циклических структурах на обоих концах молекулы. В присутствии изомеразы виолаксантин превращается [уравнение (12-30)] в неоксантин — еще одно соединение, предположительно содержащее (на одном конце) алленовую структуру. При последующем ацетилировании этого соединения образуется фукоксантин.
Некоторые каротиноиды водорослей содержат ацетиленовые тройные связи. Примером может служить аллоксантин, несущий на обоих концах, симметричной молекулы следующую структуру:
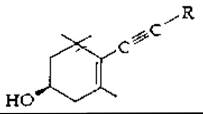
Приведенное описание касается только небольшого числа из многих описанных структурных модификаций каротиноидов [44, 78, 89].
Дополнение 12-В
Витамины: витамин А
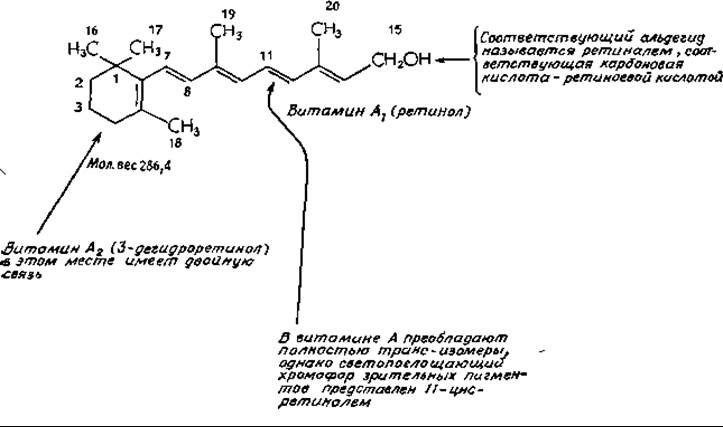
Витамин А был открыт в 20-х годах нашего столетия (дополнение 8-А); вскоре после этого он был выделен из жира печени рыба. Как витамин А, (ретинол), так и витамин А2, являются 20-углеродными полипрениловыми спиртами. Они образуются при расщеплении 40-углеродного ß-каротина (рис. 12-14) или других каротиноидов, содержащих одно ß-ионное кольцо. В то время как каротины — это продукты растительного происхождения, витамин А образуется только в тканях животных. Под действием оксигеназы углеродная цепь каротина расщепляется по центру с образованием альдегида витамина А — ретиналяб. Витамин А присутствует в тканях как в виде свободного спирта, так и в виде эфиров пальмитиновой и других жирных кислот. Это один из немногих витаминов, который может накапливаться в организме животных в относительно больших количествах. Он накапливается в основном в виде ретинилпальмитата в особых запасающих жиры клетках печенив.
Недостаточность витамина А проявляется различными симптомами, такими, как сухость кожи и волос, задержка роста, конъюнктивит и низкая сопротивляемость к инфекции. Примечательным ранним признаком А-авитаминоза является куриная слепота. Признаки поражения покровных тканей наиболее выражены в слизистых нижнего отдела дыхательных путей и пищеварительного тракта. Потребность взрослого человека в витамине А составляет около 0,7 мг/день. Содержание витамина А в пище часто выражают в международных единицах: 1 мг ретинола соответствует 3333 М. Ед.
Твердо установлено участие витамина А в виде ретиналя в зрительной функции (гл. 13, разд. Е, 2); по-видимому, он играет также определенную роль в процессе репродукции. При недостаточности витамина А у самцов не образуется сперматозоидов, а у самок происходит резорбция плода, Крысы, получающие с пищей вместо витамина А ретиноевую кислоту, постепенно становятся слепыми и бесплодными, но в остальном остаются здоровымиг. По-видимому, для репродуктивной функции необходима спиртовая или альдегидная форма, тогда как для роста костей и поддержания нормальной секреторной функции слизистых оболочек требуется только ретиноевая кислотад.
Эпителий внутренних органов, содержащих как специальные секретирующие слизь клетки, так и ресничные клетки, при недостаточности витамина А покрывается толстым слоем кератинизированных слущивающихся клеток, подобных тем, которые покрывают наружные поверхности тела. При этом резко снижается образование гликопептидов, содержащих фукозуе. Было показано, что при добавлении ретинилацетата в культуру клеток эпидермиса в них увеличивается содержание РНКЖ. Эффект становится еще более выраженным в присутствии инсулина и глюкокортикоидов. Эти данные показывают, что ретиноевая кислота или ее метаболиты служат, по-видимому, регуляторными факторами, под действием которых происходит превращение недифференцированных клеток эпителия в секреторные клетки слизистой. Другая форме витамина А, вероятно, оказывает аналогичное действие на репродуктивные ткани. По всей вероятности, в осуществлении указанных регуляторных функций участвует контроль транскрипции РНК. Стероидные гормоны и производные витамина А функционируют, видимо, сходным образом, «включая» или «выключая» гены, контролирующие синтез определенных белков.
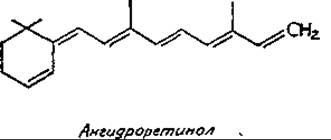
Химический механизм действия витамина А остается нерасшифрованным. Можно предположить, что ретиналь образует шиффовы основания с аминогруппами белков, как это происходит в зрительных пигментах. Нельзя исключить возможного участия ретиналя в окислительно-восстановительных реакциях. В присутствии НСl протекает неферментативное превращение ретинола в ангидроретинол путем отщепления молекулы воды; при этом остается система сопряженных связей. Ангидроретинол встречается в природе, но биологической активностью, по-видимому, не обладает:
В плазме крови витамин А транспортируется в комплексе с особым ретинолсвязывающим белком (мол. вес — 21 000). Этот белок обычно почти полностью насыщен ретинолом и связан с другим белком сыворотки — преальбуминомз,к. Во многих тканях присутствуют также ретинолсвязывающие белки и, кроме того, белки, связывающие ретиноевую кислотук. Имеются данные, что для поддержания нормального содержания витамина А в плазме крови необходим цинкл.
а Moore Т., Vitamin A, Elsevier, Amsterdam, 1957.
б Olson J. A., Vitam. Horm. (N. Y.), 26, 1—63 (1968).
в Kobayashi K., Takahashi Y., Shibasaki S., Nature (London), New Biol., 243, 186—188 (1973).
г Smith J. E., Milch P. O., Muto Y., Goodman D. S., BJ, 132, 821—827 (1973).
д Clamon G. H., Sporn M. B., Smith J. M., Saffiotti V., Nature (London), 250, 64—66 (1974).
е DeLuca L., Schumacher M., Wolf G., JBC, 245, 4551—4558 (1970).
ж Sporn M. В., Dunlop N. М., Yuspa S. H., Science, 182, 722—723 (1973).
з Vahlquist A., Peterson P. A., Biochemistry, 11, 4526—4532 (1972).
и Muto Y., Smith J. E., Milch P. O., Goodman D. S., JBC, 247, 2542—2550 (1972).
к Ong D. E., Chytil F., JBC, 250, 6113—6117 (1975).
л Smith I. C., Jr., McDaniel E. G., Fan F. F., Halsted J. A., Science, 181, 954—955 (1973).