БІОХІМІЯ - Підручник - Остапченко Л. І. - 2012
Розділ 5. БУДОВА, ВЛАСТИВОСТІ Й ФУНКЦІЇ БІЛКІВ
5.6.Різноманітність білків і їхня класифікація
5.6.1. Класифікація білків за формою молекул
Однією з найстаріших класифікацій, яка поділяє білки на дві групи (глобулярні та фібрилярні), є класифікація за формою молекул. До глобулярних належать білки, співвідношення поздовжньої та поперечної осей яких не перевищує 1 : 10, а найчастіше становить 1 : 3 або 1: 4, тобто білкова молекула має форму еліпса. Більшість індивідуальних білків людини належить до глобулярних білків. Вони мають компактну структуру і багато з них, за рахунок переміщення гідрофобних радикалів всередину молекули, добре розчинні у воді. Наочні приклади будови й функціонування глобулярних білків (гемоглобін і міоглобін) наведено вище.
Фібрилярні білки мають витягнуту, ниткоподібну структуру, в якій співвідношення поздовжньої та поперечної осей становить 1 : 10. До фібрилярних білків належать колагени, еластин, кератин, які виконують в організмі структурну функцію, а також міозин, що бере участь у м'язовому скороченні, та фібрин - білок системи згортання крові. На прикладі колагенів і еластину розглянемо особливості будови цих білків і зв'язок їхньої будови з функціями.
Колагени - родина фібрилярних білків, які секретуються клітинами сполучної тканини. Колагени є найпоширенішими білками не тільки міжклітинного матриксу, але й організму в цілому, вони становлять 1/4 усіх білків організму людини. У міжклітинному матриксі молекули колагену утворюють полімери, що називаються фібрилами колагену. Фібрили колагену дуже міцні і практично не- розтяжні. Вони здатні витримувати навантаження в 10 000 разів більше за їхню власну вагу. За міцністю колагенові фібрили перевищують міцність сталевого дроту того ж діаметра. Саме тому велика кількість колагенових волокон, що складаються з колагенових фібрил, входять до складу шкіри, сухожилля, хрящів і кісток.
Незвичайні механічні властивості колагенів пов'язані з їхньою первинною та просторовою структурами. Молекули колагену складаються з трьох поліпептидних ланцюгів, їх називають α-ланцюгами. Ідентифіковано понад 20 α-ланцюгів, більшість яких має у своєму складі 1000 амінокислотних залишків, але ланцюги дещо відрізняються амінокислотною послідовністю. До складу колагенів можуть входити три однакові або різні ланцюги.
Первинна структура α-ланцюгів колагену є особливою, тому що кожна третя амінокислота у поліпептидному ланцюзі представлена гліцином, близько 1/4 амінокислотних залишків становить пролін або 4-гідроксипролін, близько 11 % - аланін. У колагені відсутні такі амінокислоти, як цистеїн і триптофан, а гістидин, метіонін і тирозин містяться лише в дуже невеликих кількостях. У складі первинної структури α-ланцюга колагену міститься також незвичайна амінокислота - гідроксилізин. Поліпептид- ний ланцюг колагену можна зобразити як послідовність триплетів Глі-X-Y, де Х та Y можуть бути будь-якими амінокислотами, але найчастіше в положенні Х стоїть пролін, а в положенні Y - гідроксипролін або гідроксилізин. Кожна з цих амінокислот має велике значення для формування колагенових фібрил.
Пролін завдяки своїй структурі зумовлює вигини в поліпептид- ному ланцюзі, стабілізуючи лівозакручену спіральну конформацію. На один оберт спіралі припадає 3 амінокислотні залишки, а не 3,6, як це характерно для вторинної структури глобулярних білків. Спіраль пептидного ланцюга колагену стабілізована не за рахунок водневих зв'язків (тому що пролін їх не утворює), а силами стеричного відштовхування піролідинових кілець у залишках проліну. У результаті відстань між амінокислотними залишками по осі спіралі збільшується, і вона виявляється більш розгорнутою порівняно зі щільно скрученою α-спіраллю глобулярних білків.
Спіралізовані поліпептидні ланцюги, сплітаючись один з одним, утворюють триланцюгову правозакручену суперспіральну молекулу, яку часто називають тропоколагеном (рис. 5.40). Ланцюги утримуються поруч за рахунок водневих зв'язків, котрі виникають між аміно- та карбоксильними групами пептидного каркасу різних поліпептидних ланцюгів, що входять до складу триспіральної молекули. "Жорсткі" амінокислоти - пролін і гідроксипролін - обмежують обертання поліпептидного стержня, збільшуючи тим самим стабільність потрійної спіралі. Гліцин, який замість радикала має атом водню, завжди розташований у місці перехрещення ланцюгів; відсутність радикала дозволяє ланцюгам щільно прилягати один до одного.
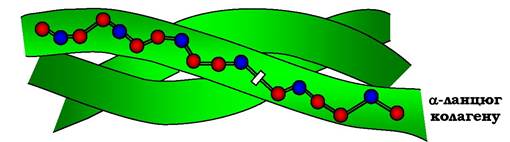
Рис. 5.40. Будова молекули тропоколагену (фрагмент)
У результаті такого скручування пептидних каркасів поліпеп- тидних ланцюгів і наявності видовженої структури два інші радикали з тріади амінокислот Глі-Х-Y опиняються на зовнішній поверхні молекули тропоколагену. Деякі комплементарні ділянки молекул тропоколагену можуть об'єднуватися одна з одною, формуючи колагенові фібрили, причому ці ділянки розміщені таким чином, що одна нитка тропоколагену зсунута відносно іншої приблизно на 1/4 (рис. 5.41). Між радикалами амінокислот виникають іонні, водневі та гідрофобні зв'язки.
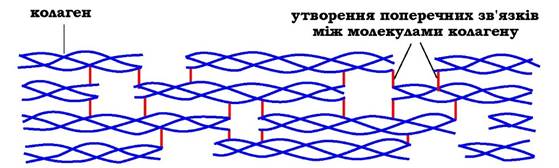
Рис. 5.41. Будова колагенової фібрили (фрагмент)
Важливу роль у формуванні колагенових фібрил відіграють модифіковані амінокислоти - гідроксипролін і гідроксилізин. Гідроксильні групи гідроксипроліну сусідніх ланцюгів тропокола- гену утворюють водневі зв'язки, які зміцнюють структуру колагенових фібрил. Радикали лізину та гідроксилізину необхідні для утворення міцних поперечних зшивок між молекулами тропоколагену, котрі ще більше зміцнюють структуру колагенових фібрил. Крім того, до гідроксильної групи гідроксилізину можуть приєднуватися вуглеводневі залишки (глікозилювання колагену), функція яких є поки що незрозумілою.
Отже, амінокислотна послідовність поліпептидних ланцюгів колагену дозволяє сформувати унікальну за своїми механічними властивостями структуру, яка надзвичайно міцна. Зміни в первинній структурі колагену можуть зумовлювати розвиток спадкових хвороб.
На відміну від колагену, що утворює міцні фібрили, здатні витримати великі навантаження, еластин (також білок міжклітинного матриксу) наділений гумоподібними властивостями. Нитки еластину, які містяться у тканинах легень, у стінках судин, в еластичних зв'язках, можуть розтягатися в декілька разів порівняно з їхньою звичайною довжиною, але після зняття навантаження вони повертаються до згорнутої конформації.
Еластин містить близько 800 амінокислотних залишків, серед яких переважають амінокислоти з неполярними радикалами, такі як гліцин, валін, аланін. В еластині є досить багато проліну та лізину, але зовсім небагато гідроксипроліну; гідроксилізин повністю відсутній.
Наявність великої кількості гідрофобних радикалів перешкоджає створенню стабільної глобули, через що поліпептидні ланцюги еластину не формують регулярну вторинну і третинну структури, а набувають у міжклітинному матриксі різних конформацій із приблизно однаковою вільною енергією (рис. 5.42). Це саме той випадок будови первинної структури, коли відсутність однієї стабільної впорядкованої конформації приводить до виникнення необхідних білку властивостей.
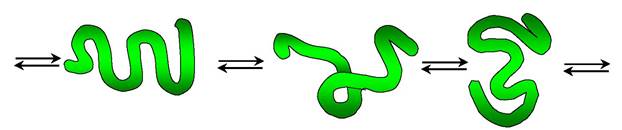
Рис. 5.42. Випадкові конформації молекули еластину