БІОХІМІЯ - Підручник - Остапченко Л. І. - 2012
Розділ 6. ОБМІН І ФУНКЦІЇ АМІНОКИСЛОТ. БІОСИНТЕЗ БІЛКА
6.8. Обмін окремих амінокислот
6.8.1.Обмін серину та гліцину
Серин - замінна амінокислота, що синтезується з проміжного продукту гліколізу - 3-фосфогліцерату, отримуючи аміногрупу від глутамінової кислоти.
Гліцин - також замінна амінокислота, основним джерелом її є серин. Реакцію синтезу гліцину із серину каталізує фермент серинксиметилтрансфераза, коферментом якої є H4-фолат:
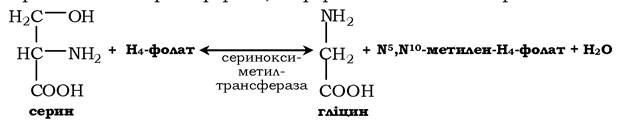
Реакція перетворення серину в гліцин є оборотною. Основний шлях катаболізму гліцину в людини та інших хребетних також пов'язаний з використанням H4-фолату:
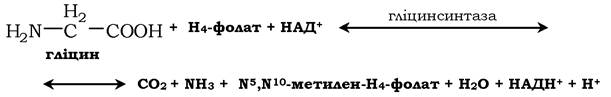
Реакція є оборотною й каталізується гліцинсинтазою - ферментним комплексом, схожим на піруватдегідрогеназний комплекс, локалізований у мітохондріях клітин печінки. За останніми даними гліцинрозщеплювальна ферментна система дещо відрізняється від гліцинсинтази і має чотири білки: Р-білок, має у складі кофермент ПФ, Н-білок, що містить ліпоєву кислоту, Т-білок, коферментом якого є Н4-фолат, L-білок, який є дигідроліпоїлдегідрогена- зою з коферментом НАД+.
Амінокислоти серин і гліцин виконують в організмі людини різноманітні й дуже важливі функції. Роль серину та гліцину в синтезі багатьох біологічно важливих сполук показано на рис. 6.24.
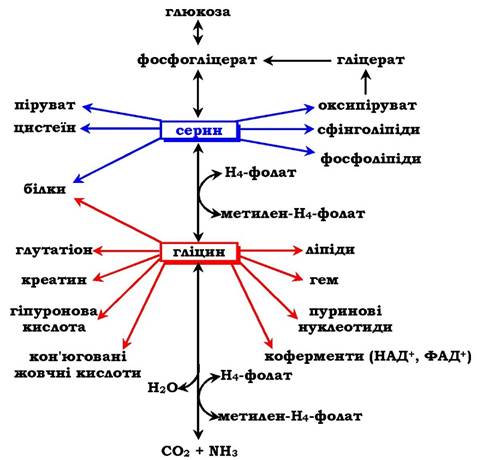
Рис. 6.24. Біологічна роль серину та гліцину
На рисунку видно, що обидві амінокислоти необхідні не тільки для синтезу білків і глюкози (у разі її недостатності в клітині), але й нуклеотидів, коферментів, гему, складних ліпідів, креатину та інших сполук. Багато з цих реакцій будуть представлені у відповідних розділах підручника.
У перетвореннях серину та гліцину головну роль відіграють ферменти, коферментами яких є похідні фолієвої кислоти. Цей вітамін дуже поширений у тваринних і рослинних харчових продуктах. Молекула фолієвої кислоти (фолату) складається з трьох частин: птеринового похідного, параамінобензойної та глутамінової кислот:
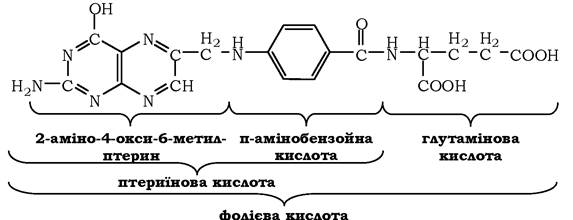
Фолієву кислоту (фолат) називають також птероїлглутаміновою кислотою. Птерини дуже поширені в природі. Деякі з них, наприклад ксантоптерин, є пігментами очей і крил комах (метеликів).
Коферментну функцію виконує відновлена форма фолату тетрагідрофолієва кислота (ТГФК, або H4-фолат):
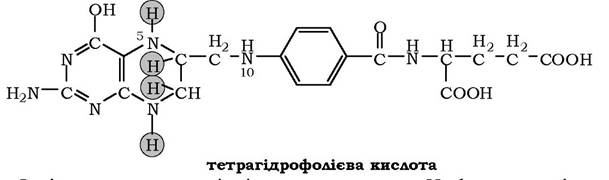
Фолієва кислота в печінці перетворюється в H4-фолат у декілька стадій за участю ферментів фолатредуктази та дигідрофолатредуктази, коферментом яких є НАДФН.
H4-фолат - акцептор β-вуглецевого атому серину. При цьому утворюється метиленовий місток між атомами азоту в молекулі H4-фолату в положеннях 5 і 10, утворюючи метилен-H4-фолат:
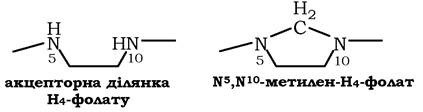
Особливе значення реакцій катаболізму серину і гліцину полягає в тому, що вони супроводжуються утворенням одновуглецевого метиленового фрагмента (-СH2-). Метиленова група в моле кулі метилен-H4-фолату може перетворюватись в інші одновуглецеві групи (фрагменти): метенільну, формільну, метильну та форміміногрупу (рис. 6.25).
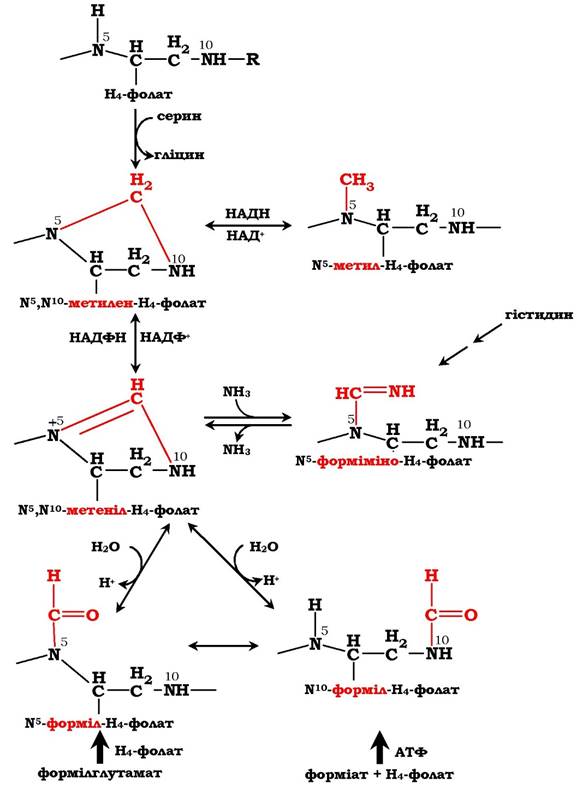
Рис. 6.25. Утворення похідних Н4-фолату
Існує ще одне джерело формільного та форміміного фрагментів - гістидин. Катаболізм гістидину відбувається переважно в печінці (дуже малий відсоток у шкірі) у результаті наступних реакцій:
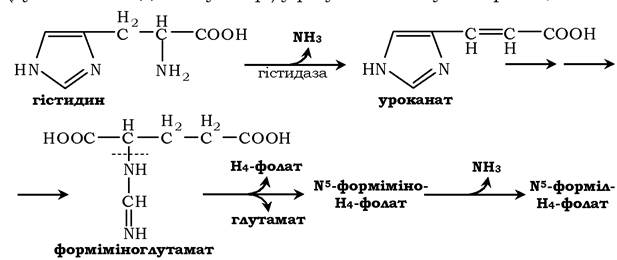
Кінцевими продуктами катаболізму гістидину є глутамат, NH3 і одновуглецеві фрагменти - форміміно- H4-фолат і форміл- H4-фолат.
Усі утворені похідні H4-фолату відіграють роль проміжних переносників і є донорами одновуглецевих фрагментів під час синтезу деяких сполук: пуринових основ і тимідилової кислоти, які необхідні для синтезу ДНК і РНК, регенерації метіоніну, синтезі різноманітних формімінопохідних (форміміногліцину тощо) (рис. 6.26). Отже, перенесення одновуглецевих фрагментів до акцептора необхідне для синтезу ряду сполук і для регенерації вільного H4-фолату в печінці.
Фолієва кислота є вітаміном для людини і тварин. Але багато патогенних бактерій здатні синтезувати цю сполуку, використовуючи параамінобензойну кислоту (ПАБК) - одну зі складових частин фолату. ПАБК надходить у бактеріальні клітини із зовнішнього середовища. Сульфаніламідні лікарські препарати - похідні сульфаніламіду (білого стрептоциду), схожі за будовою на параамінобензойну кислоту. Відрізняються вони тільки радикалами:
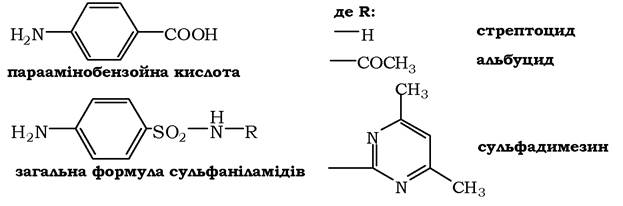
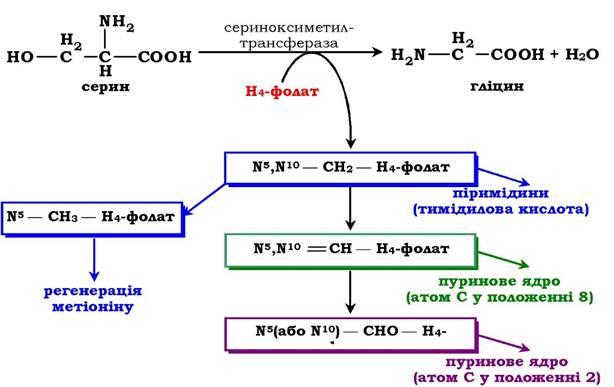
Рис. 6.26. Утворення та використання похідних Н4-фолату
Ці препарати пригнічують синтез фолієвої кислоти в бактерій оскільки:
✵ конкурентно інгібують бактеріальні ферменти синтезу фолату, тому що є структурними аналогами параамінобензойної кислоти - одного із субстратів процесу;
✵ можуть використовуватись як псевдосубстрати завдяки відносній субстратній специфічності ферментів, у результаті чого синтезується сполука, схожа на фолієву кислоту, проте не здатна виконувати її функції.
В обох випадках у клітинах бактерій порушується обмін одновуглецевих фрагментів і, відповідно, синтез нуклеїнових кислот, завдяки чому розмноження бактерій зупиняється. У клітинах хворого сульфаніламідні лікарські речовини не викликають схожих змін, оскільки людина отримує з їжею готову фолієву кислоту.
Нині відомо декілька захворювань, пов'язаних із порушеннями обміну гліцину. Причиною їх є недостатність деякого ферменту або дефект системи транспорту цієї амінокислоти. Наведемо деякі з цих порушень.
Гіпергліцинемія характеризується підвищеною концентрацією гліцину в крові внаслідок дефекту гліцинрозщеплювальної ферментної системи. Найтяжчим проявом гіпергліцинемії є стрімке пошкодження мозку, судоми, гіпотонія, порушення дихання.
Гліцинурія характеризується підвищеним виділенням гліцину із сечею (до 1 г/ добу) при нормальному вмісті його в крові. Один із симптомів цього захворювання - утворення оксалатних камінців у нирках, причому вміст оксалату в сечі - у межах норми. Надлишок оксалату має ендогенне походження. Найпевніше, він утворюється з гліцину, унаслідок дезамінування якого утворюється гліоксилат - попередник оксалату. Метаболічний ефект, напевне, полягає в порушенні метаболізму гліоксилату - неможливості перетворення його знову в гліцин через дефект гліцина- мінотрансферази. Причиною гліцинурії є, очевидно, порушення реабсорбції гліцину в нирках. Описана патологія спадкується як домінантна ознака, зчеплена, вірогідно, з Х-хромосомою.
Первинна гіпероксалатурія характеризується постійно високим виділенням оксалату з сечею, незалежно від надходження його з їжею. У подальшому прогресує двобічне утворення оксалатних камінців у сечовивідних шляхах, розвивається нефрока- льциноз та інфекція сечовивідних шляхів. Хворі гинуть у дитячому віці від ниркової недостатності або гіпертонії.