СОВРЕМЕННАЯ БОТАНИКА - П. РЕЙВН - 1990
РАЗДЕЛ I. РАСТИТЕЛЬНАЯ КЛЕТКА
ГЛАВА 3. МОЛЕКУЛЯРНЫЙ СОСТАВ КЛЕТОК
Белки
Белки, подобно полисахаридам, являются полимерами. Мономеры, образующие белки, — это азотсодержащие молекулы, называемые аминокислотами. В живых организмах обнаружено 20 аминокислот, однако в больших и сложных белковых молекулах (которые часто состоят из сотен аминокислот) число возможных последовательностей разных аминокислот огромно; отсюда — чрезвычайное разнообразие белковых молекул. Как будет показано ниже, аминокислотная последовательность определяет структуру, а, следовательно, и функцию каждого белка. Одна клетка бактерии Escherichia coli может содержать от 600 до 800 различных белков, а клетка растения или животного, вероятно, в несколько раз больше.
У растений самая высокая концентрация белков обнаружена в семенах (до 40% сухого веса). Эти белки выполняют запасную функцию; они используются зародышем после прорастания семени.
Аминокислоты
Схема аминокислоты приведена в подписи к рис. 3-14. Любая аминокислота состоит из аминогруппы и карбоксильной группы, присоединенных к атому углерода, который называется альфа-углеродом. R — это остаток молекулы, структура которого варьирует у разных аминокислот, и именно R- группа определяет их индивидуальность. На рис. 3-14 приведена структура 20 аминокислот, входящих в состав белков.
Аминокислоты можно сгруппировать на основе электрических зарядов, которые играют важную роль в определении свойств аминокислот и особенно образованных ими белков.
Рис. 3-14. Каждая аминокислота содержит аминогруппу (-NH2) и карбоксильную группу (-СООН), связанные с центральным углеродным атомом. К этому же атому присоединены атом водорода и боковая группа R, которая у каждой аминокислоты имеет свое строение. Общая формула аминокислот выглядит так:
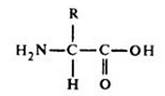
Двадцать аминокислот, входящих в состав белков, показаны слева и внизу. Можно видеть, что они имеют одинаковую структуру и отличаются только боковыми группами. В зависимости от свойств боковых групп аминокислоты подразделяют на неполярные, полярные незаряженные, отрицательно заряженные (кислотные) и положительно заряженные (основные). Неполярные молекулы нерастворимы в воде, а заряженные и полярные растворимы
Полипептиды
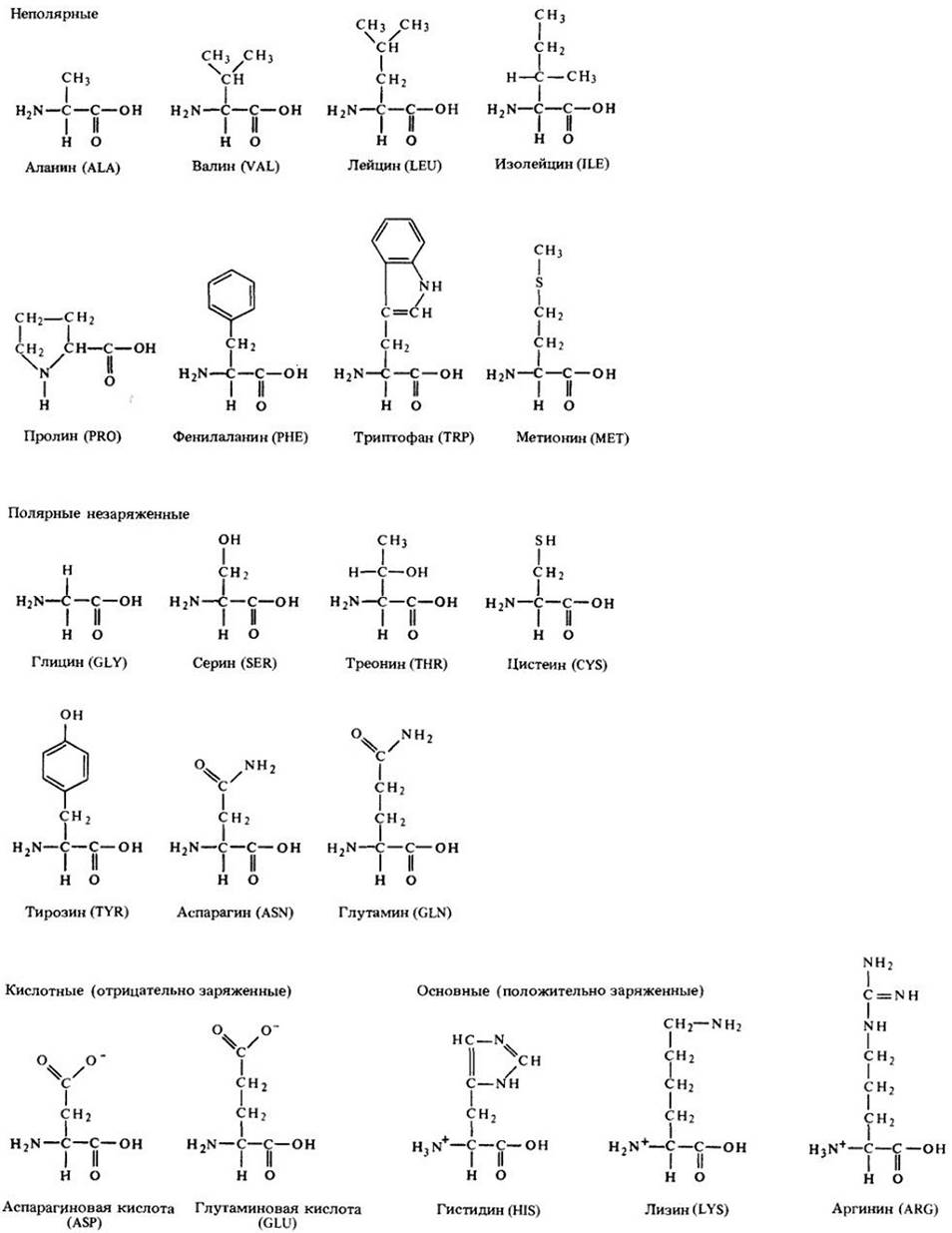
Цепь аминокислот называется полипептидом. Аминогруппа одной аминокислоты всегда соединяется с карбоксильной группой другой; при этом выделяется молекула воды. Образующаяся связь называется пептидной связью (рис. 3-15). Аминокислотные мономеры полипептида часто называют аминокислотными остатками. На одном конце цепи всегда присутствует свободная аминогруппа, на другом — свободная гидроксильная группа. Конец с аминогруппой называется N- концом, конец с карбоксильной группой — С-концом.
Рис. 3-15. Связи между аминокислотными остатками называются пептидньми. Они формируются при отщеплении молекулы воды, как и в случае полисахаридов. Связи, выделенные здесь цветом, всегда образуются между кар боксильной группой (-СООН) одной аминокислоты и аминогруппой (-NH2) соседней. Следовательно, основная структура белка — длинная неразветвленная цепь. Линейное расположение аминокислот называется первичной структурой белка. Конец цепи, несущий аминогруппу, называется N-концом, карбоксильную группу — С-концом
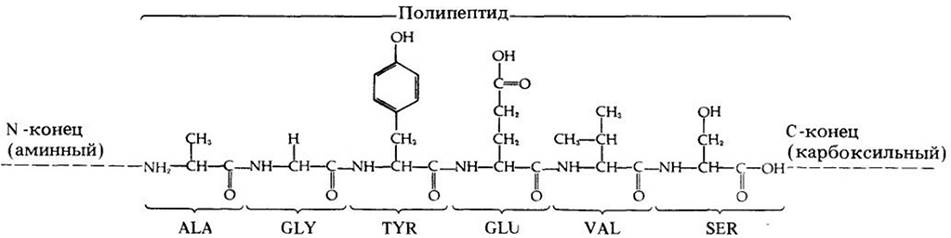
Аминокислоты могут соединяться поперечно ковалентными связями, возникающими между двумя атомами серы двух цистеиновых остатков (эти связи называют дисульфидными). Дисульфидная связь соединяет два цистеиновых остатка в одной полипептидной цепи или в двух различных цепях (рис. 3-16).
Рис. 3-16. Первичная структура фермента лизоцима (двумерная модель). Лизоцим — белок, содержащий 129 аминокислотных остатков, образующих полипептидную цепь, которая в четырех местах соединена дисульфидными связями (-S-S-)
Белки — крупные полипептиды. Их молекулярная масса колеблется от 104 до 106 и более. Для сравнения: молекулярная масса воды — 18, глюкозы — 180. (Средняя молекулярная масса аминокислотного остатка около 120, так что вы можете быстро определить примерное число аминокислот в белке на основании его молекулярной массы.)
Уровни организации белка
Последовательность аминокислот в полипептидной цепи определяет первичную структуру белка. Полипептидные цепи часто образуют спираль (вторичная структура), которая в свою очередь может быть уложена в глобулу (третичная структура). Наконец, несколько полипептидных цепей могут взаимодействовать между собой с образованием четвертичной структуры белка.
Первичная структура
Первичная структура белка — это просто линейная последовательность аминокислот в полипептидной цепи. Каждый белок имеет свою первичную структуру — уникальное белковое «слово», состоящее из уникальной последовательности аминокислотных «букв». Первичная структура одного из белков, фермента лизоцима, показана на рис. 3-16.
Вторичная структура
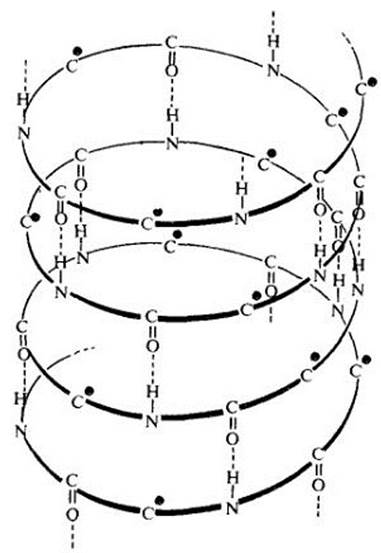
В клетке полипептидные цепи самопроизвольно образуют упорядоченные вторичные структуры, наиболее распространенная из которых — альфа-спираль— похожа на винтовую лестницу (рис. 3-17). Она имеет постоянную геометрию с одним витком спирали через каждые 3,6 аминокислот. Спиральная конфигурация ноли пептидной цепи поддерживается водородными связями между соседними витками, причем атом водорода аминогруппы одной аминокислоты соединяется с атомом кислорода гидроксильной группы другой аминокислоты, находящейся на соседнем витке спирали.
Рис. 3-17. Альфа-спираль, поддерживаемая водородными связями (пунктирные линии). Связи образуются между атомом кислорода карбоксильной группы одной аминокислоты и атомом водорода аминогруппы другой, расположенной через четыре аминокислотных остатка. Не показанные на этом рисунке R-группы присоединены к углеродным атомам, отмеченным цветными точками, и направлены наружу. Шаг спирали приходится на каждые 3,6 аминокислотных остатка
Третичная и четвертичная структура
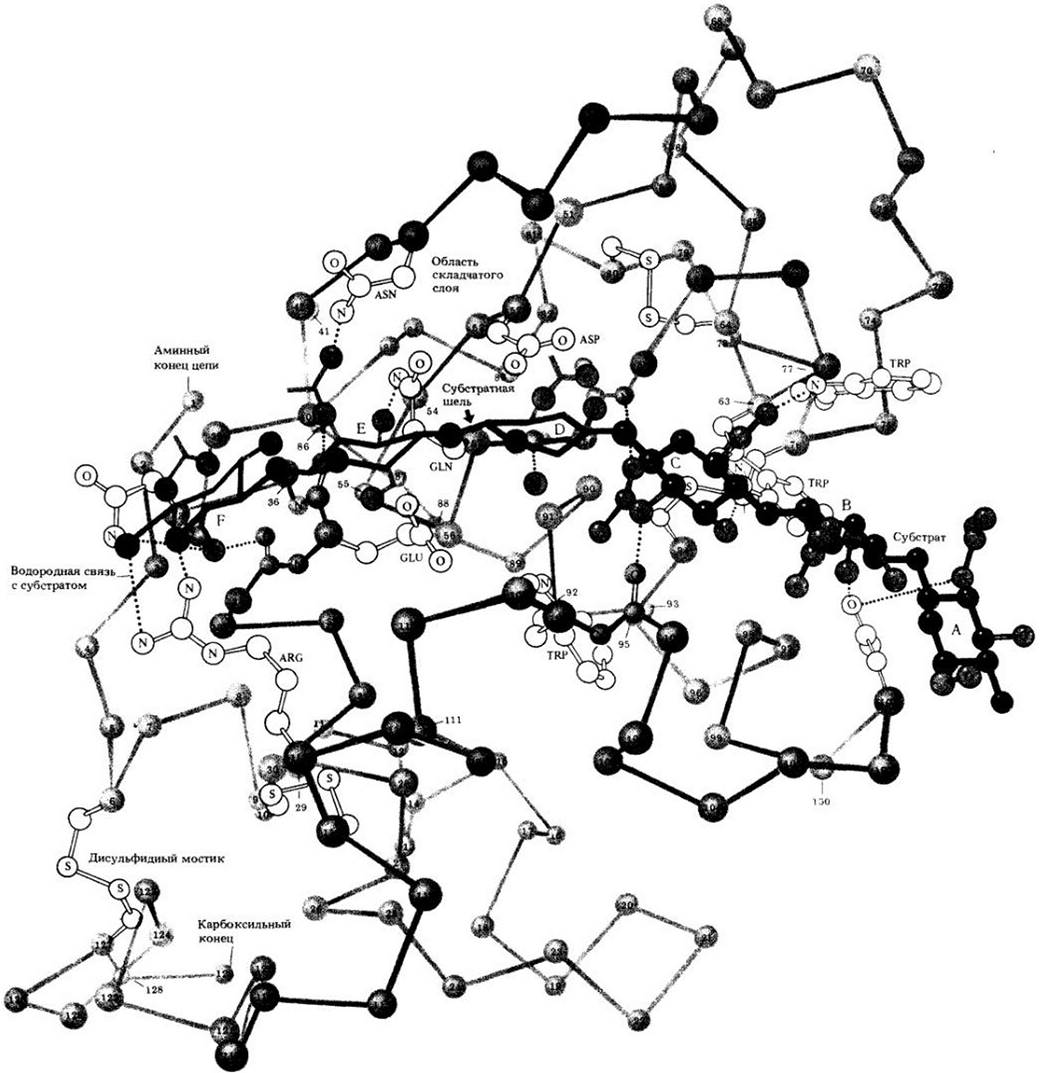
Полипептидные цепи могут быть уложены в глобулы, формируя третичную структуру белка. На рис. 3-18 показана укладка основной цени фермента лизоцима. Большинство биологически активных белков, таких, как ферменты, являются глобулярными. Глобулярное строение имеют и специализированные белки клеточных мембран. Микротрубочки построены из большого числа сферических субъединиц, каждая из которых является глобулярным белком.
Рис. 3-18. Этот рисунок дает представление о сложном характере точной укладки полипептидной цепи при формировании третичной структуры белка. (Сравните этот рисунок с относительно простой первичной структурой лизоцима на рис. 3-16.) Здесь изображена только основная цепь фермента. Субстрат выделен темным цветом, он проходит горизонтально через молекулу лизоцима
Третичная структура белка определяется его первичной структурой и поддерживается главным образом водородными и электростатическими связями (см. рис. 3-14), а также взаимодействиями между аминокислотными остатками и молекулами воды. Эти связи относительно слабы и могут довольно легко разрушаться в результате физических или химических изменений среды, например, повышения температуры или увеличения кислотности. Разрыв образующих третичную структуру связей приводит к денатурации белка. Хорошим примером денатурации служит свертывание белка при варке яиц. Когда белки денатурируют, пол и пептидные цепи развертываются, что приводит к потере биологической активности белка. Организмы не могут существовать при экстремально высокой температуре, поскольку в этих условиях их ферменты и другие белки становятся нестабильными и теряют свою активность в результате денатурации.
Четвертичная структура белка определяется тем, как расположены относительно друг друга образующие его полипептидные цепи. Большинство крупных белков построено из нескольких полипептидных цепей, как идентичных, так и различающихся между собой. Из двух или большего числа полипептидных цепей состоят, например, молекулы многих ферментов.
Ферменты
Ферменты — крупные глобулярные белки, действующие как катализаторы. (Молекулярная масса различных ферментов варьирует от 12 000 до 1 000 000 и более.) Катализаторы — это вещества, которые ускоряют химическую реакцию путем понижения энергии активации, но сами при этом не изменяются. Поскольку катализаторы не меняются в процессе химической реакции, они могут использоваться неоднократно и очень эффективно.
В лаборатории скорость химических реакций обычно повышают нагреванием, что увеличивает силу и частоту соударений молекул. Однако в клетке одновременно протекают сотни различных реакций, и тепло неизбирательно ускорило бы их все. Более того, повышение температуры может привести к плавлению липидов, денатурации белков и ряду других деструктивных изменений. Только благодаря катализаторам-ферментам химические реакции в клетке проходят с большой скоростью и при относительно низкой температуре. Если бы не было ферментов, реакции протекали бы так медленно, что их результат вряд ли бы имел значение.
Ферменты, как правило, называют, добавляя окончание -аза к корню названия субстрата. Например, амилаза катализирует гидролиз амилозы (крахмала). Сейчас известно около 2000 различных ферментов, и каждый из них способен катализировать определенную химическую реакцию. Механизм действия ферментов в биологических реакциях будет описан в гл. 5.
Нуклеиновые кислоты
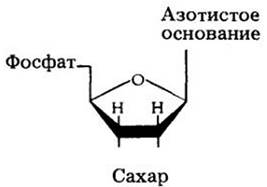
Нуклеиновые кислоты — это сложные молекулы, полимеры нуклеотидов; каждый нуклеотид состоит из трех субъединиц: фосфатной группы, пятиуглеродного сахара (пентозы) и азотистого основания, названного так потому, что в его состав наряду с углеродом входит азот.
Существуют два типа нуклеиновых кислот — ДНК (дезоксирибонуклеиновая кислота) и РНК (рибонуклеиновая кислота). ДНК — это молекула, хранящая генетическую информацию. РНК служит переносчиком этой информации ДНК через РНК «диктует» белкам их структуру, а значит, и «руководит» всей деятельностью клетки.
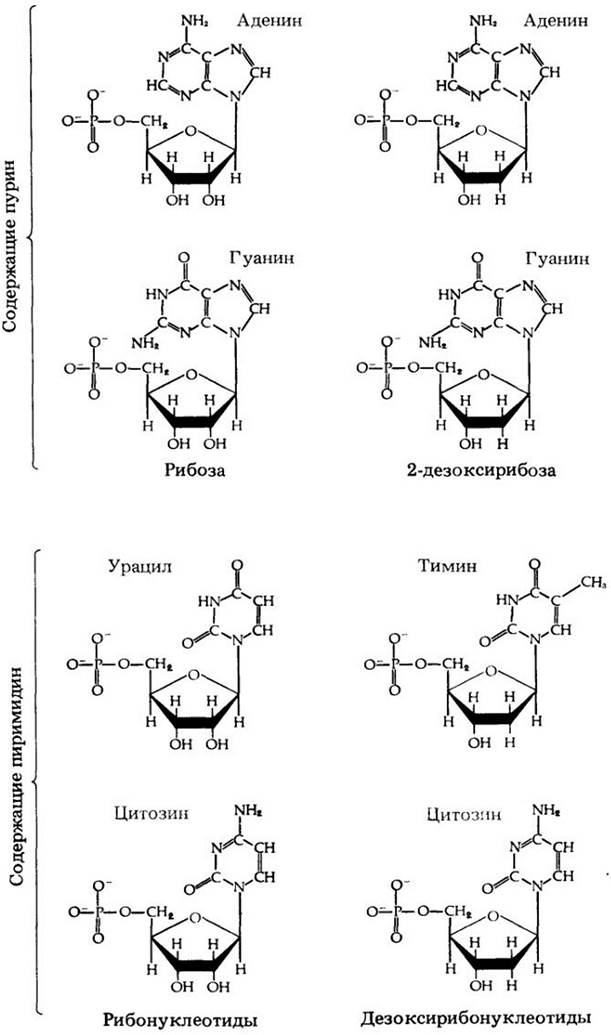
Нуклеотиды содержат азотистые основания двух типов: пиримидины, имеющие одно кольцо, и пурины, имеющие два кольца (рис. 3-19). Три пиримидина, входящие в состав нуклеотидов, — это тимин, цитозин и урацил. ДНК содержат тимин и цитозин, РНК — цитозин и урацил. Два пурина в нуклеотидах — это аденин и гуанин. И РНК, и ДНК содержат эти пурины. В состав молекул ДНК и РНК входят два сахара: в ДНК — дезоксирибоза, в РНК — рибоза. «Дезокси» означает «минус один кислород», и только в этом, как показано на рис. 3-19, заключается различие между двумя пентозами.
Взаимодействие РНК и ДНК, их структура, функции и история открытия изложены в гл. 8.
Рис. 3-19. Строительные блоки РНК и ДНК. Каждый строительный блок — нуклеотид — содержит фосфатную группу, сахар и азотистое основание (пурин или пиримидин).
В состав двух типов нуклеиновых кислот входят одинаковые пурины, однако пиримидины различаются: ДНК содержит тимин, а РНК — урацил. Кроме того, в РНК входит рибоза, а в ДНК — дезоксирибоза. Как показано в гл. 8, биологические роли двух нуклеиновых кислот совершенно различны
Другие производные нуклеотидов
Нуклеотиды и их производные выполняют в клетке разнообразные функции. Особенно большое значение имеют АТР (аденозинтрифосфат, см. рис. 5-10) и ADP(аденозиндифосфат). Почти всегда энергетические процессы в клетке связаны с переносом фосфатных групп, в котором АТР и ADP играют основную роль. Участие этих молекул в энергетическом обмене обсуждается в гл. 5.
Нуклеотиды являются важными составными частями ряда других молекул, принимающих участие в переносе энергии. К таким соединениям относится NAD (никотинамида- дениндинуклеотид), который содержит нуклеотид аденин и фосфат (см. рис. 5-8). Широкое использование связи пурин- сахар-фосфат в транспорте энергии может быть связано с тем, что образуемые с ее помощью крупные заряженные молекулы не проходят сквозь мембраны и поэтому не могут «ускользнуть» из клеток и ограниченных мембранами органелл или, наоборот, «проскользнуть» в них.