СОВРЕМЕННАЯ БОТАНИКА - П. РЕЙВН - 1990
РАЗДЕЛ II. ЭНЕРГИЯ И ЖИВЫЕ КЛЕТКИ
ГЛАВА 6. ДЫХАНИЕ
Аэробный путь
Пируват — ключевое соединение в энергетическом метаболизме клетки, и он может быть утилизирован различными путями. Каким образом он будет использован в дальнейшем, зависит от условий метаболизма и особенностей клетки. Основной внешний фактор, который обуславливает последующую утилизацию пирувата, — это кислород.
В присутствии кислорода пируват окисляется до двуокиси углерода, и гликолиз в данном случае — лишь начальная фаза дыхания. Аэробный путь приводит к полному окислению глюкозы, при этом образуется больше молекул АТР, чем в результате гликолиза. Эти реакции совершаются в митохондриях эукариотических клеток в два этапа — в цикле Кребса и в электронотранспортной цепи (рис. 6-1).
Напомним, что митохондрии окружены двумя мембранами; внутренняя имеет складки, называемые кристами. Внутреннее пространство, ограниченное кристами, заполнено относительно насыщенным раствором, содержащим ферменты, коферменты, воду, фосфаты и другие молекулы, вовлекаемые в процесс дыхания. Таким образом, митохондрия — это самостоятельная химическая фабрика. Наружная мембрана проницаема для большинства молекул, но внутренняя — только для определенных, таких, как пируват и АТР, и непроницаема для других соединений. Ферменты цикла Кребса локализуются во внутреннем компартменте митохондрий — матриксе. Ферменты и другие компоненты электронотранспортной цепи встроены в мембраны крист.
Цикл Кребса
Цикл Кребса назван в честь Ганса Кребса, который открыл его. Кребс описал этот метаболический путь в 1937 г. Позднее его блестящая работа была удостоена Нобелевской премии. Циклом Кребса называют цикл трикарбоновых кислот (ЦТК), который начинается с образования лимонной кислоты (цитрата), имеющей три карбоксильные группы.
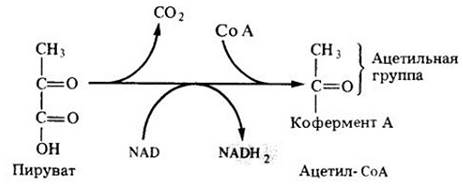
Перед тем как войти в цикл Кребса, пируват окисляется и декарбоксилируется. В ходе этой экзергонической реакции из NAD образуется NADH2. Исходная молекула глюкозы окисляется, таким образом, до двух ацетильных групп (СН3СО); при этом выделяются две молекулы СО2 и синтезируются две молекулы NADH2 из NAD (рис. 6-5).
Каждая ацетильная группа затем временно присоединяется к коферменту А (СоА), большой молекуле, состоящей из нуклеотида и пантотеновой кислоты (витамина группы В). Комплекс ацетильной группы и СоА называют ацстил-СоА (рис. 6-5).
Рис. 6-5. Трехуглеродная молекула пирувата окисляется и декарбоксилируется с образованием двухуглеродной ацетильной группы, которая объединяется с коферментом А и образует ацетил- СоА. Окисление молекулы пирувата сопровождается образованием NADH, из NAD. Ацетил-СоА необходим для того, чтобы «войти» в цикл Кребса
Жиры и аминокислоты могут тоже превращаться в ацетил-СоА и таким образом вовлекаться в процесс дыхания. Молекула жира сначала гидролизуется до глицерола и трех молекул жирных кислот. Затем, начиная с концевой карбоксильной группы, последовательно удаляются двухуглеродные группы жирных кислот. Например, из пальмитиновой кислоты (см. рис. 3-9), содержащей 16 атомов углерода, может образоваться восемь молекул ацетил-СоА.
В начале цикла Кребса (рис. 6-6) двухуглеродные ацетильные группы объединяются с четырехуглеродным соединением (оксалоацетатом) и образуют шестиуглеродное соединение (цитрат). По ходу работы цикла два из шести атомов углерода окисляются до СО2, и оксалоацетат восстанавливается; таким образом осуществляется циклический процесс. В каждом обороте цикла используется одна ацетильная группа и образуется одна молекула оксалоацетата, которая готова начать новый оборот цикла. В результате всех реакций при окислении углеродных атомов выделяется энергия, которая используется для превращения ADP в АТР (I молекула на цикл) и образования NADH2 из NAD (3 молекулы на цикл). Кроме того, часть энергии используется для восстановления второго переносчика электронов — кофермента флавинадениндинуклеотида (FAD) (рис. 6-7). Одна молекула FADH2образуется из FAD при каждом обороте цикла. Кислород прямо не участвует в цикле Кребса; электроны и протоны, которые удаляются при окислении, взаимодействуют с NAD и FAD:
Оксалоацетат + Ацетил-СоА + ADP+3NAD + FAD —> Оксалоацетат+ 2СО2 + СоА + АТР + 3NADH2 + FADH2. Цикл Кребса представлен на рис. 6-8.
Рис. 6-6. В цикле Кребса атомы углерода ацетильной группы окисляются до двуокиси углерода, а атомы водорода направляются к переносчикам электрона. Как и в гликолизе, в цикле Кребса каждую реакцию катализирует специфический фермент
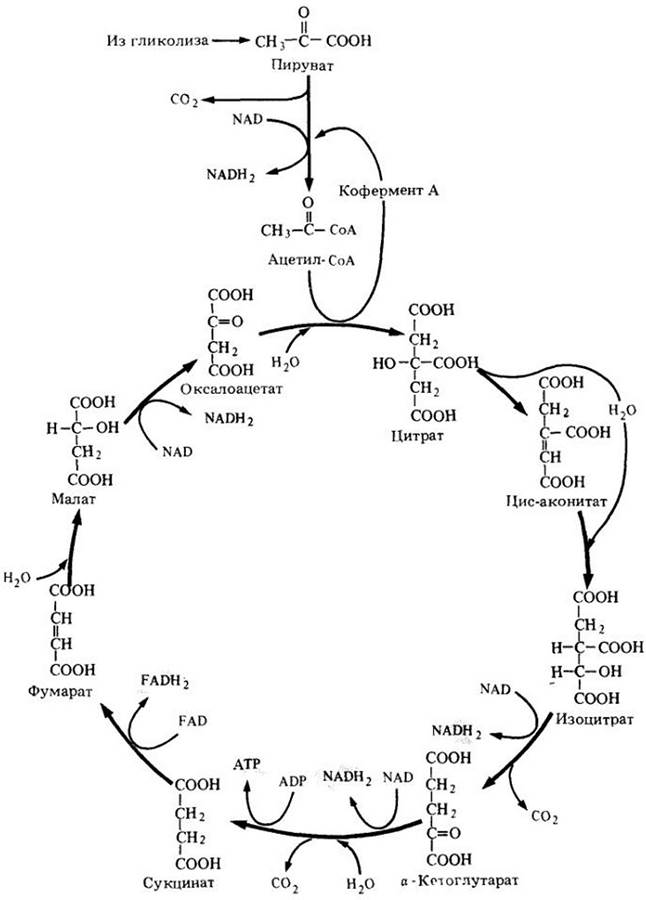
Рис. 6-8. Общая схема цикла Кребса. При окислении одной ацетильной группы за один оборот цикла образуются одна молекула АТР, три молекулы NADH2 и одна молекула FADH2, что и составляет энергетический выход цикла
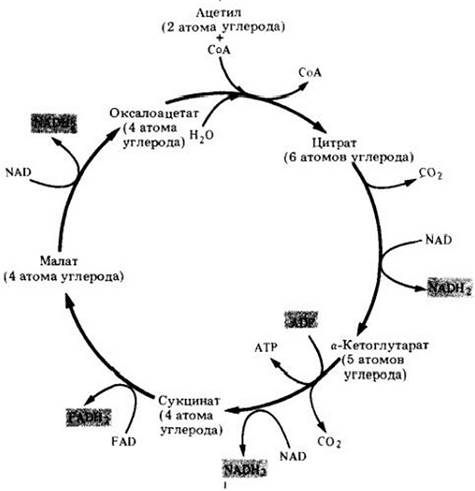
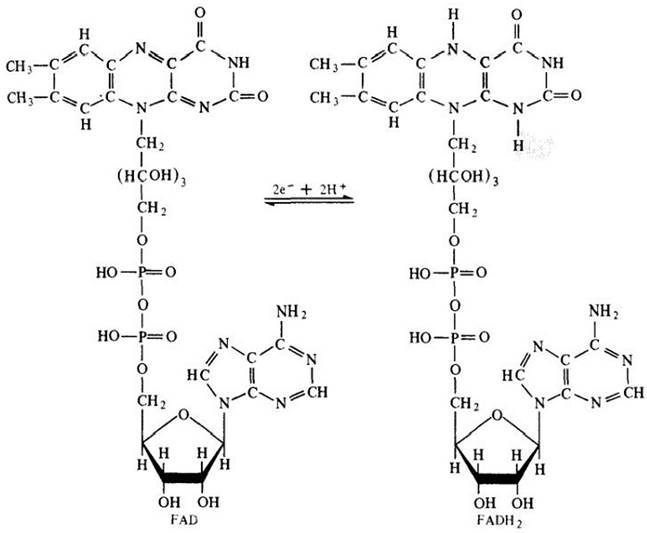
Рис. 6-7. Флавинадениндинуклеотид, акцептор электрона: окисленная форма — FАD, восстановленная — FАDН2. Рибофлавин — это витамин В2, который синтезируется всеми растениями и многими микроорганизмами. Он представляет собой пигмент и в окисленной форме имеет ярко-желтую окраску. Родственное соединение, тоже акцептор электрона — флавинмононуклеотид, FМN, состоит из рибофлавина и концевой фосфатной группы. Он получает электроны от NADН в электронотранспортной цепи
Электронотранспортная цепь
Итак, молекула глюкозы полностью окислилась. Часть ее энергии использовалась на синтез АТР из ADP. Большая часть, однако, осталась в форме электронов, образовавшихся при окислении углерода. Эти электроны перешли к переносчикам электронов NAD и FAD и находятся на высоком энергетическом уровне. При движении по электроно- транспортной цепи они спускаются «под гору» к кислороду; при этом выделяющаяся энергия используется для синтеза ATР из ADP. Данный процесс называют окислительным фосфорилированием.
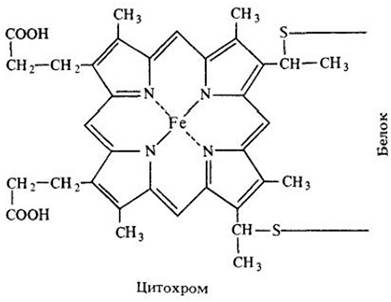
Переносчики электронов электронотранспортной цепи митохондрий по своей химической структуре отличаются от NAD и FAD. Некоторые из них относятся к классу соединений, называемых цитохромами. Цитохромы — это белковые молекулы, содержащие гем, т. е. железопорфириновое кольцо (рис. 6-9). Цитохромы различаются по строению белковой цепи и энергетическому уровню электронов. Цитохромы переносят только электроны, без протонов.
Рис. 6-9. Цитохромы — это молекулы, у которых атом железа находится в центре азотсодержащего кольца — порфирина. Порфириновое кольцо вместе с атомом железа называется гемом. Цитохромы участвуют в переносе электронов. Железо реагирует с электронами; при этом атом железа, присоединивший электрон, восстанавливается из Fе3*+до Fе2+
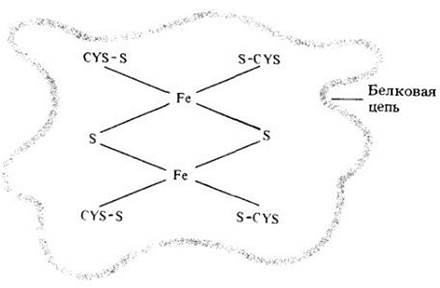
Содержащие негеминовое железо белки представляют собой другие компоненты электронотранспортной цепи. Железо в этих белках соединено не с порфириновым кольцом, а с сульфидами и с атомами серы аминокислоты цистеина, входящей в состав белковой цепи (рис. 6-10). Подобно цитохромам, белки, содержащие железо и серу, переносят электроны, но не протоны.
Рис. 6-10. Железосерные белки содержат связанные железо и серу. В центре растительного железосерного белка, показанного здесь, находятся по два атома железа и серы
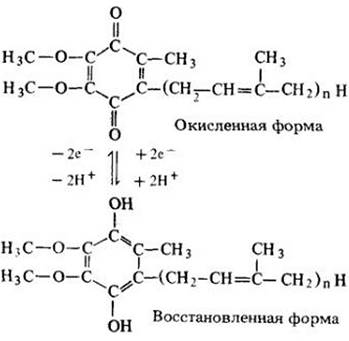
Третьим важным компонентом электронотранспортной цепи являются хиноны (рис. 6-11). Хиноны — это наиболее распространенные компоненты цепи.
В противоположность цитохромам или белкам, содержащим железо и серу, хиноны переносят эквивалент атома водорода. За счет чередования транспорта электронов между компонентами цепи, переносящими или не переносящими протоны с электронами, обеспечивается перенос протона через мембрану. Например, когда молекула хинона захватывает электрон от цитохрома, она присоединяет и протон из окружающей среды. Если хинон отдает электрон следующему переносчику — цитохрому, то протон возвращается в среду. Если переносчики электронов встроены в мембрану таким образом, что протоны на одной стороне захватываются, а на другой высвобождаются, то при этом устанавливается протонный градиент. Большинство хинонов не соединено с белками, поэтому полагают, что они способны проходить через мембрану.
Рис. 6-11. Кофермент Q (СоQ), жирорастворимый хинон в окисленной и восстановленной формах. Отмечены группы, переносящие атомы водорода
В исходной точке электронотранспортной цепи электроны удерживаются на FАDН2. В цикле Кребса образуются две молекулы FАDН2 и шесть молекул NADH2. Окисление пирувата до ацетил-СоА дает две молекулы NADH2. Вспомним, что еще две молекулы NADH2 образовались в результате гликолиза; в присутствии кислорода они транспортируются в митохондрии, где переносят электроны на флавинмононуклеотид (FMN) — акцептор электронов в электронотранспортной цепи (рис. 6-7).
Когда электроны перемещаются по электронотранспортной цепи с высокого энергетического уровня на более низкий, то выделяющаяся при этом энергия используется для синтеза АТР из ADP (рис. 6-12). В конце цепи электроны захватываются кислородом и объединяются с протонами (ионами водорода) с образованием молекулы воды. Каждый раз, когда одна пара электронов проходит от NADH2 до кислорода, образуются три молекулы АТР. Когда пара электронов поступает от FADH2, в котором они находятся на более низком энергетическом уровне, чем в NADH2, образуются две молекулы АТР.
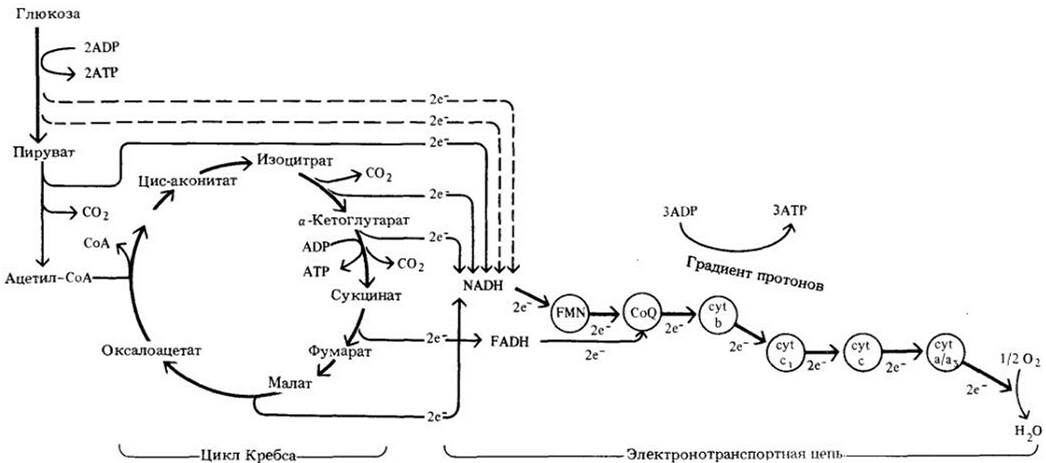
Рис. 6-12. Общая схема дыхания. Сначала глюкоза расщепляется до пирувата с образованием двух молекул АТР и восстановлением двух молекул NAD (штриховые стрелки). Пируват окисляется до ацетил-СоА, и одна молекула NAD восстанавливается (следует отметить, что в эту и последующие реакции вовлекаются бее молекулы пиру вата; путь электронов указан сплошными стрелками). В цикле Кребса ацетильная группа окисляется, а акцепторы электронов, NAD и FAD, восстанавливаются. NADH2 и FADH, затем отдают свои электроны на электронотранспортную цепь, которая в основном преоставлена комплексом цитохромов (cyt). Когда электроны проходят по цитохромам «вниз», выделяется энергия, которая используется для образования АТР из A DP, как показано на рис. 6-14. Электронотранспортная цепь показана здесь неполностью
Механизм окислительного фосфорилирования: хемиосмотическое сопряжение
Гипотеза хемиосмотического сопряжения была впервые выдвинута в 1960 г. английским биохимиком Петером Митчеллом (лауреатом Нобелевской премии по химии 1978 г.). В основе гипотезы лежит предположение, что окислительное фосфорилирование осуществляется благодаря протонному градиенту (различной концентрации Н+ с двух сторон внутренней мембраны митохондрий), который появляется при транспорте электронов. Согласно этой остроумной концепции, протоны откачиваются из митохондриального матрикса во внешнее митохондриальное пространство, тогда как электроны от NADH2, идут по электронотранспортной цепи, встроенной в митохондриальную мембрану. Каждая пара электронов пересекает мембрану три раза, когда передается от одного переносчика электронов к другому и в конце концов к кислороду. В результате появляется электрохимический градиент Н+, который направляет протон обратно в матрикс через диффузионный канал в шарообразной структуре, выступающей в матрикс.
В настоящее время установлено, что канал, через который протоны возвращаются в матрикс, содержит большой ферментный комплекс, называемой АТР-синтетазой. Он состоит из двух основных компонентов, или факторов, — F0 и F1 (рис. 6-13, А). Компонент F0 встроен во внутреннюю митохондриальную мембрану, пронизывая ее насквозь; F1 — это большая глобулярная структура, состоящая из девяти полипептидных субъединиц, соединенных с F0 со стороны матрикса. На электронных микрофотографиях фактор F1 выглядит как шарообразное выпячивание (рис. 6-13, Б). Компонент F1 не может в изолированной форме синтезировать АТР из ADP и фосфата, но способен гидролизовать АТР до ADP, т. е. функционировать как АТРаза. Однако обычная его функция вместе с фактором F0 в интактной мембране — обратная, т. е. синтез АТР. Протоны преодолевают электрохимический градиент, существующий между наружной стороной мембраны и матриксом, когда проходят через F0 и F1. Свободная энергия, которая при этом выделяется, используется для синтеза ATT из ADP и фосфата. Рис. 6-14 иллюстрирует механизм хемиосмотического сопряжения при окислительном фосфорилировании.
Рис. 6-13. А. Схема комплекса АТР-синтетазы. Часть компонента F0 погружена во внутреннюю мембрану и проходит через нее, а компонент F1, который состоит из девяти субъединиц, выдается в митохондриальный матрикс. На электронной микрофотографии видны округлые структуры, выдающиеся из мембран пузырьков. Это компоненты F1комплексов АТР-синтетазы
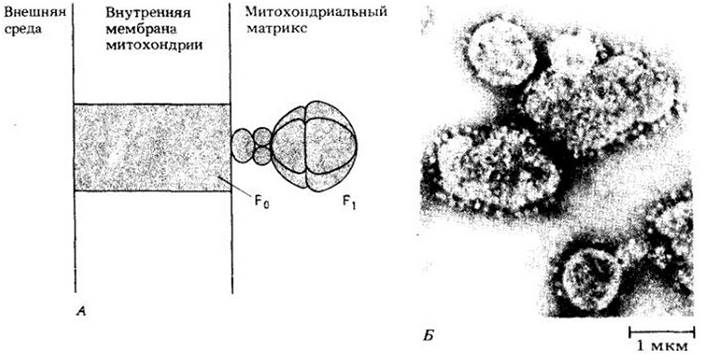
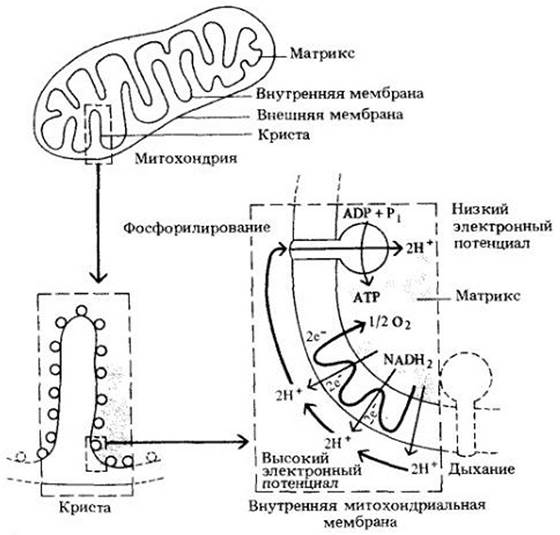
Рис. 6-14. Согласно гипотезе хемиосмотического сопряжения, протоны выкачиваются из митохондриального матрикса, когда электроны проходят по электронотранспортной цепи, входящей в состав внутренней митохондриальной мембраны. Когда протоны проходят через комплекс АТР-синтетазы по электрохимическому градиенту, они обеспечивают энергией синтез АТР из ADP и фосфата. Точное число протонов, выкачиваемых из матрикса, когда пара электронов движется по цепи, не определено, как и их число, которое должно пройти через А ТР-синтетазу для образования каждой молекулы АТР
Контроль окислительного фосфорилирования
Электроны продолжают движение по электронотранспортной цепи, если имеется ADP, доступный для синтеза АТР. Таким образом, окислительное фосфорилирование регулируется по закону «спроса и предложения». Когда в клетке снижаются энергетические потребности, утилизируется меньше молекул АТР, соответственно меньше молекул ADPвысвобождается и уменьшается поток электронов.
Общий энергетический выход
Сейчас необходимо рассмотреть, как много энергии, исходно содержащейся в молекуле глюкозы, запасается в форме АТР. «Балансовая ведомость» выхода АТР представлена в табл. 6-1. В присутствии кислорода гликолиз дает две молекулы АТР и две молекулы NADH2 (из которых может образоваться дополнительно шесть молекул АТР). Общий итог, однако, не восемь молекул АТР, как можно вычислить, а шесть. Две молекулы — это «плата» за транспорт электронов в составе двух молекул NADH2 через митохондриальные мембраны.
Таблица 6-1. Энергетический выход при расщеплении одной молекулы глюкозы
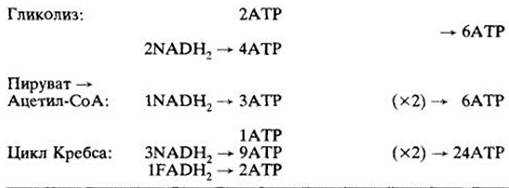
Превращение пирувата в ацетил-СоА даст две молекулы NADH2 (внутри митохондрии) на одну молекулу глюкозы, и, таким образом, образуется шесть молекул АТР.
Цикл Кребса на каждую молекулу глюкозы дает две молекулы АТР, шесть NADH2 и две FADH2: в сумме 24 молекулы АТР.
Как видно из таблицы, при окислении одной молекулы глюкозы синтезируется 36 молекул АТР. Все они, кроме двух, образуются в митохондриальных реакциях, все, кроме четырех, — при окислении NADH2 и FADH2.
Общая разница в свободной энергии между исходными соединениями (глюкоза и кислород) и конечными продуктами (СО2 и Н2О) составляет 686 ккал. Примерно 39%, или 263 ккал (7,3x36), запасается в форме высокоэнергетических связей в 36 молекулах АТР (рис. 6-15).
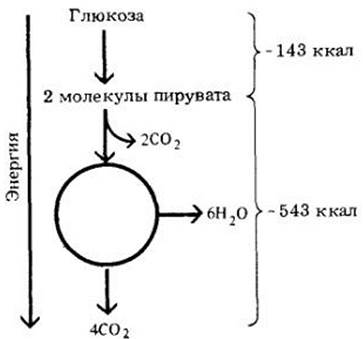
6-15. Изменения энергии при окислении глюкозы. В результате полного расщепления молекулы глюкозы должно произойти падение энергии на 686 ккал. Из этого количества 39% (263 ккал) запасается в виде 36 молекул АТР. В то же время при анаэробном дыхании образуются только две молекулы АТР, т. е. запасается только 2% общей энергии глюкозы
Другие метаболические пути, в результате которых выделяется энергия
Глиоксилатный цикл
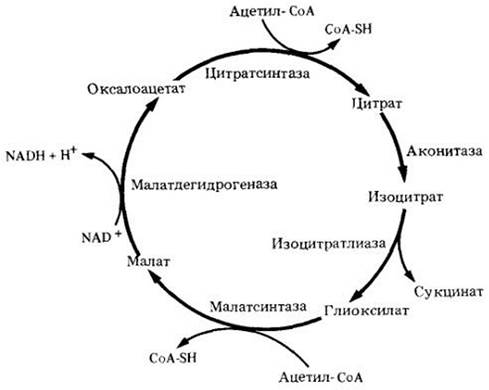
Многие семена запасают жиры в качестве источника энергии, которая используется на ранних этапах прорастания. Когда жиры расщепляются до двухуглеродных единиц в виде ацетил-СоА, то ацетил-СоА становится источником энергии. В глиоксилатном цикле (рис. 6-16), который можно считать модификацией цикла Кребса, изоцитрат расщепляется на сукцинат и глиоксилат. Молекула сукцината затем окисляется в цикле Кребса, а молекула глиоксилата конденсируется с другой молекулой ацетил-СоА с образованием малата. Молекула малата тоже может вступить в цикл Кребса или окислиться до оксалоацетата, замыкая глиоксилатный цикл. Глиоксилатный цикл обнаружен у растений, дрожжей и некоторых бактерий, но отсутствует в клетках животных. В растениях глиоксилатный цикл осуществляется в микротельцах, называемых глиоксисомами. В глиоксисомах происходит и расщепление жирных кислот. Глиоксилатный цикл можно рассматривать как анаплеротический путь (анаплеротические пути служат источниками соединений для других путей). В данном случае глиоксилатный цикл является источником четырехуглеродных кислот, вступающих в цикл Кребса.
Рис. 6-16. А. Глиоксилатный цикл. Две молекулы ацетил-СоА используются в каждом обороте цикла, и в результате образуются четырехуглеродные кислоты. Глиоксилатный цикл представляет собой модификацию цикла Кребса. В нем участвуют два специфических фермента: изоцитратлиаза, которая расщепляет изоиитрат на сукцинат (четырехуглеродную кислоту) и глиоксилат, а также малатсинтаза, которая конденсирует глиоксилат с ацетил-СоА с образованием другой четырехуглеродной кислоты — малата. Реакции, идущие с участием этих ферментов, обозначены разными цветами
Пентозофосфатный путь
Растительные ткани имеют возможность помимо гликолиза окислить глюкозу по пентозофосфатному пути. Для него характерно следующее: (1) отсутствие синтеза АТР; (2) образование пятиуглеродного сахара — рибозы, который необходим для синтеза нуклеотидов ДНК или кофакторов. Ферменты, пентозофосфатного пути в качестве кофактора используют не NAD, a NADP. NADP имеет еще одну фосфатную группу, связанную с рибозой. Образуемый NADPH2 используется в биосинтезах и окисляется в митохондриях с образованием АТР.
NADP аналогичен NAD, но имеет дополнительную фосфатную группу. Его биологическая роль, однако, совершенно другая. NADH2 передает электроны другим переносчикам, которые передают их далее поэтапно на более низкий электронный уровень. В результате образуется АТР. NADPH2 сам служит источником энергии для тех биосинтетических процессов клетки, где необходимы значительные энергетические затраты.
Пентозофосфатный путь «обходит» те этапы гликолитического пути, где имеет место регуляция. Больные растительные ткани часто окисляют глюкозу по пентозофосфатному пути, предпочитая его гликолитическому.