Фізіологія людини - Вільям Ф. Ґанонґ 2002
Функції нервової системи
Нервові основи інстинктивної поведінки й емоцій
Нейрохімія і поведінка
До фармакологічних засобів, що модифікують поведінку людини, належать галюциногенні речовини (засоби, що зумовлюють галюцинації й інші прояви психозів); транквілізатори (засоби, що загальмовують тривогу й інші психіатричні симптоми); антидепресанти (засоби, що підіймають настрій, підвищують інтерес і головні прагнення (драйв)). Ці та ще багато інших засобів модифікують передавання в синаптичних контактах головного мозку. Нейрохімію відомих і вірогідних синаптичних трансмітерів як периферійної, так і центральної нервової системи розглянуто в Розділі 4. Цей параграф присвячений значенню названих речовин у процесах інстинктивної поведінки й емоцій.
Аміноергічні системи головного мозку
Виділяють такі чотири великі аміноергічні системи, тіла нейронів яких розміщені у порівняно нечисленних ділянках головного мозку, проте аксони цих нейронів сильно розгалужені й утворюють зв’язки майже з усіма відділами нервової системи (рис. 15-6): серотонінергічну, норадренергічну, адренергічну і гістамінергічну. Тіла дофамінергічних нейронів розміщені в багатьох відділах головного мозку, однак їхні аксони теж прямують до різних ділянок.
Серотонін
Тіла серотонінвмісних нейронів розміщені в серединних ядрах шва стовбура головного мозку, а їхні аксони проходять до ділянок гіпоталамуса, лімбічної системи, нової кори і спинного мозку (див. рис. 15-6).
Галюциногенний агент діетиламідлізергінова кислота (ДЛК) є агоністом серотоніну, який виявляє дію шляхом активування 5-НТ2-рецепторів (див. Розділ 4) головного мозку. Швидкоплинні галюцинації й інші психічні відхилення, що виникають під впливом цієї речовини, уперше виявив хімік, який під час синтезу випадково вдихнув її. Це відкриття привернуло увагу дослідників до проблеми зв’язку між поведінкою і коливанням вмісту серотоніну в головному мозку. Псилоцин, сполука, що міститься в певних грибах, і N,N-діметилтриптамін (ДМТ) теж мають галюциногенний ефект і, як і серотонін, є похідними триптаміну. Сполука 2,5-диметокси-4-метиламфетамін (ДОМ), мескалін і споріднені з ним сполуки, що теж є справжніми галюциногенами, становлять радше фенілетиламіни, ніж індоламіни. Проте дія всіх цих галюциногенів, очевидно, зумовлена зв’язуванням з 5-НТ2-рецепторами. Сполука 3,4-метилендіоксиметамфетамін (МДМА), або екстазі, теж зумовлює залежність. Вона призводить до ейфорії, проте згодом виникають труднощі з концентрацією, депресія і (у мавп) безсоння. Цей засіб спричинює виділення серотоніну і вичерпання його; отже, ейфорія може бути зумовлена надлишковим виділенням серотоніну, а подальші симптоми - його вичерпанням.
Як зазначено в Розділі 11, є докази, що агоністи серотоніну - це супресори сну. Потенціал у серотонінергічних нейронах поширюється швидко під час пробудження, повільно - під час дрімання, ще повільніше - у разі засинання і зовсім не поширюється під час сну зі швидкими парадоксальними рухами очей (див. Розділ 11).
Уважають, що серотонін у головному мозку виконує ще багато інших функцій. Він може відігравати стимулювальну роль у регулюванні секреції пролактину (див. Розділ 23). Вірогідно, що системи низхідних серотонінергічних волокон гальмують передавання больової чутливості в задніх рогах спинного мозку. Крім того, відбувається значний серотонінергічний вплив на надперехресні ядра гіпоталамуса, і серотонін може брати участь у регулюванні циркадних ритмів (див. Розділ 14). З патофізіологічного погляду, ймовірно, що поява імпульсу в серотонінергічних нейронах дорсальних ядер шва спричинює мігрень, а протимігренні засоби саме сповільнюють поширення таких імпульсів.
У хворих на депресію простежується зменшення концентрації в СМР головного метаболіту серотоніну 5-НІАА (див. рис. 4-23). Цей факт використовують для заперечення того, що депресію зумовлює низька зовнішньоклітинна концентрація норадреналіну в головному мозку (див. нижче), а засоби, які інгібують зворотне поглинання норадреналіну, мають важливе значення для лікування депресії. Однак ці засоби теж інгібують зворотне поглинання серотоніну, а речовини, такі як флуоксетин (прозак), що інгібують зворотне поглинання серотоніну, не пригнічуючи зворотного поглинання норадреналіну, були такі ж ефективні, як антидепресанти. Отже, центр уваги в разі клінічної депресії переходить від норадреналіну до серотоніну. Цікаво, що всі ці сполуки треба застосовувати заздалегідь, тобто їхня антидепресивна дія виявляється через чотири-шість тижнів. Це свідчить, що їхня дія є швидше вторинною, а не власне інгібуванням, яке зумовлює поліпшення стану хворого.
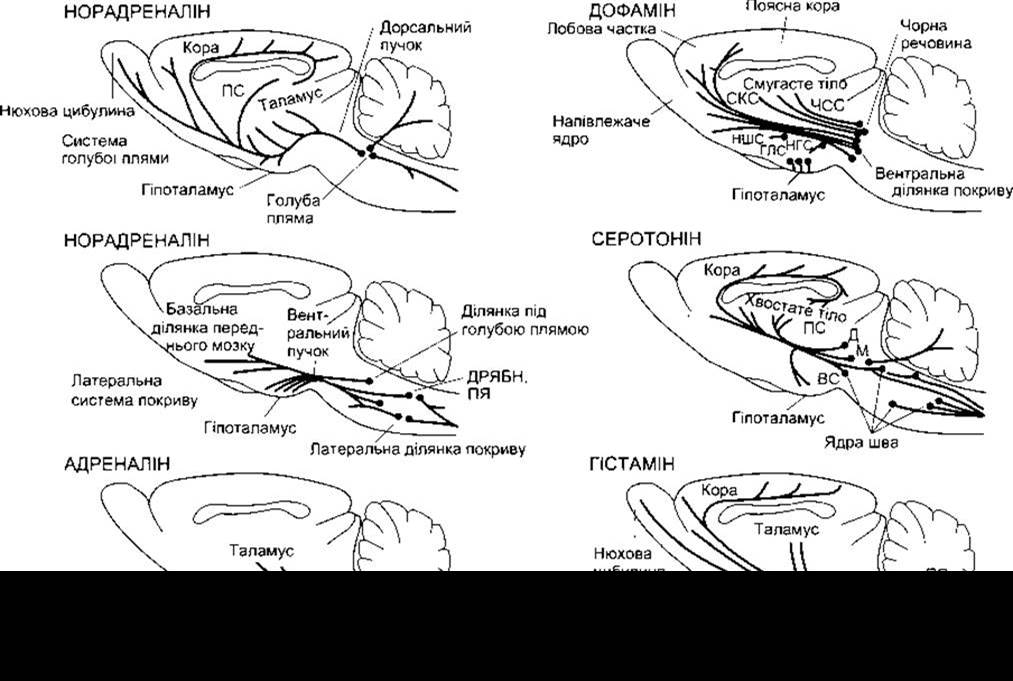
Рис. 15-6. Аміноергічні шляхи головного мозку щура. Подібні шляхи є в головному мозку людини. Дві головні норадренергічні системи (голубої плями і латеральної ділянки покриву) зображені окремо. ПС - погранична смужка; ДРЯБН - дорсальне рухове ядро блукаючого нерва; ПЯ - поодиноке ядро; ЦСР - центральна сіра речовина; ЧСС - чорноречовинно-смугаста система; СКС - середньомозково-кіркова система; НШС - навколошлуночкова система; НГС - невизначено-гіпоталамічна система; ГЛС - горбово-лійкова система; Д, М і ВЦ - дорсальне, медіальне і верхнє центральне ретикулярні ядра шва.
Як зазначено в Розділі 4, блокування NK-1-рецепторів, що опосередковують дію речовини Р, теж послаблює депресію шляхом поки що невідомого механізму.
У мишей з нокаутом гена МАО типу А (див. Розділ 4) і в людей з мутантними МАО А генами підвищується агресивність поведінки. У цьому разі в мишей кількість серотоніну в головному мозку помітно збільшується. В тварин з нокаутом ауторецептора 5-НТ1B агресивність поведінки теж зростає.
Норадреналін
Тіла нейронів головного мозку, що містять норадреналін, розміщені в голубій плямі та інших ядрах мосту і довгастого мозку. Аксони норадренергічних нейронів, що виходять з голубої плями, утворюють систему голубої плями. Вони опускаються до спинного мозку, проникають до мозочка і підіймаються до пришлуночкового, надзорового і навколошлуночкового ядер гіпоталамуса, таламуса, основи кінцевого мозку і всієї нової кори (див. рис. 15-6). Аксони норадренергічних нейронів дорсального рухового ядра блукаючого нерва, поодинокого ядра, дорсальної і латеральної ділянок покриву середнього мозку формують латеральну систему покриву, яка передає імпульси до спинного мозку, стовбура головного мозку, усіх ділянок гіпоталамуса й основи кінцевого мозку. Висхідні волокна, що відходять з голубої плями, утворюють дорсальний норадренергічний пучок, а висхідні волокна латеральної системи покриву - вентральний норадренергічний пучок (див. рис. 15-6).
Засоби, що збільшують концентрацію норадреналіну в головному мозку, поліпшують настрій, а засоби, що знижують її, спричинюють депресію. Проте, як зазначено вище, в разі дослідження патогенезу депресії акцент сьогодні переходить від норадреналіну до серотоніну. Крім того, в осіб з вродженим дефіцитом DBH депресії не простежується. Звичайно, проблема значення моноамінів у діяльності головного мозку складна, оскільки висока позаклітинна концентрація нейротрансмітерів може спричинити вторинну дію, зокрема на рецептори.
Функція системи голубої плями не з’ясована, хоч відомо, що її електрична активність зростає під впливом раптових сенсорних подразників, і це може бути пов’язане
з пильністю і безсонням. Вентральна норадренергічна система покриву впливає на секрецію гіпофізотропних гормонів, що регулюють продукування гормонів передньої частки гіпофіза (див. Розділ 14). Норадреналін і серотонін, очевидно, беруть участь у регулюванні температури тіла.
Адреналін
У довгастому мозку є система нейронів, які містять фенілетаноламін-N-метилтрансферазу і які впливають на гіпоталамус. Ці нейрони виробляють адреналін, однак функція їхня точно не відома. Адреналінопродукувальні нейрони мають зв’язки з таламусом, центральною сірою речовиною і спинним мозком. У ЦНС виявлено також значні кількості тираміну, функція якого чітко не визначена.
Дофамін
У головному мозку міститься багато дофамінергічних систем. Стосовно довжини їхніх аксонів ці системи доцільно поділяти на ультракороткі, проміжні і довгі. До ультракоротких дофамінергічних нейронів належать клітини, розміщені між внутрішнім ядерним і внутрішнім сітчастим шарами сітківки ока (див. Розділ 8), та навколоклубочкові клітини нюхової цибулини (див. Розділ 10). Дофамінергічні нейрони з аксонами проміжної довжини є в складі таких систем: горбово-лійкової системи (див. рис. 15-6 і 15-7), де дофамін надходить у гіпофізарні портальні судини і гальмує секрецію пролактину; невизначено-таламічної системи, що сполучає гіпоталамус з латеральними перегородковими ядрами; навколошлуночкової групи нейронів довгастого мозку, клітини якої розсіяні в речовині мозку вздовж стінок четвертого шлуночка. Довгоаксонні дофамінергічні системи (див. рис. 15-6) - це чорноречовинно-смугаста система, аксони нейронів якої проходять з чорної речовини до смугастого тіла, і яка бере участь у регулюванні рухової активності (див. Розділ 12); і середньомозково-кіркова система, аксони нейронів якої з покриву середнього мозку проходять до лімбічної кори, нюхового горбика, напівлежачого ядра і відповідних підкіркових ділянок лімбічної системи. Сучасні дослідження, виконані в практично здорових людей за допомогою сканувальної ПЕТ (див. Розділ 32), засвідчили, що з віком кількість дофамінових рецепторів у базальних ядрах значно зменшується. Цей процес більше виражений у чоловічому організмі, ніж у жіночому.
Питання зв’язку середньомозково-кіркової системи, зокрема її вентральної частини від покришки до напівлежачого ядра із залежністю розглянуто вище. Вірогідно, що ушкодження середньомозково-кіркової системи зумовлює щонайменше частину симптомів шизофренії. Початково дослідники зосереджували увагу на переподразненні D2- дофамінових рецепторів лімбічної системи. Амфітамін, що, як і норадреналін, зумовлює виділення дофаміну в головному мозку, спричинює подібний до шизофренії психоз. Оскільки ж кількість D2-рецепторів у головному мозку в разі шизофренії підвищена, то є логічною позитивна кореляція між протишизофренічною активністю багатьох фармакологічних засобів і їхньою здатністю блокувати D2-рецептори. Однак багато сучасних засобів, активних у лікуванні психозів, блокують не D2-, а D4-рецептори, тому сьогодні вивчають питання, чи ці рецептори не є змінені в осіб з шизофренією.
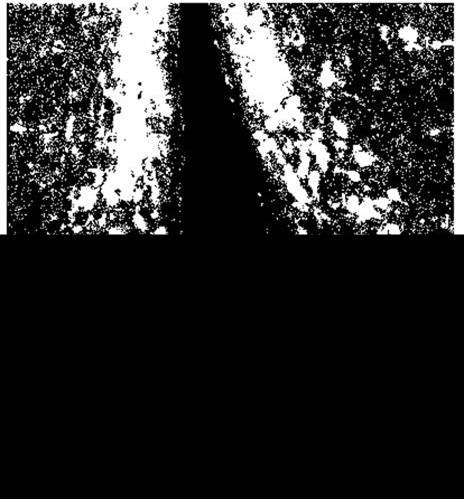
Рис. 15-7. Горбово-лійкова дофамінергічна система. Поперечний переріз гіпоталамуса щура (люмінесцентна мікроскопія). Зверніть увагу на тіла дофамінергічних клітин дугоподібного ядра з кожного боку третього шлуночка, а також на дні шлуночка, та дофамінергічні закінчення на судинах гіпофізарної портальної системи в зовнішньому шарі серединного підвищення (відтворено за дозволом з Hokfelt Т, Fuxe: On the morphology and the neuroendocrine role of the hypothalamic catecholamine neurons. In: Braine-Endocrine Interaction. Knigge К, Scott D, Weindl A [editors]. Karger, 1972).
Гістамін
Як зазначено в Розділі 4, тіла гістамінергічних нейронів містяться в горбово-сосочковому ядрі вентральної частини задньої ділянки гіпоталамуса. Аксони цих нейронів проходять до всіх частин головного мозку (див. рис. 15-6). Функція цих дифузних гістамінергічних систем остаточно не з’ясована, однак є очевидним зв’язок впливу гістаміну головного мозку на пробудження, статеву поведінку, кров’яний тиск, споживання води, поріг болю і регулювання секреції низки гормонів передньої частки гіпофіза.
Ацетилхолін
Ацетилхолін поширений по всій ЦНС. Висока його концентрація виявлена в корі великого мозку, таламусі та різних ядрах основи переднього мозку. Розподіл холінацетилтрансферази й ацетилхолінестерази відповідає розподілу ацетилхоліну. Головна кількість ацетилхолінестерази є в нейронах, проте її теж виявлено і в клітинах глії. Псевдохолінестераза міститься в багатьох відділах ЦНС. Як зазначено в Розділі 4, у головному мозку є різні типи нікотинових і мускаринових рецепторів. Множинні нікотинові холінергічні субодиниці, гени і білки, кодовані ними, утворюють різні за компонуванням пентамерні гетеродимери. В головному мозку містяться як постсинаптичні, так і пресинаптичні нікотинові холінергічні рецептори, по-різному скомпоновані в різних ділянках.
Застосування антитіл, специфічних до холінацетилтрансферази, та імуноцитохімічних методів дало змогу картувати холінергічні шляхи в головному мозку. Розподіл холінергічних нейронів подібний до їхнього розподілу в моноаміноергічній системі тим, що їхня частина дифузно спрямована до багатьох відділів головного мозку, а відрізняється в тому, що є холінергічні інтернейрони і короткі холінергічні системи по всій ЦНС. Зафіксовано також багато зв’язків базального ядра Мейнерта і сусідніх ядер з мигдалеподібним тілом та усією новою корою, і ці зв’язки забезпечують мотивацію, усвідомлення сприйняття і пізнавальну здатність. Значна втрата нейронів цієї системи простежується в разі хвороби Альцгеймера (див. Розділ 16). Система ПГО-піків, відповідальна за ШРО-сон, теж належить до холінергічних. Про зв’язок нікотину із залежністю йшлося вище. У великих дозах мускариноергічні блокувальні засоби, такі як атропін, можуть зумовлювати галюцинації, а скополамін має седативну дію.
Як зазначено у Розділах 12 і 13, соматомоторні, пре- і деякі постгангліонарні нейрони автономної нервової системи належать до холінергічних. Рівень ацетилхолінестерази в корі вищий у щурів, яких утримують групами, ніж у щурів, яких тримають в умовах ізоляції. Ацетилхолін у базальних ядрах є збуджувальним посередником, тоді як дофамін у цих структурах - інгібувальним (див. Розділ 12).
Опіоїдні пептиди
У головному мозку є три типи нейронів, що виділяють три молекули-попередники опіоїдних пептидів (див. табл. 4-4). Крім того, наявні ще два ендорфіни, прекурсори яких не відомі. Нейрони, у яких відбувається синтезування проенкефаліну, розсіяні по всьому головному мозку, тоді як тіла нейронів, що продукують проопіомеланокортин, містяться в дугоподібному ядрі, а їхні аксони проходять до таламуса і частин стовбура головного мозку (рис. 15-8). Продинорфін утворюється в нейронах, розміщених переважно в гіпоталамусі, лімбічній системі і стовбурі головного мозку. Опіоїдні пептиди беруть участь у різних процесах, зокрема розвитку толерантності і наркотичної залежності до морфіну, однак детально ці процеси не досліджені.
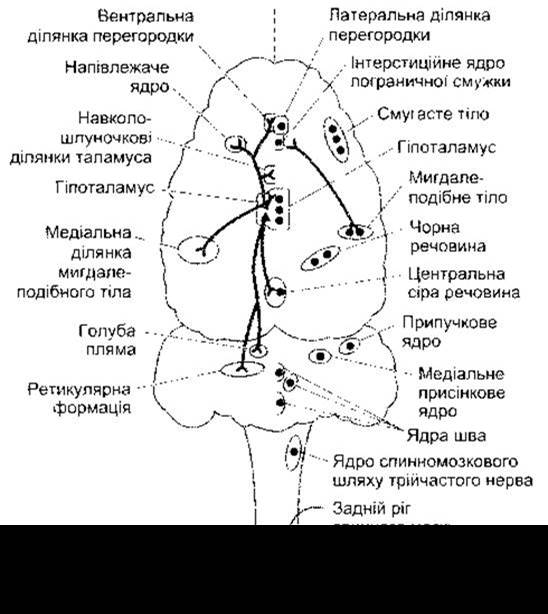
Рис. 15-8. Розподіл у головному мозку ß-ендорфінових (ліворуч) та енкефалінових (праворуч) нейронів (відтворено за дозволом з Barchas JD et al: Behavioral neurochemistry: Neuroregulatory and behavioral states. Science 1978;200:964).
Інші трансмітери
Зв’язок ГАМК з відчуттям тривоги і заспокійлива дія бензодіазепінів розглянуті в Розділі 4. Крім енкефалінів і ß-енкефаліну, ще інші пептиди, очевидно, беруть участь у забезпеченні емоційних та інших поведінкових реакцій, однак це питання не з’ясоване.