Фізіологія людини - Вільям Ф. Ґанонґ 2002
Ендокринна система, метаболізм і репродуктивна функція
Гормональне регулювання метаболізму кальцію та фізіологія кістки
Паращитоподібні залози
Анатомія
У людей в нормі є чотири паращитоподібні (синонім - прищитоподібні) залози: дві вкраплені у верхні полюси щитоподібної залози і дві - у нижні (рис. 21-9). Проте розташування паращитоподібних залоз у різних осіб та їхня кількість може помітно змінюватись. Паращитоподібну тканину іноді виявляють у середостінні. Кожна паращитоподібна залоза добре васкуляризована, розмірами близько 3x6x2 мм і містить два типи клітин. Численні головні клітини, що мають помітні апарат Ґольджі, ендоплазматичну сітку та секреторні гранули (рис. 21- 10), синтезують і секретують паратгормон. Менш численні та більші за розмірами оксифільні клітини містять оксифільні гранули та велику кількість мітохондрій у цитоплазмі. В людини до досягнення статевої зрілості їх лише декілька, однак з віком їхня кількість збільшується. Функція їхня невідома, хоча дехто й вважає їх дегенерованими головними клітинами.
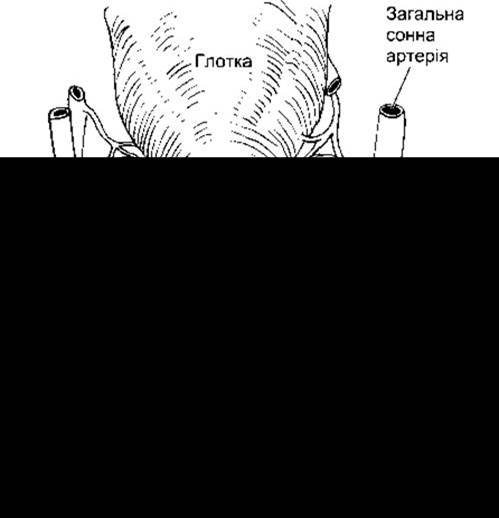
Рис. 21-9. Паращитоподібні залози людини, вигляд ззаду.
Синтез та метаболізм паратгормону
Паратгормон людини є лінійним поліпептидом з молекулярною масою 9500, що містить 84 амінокислотні залишки (рис. 21-11). Його будова дуже подібна до будови бичачого і свинячого паратгормонів. Він синтезується як частина більшої молекули, що містить 115 амінокислотних залишків (препропаратгормон). У разі надходження препропаратгормону в ендоплазматичну сітку лідерна послідовність виходить з амінокінця, утворюючи 90-амінокислотний поліпептид пропаратгормон. Шість інших амінокислотних залишків відходять з амінокінця пропаратгормону в апараті Ґольджі, і 84-амінокислотний поліпептид паратгормон входить у секреторні гранули і вивільняється як основний секреторний продукт головних клітин.
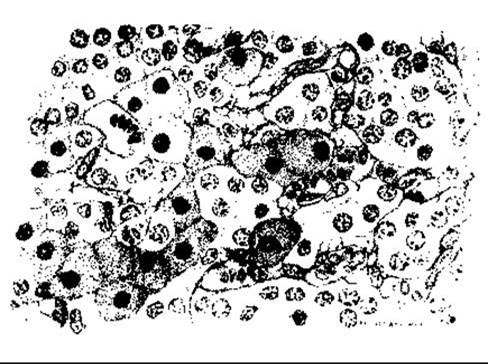
Рис. 21-10. Переріз паращитоподібної залози людини (зменшено 50% з х960). Малі клітини - це головні; великі шорохуваті (особливо виразні в лівому нижньому куті зображення) - оксифільні (відтворено за дозволом з Fawcett DW: Bloom and Fawcett, A Textbook of Histology, 11th ed. Saunders, 1986).

Рис. 21-11. Паратгормон. Символи під та над будовою гормону людини відображають відмінні амінокислотні залишки бичачого та свинячого паратгормону (відтворено за дозволом з Keutmann НТ et al: Complete amino acid sequence of human parathyroid hormone. Biochemistry 1978; 17-5723).
Нормальний рівень інтактного паратгормону в плазмі становить 10-55 пг/мл; період півжиття - близько 10 хв, секретований поліпептид швидко розщеплюють клітини Купфера в печінці до фрагментів з карбоксильного кінця та середньої частини молекули, що, очевидно, є біологічно неактивними. Паратгормон та ці фрагменти потім виходять через нирки. Цікаво, що синтетичний поліпептид, у складі амінокінця якого є 34 амінокислотні залишки паратгормону, виявляє всі відомі біологічні ефекти цілої молекули паратгормону.
Оскільки в багатьох старих радіоімунологічних аналізах на паратгормон використовували антитіла проти середньої ділянки молекули, то вони, окрім інтактного гормону, визначали також і фрагменти, тому давали помилково завищені значення. Це особливо стосувалося хворих з нирковою недостатністю, адже в них ці фрагменти не виводились. Щоб усунути цю проблему, вчені розробили двосайтові імунологічні аналізи, що використовують одні антитіла проти амінокінця, а інші - проти карбоксильного кінця молекули. Спершу плазма реагує з радіоактивно значеними амінокінцевими антитілами, а потім долучається до кульок, до яких були зв’язані незначені антитіла до карбоксильного кінця. Кульки відмивають і вимірюють їхню зв’язану радіоактивність. Лише інтактний паратгормон впізнають обидва антитіла, завдяки чому отримують точне значення паратгормону, що циркулює (1-84).
Дії
Паратгормон діє безпосередньо на кістки, збільшуючи їхню резорбцію та мобілізацію Са2+. Окрім збільшення Са2+ та зменшення рівня фосфату в плазмі, паратгормон збільшує екскрецію фосфату з сечею. Ця фосфатурична дія є наслідком зменшення реабсорбції фосфату в проксимальних канальцях. Паратгормон також збільшує реабсорбцію Ca2+ в дистальних канальцях, хоча екскреція Са2+ часто збільшена в разі гіперпаратиреозу, тому що кількість фільтрагу перевищує вплив реабсорбції. Паратгормон також збільшує утворення 1,25-дигідроксихолекальциферолу, а це посилює абсорбцію Са2+ з кишки.
У тривалішому часовому масштабі паратгормон стимулює остеокласти та остеобласти (див. табл. 21 -2), причому вплив на остеокласти переважає, завдяки чому більше Са2+ мобілізується з кістки.
Механізм дії
Тепер уважають, що є принаймні три різні рецептори паратгормону. Один з них також зв’язує пептид, залежний від паратгормону (РТНrР - від англ. pathyroid-related protein) (див. нижче) і відомий як рецептор hРТН/РТНrР. Інший рецептор - РТН2 (hPTH2-R) - не зв’язує РТНrР, його виявлено в мозку, плаценті та підшлунковій залозі. Крім того, є докази існування ще одного рецептора - СРТН, - який реагує з карбоксильним, а не амінокінцем паратгормону. Перші два рецептори серпентинові, зв’язані з Gs, і через цей гетеротримерний G-білок активують аденілатциклазу, збільшуючи вміст внутрішньоклітинного цАМФ. Рецептор hРТН/РТНrР також активує ФЛС через Gq, збільшуючи внутрішньоклітинний вміст Са2+ та активуючи протеїнкіназу С (рис. 21-12). Проте шлях, яким ці вторинні месенджери діють на Са2+ в кістці, остаточно не з’ясований.
У випадку хвороби, названої псевдогіпопаратиреозом, розвиваються ознаки та симптоми гіпопаратиреозу, однак рівень паратгормону, що циркулює, нормальний або підвищений. Оскільки тканини не відповідають надію гормону, то ця хвороба пов’язана з рецепторами. Є дві її форми. У поширенішій виникає спадкове зменшення активності Gs на 50%, і паратгормон не здатний забезпечити достатнє збільшення концентрації цАМФ. В іншій, менш поширеній формі, відповідь цАМФ нормальна, проте фосфосечова дія гормону дефектна.
Регулювання секреції
Йонізований кальцій, що циркулює, діє безпосередньо на паращитоподібні залози за механізмом негативного зворотного зв’язку, регулюючи секрецію паратгормону (рис. 21-13). Ключем до такого регулювання є рецептор Са2+ у клітинній мембрані. Цей серпентиновий рецептор зв’язаний через G-білок з фосфоінозитидним перетворенням, він виявлений у багатьох тканинах. У паращитоподібних залозах його активування пригнічує секрецію паратгормону. Якщо рівень Са2+ у плазмі високий, то секреція паратгормону пригнічена, і кальцій відкладається в кістках. Якщо ж його концентрація низька, то секреція посилюється і Са2+ мобілізується з кісток.
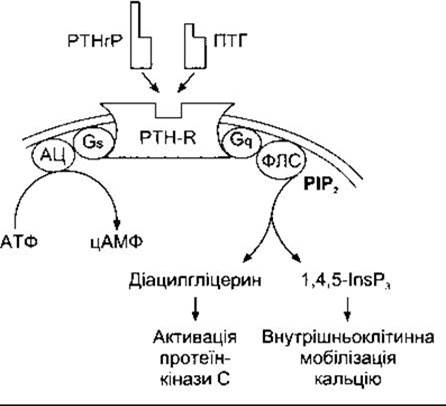
Рис 21-12. Шляхи передавання сигналів, активованих зв’язуванням ПТГ чи РТНrР з рецептором hPTH/hPTHrP. Внутрішньоклітинний цАМФ збільшується через Gs та аденілатциклазу (АЦ). Діацилгліцерин та ІФ3 (1,4,5-lnsP3) збільшуються під дією Gq та фосфоліпази С (ФЛС) (модифіковано за дозволом з Shoback DM, Strewler GJ: Disorders of the parathyroids and calcium metabolism. In McPhee SH et al. Pathophysiology of Disease, 3rd ed. McGraw-Hill, 2000).
Гормон 1,25-дигідроксихолекальциферолу впливає безпосередньою на паращитоподібні залози, зменшуючи мРНК препропаратгормону. Підвищена кількість фосфатів у плазмі стимулює секрецію паратгормону, знижуючи концентрацію Са2+ в плазмі та інгібуючи утворення 1,25-дигідроксихолекальциферолу. Для підтримання нормальної секреторної відповіді паращитоподібних залоз потрібен магній. Погіршене вивільнення паратгормону разом з послабленою відповіддю органа-мішені на дію паратгормону призводить до гіпокальціємії, що інколи простежується внаслідок нестачі магнію.
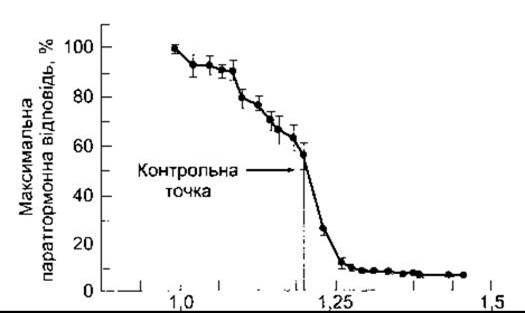
Рис. 21-13. Взаємозв’язок між концентрацією Са2+ в плазмі та відповіддю паратгормону у людини. Контрольна точка відповідає концентрації Са2+ у плазмі, за якої відбувається половина максимальної відповіді (модифіковано за дозволом з Brown Е: Extracellular Са2+ sensing, regulation of parathyroid cell functions, and role of Ca2+ and other ions as extracellular (first) messengers. Physiol Rev 1991;71:371).
Вплив паратиреоїдектомії
Паратгормон абсолютно необхідний для життя. Після паратиреоїдектомії стійко знижується рівень Са2+ в плазмі. З’являються ознаки нервово-м’язової надмірної збудливості, що супроводжуються повною гіпокальціємічною тетанією (див. вище). Звичайно, у разі зниження рівня кальцію після паратиреоїдектомії підвищується рівень фосфату в плазмі, однак не завжди.
У людей тетанія найчастіше є наслідком недбалої паратиреоїдектомії під час операцій на щитоподібній залозі. Симптоми зазвичай виникають через два-три дні після операції, проте можуть не з’являтись протягом кількох тижнів чи й більше. У щурів, які з їжею отримують малий вміст кальцію, тетанія розвивається набагато швидше, через 6-10 год після паратиреоїдектомії. Введення паратгормону усуває хімічні аномалії, і симптоми зникають. Уведення солей кальцію дає тимчасове полегшення.
Ознаки тетанії в людини охоплюють симптом Хвостека - швидке скорочення іпсилатеральних лицьових м’язів, зумовлене відгалуженням лицьового нерва на куті нижньої щелепи; та симптом Труссо - спазм м’язів верхніх кінцівок, що спричинює згинання зап’ястя та великого пальця з розгинанням інших пальців (рис. 21-14). В осіб з помірною тетанією, в яких не виявляються спазми, симптом Труссо іноді може бути зумовлений припиненням кровообігу в разі накладання манжети для вимірювання кров’яного тиску.
Надлишок паратгормону
Гіперпаратиреоїдизм унаслідок уведення великих доз екстракту паратгормону в тварин чи гіперсекреції функційної паращитоподібної пухлини в людей зумовлює гіперкальціємію, гіпофосфатемію, демінералізацію кісток, гіперкальцинурію та утворення кальцієвмісних ниркових каменів.
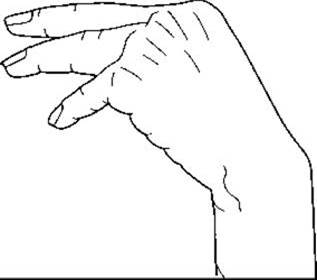
Рис. 21-14. Положення руки у випадку гіпокальціємічної тетанії (синдром Труссо).
Хвороба кісток, спричинена тривалим гіперпаратиреоїдизмом, - це остеофіброма, за якої відбувається фіброз кісткового мозку та збільшене ремоделювання кістки з резорбцією, що випереджає утворення кістки.
Вторинний гіперпаратиреоїдизм
У випадку таких станів, як хронічна хвороба нирок та рахіт, за яких рівень Са2+ у плазмі хронічно низький, стимулювання паращитоподібних залоз зумовлює компенсаторну паращитоподібну гіпертрофію та вторинний гіперпаратиреоїдизм. Рівень Са2+ в плазмі низький у разі хронічної хвороби нирок тому, що хворі нирки втрачають здатність виробляти 1,25-дигідроксихолекальциферол. Проте утримування фосфату з кінцевою гіперфосфатемією також робить внесок у зменшення Са2+ в плазмі.
Родинна гіперкальціємія та гіпокальціємія
Мутації в гені рецептора Са2+ спричинюють передбачувані довготривалі зміни рівня Са2+ в плазмі. Гетерозиготні за інактивувальною мутацією особи мають родинну м’яку гіпокальцинуричну гіперкальціємію, стан, за якого простежується хронічне помірне підвищення рівня Са2+ в плазмі, оскільки зворотне інгібування секреції паратгормону кальцієм зменшене. Рівні паратгормону в плазмі нормальні чи навіть підвищені. Проте в осіб, що є гомозиготними за інактивувальною мутацією, розвивається неонатальний важкий первинний гіперпаратиреоїдизм. В осіб з активувальними мутаціями гена рецептора Са2+ виникає родинна гіперкальцинурична гіпокальціємія внаслідок збільшеної чутливості паращитоподібних залоз до Са2+ в плазмі.
Пептид, подібний до паратгормону
Білок з активністю паратгормону утворюють багато різних тканин організму. Він має 140 амінокислотних залишків, на відміну від паратгормону, у якому їх 84, і кодований геном 12-ї хромосоми людини, тоді як паратгормон - геном в 11-й хромосомі. Незважаючи на це, паратгормон та пептид, подібний до паратгормону, мають помітну гомологію на їхніх амінокінцях. У цьому разі у 8 з перших 13 амінокислот однакове розташування і вони обидва зв’язуються з рецептором hPTH/PTHrP. У хрящі, що розвивається, РТНrР стимулює проліферацію хондроцитів і пригнічує їхню мінералізацію. Він, здається, також діє як фактор росту на розвиток шкіри, волосяних фолікулів та молочних залоз. Миша, в якої обидві копії гена РТНrР зазнали нокауту, помирає невдовзі після народження і має сильні аномалії скелета. Мутація, що робить рецептор hРТН/РТНrР конститутивно активним, пов’язана із однією з форм карликовості.
В дорослих РТНrР у великих кількостях утворюється в молочних залозах і великі його кількості знайдені в молоці. Проте його рівень у плазмі не збільшується під час лактації, а функція РТНrР в молоці невідома. Пептид РТНrР також виявлений у клубочках і канальцях нирок та в мозку, де він є в корі головного мозку, морському конику та гранулярному шарі кори мозочка.
Злоякісна гіперкальціємія
Гіперкальціємія є поширеним метаболічним ускладненням раку. Близько 20% гіперкальціємічних пацієнтів мають кісткові метастази внаслідок роз’їдання кістки (місцева остеолітична гіперкальціємія). Є докази, що цей процес відбувається під впливом пухлинних простагландинів, таких як ПГЕ. З’ясовано, що кілька лімфом секретують 1,25-дигідроксихолекальциферол, однак це рідкість. Гіперкальціємія у решти 80% пацієнтів, здається, є наслідком підвищених рівнів РТНrР (гуморальна злоякісна гіперкальціємія). Пухлини, що відповідають за гіперсекрецію, - це раки молочної залози, нирок, яєчників та шкіри.