Фізіологія людини - Вільям Ф. Ґанонґ 2002
Фізіологія нервових і м'язових клітин
Синаптичне і контактне передавання
Нервово-м'язове передавання - Нервово-м'язове з'єднання
Структура
Аксон, що іннервує скелетні м’язи, закінчується термінальними розгалуженнями. У цьому разі він втрачає мієлінову оболонку й утворює велику кількість закінчень - синаптичних бляшок (рис. 4-35). Синаптична бляшка містить багато невеликих прозорих пухирців, заповнених ацетилхоліном - трансмітером цих з’єднань. Нервові закінчення розташовані в заглибинах рухової кінцевої пластинки, що є потовщенням м’язової мембрани в місці з’єднання. Під нервовим закінченням м’язова мембрана кінцевої пластинки формує складки. Проміжок між нервовим закінченням і потовщенням м’язової мембрани відповідає синаптичній щілині інших синапсів. Цілу цю структуру називають нервово-м’язовим, або м’язово-нервовим з’єднанням, або ж нервово-м’язовим, чи м’язово-нервовим синапсом. На кожній кінцевій пластинці закінчується лише одне нервове волокно, яке називають синаптичною бляшкою, і, отже, тут не відбувається конвергенції нервових імпульсів.
Послідовність процесів під час передавання
Процеси, що відбуваються під час передавання імпульсів з рухового нерва до м’яза (див. табл. 3-2), частково відповідають процесам, які відбуваються в інших синапсах. Під впливом імпульсу, що надходить до терміналі рухового нейрона, активізується проникність нервових закінчень для Са2+. Катіон Са2+ надходить до закінчень і зумовлює помітне посилення процесу екзоцитозу ацетилхолінових пухирців. Ацетилхолін дифундує до нікотиноподібних холіно-рецепторів м’язового типу (див. рис. 4-18), що скупчені на верхівках складок мембрани рухової кінцевої пластинки. Зв’язування ацетилхоліну з цими рецепторами спричинює посилення провідності мембрани стосовно Na+ та К+, а надходження Na+ приводить до виникнення деполяризаційного потенціалу - потенціалу кінцевої пластинки. Під впливом цього локального потенціалу відбувається деполяризація суміжних ділянок м’язової мембрани, а також досягається критичний рівень деполяризації. Зі синаптичної щілини ацетилхолін розщеплює ацетилхолінестераза, що в високих концентраціях міститься в нервово-м’язовому синапсі. Потенціали дії генеруються по обидва боки від кінцевої пластинки, і їх проводить м’язове волокно в обидвох напрямах. М’язовий потенціал дії, відповідно, ініціює м’язове скорочення, як це описано в Розділі 3.
Потенціал кінцевої пластинки
Кінцева пластинка в людини містить у середньому 15—40 мільйонів ацетилхолінових рецепторів. Кожен нервовий імпульс зумовлює виділення ацетилхоліну приблизно з 60 пухирців, а кожний пухирець містить близько 10 000 молекул нейротрансмітера. Цієї кількості достатньо для активування приблизно в 10 разів більшої кількості ацетилхолінових рецепторів, ніж це необхідно для виникнення в кінцевій пластинці повноцінного потенціалу. Тому м’яз систематично відповідає скороченням, і ця відповідь приховує справжній потенціал. Потенціал кінцевої пластинки можна оцінити, якщо застосувати певний чинник, що в 10 разів знизить його, і він стане недостатнім, щоб спричинити деполяризацію суміжної м’язової мембрани. З цією метою застосовують невеликі дози кураре-речовини, що конкурує з ацетилхоліном за зв’язування з нікотиночутливими холінорецепторами. В цьому випадку реакцію можна зареєструвати лише в ділянці кінцевої пластинки, далі ж вона експоненціально загасає. За цих умов можна спостерігати часову сумацію потенціалів кінцевої пластинки.
Квантове виділення трансмітера
Невеликі кванти («пакети») ацетилхоліну безладно виділяються через мембрану аксона навіть у стані спокою, зумовлюючи кожен незначну деполяризацію постсинаптичної мембрани амплітудою близько 0,5 мВ, що називають мініатюрним потенціалом кінцевої пластинки. Кількість квантів ацетилхоліну, що виділяються таким способом, прямо пропорційна до концентрації Са2+ й обернено пропорційна до концентрації Mg2+ у кінцевій пластинці. Коли ж нервовий імпульс надходить до нервового закінчення, то кількість квантів ацетилхоліну, що виділяються, збільшується на багато порядків, і, як наслідок, виникає значний потенціал кінцевої пластинки, який зумовлює появу критичного рівня деполяризації м’язового волокна.
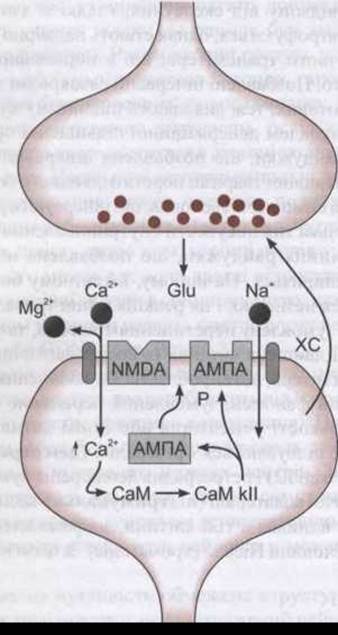
Рис. 4-34. Виникнення довготривалої потенціації (ДТП) в дендритах клітин СА1 гіпокампа. Глютамат (Glu), що виділяється з пресинаптичного нейрона, зв'язується з АМПА- та NMDA- рецепторами мембрани дендрита. Деполяризація, спричинена активуванням АМПА-рецепторів, зумовлює припинення магнієвого блокування каналів NMDA-рецепторів, і Са2+ разом з Na+ надходять у нейрон. Збільшення внутрішньоклітинної концентрації Ca2+ забезпечує активування кальмодуліну (СаМ), що, відповідно, зумовлює активування Са2+ кальмодулінкінази II (СаМ кІІ). Кіназа фосфорилює АМПА-рецептор (Р), збільшуючи його провідність і, вірогідно, сприяючи пересуванню більшої кількості АМПА-рецепторів до синаптичної ділянки клітинної мембрани. Крім того, до пресинаптичного нейрона може надходити хімічний сигнал (ХС), зумовлюючи довготривале збільшення квантового вивільнення глютамату.
Квантове виділення ацетилхоліну, що відбувається в нервово-м’язовому синапсі, характерне також для інших холінергічних синапсів. Подібні процеси виникають, очевидно, і в норадренергічних та інших синаптичних контактах.
Важка міастенія і синдром Ламберта-Ітона
Важка міастенія - це серйозне, інколи смертельне захворювання, за якого скелетні м’язи слабшають і легко втомлюються. Захворювання виникає внаслідок утворення антитіл, що циркулюють до нікотиноподібних холінорецепторів. Ці антитіла одні рецептори руйнують, а інші зв’язують з сусідніми рецепторами, після чого вони усуваються шляхом ендоцитозу (див. Розділ 1). Причина виникнення автоімунності стосовно ацетилхолінових рецепторів досі не з’ясована.
Іншим захворюванням, подібним до важкої міастенії, є синдром Ламберта-Ітона. У цьому випадку м’язова слабкість спричинена утворенням антитіл до одного з Са2+-каналів нервових закінчень нервово-м’язового синапсу. Це призводить до зменшення кількості надходження Са2+ і, відповідно, виділення меншої кількості трансмітера. Однак за умов тривалих скорочень зі збільшенням виділення Са2+ м’язова сила наростає.