ОСНОВЫ МИКРОБИОЛОГИИ - В. М. Самыгин - 2015
ГЛАВА 11. МЕТОДЫ ВЫДЕЛЕНИЯ И ИДЕНТИФИКАЦИИ МИКРООРГАНИЗМОВ
В лабораторной практике для обнаружения и идентификации микроорганизмов используют различные методы. Эти методы основаны на изучении микробных клеток, характере роста на питательных средах, биохимической активности и антигенной структуре, специфичности нуклеотидной последовательности ДНК. В их числе бактериологический, микроскопические, иммунологические и молекулярно-генетические методы.
11.1. Микроскопические методы исследования
Микроскопическое исследование материала обычно начинается с микроскопии нативных мазков. Результаты световой микроскопии недостаточны для идентификации микроорганизмов, но дают возможность получать ориентировочное представление об их количестве в материале и принадлежности к палочковидной или кокковидной микрофлоре. В случае применения окраски по Грамму определяется дальнейший ход исследования, целью которого является выделение и установление видовой принадлежности микроорганизма. Вместе с тем некоторые из микроорганизмов способны образовывать капсулы, формировать эндо- и экзоспоры или превращаться в цисты. В зависимости от условий культивирования и методов окрашивания можно наблюдать за морфологией самих клеток или отдельных клеточных структур.
Для определения формы и подвижности бактерий используют препараты «раздавленной» или «висячей» капли, т. е. проводят микроскопию бактерий в живом состоянии. Однако для того, чтобы увидеть четкие контуры микроорганизмов, готовят препараты и проводят микроскопию мазков микроорганизмов в окрашенном состоянии, т. е. применяют различные методы биологического окрашивания. Среди них методы, направленные на обнаружение кислотоустойчивых микроорганизмов, спор, капсул, клеточной стенки, жгутиков, цитоплазматических включений и др.
Для световой микроскопии биологические объекты обычно окрашивают, предварительно приготовив фиксированные препараты. При исследовании живых и неокрашенных биологических препаратов используют фазово-контрастную и темнопольную микроскопию. Клетки окрашенных микроорганизмов отчетливо выделяются на серебристо-белом фоне препарата, создавая яркую картину микробного пейзажа. Использование специальных методов окраски позволяет выявить морфологические объекты и структуры содержащихся в материале микробных клеток (наличие спор, капсул, жгутиков и пр.).
Мазки для микроскопии готовят из культур микроорганизмов с плотных или жидких питательных сред, а также из различного материала. При приготовлении мазков с плотных питательных сред на середину чистого обезжиренного предметного стекла наносят каплю водопроводной воды или физиологического раствора NаСl. В нее бактериологической петлей вносят небольшое количество исследуемой культуры. Излишек микробного материала на петле сжигают в пламени спиртовки. При приготовлении мазков из жидких питательных сред каплю бульонной культуры наносят на предметное стекло пастеровской пипеткой или бактериологической петлей и круговыми движениями распределяют равномерным слоем диаметром 8-10 мм. Мазки должны содержать достаточно материала для полноценного исследования, но не должны быть чрезмерно толстыми, т. к. содержащиеся в них клетки будет трудно дифференцировать.
Приготовленные на предметном стекле мазки высушивают на воздухе и фиксируют. Фиксация мазка преследует несколько целей:
- инактивировать содержащиеся в мазке микроорганизмы;
- зафиксировать на поверхности стекла микробные клетки, во избежание их соскальзывания со стекла при последующей окраске и промывке препарата;
- повысить восприимчивость клеток к окрашиванию, поскольку убитые микробные клетки окрашиваются значительно лучше живых.
Различают физический и химический способы фиксации. Физический способ основан на воздействии температуры на микробную клетку, химический - на применении химических средств, вызывающих коагуляцию белков цитоплазмы.
При физическом способе фиксации предметное стекло с мазком, находящимся на верхней поверхности стекла, проносят 2- 3 раза над пламенем горелки. Весь процесс фиксации занимает 2- 3 секунды. Для фиксации микробов с помощью химических веществ применяют метиловый и этиловый спирты, ацетон, смеси Никифорова, Пешкова, Карнуа, Буэна, а также коммерческий формалин. В этих случаях в зависимости от используемого вещества время фиксации составляет от 5 до 20 минут.
Методы окраски микроорганизмов подразделяют на простые и сложные дифференциальные. Простыми методами пользуются для обнаружения в материале микробов, определения их количества, формы и расположения. При простых способах окраски применяют один краситель, чаще всего метиленовый синий или водно-спиртовой раствор фуксина.
При использовании сложных дифференциальных методов мазок окрашивается первично тем красителем, при помощи которого надеются выявить предполагаемый микроорганизм на основании его физико-химических особенностей. За ним следует протрава мазка химическими соединениями (кислотами, щелочами, спиртом, фенолом и пр.), результатом чего является обесцвечивание всех остальных находящихся в мазке микроорганизмов. После протравы проводят дополнительное окрашивание краской контрастного цвета.
Многие сложные дифференциально-диагностические методы окраски можно рассматривать как один из начальных этапов идентификации микроорганизма. Наиболее распространенными среди них являются следующие методы.
Окраска по методу Грама. Предложенный в конце XIX века датским бактериологом Грамом метод дифференциальной окраски позволил разделить большую часть известных микроорганизмов на две группы: грамположительные и грамотрицательные. Восприимчивость к окраске по Граму определяется толщиной клеточной стенки и ее химической структурой. Клеточная стенка грамположительных микроорганизмов представляет собой многослойные пептидогликановые структуры (20-60 нм), ковалентно связанные с тейхоевыми и липотейхоевыми кислотами, выступающими на поверхность клетки через поры пептидогликанового каркаса. Способность грамположительных клеток удерживать комплекс йода с кристаллическим фиолетовым связана со способностью пептидогликана взаимодействовать с красителем, а также со структурой пор пептидогликана, которая препятствует вымыванию красителя при обработке мазка бактерий спиртом.
Толщина клеточной стенки грамотрицательных микроорганизмов значительно меньше (10-20 нм), чем у грамположительных микроорганизмов, но устроена сложнее. В ее состав дополнительно входит наружная мембрана, связанная бимолекулярным слоем липидов поверхностного слоя пептидогликана. Грамотрицательные бактерии при обработке препарата спиртом вследствие недостаточного количества пептидогликана в клеточной стенке утрачивают комплекс йода с кристаллическим фиолетовым, обесцвечиваются и затем приобретают контрастный цвет дополнительного красителя (фуксина или сафранина).
Для окраски бактерий по методу Грама приготовленный на предметном стекле мазок высушивают на воздухе и фиксируют над пламенем горелки. На мазок наливают раствор основного красителя - кристаллического фиолетового - на 1-2 мин. Сливают остаток краски и наливают раствор Люголя до почернения препарата (обычно на 1-2 мин.). Затем сливают раствор Люголя, и в течение 20-30 с. препарат обрабатывают этиловым спиртом, тщательно промывают водой, докрашивают водно-спиртовым раствором фуксина в течение 2 мин. Окрашенный мазок высушивают и микроскопируют.
Важно соблюдать время обесцвечивания мазка, поскольку более продолжительная обработка спиртом ведет к обесцвечиванию грамположительных микробов, а при недостатке времени обесцвечивания клеток не происходит, и они сохраняют фиолетовый цвет основного красителя.
Окраска кислотоустойчивых бактерий. Кислотоустойчивыми называют микробы, которые будучи окрашенными карболовым фуксином не обесцвечиваются под действием концентрированных неорганических кислот. Особенностью микробов этой группы является то, что они плохо воспринимают окраску. Это свойство обусловлено наличием в клеточной стенке и цитоплазме кислотоустойчивых бактерий длинно цепочных жирных кислот с 50-100 атомами (миколовая, туберкулостеариновая), которые делают клеточную стенку микроорганизма непроницаемой для кристаллвиолета и других красителей. Поэтому, чтобы обеспечить проникновение краски в клеточную стенку этих бактерий, применяют более концентрированные растворы красок в подогретом состоянии, добавляют в них детергенты и удлиняют сроки окраски. После того как краска введена в клетку, ее нельзя обесцветить обычными кислотами и спиртовыми растворителями.
Для окрашивания кислотоустойчивых бактерий обычно применяют метод Циля-Нильсена и некоторые другие модифицированные методы.
При окраске по методу Циля-Нильсена фиксированный мазок окрашивают 3-5 минут раствором карболового фуксина Циля. Дают препарату остыть, сливают избыток красителя, препарат промывают водой. Окрашенный препарат обесцвечивают 5 % раствором серной кислоты в течение 3-5 с или 95 % этиловым спиртом, содержащим 3 % (по объему) хлористоводородной кислоты (НСl), несколько раз погружая предметное стекло в сосуд с солянокислым спиртом. После обесцвечивания остаток кислоты сливают и тщательно промывают препарат водой. Докрашивают дополнительно водным раствором метиленового синего Леффлера в течение 3- 5 минут. Окрашенный препарат промывают водой, подсушивают и микроскопируют.
При окраске препаратов по методу Циля-Нильсена кислотоустойчивые бактерии окрашиваются фуксином в рубиново-красный и не обесцвечиваются кислотой. Некислотоустойчивые бактерии под действием кислоты обесцвечиваются и приобретают цвет дополнительного красителя.
Методы выявления и окраски капсул. Некоторые виды микроорганизмов продуцируют капсульное вещество, которое, концентрируясь вокруг микробной клетки, образует капсулу. При обычных методах окраски капсулы остаются бесцветными. Это позволяет для их выявления применять простые методы окраски. При окраске метиленовым синим бактериальные клетки окрашиваются в голубой цвет, тогда как вокруг бактерий сохраняется бесцветная зона - капсула, выявляемая на темном фоне. Для окрашивания вещества капсул применяют специальные методы окраски. При выявлении капсул по методу Бурри на конец предметного стекла наносят каплю туши, в которой эмульгируют бульонную культуру или часть колоний, снятой с плотной питательной среды. После тщательного перемешивания смеси петлей делают мазок, который высушивают на воздухе и, не фиксируя, микроскопируют с иммерсионной системой. Фон препарата становится окрашенным в темно-дымчатый цвет, микробные клетки и капсулы не окрашиваются тушью и остаются бесцветными, вследствие чего этот метод получил название негативного. Способом Бурри можно пользоваться не только для выявления капсул микроорганизмов, но и для обнаружения в исследуемом материале спирохет.
Окраска клеточной стенки. При обычных способах окраски выявить клеточную стенку невозможно. Для ее контрастирования мазок нуждается в специальной обработке, предшествующей окрашиванию. Препарат готовят из сильно разбавленной микробной взвеси, чтобы между микробными клетками было свободное пространство, и они не накладывались бы друг на друга.
При окраске клеточной стенки по способу Гутштейна препарат, приготовленный из микробной взвеси, подсушивают на воздухе, фиксируют в жидкости Буэна (насыщенный раствор пикриновой кислоты), протравливают водным раствором танина, промывают водопроводной водой. Окрашивают спиртоводным раствором кристаллического фиолетового, остаток краски сливают и препарат, не промывая водой, высушивают.
При микроскопии клеточные стенки имеют вид длинных тонких нитей темно-фиолетового или черного цвета, очерчивающих клетки с белой или светло-голубой цитоплазмой.
Окрашивание эндоспор. Споры имеют вид образований округлой или овальной формы. Форма, величина и расположение спор постоянны для каждого вида бактерий. В отличие от вегетативной части клетки споры содержат значительно меньше свободой воды и большое количество липидов и кальция. Плотная оболочка спор, непроницаемая для воды, окрашивается с большим трудом, поэтому при обычных методах окраски споры имеют вид неокрашенных пустот внутри клетки. Для окраски спор пользуются специальными методами с применением протрав (кислоты или щелочи). Протравы разрыхляют оболочку споры, облегчая проникновение в нее красителя. Окрасившиеся споры обладают кислотоустойчивостью, в отличие от вегетативной клетки, обесцвечивающейся под действием кислоты. Поэтому принцип окраски спор и кислотоустойчивых бактерий одинаков: препарат окрашивают основным красителем, затем обесцвечивают кислотой и докрашивают дополнительно в какой-нибудь контрастный цвет.
При окраске спор методом Ожешко на высушенный нефиксированный препарат (мазок готовится толстым слоем на краю стекла) наливают несколько капель 0,5 % раствора НСl и подогревают 1-2 мин над пламенем горелки до закипания, после чего остатки кислоты сливают. Остывший препарат промывают водой, подсушивают и фиксируют над пламенем горелки. Окрашивают карболовым фуксином Циля с подогреванием до паров, обесцвечивают 5 % раствором серной кислоты в течение нескольких секунд и промывают водой. Докрашивают в течение 3-5 минут метиленовым синим Леффлера или 1 % водным раствором малахитового зеленого. Окрашенные споры имеют рубиново-красный цвет, вегетативные клетки приобретают цвет дополнительного красителя - голубой при применении метиленового синего или зеленый при использовании малахитового зеленого.
При окраске спор методом Пешкова на фиксированный мазок наливают метиленовый синий Леффлера, дают краске закипеть. Окрашивание мазка кипящим красителем производится в течение 20-30 с. Препарат промывают водой, докрашивают 0,5 % раствором нейтрального красного в течение 30-60 с. Промывают водой и высушивают. Споры, окрашенные метиленовым синим Леффлера, имеют голубой цвет, вегетативные бактерии - красный.
Помимо световой микроскопии, для обнаружения и идентификации микроорганизмов часто используют фазово-контрастную и люминесцентную микроскопию, а также бактериологический метод исследования.
11.2. Бактериологический метод
Бактериологический метод заключается в посеве материала на искусственные питательные среды, выделении чистых культур и их последующей идентификации. Этот метод имеет чрезвычайно большое значение и в настоящее время является «золотым стандартом». Для получения полной информации необходимо изолировать все виды бактерий, находящихся в материале. Поэтому должны быть созданы необходимые условия обитания, включая адекватные питательные вещества и физико-химическое окружение.
В большинстве природных объектов присутствует множество различных видов микроорганизмов. Их количество зависит от целого ряда факторов, таких как структура, химический состав природного объекта и др. Материалом для посева могут служить вода, почва, продукты питания, биологические объекты и др. При посеве материала, подлежащего исследованию, на искусственные питательные среды микроорганизмы попадают в совершенно новую непривычную для них среду. Для успешной жизнедеятельности микроорганизмов недостаточно в первых генерациях обеспечить их в нужном количестве адекватными питательными веществами и ростовыми факторами. Для выделения конкретной культуры не меньшее значение имеет воспроизведение физико-химических факторов, характерных для естественных условий обитания микроорганизмов. К числу таких факторов относятся температура, pH среды выделяемого микроорганизма, газовый состав атмосферы культивирования (определенное соотношение кислорода, окиси углерода, азота), влажность. Только обеспечение перечисленных факторов гарантирует рост микроорганизмов, содержащихся в материале, и получение чистой культуры в количестве, необходимом для идентификации.
Для роста микроорганизмов необходимы питательные вещества, из которых микроорганизмы строят свои клетки и получают энергию. В принципе питательные среды должны отвечать следующим минимальным требованиям: в них должны присутствовать все элементы, из которых строится клетка, причем в такой форме, в какой микроорганизмы способны их усваивать. Многие нетребовательные микроорганизмы, например, большинство живущих в воде и почве псевдомонад, а также кишечная палочка, хорошо растут на глюкозо-минеральных средах. Более требовательные виды нуждаются в большом числе дополнительных веществ, причем потребности в таких веществах не всегда хорошо известны.
Чтобы выделить желаемый микроорганизм из природных образцов, важно иметь подходящий материал из соответствующего места обитания. Например, термофильные бактерии с большой вероятностью можно выделить из воды горячих источников, анаэробные - из иловых отложений. По аналогии с этим метод накопительных культур основан на подборе селективной (элективной) среды, благоприятной для искомого организма и неблагоприятной для других, а также селективных физико-химических условий культивирования. К сожалению, при использовании такого метода в накопительной культуре, как правило, доминируют быстрорастущие виды, которые подавляют все остальные формы. Медленнорастущие виды удается выделить только в том случае, если своевременно пересевать пробы из накопительной культуры на плотную среду на чашки Петри. Можно также высевать непосредственно природные пробы на плотную элективную среду, где медленно растущие виды при длительной инкубации образуют видимые колонии. Селективные условия создают путем комбинирования различных источников энергии, углерода и других элементов (N, Р, S и т. д.).
Для ингибирования сопутствующей микрофлоры с учетом особенностей предполагаемого микроорганизма исследуемый материал может быть подвергнут физической, химической или биологической обработке. Например, при выделении спорообразующих бактерий материал прогревают при 80 °С в течение 10 минут, убивая таким образом вегетативные формы.
В лабораторной практике часто используют питательные среды, предназначенные для избирательного культивирования определенных видов микроорганизмов. В соответствии с этим различают элективные (селективные), дифференциально-диагностические (индикаторные) накопительные и консервирующие (транспортные) среды.
Элективные (селективные) среды применяют главным образом для выделения из мест их естественного обитания или получения накопительных культур. Понятия «элективность» и «селективность» указывают на избирательное действие среды по отношению к микроорганизмам. Эти среды обеспечивают преимущественное развитие одного вида или группы микроорганизмов. Избирательность питательной среды для определенных видов микроорганизмов достигается путем создания оптимальных для них условий (pH, концентрация солей, состав питательных веществ), т. е. положительной селекцией (элективные), или путем добавления в среду веществ, угнетающих другие микроорганизмы (желчь, азид натрия, теллурит калия, антибиотики и др.) - отрицательной селекцией (селективные). Сопутствующие микроорганизмы или совсем не растут на таких средах, или развитие их в значительной степени задерживается. Например, элективной средой для стафилококков является желточно-солевой агар (ЖСА), для холерного вибриона - щелочной агар.
С целью придания элективности в качестве ингибиторов роста посторонней микрофлоры в составе питательных сред используют различные химические соединения, в том числе антибиотики, красители, соли и другие. Среди них ампициллин, полимиксин, эритромицин, нистатин, пенициллин, новобиоцин, метициллин, генциан фиолетовый, этилвиолет, азид натрия и цинка, циклогексемид, теллурит калия, борная кислота и ее производные, соли желчных кислот и другие. При получении чистой культуры из изолированных колоний предпочтительно производить высев исследуемого материала на неселективные среды, поскольку в случае использования селективных сред в колонии или рядом с ней могут присутствовать жизнеспособные, но не растущие на этих средах сопутствующие микроорганизмы, которые будут пересеяны вместе с выделяемым микроорганизмом. На неселективных же средах сопутствующие микроорганизмы образуют видимые колонии.
Техника посева при получении чистой культуры зависит от характера исследуемого материала, консистенции питательной среды и цели исследования. Жидкий материал для посева берут петлей или пипеткой. При взятии петлей жидкость должна образовывать в кольце петли тонкую прозрачную пленку. Пипетками пользуются, когда материал засевают в большом или точно измеряемом объеме. Способ взятия плотного материала определяется его консистенцией, при посевах чаще всего пользуются бактериологической петлей.
Для выделения чистых культур микроорганизмов используют различные методы. Обрабатывая исследуемый материал кислотой, можно выделить устойчивые к кислоте микобактерии, а прогревание материала перед посевом убивает все вегетативные формы бактерий и позволяет выделить чистую культуру спорообразующих микроорганизмов. Наиболее распространенными методами получения чистой культуры микроорганизмов являются следующие.
- Метод Пастера - последовательное разведение исследуемого материала в жидкой питательной среде до концентрации одной клетки в объеме.
- Метод Коха («пластинчатые разводки») - последовательное разведение исследуемого материала в расплавленном агаре с последующим разливом в чашки Петри. При получении чистой культуры методом рассева три пробирки, содержащие по 15 мл мясопептонного агара, ставят в водяную баню для расплавления агара. Расплавленную среду остужают до 48-50 °С. В пробирку вносят одну бактериологическую петлю исследуемого материала. Для лучшего перемешивания материала со средой засеянную пробирку вращают несколько раз, зажав между ладонями. После этого одну петлю (прокаленную и остуженную) содержимого первой пробирки переносят во вторую и таким же образом из второй в третью. Приготовленные разведения микробов выливают из пробирок в стерильные чашки Петри, обозначенные номерами, соответствующими номерам пробирок. После застывания среды с исследуемым материалом чашки помещают в термостат. Количество колоний в чашках с питательной средой уменьшается по мере разведения материала. Это метод, предложенный Р. Кохом, используется в настоящее время для определения общего количества бактерий, находящихся в воде и пищевых продуктах.
- Метод Шукевича применяется для выделения чистой культуры микроорганизмов, обладающих «ползучим» ростом (например, протея). Для этого материал засевают в конденсационную воду у основания, скошенного агара. Протей способен подниматься по скошенному агару вверх, а неподвижные формы остаются расти внизу, на месте посева.
- Метод Дригальского заключается в разведении исследуемого материала, находящегося в пробирке, стерильным физиологическим раствором или бульонном и последующим внесением в чашки Петри. Для выделения чистой культуры расплавленную питательную среду разливают в три чашки Петри. Застывшую среду обязательно подсушивают, так как влажная поверхность способствует сливному росту. В первую чашку вносят одну каплю исследуемого материала и стерильным шпателем втирают его в поверхность питательной среды. Далее, не набирая нового материала и не прожигая шпателя, последний переносят во вторую, а затем в третью чашки, втирая в поверхность питательных сред оставшийся на нем материал. При посеве материала, обильно обсемененного микрофлорой, на второй и на третьей чашках вырастают изолированные колонии. Полученные отдельные колонии служат для пересева в пробирки с жидкой или плотной средой и получения чистой культуры микроорганизма.
Вместо шпателя посев исследуемого материала можно производить бактериологической петлей. Материал распределяют на питательной среде по четырем квадратам, проводя параллельные штрихи, не обжигая петлю после засева каждого квадрата (рис. 12).
Рис. 12. Метод рассева по Дригальскому
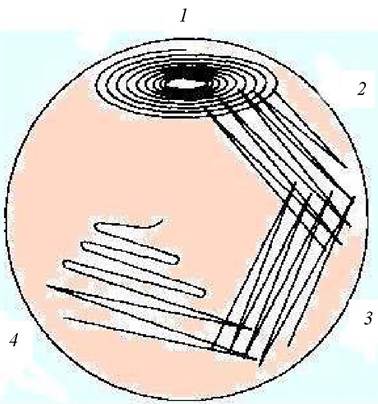
Чашки инкубируют в течение 18-24 часов, после чего в различных секторах определяют количество колоний микроорганизмов. При таком способе посева материал, находящийся в петле, расходуется постепенно, и по линиям штрихов, нанесенных в конце посева, вырастают изолированные колонии микробов. В случае подозрения медленнорастущих микроорганизмов чашки оставляют на более продолжительный срок (до 5-7 и более суток).
- Метод Вейнберга. Сущность метода заключается в том, что разведения исследуемого материала проводят в расплавленной и охлажденной до 45-50 °С агаризованной питательной среде. Делают 6-10 последовательных разведений, затем среду в пробирках быстро охлаждают и заливают поверхность слоем смеси парафина и вазелинового масла, чтобы помешать проникновению воздуха в толщу питательной среды. Для извлечения изолированных сформировавшихся внутри среды колоний анаэробов пробирку слегка нагревают, вращая ее над пламенем, при этом агар, прилегающий к стенкам, плавится и содержимое пробирки в виде агарового столбика выскальзывает в стерильную чашку Петри. Столбик агара разрезают стерильным пинцетом и извлекают петлей колонии, которые помещают в благоприятную для этих микроорганизмов жидкую среду (например, среду Кит-Тароцци). Метод используется для выделения анаэробных микроорганизмов.
- Метод Хангейта используют, когда хотят получить изолированные колонии строгих анаэробов, высокочувствительных к кислороду. Для этого расплавленную агаризованную среду засевают бактериями при постоянном токе через пробирку инертного газа. Применение тонкого слоя в пробирке, заполненной инертным газом, позволяет получать изолированные колонии микроорганизмов.
- Выделение отдельных клеток с помощью микроманипулятора - прибора, позволяющего с помощью микропипетки или микропетли извлекать из суспензии отдельные клетки. Манипуляцию проводят под микроскопом, при этом на предметном столике микроскопа устанавливают влажную камеру, в которую помещают препарат «висячая капля». Микропипетки (микропетли) закрепляют в держателях штативов, и с помощью системы винтов и рычагов исследователь, глядя в микроскоп, с микронной точностью извлекает отдельные клетки микропипетками и переносит их в пробирки со стерильной жидкой средой для получения клона клеток.
Таким образом, для выделения чистых культур материал рассевают, чтобы получить изолированные колонии. Выделение чистых культур достигается с помощью механического разобщения на поверхности плотной питательной среды (методы штриха, разведений в агаре, распределения по поверхности плотной питательной среды шпателем (метод Дригальского), использования элективных питательных сред и создания условий, благоприятных для развития одного вида (рода) бактерий (среды обогащения). Культуральные признаки микробов определяются характером их роста на питательных средах. Будучи постоянными для каждого вида, они являются важными диагностическими признаками.
Для характеристики роста на плотной питательной среде чашки Петри просматривают сначала невооруженным глазом или через лупу, затем помещают на столик микроскопа вверх дном и просматривают колонии в проходящем свете при малом увеличении микроскопа. Просмотр чашек может дать предварительную информацию относительно результатов посева. Определяют размер, форму, контуры края, рельеф (приподнятость ее над поверхностью, каплеобразные, куполообразные, плоско-выпуклые), поверхность (матовая, блестящая, сухая, влажная), цвет структуру (мелко- или грубозернистая, нитевидная, волокнистая), консистенцию колонии.
Характер роста микроорганизмов в жидких питательных средах менее разнообразен, чем на плотных. В жидких питательных средах может наблюдаться рост бактерий с равномерным помутнением среды, придонный, пристеночный или поверхностный рост с образованием пленки.
Для выявления особенностей микробного роста в полужидкой питательной среде, в первую очередь активной подвижности бактерий, исследуемую культуру засевают, делая укол в среду в непосредственной близости от стенки пробирки. Подвижные микробы в столбике полужидкого агара вызывают выраженное равномерное помутнение по всей толщине среды.
11.3. Биохимические тесты идентификации
Изучение начинают с фенотипической идентификации свежевыделенных чистых культур. Определяют окислительно-восстановительные ферменты бактерий, гидролитические свойства, способность декарбокисилировать отдельные аминокислоты, ассимилировать сахара и другие органические соединения. Наиболее распространенными тестами являются следующие:
- оксидазные тесты, основанные на том, что у некоторых бактерий биологическое окисление осуществляется при помощи ферментов цитохромоксидазы либо индолоксидазы. Визуальное выражение процесса связано с введением в питательную среду искусственных бесцветных реагентов в восстановленном состоянии, которые в присутствии микробной оксидазы окисляются и приобретают соответствующую им окраску;
- тест с лакмусовым молоком основан на комплексе ферментативных реакций, проявлению которых соответствуют характерные изменения первоначальных свойств питательной среды (ферментация лактозы, синтез протеолитических ферментов, образование растущими бактериями декарбоксилаз и др.);
- тест на редукцию метиленового синего основан на способности молока с добавленным в него метиленовым синим обесцвечиваться, если микроорганизмы обладают редуцирующими свойствами;
- тест на редукцию ТТХ (хлорида трифенилтетразолия - С19Н15СlN4) основан на восстановлении ТТХ - бесцветного соединения до трифенилформазана, который в органических растворителях и под действием продуктов жизнедеятельности некоторых видов микроорганизмов, в частности энтерококков, восстанавливается и приобретает вишневую окраску;
- тест на каталазу - фермента, способствующего расщеплению перекиси водорода на воду и молекулярный кислород. Тест основан на том, что с первых же секунд контакта перекиси водорода с каталазой начинается ее расщепление, сопровождающееся выделением пузырьков кислорода;
- тест на сахаролитическую активность основан на способности исследуемого микроорганизма утилизировать углевод, введенный в питательную среду, с образованием кислоты или кислоты и газа, определяемых по изменению цвета индикатора среды и образованию пузырьков;
- тест на гидролиз крахмала применяется для выявления способности микроорганизма синтезировать фермент амилазу, расщепляющий крахмал до глюкозы;
- тест окисления-ферментации (тест ОF) основан на том, что при окислительном процессе молекулы кислорода являются конечным акцептором Н (протонов) и электронов. Ферментация (брожение) углеводов происходит как в анаэробных, так и в аэробных условиях с участием сахаролитических ферментов;
- тест ОNРG (тест на β-галактозидазу с нитрофенил-β-D- галактопиранозидом,) основан на гидролизе лактозы бактериями и определяется тем, что фермент β-галактозидаза (лактаза) катализирует расщепление дисахарида лактозы на два моносахарида - глюкозу и галактозу. При гидролизе ONPG высвобождается 0-
нитрофенил, окрашивающий раствор в желтый цвет, что является индикатором присутствия в культуре фермента β-галактозидазы;
- тест на образование ацетилметилкарбинола (реакция Фогес- Проскауэра) основан на сбраживании глюкозы (в среде Кларка) до пировиноградной кислоты, превращения ее в ацетоин или ацетил- метилкарбинол с образованием азотсодержащих комплексов вишнево-красного цвета;
- тест на гидролиз эскулина (химического соединения, относящегося к гликозидам) основан на расщеплении эскулина на глюкозу и эскулатин, который, реагируя с цитратом железа, выпадает в осадок, образуя вокруг колоний зоны коричнево-черного цвета;
- тест на утилизацию цитрата (на среде Симмонса или Кристенсена) применяется для дифференциальной диагностики шигелл и эшерихий;
- тест на декарбоксилирование аминокислот (отщепление СО2 от СООН). Процесс происходит с участием ферментов в кислой среде, при этом образующиеся амины(производные аммиака) при расщеплении дают щелочную реакцию;
- тест на образование индола (тест на триптофаназу) основан на том, что в процессе размножения микроорганизмов содержащийся в питательной среде триптофан расщепляется с образованием индола, наличие которого определяется по окрашиванию соединений в розовый или красный цвет;
- тест на уреазу (тест на ферментативное расщепление мочевины) основан на гидролизе бактериями мочевины с образованием аммиака, смешением pH в щелочную сторону и изменении цвета индикатора в среде;
- тест на восстановление нитратов до нитритов (тест нитрат- редуктазный). Тест основан на способности некоторых микроорганизмов восстанавливать нитраты в нитриты и выявлении нитритов при помощи реактива Грисса, добавление которого к среде с нитритами вызывает окрашивание содержимого пробирки в красный цвет;
- тест на протеолитическое разжижение желатина (смеси белковых субстратов) основан на необратимом полном или частичном разжижении желатина под воздействием микробных протеаз;
- тест на ферментативный гидролиз казеина основан на продуцировании некоторыми микроорганизмами протеолитического фермента, который гидролизует содержащийся в молоке белок казеин до полипептидов, с образованием вокруг колоний зон просветления;
- тест на гемолизин основан на способности некоторых бактерий продуцировать вещества белковой природы, способные к ферментативному разрушению эритроцитов с высвобождением гемоглобина. Гемолитическая активность бактерий наблюдается на кровяном агаре;
- тест на образование сероводорода (Н2S) основан на культивировании на питательных средах с источниками Н2S (серосодержащие аминокислоты или неорганические соединения серы - сульфаты и тиосульфаты) бактерий, способных к ферментативному высвобождению сернистых соединений. При этом Н2S в кислой среде вступает в соединение с индикатором, образуя коричневочерный преципитат - сульфат железа или сульфат свинца;
- тест на плазмокоагуляцию основан на свертывании плазмы в результате продукции плазмокоагулирующим микробом тромбиноподобного вещества;
- тест на спорообразование основан на искусственном создании неблагоприятных для испытуемого микроорганизма условий, ведущих к образованию спор.
11.4. Методы иммунологической (серологической) диагностики
Иммунологические методы, используемые для обнаружения и идентификации микроорганизмов, основаны на реакции взаимодействия антигена с антителом. Антигенами (anti -против, genos - род, происхождение) называют макромолекулярные чужеродные для конкретного организма вещества, способные вызывать иммунный ответ. Чаще всего к ним относятся разнообразные микробные клетки, их структурные элементы и продукты метаболизма. Основными свойствами антигена являются иммуногенность и специфичность. Иммуногенность - это способность индуцировать иммунный ответ. Специфичность - способность антигена взаимодействовать со специфичными к нему антителами. В зависимости от химической природы и молекулярной массы антигены могут быть полными (иммуногенными) и неполными (гаптенами). Существующие антигены классифицируют на основании происхождения (естественные, искусственные, синтетические), химической природы (белки, углеводы, нуклеиновые кислоты, липиды) и некоторым другим признакам.
В зависимости от локализации различают капсульные, жгутиковые, соматические, цитоплазматические и внеклеточные антигены. Комплекс антигенов целых микробных клеток и экзотоксины бактерий являются полными антигенами и стимулируют реакции иммунного ответа. По степени специфичности антигены микроорганизмов делят на перекрестно-реагирующие, группоспецифические, видоспецифические и типоспецифические. Наиболее характерные антигены являются основой при конструировании иммунобиологических препаратов для обнаружения микроорганизмов и специфических иммуноглобулинов.
Антитела, или иммуноглобулины - это группа структурно родственных белков сыворотки крови с характерными физикохимическими и биологическими свойствами. Важным свойством иммуноглобулинов является способность вступать в контакт и связывать цельные, нативные молекулы антигена в неизмененном виде. Соединения антигена и антитела называют иммунными комплексами.
Методы серологической диагностики условно можно разделить на две группы:
- прямые методы взаимодействия и визуального определения результатов реакции антиген-антитело. Это реакции агглютинации, преципитации, лизиса и связывания комплемента;
- методы с использованием «свидетелей», к которым относятся носители антигена или антитела (эритроциты, липосомы) или различные метки одного из участков взаимодействия антиген-анти- тело (ферментные, флюоресцирующие, радиоизотопные и др.). В зависимости от используемой метки эти методы называются иммуноферментный анализ (ИФА), реакция иммунофлюоресценции (РИФ), радиоиммунологический анализ (РИА) и др.
Реакция агглютинации обусловлена склеиванием целых микробных клеток (агглютиногенов) гомологичными антителами (агглютининами) в присутствии электролитов, что проявляется образованием хорошо видимых хлопьев агглютината, выпадающего в растворе в осадок. Существуют различные модификации постановки этой реакции.
Реакции преципитации характеризуются осаждением антигена- преципитиногена из раствора в виде мелких хлопьев в результате взаимодействия с иммунной сывороткой, содержащей антитела- преципитины. Антигеном может быть полисахарид (гаптен) или бактериальный белок (полный антиген), содержащийся, например, в экстрактах микробных клеток. Реакции преципитации являются качественными методами исследования и характеризуются высокой специфичностью. Их применяют главным образом для определения антигена и его природы.
Реакция связывания комплемента (РСК) основана на том, что при взаимодействии антигена с антителом образуется комплекс, который адсорбирует (связывает) комплемент (сложный комплекс протеолитических ферментов, регуляторных белков и белков, способных лизировать клетки). Однако этот феномен протекает в пробирке без видимых проявлений. Для выявления результатов реакции в качестве индикаторной системы используют реакцию гемолиза.
Реакция пассивной (непрямой) гемагглютинации (РПГА или РИГА) основана на способности эритроцитов различных видов животных, птиц и человека (1(0) группы крови) адсорбировать на своей поверхности антигены бактерий или антитела. РПГА применяют либо для выявления неизвестного антигена на основе его взаимодействия с известным антительным диагностикумом, либо для обнаружения антител в сыворотке крови путем использования известного эритроцитарного антигенного диагностикума. В положительных случаях РПГА в лунках полистироловой пластины образуется осадок в виде перевернутого «зонтика». При отрицательной реакции эритроциты скатываются на дно лунки, и образуется осадок в виде «пуговки».
Реакция латекс-аглютинации (РЛА) является одним из видов реакции агглютинации, в которой в качестве носителя антигена или антитела используются синтетические полимерные (латексные) частицы.
Реакция коагглютинации (КОА) проявляется склеиванием сенсибилизированных антителами клеток золотистого стафилококка (штамм Cowan I) в результате взаимодействия с гомологичными антигенами.
Реакция иммунофлюоресценции (РИФ) используется как метод экспресс-диагностики для выявления антигена в исследуемом материале. Метод заключается в обработке фиксированного на стекле материала, содержащего антиген, гомологичной иммунной сывороткой, конъюгированной с флюорохромом, например, флюоресцеинизотиоционатом - ФИТЦ. Препарат микроскопируют с использованием люминесцетного микроскопа. В положительных случаях по периферии объекта появляется светящаяся кайма зеленого цвета.
Иммуноферментный анализ (ИФА) - это иммунологическая реакция специфического взаимодействия антигена и антитела, в которой в качестве индикатора используются молекулы фермента (пероксидазы хрена, щелочной фосфатазы и др.). Способность маркерного фермента расщеплять субстрат приводит к изменению цвета реактивной среды, что и лежит в основе этого теста.
Радиоиммунный анализ (РИА) основан на выявлении иммунных комплексов при помощи радиоактивной метки, введенной в состав одного из компонентов реакции - антигена или антитела. Количественное определение проводится при помощи счетчиков радиоактивности. РИА считается одним из наиболее чувствительных иммунохимических методов и позволяет обнаруживать 0,1-10 нг белка в пробе.
Серологические методы позволяют точно и быстро определить видовую принадлежность исследуемого объекта и обнаруживать микроорганизмы как в чистой культуре, так и в загрязненном материале, причем в относительно небольших количествах.
11.5. Методы молекулярно-генетического анализа. Полимеразная цепная реакция
Внедрение полимеразной цепной реакции (ПЦР) в лабораторную практику стало одним из наиболее важных событий в микробиологии, молекулярной биологии и медицине в последние десятилетия. ПЦР позволяет определять чрезвычайно малые количества нуклеиновых кислот. Метод поднял лабораторную диагностику на новый уровень, когда появилась возможность прямого обнаружения вирусов и бактерий, а также возможность определять любое изменение в генетическом материале, даже отдельные мутации.
ПЦР была открыта в 1984 г. американским биохимиком Кэри Мюллисом, который впервые показал возможность амплификации (многократного увеличения числа копий) участков ДНК в процессе реакции. Синтез копий молекул ДНК (полимеразная реакция) происходит во всех организмах (in vivo) во время клеточного деления с помощью ферментов ДНК-полимераз. ПЦР - это получение множества копий специфического фрагмента ДНК в пробирке (in vitro). Таким образом, принцип ПЦР заключается в амплификации участка генома, ограниченного парой специфических праймеров (специфических одноцепочечных участков ДНК), с помощью фермента ДНК-полимеразы и последующим обнаружением результатов реакции методом электрофореза или другими методами.
В настоящее время ПЦР используется в различных областях, в частности в палеонтологии для ДНК-диагностики, для получения рекомбинантных вакцин, для контроля генотерапии, при исследовании трансгенных животных, для диагностики инфекционных заболеваний бактериальной и вирусной природы, для оценки эффективности лечения различных заболеваний. ПЦР нашла применение в пищевой промышленности, в том числе для контроля качества продуктов животного и растительного происхождения.