БИОТЕХНОЛОГИЯ РАСТЕНИЙ И БИОБЕЗОПАСНОСТЬ - А. П. Ермишин - 2015
ГЛАВА 6. КЛЕТОЧНАЯ СЕЛЕКЦИЯ
Одним из основных методов селекции микроорганизмов является отбор, проводимый на питательной среде, содержащей какой- либо селективный агент, или в условиях действия селективных факторов внешней среды, например, пониженных или повышенных температур. Таким образом достаточно просто отобрать, например, мутанты, устойчивые к отдельным антибиотикам, токсинам, осмотическим стрессам. Культура клеток растений во многом напоминает культуру микроорганизмов. В связи с этим было естественным применение к растениям методов, хорошо зарекомендовавших себя в селекции микроорганизмов. Отбирая в культуре in vitro мутантные клеточные линии, устойчивые к определенным селективным агентам или факторам среды, можно, в принципе, получить растения- регенеранты, обладающие соответствующими признаками, имеющими хозяйственное значение.
Отбор мутантов на клеточном уровне, безусловно, имеет преимущество по сравнению с аналогичным отбором, проводимым на уровне организменном. В культуральном сосуде содержится огромное количество клеток, среди которых несложно отобрать обладающие нужными свойствами мутантные клетки, получить из них клеточную линию, из которой регенерировать растение.
Как видно из содержания предыдущих глав, культивируемые клетки не всегда воспроизводят свойства растений, из которых была получена культура. Соответственно у растений-регенерантов могут не проявляться признаки, характерные для исходных клеточных культур. Тем не менее, как показала практика, имеется ряд направлений клеточной селекции, позволяющих получать растения-регенеранты с хозяйственно важными признаками: устойчивостью к гербицидам; к стрессовым факторам; некоторым заболеваниям; обладающих сверхпродукцией незаменимых аминокислот.
Клеточная селекция представляет интерес не только в связи с получением мутантных растений. Как отмечалось в гл. 4, важное направление биотехнологии растений - производство вторичных метаболитов в культуре клеток - основано в том числе на отборе клеточных линий, обладающих повышенной продукцией хозяйственно ценных веществ. Знание закономерностей и методических подходов клеточной селекции необходимо для повышения эффективности отбора линий-суперпродуцентов ВМ.
6.1. Гетерогенность и генетическая изменчивость клеток в культуре in vitro как основа клеточной селекции. Сомаклональная изменчивость
Любая селекция может быть эффективной только в случае, если имеет место генетическая изменчивость селекционного материала (гибридов, линий, клеток). Долгое время считалось, что культивируемые клетки растений имеют генотип исходного растения, который они могут сохранять длительное время. Случаи появления измененных форм среди растений-регенерантов игнорировались или объяснялись физиологическими отклонениями, которые носят ненаследуемый характер.
В работах Р. Готрэ (1955) и П. Нобекура (1955) была отмечена цитологическая нестабильность клеток при их длительном культивировании in vitro. Позднее появились публикации, в которых были описаны растения-регенеранты с различными нарушениями хромосомного состава (T. Murashige, R. Nakano, 1966; Р. Бутенко и др., 1967), а также обладающие новыми хозяйственно ценными признаками, способными сохраняться в течение длительного времени (D. Heinz, G. Mee, 1971). Это привело к мысли, что прохождение клетками стадии неорганизованного роста в условиях in vitro может сопровождаться существенными изменениями их генотипа, которые могут проявляться на уровне растений, регенерированных из таких измененных клеток (рис. 6.1). Явление изменчивости клеточных линий и растений-регенерантов получило название сомаклональная вариабельность (изменчивость) (P. Larkin, W. Scowcroft, 1981).
Рис. 6.1. Генетически обусловленная фенотипическая изменчивость сомаклональных вариантов садовой земляники (Fragaria х ananassa Duch.): 1-3 - сомаклональные варианты, к - исходная линия (контроль). Сомаклоны земляники отличаются от исходной линии по форме и габитусу куста (а), форме и размеру листьев (б), форме и размеру цветоносов (в), форме, размеру и окраске ягод (г). На рисунках д и е показано отличие электрофоретических профилей амплифицированной ДНК сомаклональных вариантов (1-3) от исходной линии (4) при использовании двух произвольных праймеров (по M. K. Biswas и др., 2009)
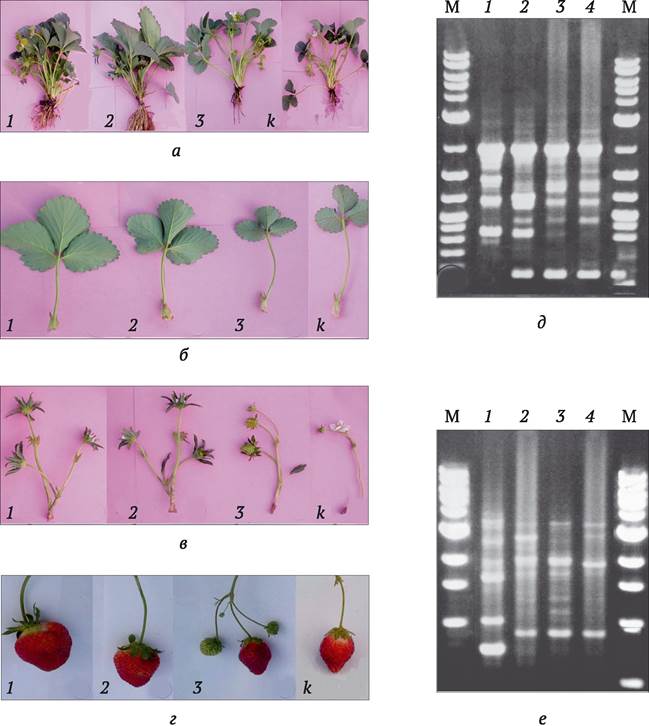
Различают два основных источника возникновения сомаклональных вариантов: генетическая гетерогенность клеток эксплантата и генетическая изменчивость, возникшая в процессе культивирования клеток in vitro.
Относительно высокая генетическая стабильность характерна лишь для меристемных клеток взрослого растения (см. гл. 5). Цитогенетическая стабильность клеток специализированных тканей не такая высокая. В частности, у многих видов растений клетки коры и сердцевины стебля - полиплоидные (явление полиплоидизации соматических клеток называется полисоматия). Другой тип хромосомной вариабельности, характерной для соматических клеток растений, например, межвидовых гибридов, искусственно полученных автополиплоидов, - анеусоматия, т. е. присутствие анеуплоидных клеток.
Длительно размножаемые вегетативным способом растения могут накапливать точковые мутации соматических клеток, в результате чего они становятся химерными. Известны сорта и породы вегетативно размножаемых растений (картофеля, декоративных луковичных, древесных культур), а также мутанты, полученные на их основе, которые успешно выращивают в течение многих десятков лет. Например, широко выращиваемый в Америке сорт картофеля Russet Burbank, зарегистрированный в США в 1914 г., является спортом (клоном от почковой мутации) сорта Burbank, появившегося на рынке в 1876 г. Естественно предположить, что чем более длительное время возделывают какой-либо сорт, породу, тем больше измененных клеток он содержит.
Некоторые из соматических мутаций легко обнаружить, например, у пестролистных декоративных растений. В большинстве же случаев полисоматия, анеусоматия и химеризм никак не проявляются. Однако при получении культуры клеток из эксплантатов, содержащих измененные клетки, возможна их дедифференциация, приобретение ими способности к делению, вторичная дифференциация, приводящая к регенерации измененных растений.
Изменчивость клеток может возникать и в процессе их культивирования in vitro. Условия существования клеток в составе интактного растения и при культивировании на агаризованной питательной среде или в виде клеточной суспензии значительно различаются. На уровне растения действует выработанная в процессе эволюции и приспособленная к определенным условиям окружающей среды система гомеостаза, в которой каждая группа клеток организма выполняет в процессе онтогенеза определенные функции. При этом все клетки связаны между собой коррелятивными отношениями, их изменчивость возможна в пределах нормы реакции, характерной для данного организма. Наиболее стабильны в генетическом отношении клетки генеративных органов и меристем, что обеспечивает возможность воспроизведения генотипа растения при размножении (половом и вегетативном).
Питание клеток и их гормональный статус в культуре in vitro существенно отличаются от такового у клеток интактного растения. В питательной среде нередко содержатся синтетические регуляторы роста растений, которые имеют выраженный мутагенный эффект. В частности, имеется много публикаций, в которых отмечено существенное влияние 2,4-Д на изменчивость культивируемых клеток растений. Некоторые из авторов рассматривают этот ауксин в качестве непосредственного индуктора полиплоидизации клеток или фактора, селективно стимулирующего деления полиплоидных клеток. Помимо регуляторов роста, на цитогенетическое разнообразие клеток в культуре in vitro могут оказывать влияние и другие компоненты питательной среды, например, различные источники азотного питания (органический, неорганический). Длительное пассирование культур способствует повышению генетического разнообразия клеток и растений-регенерантов.
В качестве возможных генетических механизмов возникновения сомаклональных вариантов рассматривают следующие (A. Karp, S. Bright, 1985):
✵ грубые кариологические изменения (полиплоидию и анеуплоидию, крупные перестройки хромосом);
✵ криптические, незаметные при цитологическом анализе, хромосомные перестройки (мелкие делеции, дупликации, транслокации, инверсии);
✵ точковые мутации;
✵ перемещения мобильных генетических элементов;
✵ амплификацию и редукцию генов;
✵ митотический кроссинговер.
Кроме сомаклональной вариабельности, связанной с наследуемыми перестройками генома, могут иметь место и эпигенетические изменения, которые стабильно передаются дочерним клеткам, но не проявляются у растений-регенерантов или у их полового потомства. Классический генетический анализ наследования каких-либо новых признаков, обнаруженных у растений-регенерантов и отсутствующих у исходных растений, позволяет сделать окончательное заключение, являются ли эти признаки результатом какой-либо мутации или ненаследуемым отклонением в физиологии растения.
Результаты генетических исследований на растениях разных видов убедительно доказывают, что большая часть сомаклональных вариаций обусловлена стабильными генетическими изменениями, т. е. мутациями. Частота спонтанных мутаций при культивировании клеток растений варьирует в зависимости от объекта в пределах 10-5-10-8 (В. Сидоров, 1990). В качестве примера сомаклональной вариации можно привести результаты, полученные при изучении растений-регенерантов томатов (В. Сидоров, 1990):
✵ у сомаклонов различных сортов обнаружено несколько одиночных генных мутаций, наследуемых в соответствии с законами Менделя;
✵ идентифицированы доминантные, семидоминантные и рецессивные ядерные мутации;
✵ показано, что растения-регенеранты с одиночными генными мутациями могут возникать с высокой частотой: один мутант на 20-25 растений- регенерантов;
✵ среди сомаклонов выявлены новые мутации, которые не встречались среди спонтанных мутантов или полученных с помощью традиционных мутагенов;
✵ получены экспериментальные данные, доказывающие, что одной из причин сомаклональной изменчивости может быть митотический кроссинговер;
✵ у сомаклонов обнаружены мутации хлоропластной ДНК.
Следует отметить, что в литературе накоплен большой объем фактов по сомаклональной вариации, связанной не только с изменчивостью генома, но и плазмона. Довольно частое явление - регенерация альбиносных растений с нарушенной структурой хлоропластного генома. Особенно много таких растений получают в культуре пыльников злаковых (подробнее этот вопрос будет рассмотрен в гл. 7). Получены экспериментальные данные, показывающие изменчивость и митохондриального генома у растений-регенерантов. Так, В. G. Gengenbach и другие (1977) отобрали мужски фертильные сомаклоны среди растений-регенерантов, полученных из каллюсной культуры мужски стерильных линий кукурузы (с Т-цитоплазмой). При этом в отличие от исходных линий они обладали также устойчивостью к южному гельминтоспориозу кукурузы (возбудитель - Неlmintospotium mayidis). Молекулярно-генетический анализ показал, что мужская фертильность и устойчивость к заболеванию не связаны у них с реверсией цитоплазмы от Т-типа к нормальному, а обусловлены определенными изменениями митохондриального генома Т-цитоплазмы, которые привели к появлению фертильных и устойчивых сомаклонов.
Уже в ранних исследованиях по сомаклональной изменчивости была показана возможность отбора среди растений-регенерантов мутантов с новыми признаками, имеющими важное хозяйственное значение. Б. J. Неinz, G. W. Р. Мее (1971) на Гавайях и их коллеги на Фиджи (М. Krishnamurthi, J. Тlasкаl, 1974) выделили среди растений-регенерантов сахарного тростника сомаклоны с повышенной продуктивностью, устойчивые к вирусам, гельминтоспориозу, ложной мучнистой росе. Появление работ этих авторов фактически положило начало широкому развитию нового направления в селекции растений, основанного на отборе сомаклонов с улучшенными хозяйственно-ценными признаками. Интересные результаты были получены для ряда продовольственных, кормовых, технических, декоративных и лекарственных культур (см. рис. 6.1).
J. F. Shepard с сотрудниками (1980), G. Secor, J. Shepard (1981) выделили ряд ценных сомаклональных вариантов среди растений-регенерантов, полученных в культуре протопластов картофеля сорта Russet Burbank: с повышенной продуктивностью, устойчивых к альтернариозу, фитофторозу. Эти признаки сохраняли стабильность в течение четырех лет вегетативного размножения. В. A. Сидоров с сотрудниками (1984, 1985) отобрали среди протоклонов сорта «Зарево» мутанты, отличающиеся высокой урожайностью, повышенной устойчивостью к заболеваниям, более высоким содержанием в клубнях протеина и крахмала. Имеется ряд сообщений по выделению сомаклонов картофеля с измененной формой клубней и их окраской, с устойчивостью к парше, к вирусам PVY и PLRV, тлям-переносчикам вирусов.
D. A. Evans с сотрудниками (1983; 1984; 1986) выделили сомаклональные варианты, отличающиеся от исходных сортов томатов по таким признакам, как цвет плодов, архитектура растений, пригодность к механической уборке, устойчивость к болезням (рис. 6.2). Эти сомаклоны были подвергнуты детальному генетическому анализу, который показал, что измененные признаки связаны с единичными генными мутациями. Например, было установлено, что признак цвета плодов имел рецессивный характер наследования, а устойчивость к фузариозу - доминантный. Один из сомаклонов томатов с более высоким, чем у исходного сорта, содержанием сухого вещества (20 %), улучшенным вкусом и консистенцией плодов, отличающийся по цвету плодов, был зарегистрирован DNA Plant Technology Corporation (США) в качестве нового сорта.
Рис. 6.2. Селекция томата с использованием сомаклональной вариабельности: а - схема клеточной селекции томата: исходное растение (1); вычленение эксплантатов из вегетативных тканей, например листьев, или генеративных тканей (пыльников, пыльцы) (2); эксплантаты на питательной среде (3); формирование каллюса (4), регенерация побегов (5); укоренившиеся in vitro растения-регенеранты (6), рассада растений-регенерантов (7), взрослые растения-регенеранты (поколение R1), получение семян от самоопыления (поколение R2) (9); отбор селекционно-ценных линий среди R1 и R2 при выращивании их в условиях открытого грунта или в теплице (10); б - пестролистное растение, отобранное в поколении R2 (от самоопыления пестролистной линии R1) (наличие пестролистности у генеративного потомства подтверждает наследуемый характер сомаклональной изменчивости); в - нормальные и хлорофилл-дефектные сомаклоны R2; г - плоды нормальной линии томата UC82B (слева) и сомаклона с повышенным содержанием пигмента (справа); д - плоды контрольного растения томата (красные) и сомаклональных вариантов с измененной окраской (оранжевые и желтые) (по D. Evans и др., 1984)
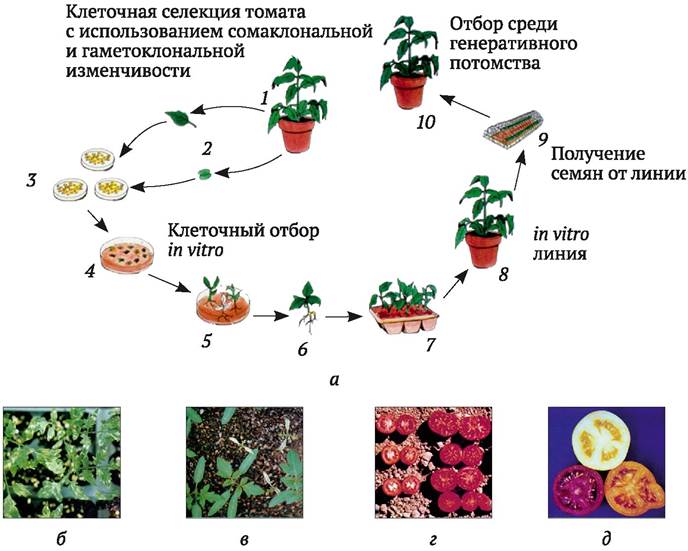
A. Cassells и другие (1983) показали возможность выделения перспективных сомаклонов не только среди растений-регенерантов, полученных из каллюсных, суспензионных культур или из протопластов, но и среди растений, регенерированных непосредственно из стеблевых эксплантатов.
6.2. Использование мутагенов для клеточной селекции
Использование мутагенов позволяет существенно расширить спектр сомаклональной изменчивости и благодаря этому повысить эффективность клеточной селекции. В качестве исходного материала для экспериментального мутагенеза используют каллюсные и суспензионные культуры, культуры протопластов. Также нашли применение обработки мутагенами семян с последующим получением из зародышей или проростков культуры клеток in vitro, в которой, собственно, проводят клеточную селекцию. В этих же целях проводят обработку мутагенами пробирочных растений или эксплантатов, которые дают морфогенный каллюс, или культуры, способные к эмбриогенезу.
Каллюсные культуры - наиболее доступный материал для мутагенеза. Применяют, как правило, каллюс, который еще не пассировали, или культуру после нескольких пассажей, не утратившую способность к регенерации растений. Для каллюсной культуры как объекта мутагенеза характерен ряд недостатков: относительно медленный рост, неравноценный для разных слоев клеток эффект мутагенов или селективных агентов. Наряду с устойчивыми к селективному агенту клетками возможно выживание чувствительных клеток, находящихся в непосредственном контакте с мутантными, в связи с чем не исключено выделение химерных клеточных линий и растений-регенерантов. Рост отдельных устойчивых клеток может подавляться мертвыми клетками. Из-за полиплоидизации культур сложно индуцировать рецессивные мутации.
Некоторых из этих недостатков лишены суспензионные культуры. Однако следует иметь в виду, что в суспензиях во многих случаях преобладают не единичные клетки, а клеточные агрегаты, для которых характерны те же недостатки, что и для каллюсных культур. В мутационной клеточной селекции наибольшее распространение получил метод высева суспензий в агаризованные селективные среды.
Во многих случаях оптимальным объектом для клеточной селекции является культура протопластов. Использование больших однородных популяций, активно делящихся гаплоидных или диплоидных мезофильных протопластов позволяет не только получать и эффективно отбирать интересующие исследователя мутанты, но и проводить количественные исследования мутагенеза, анализировать степень экспрессии индуцируемых фенотипических изменений на клеточном и организменном уровне. Однако для многих важных сельскохозяйственных, древесных и декоративных растений методы культуры протопластов практически не применимы (например, для большинства злаковых культур) или недостаточно отработаны.
Методы экспериментального мутагенеза растений начали применять задолго до того, когда появилась возможность использования мутагенов для клеточной селекции. В настоящее время накоплен обширный объем знаний об активности и особенностях использования различных химических веществ и физических факторов для индукции хозяйственно-ценных мутаций растений. В результате в распоряжении исследователей имеется широкий арсенал высоко активных химических мутагенов. Для клеточной селекции широкое распространение получили такие мутагены, как этил-метансульфонат (ЭМС), N-метил-N-нитро-N-нитрозогуанидин (НГ), N-этил-N-нитрозомочевина (НЭМ), N-нитрозометилмочевина (НММ) и др. С их помощью получен ряд мутантов, представляющих научный и практический интерес: с различными типами хлорофилл-дефектности; устойчивые к аналогам аминокислот и основаниям нуклеиновых кислот, антибиотикам, токсинам; различные ауксотрофы.
Из названных мутагенов выделяется НЭМ. Из-за химической нестабильности это вещество быстро разлагается в питательной среде, благодаря чему оно может применяться для мутагенной обработки клеточных культур без последующего отмывания их от мутагена. Помимо удобства в использовании для НЭМ характерна высокая мутагенная активность. Так, в исследованиях L. Маrton и сотрудников (1982) применение НЭМ позволило в 20 раз увеличить частоту устойчивых к хлорату клонов в культуре гаплоидных протопластов табака N. plumbaginifolia, а при мутагенезе диплоидных протопластов этого же вида появление клонов, устойчивых к стрептомицину, возросло в 30 раз (Р. Маligа и др., 1982).
Наряду с химическими мутагенами для клеточной селекции широко применяют физические мутагенные факторы - ионизирующее (рентгеновские и гамма-лучи) и ультрафиолетовое облучение.
Следует, однако, признать, что для клеточной селекции сельскохозяйственных растений предпочтительным считается использование спонтанной сомаклональной изменчивости. В этом случае частота появления мутантов с нежелательными отклонениями развития не так высока, как при использовании мутагенов. Ауксотрофные и другие редкие мутанты удалось выделить только благодаря использованию эффективных мутагенов.
6.3. Селекция мутантов in vitro. Экспрессия мутаций у растений-регенераторов
Первый этап процедуры выделения мутантов через культуру клеток растений in vitro включает селекцию определенных фенотипических вариантов путем помещения культур после обработки мутагеном (или без обработки) на питательную среду, содержащую селективный агент, или воздействия на культуры селективным фактором среды, например, повышенной/ пониженной температурой. К непосредственной селекции клеточных вариантов приступают не сразу после мутагенной обработки, а через определенный промежуток времени (от 2 ч до недели после обработки), необходимый для экспрессии мутаций. Выбор времени переноса культур на селективную среду зависит от типа мутаций, которые хотят получить, стадии клеточного цикла, количества клеток в исходных колониях и числа делений в предполагаемых мутантных клетках до начала селекции.
Наиболее распространенным методом отбора мутантных клеточных вариантов является прямая (позитивная) селекция. Ее используют для выделения мутантов, устойчивых к различным антиметаболитам: гербицидам, антибиотикам, токсинам. Применяют две основные стратегии прямой селекции: одношаговую и многошаговую, или ступенчатую. В первом случае концентрация селективного агента в среде в 2-3 раза превышает концентрацию, при которой наблюдается 100 % ингибирование роста и гибель культуры (minimum inhibitionconcentration - MIC100). В этом случае вероятность выживания неустойчивых клеток минимальна, однако могут погибнуть из-за малочисленности и устойчивые клетки. При ступенчатой селекции концентрацию селективного агента повышают постепенно в ряду последовательных пассажей культуры, начиная с концентрации, при которой наблюдается ингибирование роста приблизительно половины клеток (MIC50). В результате применения ступенчатой селекции доля в популяции устойчивых клеток увеличивается и к моменту достижения MIC100 их количество достаточно велико, чтобы поддерживать деления. С помощью прямой селекции выделены представляющие практический интерес мутанты, обладающие устойчивостью к гербицидам, засолению и некоторым болезням.
Для отбора условно летальных мутантов (ауксотрофных, чувствительных к стрессовым воздействиям) применяют непрямую (негативную) селекцию. Этот метод селекции основан на избирательной гибели в присутствии селективного фактора делящихся клеток дикого типа и выживании метаболически неактивных мутантных клеток. Например, в целях отбора температурочувствительных клеток культуры помещают в условия повышенной температуры (32 °С), в питательную среду при этом добавляют токсин (например, 5-бромдезоксиуридин, П-фторфенилаланин, арсенат натрия и др.). В таких условиях делящиеся клетки дикого типа погибают, а неактивные мутантные клетки сохраняются. При переносе культур в условия нормальной температуры на среде без токсина выжившие клетки возобновляют деления.
Для отбора ауксотрофов культуры переносят с минимальной среды (с токсином) на обогащенную среду без токсина, т. е. дополненную комплексом аминокислот, витаминов или гидролизатом казеина, дрожжевым экстрактом. Затем выясняют пищевую потребность для роста каждой выжившей колонии, помещая их на среды, дополненные определенными добавками: отдельными аминокислотами, витаминами и др.
В некоторых случаях отбор клеточных вариантов можно проводить визуально по внешним признакам, например, по интенсивности их окраски, обусловленной биосинтезом каких-либо пигментов, например, шиконина. Еще один метод - тотальная селекция, которая основана на индивидуальном тестировании отдельных клеточных клонов. Так, если визуальная селекция невозможна, проводят отбор клеточных линий-суперпродуцентов каких-либо вторичных метаболитов по результатам количественного их определения на давленных цитологических препаратах с помощью стандартных гистохимических или других методов (см. гл. 4). Основной недостаток тотальной селекции - ее высокая трудоемкость.
Второй этап процедуры выделения мутантов - получение растений-регенерантов из клеточных клонов, отобранных в селективных условиях, их размножение и тестирование. Как отмечалось выше, не все признаки, проявляющиеся на клеточном уровне, могут экспрессироваться на уровне организменном. Кроме того, в ходе отбора клеточных вариантов могут сохраняться клетки дикого типа, что может иметь место, например, при проведении клеточной селекции на каллюсных культурах. Поэтому для того чтобы гарантировать получение растений с интересующей исследователя мутацией, культуры после проведения клеточной селекции переносят на регенерационные среды, содержащие селективный агент. Селективный агент может присутствовать и в питательных средах, применяемых для укоренения растений- регенерантов, их клонального размножения in vitro.
Пробирочные растения предположительно мутантных клонов могут быть подвергнуты биохимическим, молекулярно-генетическим или другим анализам, необходимым для изучения природы мутационных изменений.
Для подтверждения генетической детерминированности выявленной изменчивости у растений-регенерантов, изучения наследования выделенных мутаций проводят классический генетический анализ, основанный на определении характера расщепления в их половых поколениях (F1, F2) от скрещивания с исходными растениями.
6.4. Основные направления практического использования клеточной селекции
Получение растений, толерантных к гербицидам. Одна из основных проблем сельскохозяйственного производства - это борьба с сорняками. В индустриально развитых странах наряду с агротехническими мероприятиями (обработка почвы) основным методом в этой области является применение гербицидов, т. е. химических препаратов, способных тотально или избирательно подавлять рост растений. Гербициды можно использовать перед посадкой или севом растений, внося в почву или опрыскивая тронувшиеся в рост сорняки, либо ими обрабатывают вегетирующие растения. Первый из этих способов не может в полной мере решить проблему, поскольку сорняки могут появляться и после всходов основной культуры, и в ходе всего периода вегетации. Кроме того, вносимые в почву гербициды, как правило, длительное время разлагаются, загрязняют окружающую среду. Обработка гербицидами вегетирующих растений более эффективна, так как позволяет защищать посевы в течение всего сезона. Однако при использовании гербицидов тотального действия возникают серьезные проблемы защиты от них культурных растений, которые к ним не устойчивы. Для этого созданы специальные приспособления, например, позволяющие смачивать гербицидом более высокие сорные растения, не затрагивая культурные. Эта процедура значительно упрощается, если в распоряжении растениевода имеются сорта растений, толерантные к используемому гербициду.
В решении проблемы создания сортов сельскохозяйственных растений, толерантных к гербицидам, оказались весьма эффективными методы экспериментального мутагенеза, клеточной селекции и, позднее, генетической инженерии.
Изучение спонтанных и индуцированных мутантов, толерантных к гербицидам, позволило установить основные механизмы гербицидоустойчивости:
✵ мутация мишени (прежде всего, фермента, на который действует гербицид);
✵ дезактивация/деструкция гербицида;
✵ сверхпродукция фермента-мишени за счет амплификации гена, его кодирующего, или изменения регуляции его активности.
Механизм мутации мишени связан с изменением последовательности аминокислот в той области молекулы фермента, в которой происходит его связывание с гербицидом. В результате гербицид «не узнает» свою мишень, фермент сохраняет свою активность, а организм становится толерантным к действию гербицида. Второй механизм связан с выработкой у устойчивых организмов ферментов, способных дезактивировать гербицид, например, путем присоединения к нему какого-либо химического радикала (ацетильной группы, нитрата и т. д.), либо превратить его в нетоксичный метаболит, который быстро распадается.
Комбинация экспериментального мутагенеза с клеточной селекцией на питательной среде, содержащей в качестве селективного агента определенный гербицид, показала высокую эффективность для выделения гербицидоустойчивых мутантов (некоторые из таких мутантов нашли применение на практике). В частности, зарегистрирован ряд толерантных к так называемым ALS-гербицидам генно-инженерных сортов сельскохозяйственных и декоративных растений, при создании которых использованы соответствующие гены от мутантов, полученных с помощью этой технологии.
Мишенью названной группы гербицидов является ацетолактатсинтаза (ALS), важный фермент в биосинтезе незаменимых разветвленных аминокислот валина, лейцина и изолейцина. Активность этого фермента может быть блокирована рядом веществ, имеющих разную структуру, относящихся к производным сульфонимочевины, имидозолинона, триазолопиримидина и пиримидил-окси-бензоата. Для получения толерантных к этим гербицидам трансгенных сортов сои, хлопчатника, льна, гвоздики и других растений были использованы мутантные ALS-гены от арабидопсиса и табака. Так, ген арабидопсиса csr 1-1 отличается от нормального гена мутацией, в результате которой у кодируемой им ацетолактатсинтазы имеет место замена серина на пролин в позиции 197, а у продукта гена csr 1-2 - замена серина на аспарагин в позиции 653. Мутация ALS-гена табака SuRB-Hrаприводит к двум заменам аминокислот: пролина на аланин в позиции 196 и триптофана на лейцин в позиции 573. Эти небольшие изменения первичной структуры фермента затронули сайт связывания с гербицидами (мутация мишени), что нарушило этот процесс и в результате обеспечило нечувствительность мутантов к ALS-гербицидам.
Получение растений, устойчивых к стрессам. Технология клеточной селекции показала высокую эффективность для выделения мутантов, устойчивых к различным стрессовым воздействиям, которые могут существенно снижать урожайность и качество продукции сельскохозяйственных растений. Одним из существенных стрессовых факторов является засоление почв. Процесс накопления вредных для растений солей в почве, главным образом хлористого и сернокислого натрия, происходит, как правило, в засушливых районах, а также при неправильном режиме орошения (вследствие излишнего полива орошаемых земель и плохой работы водосборной сети). Происходит смыкание поливных и грунтовых вод, капиллярный подъем солей к поверхности и засоление. Угнетение сельскохозяйственных культур начинается при содержании в профиле солей более 0,25 % массы почвы. Вредное действие засоления обусловлено нарушением осмотического баланса клетки, сопровождающегося снижением тургора, а также прямым токсическим влиянием ионов на физиологические и биохимические процессы в клетке. Полевые, овощные и плодовые культуры неодинаково относятся к засолению почв. Наиболее устойчива к засолению свекла, среднеустойчивы - зерновые, томаты, капуста, картофель, морковь, неустойчивы - подсолнечник, зернобобовые, редис, лук, чеснок, огурец. Из плодовых культур к засолению более устойчивы косточковые, менее - семечковые. Но даже устойчивые растения переносят сравнительно невысокие концентрации солей.
Решение проблемы борьбы с засолением включает не только использование комплекса агротехнических мероприятий, соблюдение технологии полива, но и селекцию сортов сельскохозяйственных культур, толерантных к воздействию солевого стресса. Традиционная селекция по этому признаку во многих случаях малоэффективна из-за невысокой изменчивости внутри видов культурных растений, у их диких сородичей. Усложняет селекцию и участие в детерминации признака различных генетических систем: контролирующих ионный гомеостаз, детоксикацию, биосинтез осмолитов (органических соединений, таких как сахара, некоторые аминокислоты, например, пролин, соединения четвертичного аммония, бетаин, оказывающих влияние на передвижение воды в клетке, поддержание водного баланса).
Отбор клеточных вариантов, способных поддерживать рост на питательных средах с повышенным содержанием солей, проводят, применяя как одношаговую (концентрация хлорида натрия, смеси солей или морской соли около МlС100), так и ступенчатую селекцию. Хороший эффект дает применение мутагенов. Рекомендуют достаточно длительную экспозицию (до трех месяцев) выдерживания культур на селективных средах (рис. 6.3). Показано, что при селекции на средах с умеренным содержанием соли (0,17М) обнаруживается феномен обратимой адаптации, которая не носит наследственный характер (утрачивается при культивировании на среде без соли). Следовательно, необходимо проводить окончательный отбор толерантных к засолению клеточных клонов при высоких концентрациях солей.
Рис. 6.3. Клеточная селекция in vitro на устойчивость к засолению у померанца (Citrus aurantium L.): а - культивирование каллюсов померанца в течение двух месяцев на питательных средах с разной концентрацией хлорида натрия; б - отбор толерантных к засолению каллюсных культур на среде со 100 мМ хлорида натрия; в - регенерация проростков из каллюса на среде со 100 мМ хлорида натрия и 3 % глицерола; 2 - растение-регенерант (слева) и контрольное растение того же возраста (справа) на среде с 300 мМ хлорида натрия; у контрольного растения наблюдается пожелтение листьев
(по N. Koc и др., 2009)
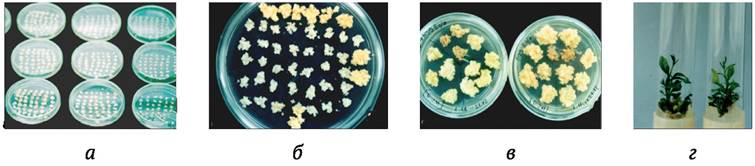
Несмотря на сложный характер генетического контроля признака, на большом количестве культур выделены клеточные клоны, способные сохранять рост при высоких концентрациях соли в питательной среде (0,17-0,34 М NaСl; для сравнения: содержание NaСl в морской воде составляет 500 мМ). Во многих случаях из таких культур были получены солеустойчивые растения-регенеранты, способные передавать приобретенный признак потомству. Изучение природы солеустойчивости у таких мутантов внесло значительный вклад в понимание механизмов защиты растений от подобных стрессовых воздействий. В настоящее время проблему солеустойчивости решают с помощью методов генетической инженерии, манипулируя конкретными генами, вовлеченными в данный процесс.
С использованием клеточной селекции получены интересные результаты не только по устойчивости к засолению, но и к другим стрессовым воздействиям: засухе, ионному, радиационному стрессу, экстремальным температурам. Отбор засухоустойчивых клеточных клонов проводят на селективных средах, содержащих осмотически активные вещества, понижающие внешний водный потенциал, например, полиэтиленгликоль (ПЭГ 6000, концентрация около 15-20 %), маннитол (100-900 мМ). Для отбора клеточных клонов, толерантных к ионным стрессам, в селективные среды добавляют в повышенных концентрациях соли токсичных металлов: алюминия, цинка, кадмия, ртути, меди. Для изучения механизмов устойчивости к радиационному стрессу получают с помощью клеточной селекции мутанты, устойчивые к ультрафиолетовому излучению и ионизирующей радиации. Клеточная селекция показала достаточно высокую эффективность и для выделения мутантов, устойчивых к повышенным и пониженным температурам.
Получение растений, устойчивых к болезням. В целях получения мутантов, устойчивых к определенным патогенам (возбудителям болезней), применяли
клеточную селекцию, при которой в селективные среды вводили сами патогены (в различной форме), их культуральные фильтраты, выделенные из них очищенные токсины. Лучшие результаты были получены при использовании в качестве селективных агентов специфических токсинов фитопатогенов. Следует иметь в виду, что развитие большинства болезней растений не связано с токсическим действием возбудителя на клетки хозяина. Однако в тех случаях, когда такое воздействие имеет место, клеточная селекция позволяет отбирать мутанты, устойчивые к токсину и соответственно вырабатывающему его патогену.
Первым продемонстрировал возможность выделения с помощью клеточной селекции мутантов, устойчивых к патотоксинам, P. S. Carlson (1973). Растения-регенеранты, полученные в культуре протопластов табака, обработанных мутагеном этилметансульфонатом и прошедших селекцию in vitro на устойчивость к метилсульфоксимину (MSO), обладали повышенной устойчивостью к Pseudomonas syringae pv. tabaci. Предполагалось, что MSO - это аналог табтоксина P. syringae pv. tabaci, поскольку он вызывает хлоротичные ареолы на листья, аналогичные тем, что появляются при поражении растений этим патогеном. Позднее было показано, что это не так (P. Thanutong и др., 1983). Тем не менее растения, полученные с помощью клеточной селекции по устойчивости к MSO, были устойчивы ик P. syringae pv. tabaci.
Классический пример успешной клеточной селекции на устойчивость к фитотоксинам представляет собой упомянутая выше работа B. G. Gengenbach и др. (1977) по отбору мутантов кукурузы, устойчивых к токсину Hel- mintosporium (синоним Drechslern) mayidis расы Т. Основанием для проведения их исследования было сильное поражение названным патогеном мужски стерильных линий кукурузы с цитоплазмой Т (cms-T). Авторы получали каллюсные культуры из зародышей и проводили ступенчатую селекцию на питательных средах, содержащих токсин H. mayidis. Из устойчивых к токсину каллюсных культур были регенерированы растения, обладающие высокой устойчивостью к гельминтоспориозу. Правда, при этом они приобрели нежелательный в данном случае признак - мужскую фертильность. Последующий генетический и молекулярно-генетический анализ показал, что оба этих детерминированных митохондриальными генами признака тесно сцеплены.
Положительные результаты были получены в результате клеточной селекции на устойчивость к токсинам и других видов Helmintosporium, а также к другим хозяиноспецифичным токсинам (R. Van den Bulk, 1991). Определенные перспективы имеет и клеточная селекция с использованием неспецифических токсинов, которые часто выступают в качестве факторов вирулентности, вызывающих усиление симптомов болезни, но не вовлеченных в первичное взаимодействие между патогеном и хозяином. Как правило, полученные с помощью такой селекции мутанты имеют повышенную, но не абсолютную устойчивость к заболеванию (пример: растения пшеницы, относительно устойчивые к бактериальному увяданию, отобранные с помощью селекции in vitro на устойчивость к сирингомицину, фитотоксину Pseudomonas syringae pv. syringae).
Получение растений с повышенным синтезом незаменимых аминокислот. Растительные белки занимают значительное место в пищевом рационе человека и животных. Вместе с тем характерной особенностью белков некоторых важных продовольственных и кормовых культур является относительно невысокий уровень незаменимых аминокислот (аминокислот, которые не могут быть синтезированы в организме человека и животных). Так, белки злаковых культур имеют пониженный уровень лизина. Кроме того, у кукурузы отмечено низкое содержание триптофана, у пшеницы и риса - треонина. Для белка важнейшей кормовой культуры сои типичным является недостаток метионина.
Традиционная селекция, направленная на улучшение качества растительного белка, достаточно сложная (так как предполагает проведение большого количества биохимических анализов) и во многих случаях неэффективная. В решении этой проблемы большие надежды связывают с применением клеточной селекции. Регуляция биосинтеза аминокислот у растений осуществляется путем обратного ингибирования, при этом некоторые ключевые ферменты биосинтеза ингибируются конечным продуктом, т. е. уровень аминокислоты определяет интенсивность ее биосинтеза. Для того чтобы значительно повысить содержание какой-либо аминокислоты в белке, необходимо вывести регуляцию ее биосинтеза из-под жесткого контроля конечным продуктом. Предполагается, что возможен отбор мутантов с нарушенной регуляцией биосинтеза определенных аминокислот на питательных средах, содержащих эти аминокислоты, благодаря чему их уровень в белках таких мутантов может превышать естественный уровень, характерный для конкретной продовольственной или кормовой культуры.
Эффективность селекции in vitro сверхпродуцентов аминокислот может быть повышена благодаря использованию в качестве селективных агентов не самих аминокислот, а их аналогов. Аналоги, подобно аминокислотам, могут ингибировать ключевые ферменты биосинтеза аминокислот, выступая в качестве обратного ингибитора. Вместе с тем многие из них обладают сильным токсическим действием на клетки. Например, в качестве токсических аналогов аминокислоты триптофана могут использоваться 5-метилтриптофан, 4-метилтриптофан, 5-фтортриптофан, 6-ортотриптофан, в качестве аналога фенилаланина - П-фторфенилаланин, лизина - S-аминоэтилцистеин.
В литературе описаны примеры успешной клеточной селекции суперпродуцентов аминокислот как при использовании в качестве селективных агентов самих аминокислот, так и их аналогов. K. A. Hibberd, C. E. Green (1982) для отбора линий кукурузы с повышенным содержанием в зерне лейцина и треонина (LT) помещали каллюсную ткань, полученную из незрелых зародышей, первоначально на селективную среду, содержащую 1 мМLT. Затем те клеточные клоны, которые сохраняли высокую интенсивность роста, переносили на среды с более высокими концентрациями селективного агента. В результате такой ступенчатой селекции были отобраны клеточные клоны, способные расти на среде с 2-2,5 мМLT. От одного из них (LT-19) удалось получить растения-регенеранты, у которых отмечено шестикратное, по сравнению с исходными растениями, превышение свободного треонина и 1,5-2-кратное - изолейцина. Анализ полового потомства регенерантов показал, что устойчивость к LT обусловлена одним доминантным геном, который был обозначен как Ltr-19. При этом гетерозиготы по этому гену показывали 33-кратное, а гомозиготы - 77-кратное превышение уровня свободного треонина по сравнению с исходными растениями.
J. M. Widholm (1972) первым выделил клеточные линии табака и моркови, устойчивые к 5-метилтриптофану, используя мутагенную обработку исходных культур этилметансульфонатом и ультрафиолетовым излучением. Для большинства клонов устойчивость была обусловлена уменьшением чувствительности к ингибированию триптофаном фермента антранилатсинтазы, что приводило к увеличению свободного триптофана у линий табака на 33 %, а у линий моркови - на 27 %. Правда, полученные из устойчивых линий табака растения-регенеранты имели триптофан-чувствительную форму антранилатсинтазы и не обладали сверхпродукцией триптофана. В аналогичном эксперименте, проведенном J. P. Ranch и другими (1983) на дурмане Datuta innoxia, были получены растения-регенеранты от отобранных с помощью ступенчатой селекции in vitro устойчивых к 5-метилтриптофану клеточных линий, которые характеризовались сверхпродукцией свободного триптофана (уровень триптофана был в 4-44 раз выше, чем у растений дикого типа).
Заключение
Клеточная селекция - отбор в культуре in vitro мутантных клеточных линий, устойчивых к определенным селективным агентам или факторам среды, и получение от них растений-регенерантов, обладающих соответствующими признаками.
В основе клеточной селекции лежит сомаклональная вариабельность - явление генетической изменчивости клеточных линий и растений-регенерантов. Различают два основных источника возникновения сомаклональных вариантов: генетическая гетерогенность клеток эксплантата и генетическая изменчивость, возникшая в процессе культивирования клеток invitro.
В качестве возможных генетических механизмов возникновения сомаклональных вариантов рассматривают: грубые и криптические кариологические изменения, точковые мутации, перемещения мобильных генетических элементов, амплификацию и редукцию генов, митотический кроссинговер. Кроме сомаклональной вариабельности, связанной с наследуемыми перестройками генома, могут иметь место и эпигенетические изменения, которые стабильно передаются дочерним клеткам, но не проявляются у растений-регенерантов или у их полового потомства.
Результаты генетических исследований на растениях разных видов убедительно доказывают, что большая часть сомаклональных вариаций обусловлена стабильными генетическими изменениями, т. е. мутациями. Частота спонтанных мутаций при культивировании клеток растений варьирует в зависимости от объекта в пределах 10-5-10-8. Показано, что растения-регенеранты с генными мутациями могут возникать с высокой частотой: один мутант на 20-25 растений-регенерантов; идентифицированы доминантные, семидоминантные и рецессивные ядерные мутации. Среди сомаклонов выявлены новые мутации, которые не встречались среди спонтанных мутантов, или полученных с помощью традиционных мутагенов. У сомаклонов обнаружены мутации хлоропластной и митохондриальной ДНК.
Уже в ранних исследованиях по сомаклональной изменчивости была показана возможность отбора среди растений-регенерантов мутантов с новыми признаками, имеющими важное хозяйственное значение: повышенной продуктивностью, улучшенными показателями качества продукции, устойчивостью к болезням. Интересные результаты в этом направлении были получены для ряда продовольственных, кормовых, технических, декоративных и лекарственных культур.
Использование мутагенов позволяет существенно расширить спектр сомаклональной изменчивости и благодаря этому повысить эффективность клеточной селекции. В качестве исходного материала для экспериментального мутагенеза используют каллюсные и суспензионные культуры и культуры протопластов. Также нашли применение обработки мутагенами семян с последующим получением из зародышей или проростков культуры клеток in vitro, в которой, собственно, проводят клеточную селекцию. Для этих же целей проводят обработку мутагенами пробирочных растений или эксплантатов, которые дают морфогенный каллюс, или культуры, способные к эмбриогенезу.
Для целей клеточной селекции широкое распространение получили такие химические мутагены, как этил-метансульфонат (ЭМС), N-метил-N- нитро-N-нитрозогуанидин (НГ), N-этил-N-нитрозомочевина (НЭМ), N-нитрозометилмочевина (НММ) и др. Наряду с химическими мутагенами для клеточной селекции широко применяют физические мутагенные факторы - ионизирующее излучение (рентгеновские и гамма-лучи) и ультрафиолетовое облучение.
Для клеточной селекции сельскохозяйственных растений предпочтительным считается использование спонтанной сомаклональной изменчивости. В этом случае частота появления мутантов с нежелательными отклонениями развития не так высока, как при использовании мутагенов. Ауксотрофные и другие редкие мутанты удалось выделить только благодаря использованию эффективных мутагенов.
Наиболее распространенным методом отбора мутантных клеточных вариантов является прямая (позитивная) селекция. Ее используют для выделения мутантов, устойчивых к различным антиметаболитам: гербицидам, антибиотикам, токсинам. Применяют две основные стратегии прямой селекции: одношаговую и многошаговую, или ступенчатую. Для отбора условно летальных мутантов (ауксотрофных, чувствительных к стрессовым воздействиям) применяют непрямую (негативную) селекцию. Этот метод селекции основан на избирательной гибели под действием селективного фактора делящихся клеток дикого типа и выживании метаболически неактивных мутантных клеток.
В некоторых случаях отбор клеточных вариантов можно проводить визуально по внешним признакам, например, по интенсивности их окраски, обусловленной биосинтезом каких-либо пигментов. Еще один метод - тотальная селекция, которая основана на индивидуальном тестировании отдельных клеточных клонов.
Имеется ряд направлений клеточной селекции, позволяющих целенаправленно получать растения-регенеранты с хозяйственно важными признаками: устойчивостью к гербицидам, к стрессовым факторам, некоторым заболеваниям, обладающих сверхпродукцией незаменимых аминокислот.
Контрольные вопросы
1. В чем состоит клеточная селекция, осуществляемая в культуре клеток растений, и что лежит в ее основе?
2. Каковы возможные причины сомаклональной вариации?
3. Назовите генетические механизмы возникновения сомаклональных вариантов.
4. Какие особенности имеет мутагенез в культуре in vitro?
5. Какие мутагены используют для усиления сомаклональной изменчивости?
6. Назовите возможные методы применения мутагенов в клеточной селекции.
7. Целесообразно ли использовать мутагенез в клеточной селекции, имеющей целью отбор по хозяйственно-ценным признакам?
8. Назовите методы отбора мутантных вариантов при проведении клеточной селекции.
9. Почему необходимо использовать селективные среды не только для отбора клеточных вариантов, но и при укоренении растений-регенерантов, их размножении?
10. Каким образом можно доказать генетическую природу новых признаков, выявленных у растений-регенерантов?
11. Назовите основные направления практического использования клеточной селекции.
12. Приведите примеры получения хозяйственно-ценных мутантов с помощью клеточной селекции.