Молекулярная биотехнология. Принципы и применение - Глик Б., Пастернак Дж. 2002
Основы молекулярной биотехнологии
Молекулярно-биотехнологическая революция
Возникновение молекулярной биотехнологии
В начале 70-х годов традиционная биотехнология как научная дисциплина была не слишком известна; исследования в этой области в основном проводились в отделах инженерной химии и иногда в рамках социальных микробиологических программ. В широком смысле биотехнология занимается производством коммерческих продуктов, образуемых микроорганизмами в результате их жизнедеятельности. Более формально биотехнологию можно определить как «применение научных и инженерных принципов к переработке материалов живыми организмами с целью создания товаров и услуг». В историческом смысле биотехнология возникла тогда, когда дрожжи были впервые использованы при производстве пива, а бактерии — для получения йогурта. Термин «биотехнология» был придуман в 1917 г. венгерским инженером Карлом Эреки для описания процесса крупномасштабного выращивания свиней с использованием в качестве корма сахарной свеклы. По определению Эреки, биотехнология — это «все виды работ, при которых из сырьевых материалов с помощью живых организмов производятся те или иные продукты». Однако это совершенно точное определение не получило широкого распространения. Долгое время термин «биотехнология» относился к двум очень разным дисциплинам. С одной стороны, его употребляли, говоря о промышленной ферментации, с другой — применительно к той области, которая сейчас называется эргономикой. Такой двойственности пришел конец в 1961 г., когда шведский микробиолог Карл Герен Хеден порекомендовал изменить название научного журнала «Journal of Microbiological and Biochemical Engineering and Technology» («Журнал микробиологической и химической инженерии и технологии»), специализирующегося на публикации работ по прикладной микробиологии и промышленной ферментации, на «Biotechnology and Bioengineering» («Биотехнология и биоинженерия»). С этого момента биотехнология оказалась четко и необратимо связана с исследованиями в области «промышленного производства товаров и услуг при участии живых организмов, биологических систем и процессов» и встала на прочный фундамент микробиологии, биохимии и химической инженерии.
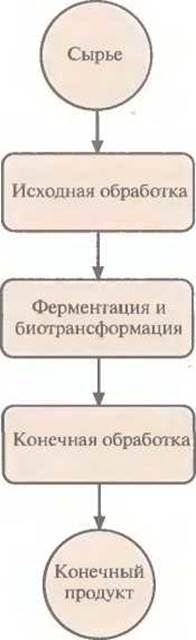
Рис. 1.1. Основные этапы биотехнологического процесса. Термин был введен Карлом Эреки и относился к крупномасштабному получению свинины (конечный продукт) с использованием дешевой сахарной свеклы (сырье) в качестве корма для свиней (биотрансформация).
Промышленный биотехнологический процесс, в котором для производства коммерческих продуктов используются микроорганизмы, обычно состоит из трех ключевых этапов (рис. 1.1.).
1. Исходная обработка: обработка сырья таким образом, чтобы его можно было использовать как источник питательных веществ для микроорганизма-мишени.
2. Ферментация и биотрансформация: рост микроорганизма-мишени в большом (обычно более 100 л) биореакторе (ферментация) с последующим образованием нужного метаболита, например антибиотика, аминокислоты или белка (биотрансформация).
3. Конечная обработка: очистка нужного вещества от компонентов культуральной среды или от клеточной массы.
Целью биотехнологических исследований является максимальное повышение эффективности каждого из этих этапов и поиск микроорганизмов, с помощью которых можно получить нужные вещества (пищевые добавки, антибиотики и т. д.). В 60—70-е годы все эти исследования касались только исходной обработки, устройства биореакторов и получения конечного продукта. Благодаря этому был усовершенствован инструментальный контроль процесса ферментации и значительно расширены возможности крупномасштабного культивирования, что позволило повысить эффективность производства некоторых продуктов.
Наиболее трудным для оптимизации был этап биотрансформации. Когда использовались природные микробные штаммы, выход конечного продукта часто оказывался намного ниже оптимального. Поэтому предпринимались попытки изменить генетическую конституцию существующих штаммов-продуцентов с помощью химического мутагенеза или ультрафиолетового облучения. При таком подходе уровень повышения продукции обычно лимитировался чисто биологическими факторами. Например, если мутантный штамм синтезировал слишком много того или иного вещества, часто это отрицательно влияло на прочие метаболические процессы и приводило к угнетению роста культуры при крупномасштабном культивировании. Несмотря на это традиционные стратегии «индуцированного мутагенеза и селекции», направленные на усовершенствование штамма-продуцента, были исключительно плодотворны для многих процессов, например для производства антибиотиков.
Традиционные схемы генетического усовершенствования бактерий включают скрининг, отбор и тестирование огромного количества колоний, поэтому такие схемы высокозатратны и занимают много времени. Более того, при этом можно рассчитывать только на усовершенствование уже существующих, передаваемых по наследству свойств штамма, а не на расширение его генетических возможностей. И все же к концу 70-х годов таким образом были усовершенствованы производственные процессы получения целого ряда продуктов.
С развитием технологии рекомбинантных ДНК природа биотехнологии изменилась окончательно и бесповоротно. Появилась возможность оптимизировать этап биотрансформации более прямым путем, создавать, а не просто отбирать высокопродуктивные штаммы, использовать микроорганизмы и эукариотические клетки как «биологические фабрики» для производства инсулина, интерферона, гормона роста, вирусных антигенов и множества других белков. Технология рекомбинантных ДНК позволяет получать в больших количествах ценные низкомолекулярные вещества и макромолекулы, которые в естественных условиях синтезируются в минимальных количествах. Растения и животные стали естественными биореакторами, продуцирующими новые или измененные генные продукты, которые никогда не могли бы быть созданы методами мутагенеза и селекции или скрещивания. Наконец, эта новая технология способствует развитию принципиально новых методов диагностики и лечения различных заболеваний. На стыке технологии рекомбинантных ДНК и биотехнологии возникла новая область исследований, динамичная и высококонкурентоспособная, — молекулярная биотехнология. Эта молодая дисциплина, как и молекулярная биология в период своего становления, весьма амбициозна, заявляемые ею притязания не всегда соответствуют реальным возможностям. Ее стратегия и экспериментальная база претерпевают быстрое изменение, одни подходы все время вытесняются другими. Но несомненно одно: в будущем молекулярная биотехнология станет рутинным методом создания живых систем, обладающих новыми функциями и возможностями.
Таблица 1.1. История развития молекулярной биотехнологии
|
Дата |
Событие |
|
1917 |
Карл Эреки ввел термин «биотехнология» |
|
1943 |
Произведен пенициллин в промышленном масштабе |
|
1944 |
Эвери. МакЛеод и МакКарти показали, что генетический материал представляет собой ДНК |
|
1953 |
Уотсон и Крик определили структуру молекулы ДНК |
|
1961 |
Учрежден журнал «Biotechnology and Bioengineering» |
|
1961-1966 |
Расшифрован генетический код |
|
1970 |
Выделена первая рестрицирующая эндонуклеаза |
|
1972 |
Корана и др. синтезировали полноразмерный ген тРНК |
|
1973 |
Бойер и Коэн положили начало технологии рекомбинантных ДНК |
|
1975 |
Колер и Мильштейн описали получение моноклональных антител |
|
1976 |
Изданы первые руководства, регламентирующие работы с рекомбинантными ДНК |
|
1976 |
Разработаны методы определения нуклеотидной последовательности ДНК |
|
1978 |
Фирма Genentech выпустила человеческий инсулин, полученный с помощью Е. coli |
|
1980 |
Верховный суд США, слушая дело Даймонд против Чакрабарти, вынес вердикт, что микроорганизмы, полученные генноинженерными методами, могут быть запатентованы |
|
1981 |
Поступили в продажу первые автоматические синтезаторы ДНК |
|
1981 |
Разрешен к применению в США первый диагностический набор моноклональных антител |
|
1982 |
Разрешена к применению в Европе первая вакцина для животных, полученная по технологии рекомбинантных ДНК |
|
1983 |
Для трансформации растений применены гибридные Ті-плазмиды |
|
1988 |
Выдан патент США на линию мышей с повышенной частотой возникновения опухолей, полученную генноинженерными методами |
|
1988 |
Создан метод полимеразной цепной реакции (ПЦР) |
|
1990 |
В США утвержден план испытаний генной терапии с использованием соматических клеток человека |
|
1990 |
Официально начаты работы над проектом «Геном человека» |
|
1994-1995 |
Опубликованы подробные генетические и физические карты хромосом человека |
|
1996 |
Ежегодный объем продаж первого рекомбинантного белка (эритропоэтина) превысил 1 млрд, долларов |
|
1996 |
Определена нуклеотидная последовательность всех хромосом эукариотического микроорганизма (Saccharomyces cerevisiae) |
|
1997 |
Клонировано млекопитающее из дифференцированной соматической клетки |
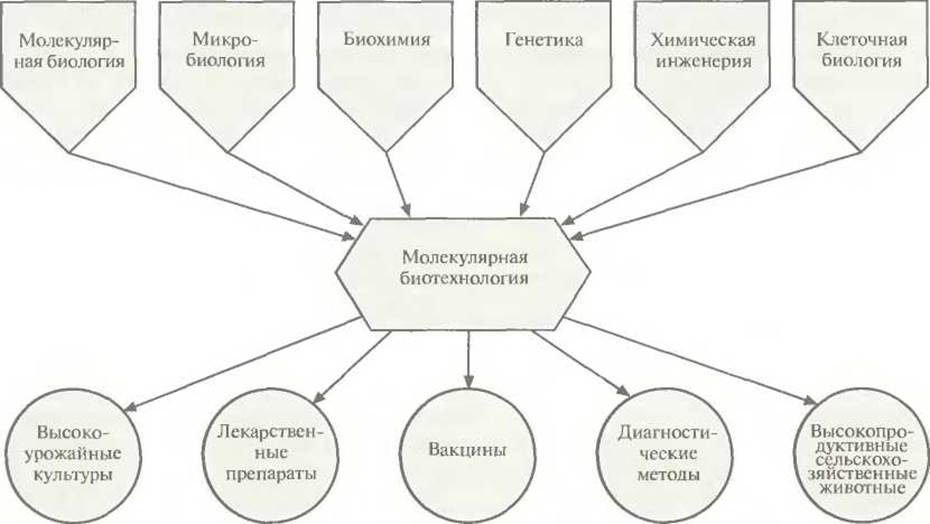
Рис. 1.2. Молекулярная биотехнология использует достижения многих областей науки и позволяет создавать широкий ассортимент коммерческих продуктов и методов.
Очень редко новые научные дисциплины возникают «на пустом месте»; как правило, их фундаментом служат различные области науки. Что касается молекулярной биотехнологии, то ее биотехнологическая составляющая относится к сфере промышленной микробиологии и химической инженерии, а молекулярная — к областям молекулярной биологии, молекулярной генетики бактерий и энзимологии нуклеиновых кислот (табл. 1.1). В широком смысле молекулярная биотехнология пользуется достижениями самых разных областей науки и применяет их для создания самых разных коммерческих продуктов (рис. 1.2).