Молекулярная биология клетки - Том 2 - Албертс Б., Брей Д., Льюис Дж., Рэфф М., Робертс К., Уотсон Дж. 1993
Цитоскелет
Организация цитоскелета
До сих пор мы рассматривали микротрубочки, актиновые филаменты и промежуточные филаменты так, как будто это независимые составные части цитоскелета. В действительности, конечно, различные элементы цитоскелета должны быть связаны в единое целое, а их функции скоординированы, чтобы клетка могла осуществлять разного рода движения и изменять свою форму. Например, когда находящийся в культуре фибробласт округляется, готовясь к делению, реорганизуется весь его цитоскелет в целом: исчезают стрессовые волокна и цитоплазматические микротрубочки, появляется митотическое веретено, а затем и сократимое кольцо, и все это происходит как единая контролируемая цепь событий.
В этом разделе мы рассмотрим взаимодействия между главными системами филаментов цитоскелета в связи с тремя его функциями. Сначала мы выясним, каким образом цитоскелет организует содержимое цитоплазмы, включая те ее компоненты, которые обычно считают свободно растворенными. Затем мы перейдем к вопросу о том, как координированная работа цитоскелета обеспечивает направленное передвижение животной клетки по твердому субстрату. И наконец, мы обсудим, как цитоскелет порождает те многочисленные морфологические изменения, которые происходят в процессе развития зародыша. В результате этого рассмотрения станет ясно, насколько фрагментарны пока наши представления о молекулярных механизмах этих фундаментальных процессов.
11.6.1. В цитоплазме имеется сложная трехмерная сеть белковых нитей [58]
Мы уже знаем, что кортикальная цитоплазма многих животных клеток содержит сети из поперечностных актиновых филаментов. Подобные же сети, но образованные взаимодействующими актиновыми филаментами, микротрубочками и промежуточными филаментами, пронизывают всю цитоплазму. Наиболее отчетливо они видны после экстракции клеток неионным детергентом, которая удаляет фосфолипиды и растворимые белки. Если обработанные таким образом клетки быстро заморозить и подвергнуть глубокому травлению, то металлическая реплика с полученного препарата выявит поразительную картину цитоскелета (рис. 11-78). Различные типы белковых филаментов можно распознать по их толщине, а в некоторых случаях и по расположению их белковых субъединиц. Часто бывает видно, что соседние филаменты соединены более тонкими нитями, белки которых тоже были в ряде случаев идентифицированы с помощью антител. Это оказались различные виды белков, ассоциированных с микротрубочками, и длинные гибкие боковые отростки, отходящие от субъединиц промежуточных филаментов некоторых типов (см. рис. 11-77, А). Однако в большинстве случаев белки, образующие поперечные сшивки, пока не известны.
В клетках, не обработанных детергентом, структура цитоплазмы еще сложнее. Пространство между филаментами цитоскелета заполнено зернистым «основным веществом» ("ground substance"), которое, как считают, представляет собой очень концентрированную смесь «растворимых» белков, имеющихся в живой клетке. Разнообразные мембранные органеллы тоже погружены в этот плотный матрикс и соединены с филаментами цитоскелета тонкими белковыми нитями. И гранулярного материала, и органелл тем больше, чем ближе к центральной области клетки, где сосредоточены микротрубочки и промежуточные филаменты и где, как можно увидеть при помощи светового микроскопа с видеоприставкой, происходит большая часть процессов цитоплазматического транспорта. В более периферийных участках значительно гуще сеть актиновых филаментов, которые как бы вытесняют оттуда большую часть мембранных органелл, а возможно, и какую-то долю гранулярного материала (рис. 11-79). Эта густая сеть прикреплена к плазматической мембране и соответствует богатому актином кортексу клетки, о котором уже говорилось ранее (разд. 11.2).
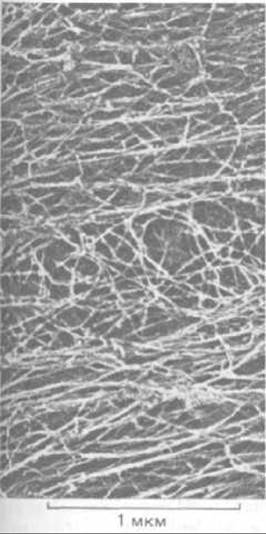
Рис. 11-78. Цитоплазма фибробласта, экстрагированного неионным детергентом (электронная микрофотография, глубокое травление). Большинство тянущихся слева направо прямых волокон, образующих рыхлые пучки, - это актиновые филаменты, а перепутанные волокна в середине фото - в основном промежуточные филаменты. (С любезного разрешения John Heuser и Marc Kirschner.)
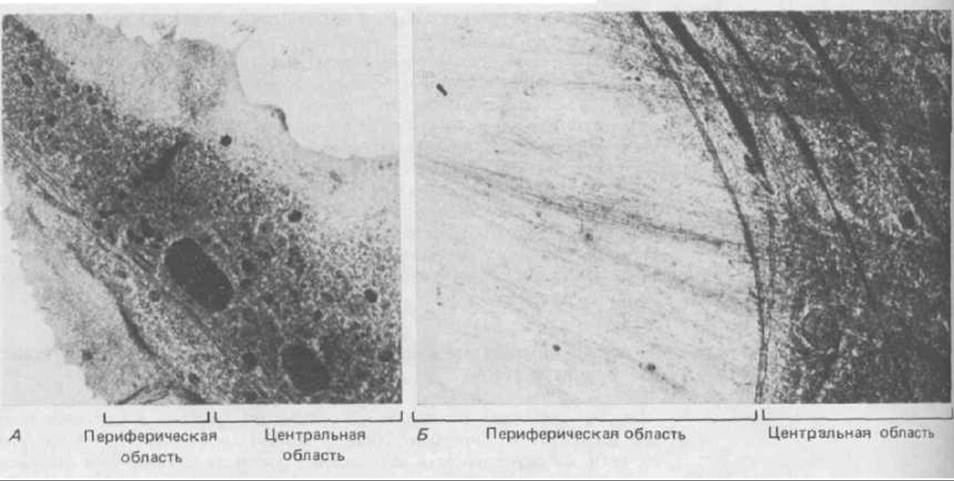
Рис. 11-79. Трансмиссионная электронная микрофотография фибробласта, замороженного «живьем», выявляет на периферии клетки участок, свободный от органелл, а ближе к центру-наоборот, богатую органеллами область (А). Граница между этими двумя областями при сильном увеличении видна более отчетливо (Б). (Р. С. Bridgman, В. Kachar, Т. S. Reese, J. Cell Biol. 102: 1510-1521, 1986. С разрешения Rockefeller Univ. Press.)
11.6.2. Насколько упорядочена организация цитоплазмы? [59]
Когда мембранные органеллы цитоплазмы быстро перемещаются с места на место, они движутся по белковым «дорожкам», с которыми соединены специальными мостиками. Как мы уже говорили, движение вдоль микротрубочек осуществляется с помощью кинезина и динеино-подобных белков (разд. 11.4.9), а вдоль актиновых филаментов с помощью миозиноподобных белков (разд. 11.2.4). Кластеры рибосом в цитозоле тоже нередко находятся в ассоциации с филаментами; при экстрагировании клеток неионными детергентами значительная часть аппарата белкового синтеза остается связанной с цитоскелетом. Даже растворимые ферменты, в том числе некоторые ферменты гликолиза, по-видимому, «сидят» на специфических участках миофибрилл в мышечных клетках и стрессовых волокон в фибробластах, и здесь их можно выявить с помощью флуоресцентных антител.
Степень структурной организованности цитозоля в настоящее время является предметом споров. Источник наших знаний об идущих в цитозоле процессах - это в основном биохимические исследования, а они начинаются с гомогенизации клетки, так как только после этого можно определять активность ферментов и выделять их в очищенном виде. Успехи такого подхода привели многих биохимиков к представлению о цитозоле как о простом растворе ферментов. Однако другие исследователи склонны полагать, что едва ли не большинство ферментов цитозоля собрано в группы по принадлежности к тому или иному биохимическому пути и прикреплено к цитоскелету так, чтобы обеспечить более быстрое и эффективное прохождение метаболитов по каждому из таких путей. Поскольку это прикрепление, вероятно, непрочно и связи легко разрушаются, для его убедительной демонстрации могут потребоваться новые методы - такие, например, как инъекции в живые клетки белков с флуоресцентными метками (разд. 4.2.3).
11.6.3. Растягивание актинового кортекса способно вызывать поляризацию клетки, необходимую для ее направленного движения [60]
Цитоскелет не только служит каркасом для прикрепления и перемещения питоплазматических компонентов, но и обеспечивает возможность миграции клеток. Несмотря на новейшие успехи в выяснении структуры и функции цитоскелета, механизм, с помощью которого животные клетки ползают по поверхности субстрата, пока еще плохо изучен. Для эффективного передвижения необходимо, чтобы клетка была поляризована: нужно, чтобы вся ее плазматическая мембрана находилась в относительном покое, за исключением переднего края, где клетка периодически выпускает ламеллоподии и микрошипы, когда движется вперед.
Когда неполяризованная мигрирующая клетка первоначально прикрепляется к поверхности культуральной чашки, микрошипы и ламеллоподии выдвигаются во всех направлениях и тянут клетку в разные стороны, в результате чего она остается на месте. Но, если случайно две противоположно направленные ламеллоподии достаточно прочно прикрепятся к субстрату, мы увидим, что растягивание клеточного кортекса между ними подавляет дальнейшее образование микрошипов и ламеллоподии в растянутой области-вероятно, потому, что актиновые филаменты в этом участке лежат параллельно плазматической мембране (рис. 11-80), а не перпендикулярно к ней, как нужно для возникновения ламеллоподии и микрошипов (разд. 11.2.11). Таким образом, тот факт, что в растянутых участках выступы цитоплазмы не образуются, можно объяснить чисто механическими причинами.
Дальнейшая «борьба» между ламеллоподиями похожа на перетягивание каната: те, что тянут клетку слабее, отрываются от субстрата и становятся частью пассивного растянутого кортекса. В конце концов останется только один активный участок плазматической мембраны; он и будет передним краем теперь уже поляризованной клетки, которая начнет движение в одном направлении (рис. 11-81).
Когда клетка находится на ровной плоской поверхности, выбор направления движения (т. е. «победа» каких-то ламеллоподии) будет делом непредсказуемым, зависящим от случайных вариаций в организации цитоскелета. Однако на неоднородной поверхности, например на культуральном субстрате с градиентом вещества, способствующего адгезии, «отбор» ламеллоподии и микрошипов будет направляться факторами внешней среды; эти выступы будут работать как щупальца, которые определяют, куда клетке двигаться.
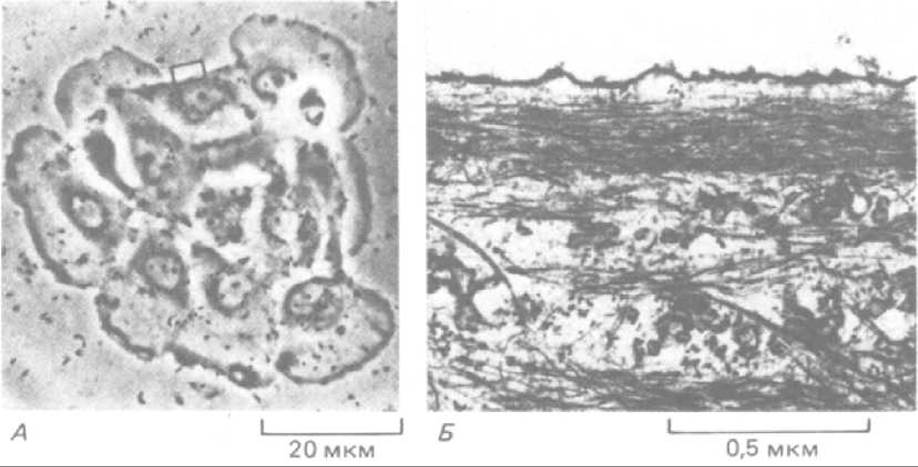
Рис. 11-80. Организация актиновых филаментов в зоне растянутого клеточного кортекса. Тянущее действие противоположных ламеллоподии в группе из восьми эпителиальных клеток, показанных на световой микрофотографии (А), создает в одной из клеток покоящийся участок, где образование выступов подавлено (показан прямоугольником). При исследовании этого участка в электронном микроскопе (Б) в нем можно видеть пучки актиновых филаментов, идущих параллельно плазматической мембране, т. е. перпендикулярно к той ориентации, которая нужна для образования ламеллоподии и микрошипов. (John Kolega, i. Cell Biol. 102: 1400-1411, 1986. С разрешения Rockefeller Univ. Press.)
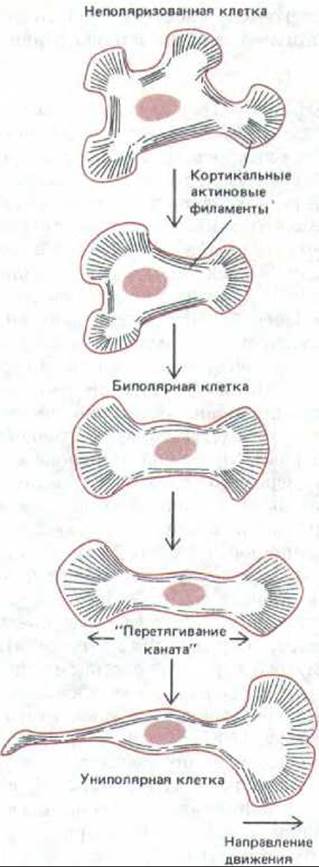
Рис. 11-81. Возникновение полярности у мигрирующей клетки. Хотя здесь изображена клетка в культуре, сходные процессы, вероятно, играют фундаментальную роль в морфогенезе многих тканей. Прикрепившись к поверхности культуральной чашки, клетка выбрасывает ламеллоподий во всех направлениях. По мере того как они растягивают клетку, возникают участки, где кортекс растянут и дальнейшее образование ламеллоподий подавлено (см. рис. 11-80). «Перетягивание каната» продолжается до тех пор, пока не возьмет верх какая-то одна ламеллоподия - вероятно, случайно, например потому, что субстрат под ней оказался более «липким», или благодаря небольшому хемотаксическому градиенту, который благоприятствует движению вперед одной из сторон клетки (разд. 11.2.13). Теперь клетка становится униполярной и перемещается в направлении «удачливой» ламеллоподий. С помощью подобного механизма клетки в развивающихся тканях будут двигаться в сторону тех клеток или элементов внеклеточного матрикса, к которым они прикрепляются наиболее прочно, зачастую делая выбор между субстратами, лишь слегка различающимися по адгезивности (разд. 14.3.9).
11-34
11.6.4. Относительная роль актиновых филамептов и микротрубочек в миграции зависит от типа клеток [61]
При миграции клеток микротрубочки и актиновый цитоскелет обычно работают совместно, так что вклад их разделить трудно. Степень участия микротрубочек в направленном движении клетки у разных типов клеток различна. Если деполимеризовать микротрубочки фибробласта колхицином, он перестает двигаться в определенную сторону и начинает выпускать ламеллоподии в случайных направлениях. С другой стороны, на направленное движение нейтрофила колхицин практически не влияет. Более того, если нейтрофил кратковременно прогреть до 42 "С, значительная часть его кортикальной цитоплазмы отделяется от остальной клетки и начинает двигаться сама по себе. Хотя эти подвижные фрагменты клеток лишены микротрубочек и ядра, они способны ползать по культуральной чашке в течение дня и дольше, прежде чем подвергнутся распаду (рис. 11-82). Поначалу фрагменты обладают такой же способностью к хемотаксису, как и исходные нейтрофилы; например, они направленно движутся «вверх» по градиенту концентрации N-формилированных пептидов (разд. 11.2.13). Однако миграция прекращается, если актиновые нити в нейтрофилах (или в образовавшихся из них фрагментах) деполимеризовать цитохалазином. По-видимому, этим клеткам для направленной миграции необходимы актиновые филаменты, но не микротрубочки.
Однако движение конусов роста нервных клеток, судя по всему, зависит и от микротрубочек, и от актиновых филаментов. В аксонах и дендритах (обобщенно называемых нейритами) содержатся необычайно упорядоченные пучки микротрубочек. Каждый нейрит «вытягивается» из тела нервной клетки под действием тянущей силы, создаваемой конусом роста на его кончике. Если нервные клетки в культуре обработать колхицином, рост нейритов останавливается, что указывает на участие микротрубочек в продвижении конуса роста. Конус роста эквивалентен переднему краю нейтрофила или фибробласта, и формирование на нем ламеллоподий и микрошипов тоже зависит от актиновых филаментов и подавляется при обработке цитохалазином. Тем не менее у нервных клеток, растущих на высокоадгезивной поверхности (например, на культуральной чашке, покрытой поликатионом полилизином), нейриты будут расти и в присутствии цитохалазина, хотя направление их роста будет меняться неупорядоченным образом. По-видимому, ламеллоподии и микрошипы нужны для того, чтобы направлять конус роста и позволять ему преодолевать слабоадгезивные поверхности. Организация микротрубочек и актиновых филаментов в конусе роста и в переднем крае фибробласта для сравнения показана на рис. 11-83.
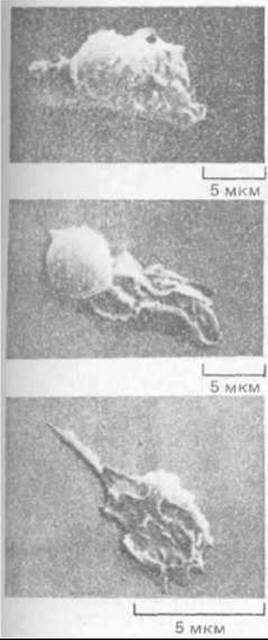
Рис. 11-82. Нейтрофил, нз которого в результате кратковременной тепловой обработки (42°С) был получен большой фрагмент, способный к непрерывному движению и хемотаксису, хотя в нем не было ядра и митохондрий. Микрофотография, полученная с помощью сканирующего электронного микроскопа. (S. R. Malawista и A. DeBoisfleury Chevance, J. Cell Biol. 95: 960-973. 1982; с разрешения Rockefeller Univ. Press.)
11.6.5. Натяжение актинового кортекса, возможно, помогает управлять движением животных клеток [62]
Каков молекулярный механизм продвижения клетки вперед? Ответа на этот ключевой вопрос пока нет. Одна из гипотез, отводящая главную роль актиновому кортексу, представлена на рис. 11-84. Есть четкие свидетельства того, что кортекс в животных клетках находится в натянутом состоянии. Это натяжение кортекса, которое удалось измерить в очень крупных клетках, например в яйцеклетках морского ежа, стремится придать клеткам суспензии сферическую форму (т.е. такую, при которой их поверхность минимальна). Кроме того, клетки, видимо, способны «расслаблять» кортекс в определенных участках своей поверхности, например в переднем крае, хотя механизм этого расслабления неизвестен. В результате на переднем крае периодически образуются ламеллоподии - предположительно вследствие активации в плазматической мембране специальных кэпирующих белков, которая позволяет субъединицам актина присоединяться к плюс-концам актиновых филаментов в этом участке (разд. 11.2.15). Те ламеллоподии, которым не удалось прочно прикрепиться к субстрату, оттягиваются назад за счет кортикального натяжения, и это приводит к «раффлингу» (см. рис. 11-42). Но если какая-нибудь ламеллоподия прочно прикрепится, то ее актиновые филаменты будут связаны с субстратом при помощи трансмембранных соединительных белков (см. рис. 11-43); теперь то самое натяжение кортекса, которое оттягивало свободную ламеллоподию назад, будет двигать всю клетку вперед к новой точке прикрепления (см. рис. 11-84).
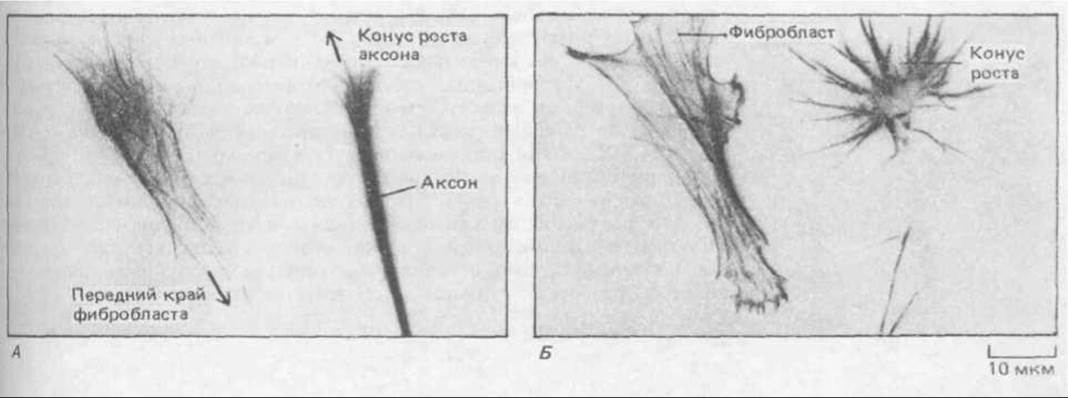
Рис. 11-83. Организация микрогрубочек и актиновых филамектов в подвижных клетках двух типов. Окраска антителами к тубулину, меченными флуоресцеином (А), выявляет микротрубочки в виде тонкой сети во всей цитоплазме фибробласта и в виде плотного пучка, идущего по оси аксона. При окраске тех же клеток родамин-фаллоидином (Б) видны актиновые филаменты как пучки, которые в фибробласте тянутся к переднему краю, а в аксоне концентрируются в микрошипах конуса роста. (С любезного разрешения Peter Hollenbeck.)
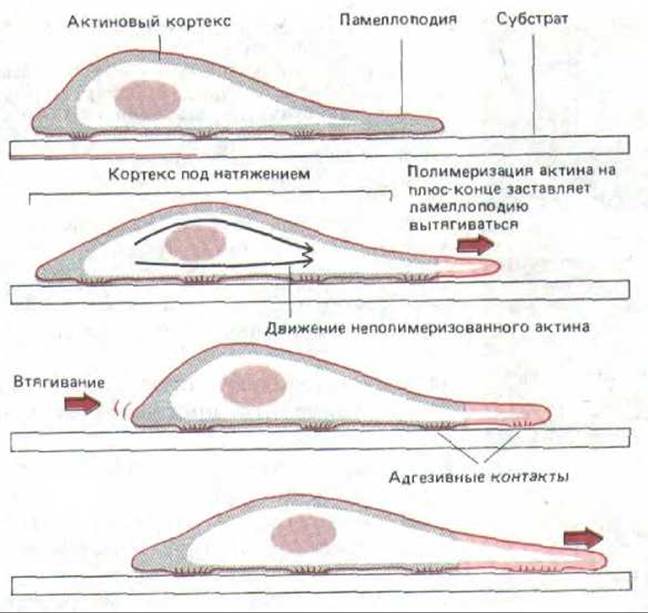
Рис. 11-84. Одна из моделей, показывающая, как богатый актином кортекс мог бы продвигать клетку вперед. Полимеризация актина ведет к вытягиванию ламеллоподии на переднем крае; прикрепившись к субстрату, ламеллоподия растягивает актиновый кортекс, и в результате его натяжения тело клетки продвигается вперед, частично ослабляя это натяжение. Такой цикл может повторяться снова и снова, шаг за шагом продвигая клетку.
По аналогии с мышцей - наиболее изученной двигательной системой на основе актина - можно было бы ожидать, что вызывающие сокращение силы в кортексе создаются при взаимодействии актиновых и миозиновых филаментов. Однако против этой возможности говорят эксперименты с клеточным слизевиком Dictyostelium discoideum (разд. 14.3.1). Удалось получить таких мутантов этого слизевика, у которых нормальный ген фибриллярного миозина был заменен искусственно модифицированным геном. В этом гене был вырезан длинный участок, кодирующий белок (см. разд. 4.6.14), и в результате эти мутанты были лишены миозиновых нитей. Неудивительно, что у мутантных клеток не могло формироваться сократительное кольцо, и поэтому они превращались в гигантские многоядерные клетки, которые лишь изредка делились, просто разрываясь надвое. Тем не менее эти клетки сохраняли способность к миграции и даже к хемотаксической реакции на сАМР (разд. 14.3.2), хотя оба процесса были заметно нарушены. По-видимому, координированное перемещение клетки, так же как и натяжение кортекса, не зависит всецело от биполярных миозиновых филаментов; возможно, что натяжение может создаваться эластичной сетью актиновых филаментов (действующей подобно резиновой пленке) или другими стягивающими силами, источником которых могли бы быть, например, процессы разборки актиновых филаментов или мини-миозин.
11.6.6. Движению переднего края мигрирующей клетки может способствовать эндоцитозный цикл [63]
Как уже говорилось в гл. 6, все животные клетки непрерывно «заглатывают» небольшие участки своей плазматической мембраны и возвращают их обратно на клеточную поверхность в процессе, получившем название эндоцитозного цикла (разд. 6.5). Есть данные о том, что у ползущих по субстрату поляризованных клеток кусочки мембраны переходят внутрь со всей поверхности клетки, а возвращаются главным образом на передний край. По-видимому, такая асимметрия эндоцитозного цикла мигрирующей клетки помогает продвижению переднего края (разд. 6.5.13). Вероятно, возврат перешедших в цитоплазму участков мембраны на передний край поляризованной клетки зависит от ориентированных микротрубочек и актиновых филаментов: те и другие способны при участии вспомогательных белков направлять активный транспорт мембранных пузырьков в сторону своих плюс-концов (разд. 11.1.10 и 11.4.9). Таким образом, в мигрирующей клетке есть по меньшей мере два типа направленных «движителей», обеспечивающих ее локомоцию: 1) механизм на основе актиновых филаментов в клеточном кортексе - он выдвигает ламеллоподии и создает кортикальное натяжение; и 2) механизм, находящийся в глубине клетки, для которого нужны ориентированные микротрубочки или актиновые филаменты (или те и другие),- он обеспечивает активный транспорт мембранных пузырьков к переднему краю клетки (рис. 11-85).
11.6.7. Общими организаторами цитоскелета могут быть микротрубочки
Помимо участия в движении клеток микротрубочки играют также ключевую роль в определении их формы. Всем эукариотическим клеткам свойственна определенная геометрия, которая проявляется как во внешней структуре клетки, так и в расположении органелл. В то время как все другие компоненты цитоскелета лишь отражают эту геометрию, микротрубочки, по-видимому, часто играют уникальную роль в ее создании. Хорошо известно, например, что микротрубочки обычно располагаются вдоль длинной оси клетки и что во многих случаях их присутствие необходимо для поддержания удлиненной формы клетки в целом.
Как уже упоминалось, микротрубочки определяют положение аппарата Гольджи и эндоплазматического ретикулума в каждой клетке (разд. 11.4.10), а также влияют на распределение промежуточных филаментов, которые спадаются в околоядерную шапку при обработке клетки колхицином (разд. 11.5.3); кроме того, от них может зависеть и распределение актиновых нитей. Сократимое кольцо, которое построено из актиновых филаментов и перетягивает клетку пополам при завершении клеточного деления, всегда образуется в плоскости, перпендикулярной оси митотического веретена. Если образующееся веретено механически сместить, то соответственно изменится и место, где образуется затем сократимое кольцо; значит, положение этого кольца определяется положением веретена (разд. 13.5.13).
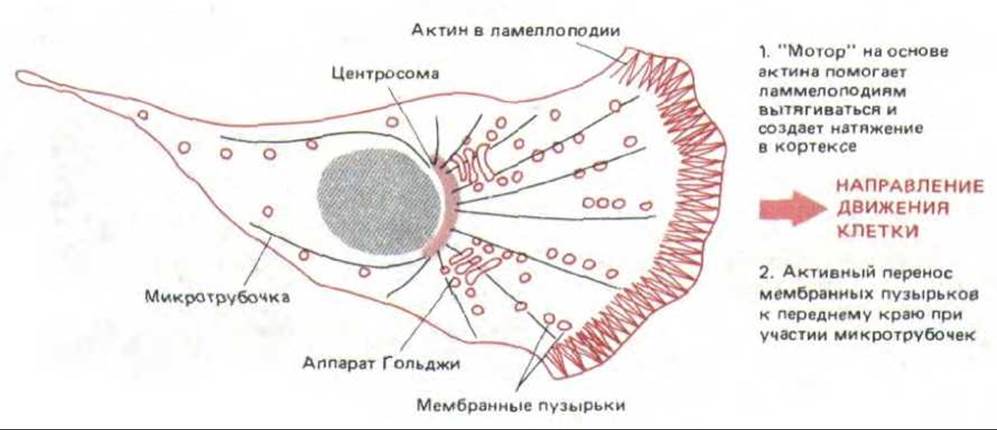
Рис. 11-85. Два направленных «двигателя» в мигрирующей клетке: в основе одного лежат актиновые филаменты кортекса, а другой основан на переносе мембранных пузырьков к переднему краю вдоль микротрубочек (и, возможно, актиновых филаменюв). Вероятно, эти механизмы совместно обеспечивают движение клетки в одном направлении.
Механизмы, с помощью которых микротрубочки влияют на положение актиновых филаментов кортекса и промежуточных филаментов, неизвестны, хотя предположительно в них участвуют белки, образующие связи между белковыми нитями разных типов.
11.6.8. Структурная организация цитоскелета одной клетки может передаваться соседним клеткам [64]
Цитоскелет данной клетки может влиять на цитоскелет ее соседей. Как полагают, этот способ межклеточной коммуникации играет важную роль в определении морфологии тканей и органов. Один из простейших видов взаимодействия между цитоскелетами можно наблюдать, когда передние края двух мигрирующих клеток касаются друг друга. У клеток большинства типов это вызывает немедленный «паралич» переднего края у той и другой клетки - феномен, известный как контактное ингибирование движения. В результате два столкнувшихся in vitro фибробласта перестают вытягивать микрошипы и ламеллоподии в зоне соприкосновения и начинают выпускать их повсюду, кроме этого места, так что постепенно клетки «уходят» друг от друга, меняя направление движения (рис. 11-86). По-видимому, такая реакция связана с быстрыми изменениями в кортикальном актиновом цитоскелете в зоне контакта, но молекулярные механизмы этих изменений не выяснены.
Контактное ингибирование движения не следует смешивать с контактным ингибированием (торможением) клеточного деления; последнее наблюдается у клеток в культуре, которые делятся до тех пор, пока не покроют всю поверхность культуральной чашки. Как мы увидим в гл. 13, остановка роста и пролиферации в этих условиях зависит не только от контакта между клетками; она зависит также от той формы, которую клетки вынуждены принимать в условиях скученности, и от возрастающего дефицита питательных веществ (разд. 13.3.5).
Контактное ингибирование движения играет важную роль в заживлении ран. Пласты эпителиальных клеток на краях раны, вытягивая ламеллоподии, начинают быстро двигаться, стремясь «наползти» на поврежденную поверхность; это движение прекращается, как только клетки различных краев вступают в контакт, закрыв щель раны. Теперь. когда непрерывный пласт клеток восстановлен, между новыми соседями образуются межклеточные соединения, которые становятся точками прикрепления для белковых филаментов, соединяющих цитоскелеты всех клеток пласта (разд. 14.1.2). Контактное ингибирование движения может также способствовать избирательному объединению аксонов в пучки в развивающейся нервной системе: конусы роста центральных нейронов останавливаются и даже втягиваются обратно, если сталкиваются с аксонами нейронов периферической нервной системы, хотя вдоль аксонов других центральных нейронов они продолжают охотно расти.
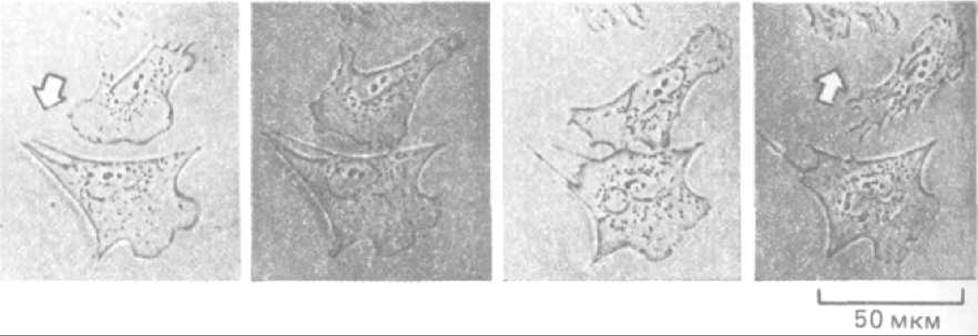
Рис. 11-86. Контактное торможение движения фибробластов. Если два ползущих по поверхности культуральной чашки фибробласта сталкиваются, их ламеллоподии в точке контакта парализуются. Спустя 10-15 мин клетки обычно начинают двигаться в разные стороны друг от друга. (С любезного разрешения Graham Dunn.)
Еще один механизм, с помощью которого цитоскелет одной клетки может оказывать влияние на цитоскелет ее соседей, обусловлен взаимодействием между цитоскелетом и секретируемым клеткой внеклеточным матриксом. Как выяснилось (см. гл. 14), клетка с ориентированным цитоскелетом нередко образует сходным образом ориентированный внеклеточный матрикс, а это в свою очередь влияет на ориентацию цитоскелетов в других клетках, соприкасающихся с таким матриксом (см. рис. 14-84). Так благодаря межклеточным взаимодействиям через места соединения клеток и внеклеточный матрикс организация цитоскелета отдельной клетки часто определяется не автономно самой этой клеткой, а организацией ткани в целом.
11.6.9. В основе изгибания эпителиальных слоев у зародыша лежат координированные сокращения цитоскелета [65]
Взаимодействие между цитоскелетами соседних клеток лежит в основе изгибания клеточных пластов - одного из фундаментальных морфогенетических процессов у животных. Как реализуется это взаимодействие? Возможно, оно передается с помощью механических стимулов, передающихся от клетки к клетке. Представьте себе, например, слой эпителиальных клеток, в которых кратковременное натяжение всего слоя ведет к сокращению апикальных пучков актиновых филаментов, расположенных в опоясывающих десмосомах (разд. 14.1.3). Если в одной клетке такой пучок сократится, то в соседних с ней клетках возникнет натяжение, которое может заставить сократиться аналогичные структуры и в этих клетках, и тогда волна сокращения распространится по всему клеточному пласту. Созданные на основе этого простого механизма компьютерные модели дают большое разнообразие конечных форм, зависящих от первоначальной геометрии пласта. Например, слой эпителиальных клеток, окружающих сферическую полость, будет впячиваться, образуя двуслойную структуру, что весьма напоминает гаструляцию у зародышей морского ежа (рис. 11-87).
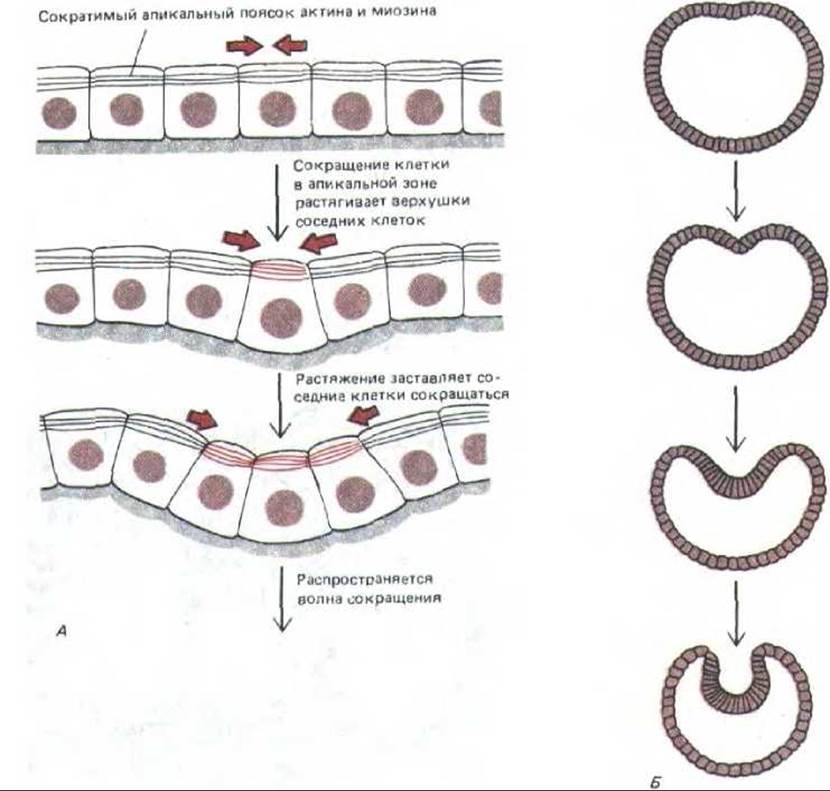
Рис. 11-87. Компьютерная модель гаструляции, в основу которой положена волна сокращений цитоскелета, распространяющаяся от клетки к клетке. Каждая клетка эпителиального пласта имеет опоясывающую десмосому (межклеточное соединение с сократительным пучком актиновых филаментов, который, как было постулировано, сокращается в ответ на растяжение). А так как опоясывающая десмосома расположена в апикальном конце клетки, сокращение изменяет форму последней с цилиндрической на коническую. В пласте, состоящем из соприкасающихся клеток, сокращение одной из них будет растягивать соседние, заставляя их в ответ тоже сокращаться (А). Если такой принцип будет действовать в сферическом или цилиндрическом слое клеток, это приведет к инвагинации (Б). Точная геометрическая форма этой инвагинации будет зависеть от механических свойств модельной системы клеток; система, представленная справа (Б), рассчитана на моделирование гаструляции у эмбриона морского ежа. (G. Odell st al., Dev. Biol. 85: 446-462, 1981.)
Хотя эти модели полностью умозрительны, нет сомнений, что цитоскелет играет фундаментальную роль в формообразовании тканей. Сложная форма и организация клеток в тканях и органах позвоночных зависит от белков цитоскелета в их разнообразных структурных сочетаниях. Часто тем элементом, который, видимо, управляет морфогенетическими движениями, бывают микротрубочки. В других случаях ведущую роль играют актиновые филаменты, как, например, при развитии волосковых клеток в ухе позвоночных.
11.6.10. Развитие волосковых клеток в улитке внутреннего уха зависит от точного контроля полимеризации актина [66]
Волосковые клетки - это специализированные эпителиальные клетки, находящиеся в улитке и преддверии внутреннего уха. Эти клетки чрезвычайно чувствительны к малейшему движению, будь то вибрация, вызываемая звуковыми волнами, или перемещение жидкости в полукружных каналах при изменении положения головы. Эти движения детектируются с помощью пучков стереоцилий, расположенных на поверхности каждой волосковой клетки в гексагональном порядке; в каждом таком пучке стереоцилий расположены рядами «по росту», подобно трубам органа (рис. 11-88). Едва заметные колебания стереоцилий, вызываемые звуками, преобразуются в волосковой клетке в электрические сигналы, которые затем передаются в мозг (разд. 19.6.2).
Тонкость структурной организации стереоцилий выражается не только в их строго упорядоченном расположении на поверхности волосковой клетки, но и в закономерном изменении их размеров, числа и ориентации от одного конца улитки к другому. У кур каждая волосковая клетка на проксимальном конце улитки несет более 250 стереоцилий со средней длиной 1,7 мкм, тогда как на противоположном конце каждая клетка имеет только 50 стереоцилий, средняя длина которых 5,2 мкм. Эти и другие градации в структуре отражают функциональную организацию волосковых клеток, которые «настроены» в одном конце улитки на низкие частоты, а в другом - на высокие. Размеры пучка стереоцилий на любой клетке удивительно точны и воспроизводимы - их можно использовать как надежный признак локализации клетки в определенном месте между двумя концами улитки.
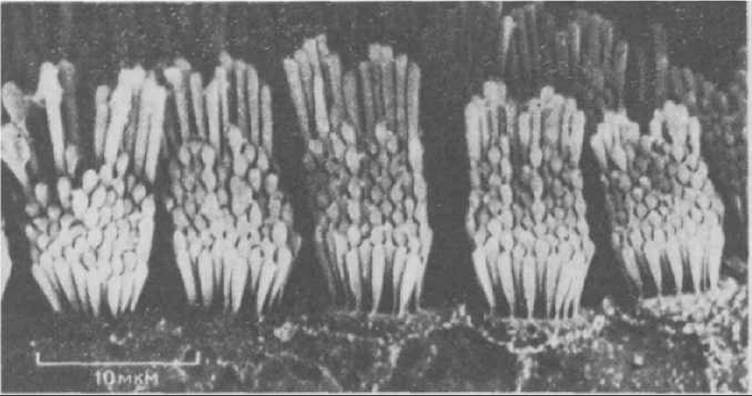
Рис. 11-88. Стереоцилий расположены на поверхности волосковых клеток наподобие органных труб. Микрофотография получена с помощью сканирующего электронного микроскопа. (С любезного разрешения Lewis Tilney.)
Стереоцилий - это очень крупные специализированные микроворсинки, не имеющие никакого отношения к настоящим ресничкам (цилиям). Они образуются как выпячивания плазматической мембраны и содержат пучок актиновых филаментов (рис. 11-89). Таким образом, формирование улитки четко демонстрирует способность клеток контролировать число, местоположение и длину актиновых филаментов совершенно определенным образом во всем пространстве ткани.
С помощью сканирующего электронного микроскопа можно увидеть, что у куриного эмбриона рост стереоцилий проходит три раздельные стадии (рис. 11-90). Сначала более или менее одновременно на поверхности каждой волосковой клетки появляются коротенькие стереоцилий. Затем они начинают удлиняться; первыми удлиняются те, которые будут в зрелом пучке самыми длинными, затем — будущие «вторые по росту» и т.д. Начав расти, стереоцилии данного ряда продолжают удлиняться с постоянной малой скоростью (около 0,5 мкм в день), по- видимому, за счет присоединения мономеров актина на дистальном конце (плюс-конце, см. разд. 11.2.10) каждого актигнового филамента. Через три-четыре дня такого равномерного роста на поверхности каждой волосковой клетки образуется нечто вроде подстриженного газона из небольших стереоцилии.

Рис. 11-89. Сравнение размеров типичной стереоцилий и типичней микроворсинки; структура той и другой поддерживается находящимся внутри пучком актиновых филаментов.
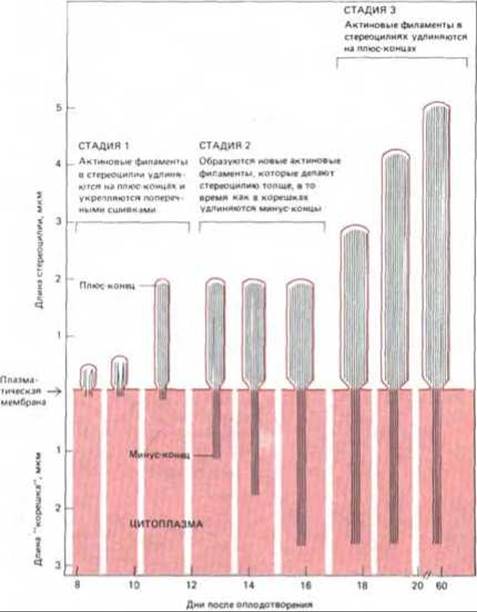
Рис. 11-90. Три стадии роста единичной стереоцилий в улитке уха цыпленка. Все стереоцилий проходят в своем развитии одни и те же три стадии, но время начала и продолжительность роста варьируют как у отдельных стереоцилий одной волосковой клетки, так и от клетки к клетке. Таким образом создается весьма точная ступенчатая градация длин стереоцилий. Цыплята вылупляются на 21-й день. (Из L.C. Tilney, M. S. Tilney, Hearing Research 22: 55-77, 1986.)
В течение следующих шести дней присоединение мономеров актина происходит, видимо, только в основании стереоцилии, так что активные филаменты растут своими «корешками», уходящими в кортекс волосковых клеток. На этой стадии рост, очевидно, происходит на минус-концах актиновых филаментов; значит, при необходимости клетка может использовать и этот необычный способ роста. В это же время стереоцилии в определенных участках улитки утолщаются за счет добавления новых актиновых филаментов к их сердцевинным пучкам.
Наконец, на третьей стадии роста (от 17-го дня эмбрионального развития до вылупления) возобновляется присоединение мономеров актина к плюс-концам филаментов в пучках, и стереоцилии вновь начинают удлиняться. Теперь быстрее растут волосковые клетки в дистальном конце улитки; они перестают расти, когда создается градиент длины стереоцилии, присущий взрослой курице.
Механизм, позволяющий клеткам так точно регулировать сборку актиновых филаментов, не известен. Чем столь жестко определяется первоначальное число стереоцилии на поверхности каждой волосковой клетки? Каким образом клетка контролирует конечную длину каждого пучка актиновых филаментов, обеспечивая при этом строгую градацию длин стереоцилии? Это лишь два из множества интригующих вопросов, которые встают перед исследователями цитоскелета.
Заключение
Актиновые филаменты, микротрубочки, промежуточные филаменты и связанные с ними белки способны к самопроизвольной сборке в сложную сеть белковых нитей, структурирующих цитоплазму. Цитоскелет играет ведущую роль в определении формы и полярности клеток, а также в их подвижности. Когда животная клетка движется, пучок актиновых филаментов периодически «выталкивает» наружу ламеллоподии и микрошипы на одной из сторон клетки (переднем крае) и растягивает клеточный кортекс, поляризуя клетку, что помогает ей продвигаться вперед. Эта полярность поддерживается с помощью микротрубочек или актиновых филаментов, которые направляют поток материала плазматической мембраны к переднему краю клетки.
Цитоскелет одной клетки может влиять на цитоскелет ее соседей как через межклеточные соединения, так и опосредованно, через внеклеточный матрикс. Таким способом координируются изменения формы клеток в процессе развития тканей и органов.
Литература
Общая
Bershadsky A.D., Vasiliev J.M. Cytoskeleton. New York. Plenum Press, 1988.
Lackie J. M. Cell Movement and Cell Behaviour. London, Alien and Unvvin, 1985.
Schliwa M. The Cytoskeleton. New York, Springer-Verlag, 1986.
Shcterline P. Mechanisms of Cell Motility. London, Academic Press, 1983.
Цитированная
1. Amos L. A. Structure of muscle filaments studied by electron microscopy. Annu. Rev. Biophys. Biophys. Chem., 14, 291-313, 1985.
Huxley A. F. Reflections on Muscle. Princeton, NJ, Princeton University Press, 1980.
Squire J. M. Muscle: Design, Diversity and Disease. Menlo Park CA, Benjamin-Cummings, 1986.
2. Cooke R. The mechanism of muscle contraction. CRC Crit. Rev. Biochem., 21, 53-118, 1986.
Huxley H, E. The mechanism of muscular contraction. Science, 164, 1356-1366, 1969.
3. Cohen C., Parry D. A. D. a-Helical coiled coils a widespread motif in proteins. Trends Biochem. Sci., 11, 245-248, 1986.
Davis J. S. Assembly processes in vertebrate skeletal thick filament formation. Annu. Rev. Biophys. Biophys. Chem., 17, 217 239, 1988.
4. Bessman S. P., Carpenter C. L. The creatine-creatine phosphate energy shuttle. Annu. Rev. Biochem., 54, 831-862, 1985.
5. Warrick H.M., Spudich J.A. Myosin structure and function in cell motility. Annu. Rev. Cell Biol., 3, 379-421, 1987.
6. Pollard Т.О., Cooper J.A. Actin and actin-binding proteins. A critical evaluation of mechanisms and functions. Annu. Rev. Biochem., 55, 987-1035, 1986.
7. Irring M. Muscle mechanics and probes of the crossbridge cycle. In: Fibrous Protein Structure (J. M. Squire, P. J. Vibert, eds.). San Diego, CA, Academic Press, 1987.
Pollard Т.О. The myosin crossbridge problem. Cell, 48, 909, 910, 1987.
8. Katz B. Nerve, Muscle and Synapse. New York, MaGraw-Hill, 1966. [Имеется перевод: Катц Б. Нерв, мышца и синапс. М.: Мир, 1969].
LaiF. A., Erickson H.P., Rousseau Е., Liu O.-Y., Meissner G. Purification and reconstruction of the calcium release channel from skeletal muscle. Nature, 331, 315-319, 1988.
Saito A., Inui M., Radermacher M., Frank J., Fleischer S. Ultrastructure of the calcium release channel of sarcoplasmatic reticulum. J. Cell Biol., 107, 211 219, 1988.
9. Murray J. M., Weber A. The cooperative action of muscle proteins. Sci. Am., 230(2), 59-71, 1974.
Phillips G. N., Fillers J. P., Cohen C. Tropomyosin crystal structure and muscle regulation. J. Мої. Biol., 192, 111-131, 1986.
Zot A.S., Potter J. D. Structural aspects of troponin-tropomyosin regulation of skeletal muscle contraction. Annu. Rev. Biophys. Chem., 16, 535-559, 1987.
10. Wang K. Sarcomere-associated cytoskeletal lattices in striated muscle. Review and hypothesis. In: Cell and Muscle Motility (J.W. Shay, ed.). Vol. 6, pp. 315-369. New York, Plenum Press, 1985.
11. Fawcett D.W. A Textbook of Histology, llth ed. Philadelphia, Saunders, 1986.
12. Korn E.D., Hammer J.A. Myosins of nonmuscle cells. Annu. Rev. Biophys. Biophys. Chem., 17, 23-45, 1988.
Sellers J. R., Adelstein R. S. Regulation of contractile activity. In: The Enzymes (P. Bover, E.G. Krebs, ed), Vol. 18, pp. 381-418. San Diego, CA, Academic Press, 1987.
13. Citi S., Kendrick-Jones J. Regulation of non-muscle myosin structure and function. Bioessays, 7, 155- 159, 1987.
14. ByersH.R., Fujiwara K. Stress fibers in cells in situ: immunofluorescence visualization with anti-actin, anti-myosin and anti-alpha-actinin. J. Cell Biol., 93, 804-811, 1982.
Langanger B. et al. The molecular organization of myosin in stress fibers of cultured cells. J. Cell Biol., 102, 200-209, 1986.
Schroeder Т.Е. Actin in dividing cells: contractile ring filaments bind heavy meromyosin. Proc. Natl. Acad. Sci. USA, 70, 1688-1692, 1973.
15. Buckingham M.E. Actin and myosin multigene families: their expression during the formation of skeletal muscle. Essays Biochem., 20, 77-109, 1985.
Emerson C. P., Bernstein S. I. Molecular genetics of myosin. Annu. Rev. Biochem., 56, 695-726, 1987.
Otey C.A., Kalnoski M.H., Bulinski J.C. Identification and quantification of actin isoforms in vertebrate cells and tissues. J. Cell. Biochem., 34, 113-124, 1987.
16. Breitbart R.E., Andreadis A., Nadal-Ginard B. Alternative splicing: a ubiquitous mechanism for the generation of multiple protein isoforms from single genes. Annu. Rev. Biochem., 56, 467-495, 1987.
17. Bray D., Heath J., Moss D. The membrane-associated "cortex" of animal cells: its structure and mechanical properties. J. Cell Sci. Suppl. 4, 71-88, 1986.
Korn Е. D. Actin polymerization and its regulation by proteins from nonmuscle cells. Physiol. Rev., 62, 672-737, 1982.
Pollard Т.О., Cooper J. A. Actin and actin-binding proteins. A critical evaluation of mechanisms and functions. Annu. Rev. Biochem., 55, 9871035, 1986.
Tilney L. G. Interactions between actin filaments and membranes give spatial organization to cells. In: Modern Cell Biology, Vol. 2. Spatial Organization of Eukaryotic Cells (J. R. Mclntosh, В. Н. Satir esdl.) pp. 163-199. New York: Liss, 1983.
18. Sato M., Schwartz W.H., Pollard Т.О. Dependence of the mechanical properties of actin/alpha-actinin gels on deformation rate. Nature, 325, 828-830, 1987.
Stossel T. P. et el. Non-muscle actin binding proteins. Annu. Rev. Cell Biol., 1, 353-402, 1985.
19. Matsudaira P., Janmev P. Pieces in the actin-severing protein puzzle. Cell, 54, 139-140, 1988.
Yin H. L. Gelsolin: calcium and polyphosphoinositide-regulated actin modulating protein. Bioessays, 7, 176 179, 1987.
20. Korn E. D., Hammer J. A. Myosins of nonmuscle cells. Annu. Rev. Biophys. Biophys. Chem., 17, 23-45, 1988.
Warrick H.M., Spudlich J.A. Myosin structure and function in cell motility. Annu. Rev. Cell Biol., 3, 379-421, 1987.
21. Adams R. J., Pollard T.D. Propulsion of organelles isolated from Acanthamoeha along actin filaments by myosin-I. Nature, 322, 754 756, 1986.
Sheetz M. P., Spudich J. A. Movement of myosin-coated fluorescent beads on actin cables in vitro. Nature, 303, 31-35, 1983.
22. Bennett V. The membrane skeleton of human erythrocytes and its implications for more complex cells. Annu. Rev. Biochem., 54, 273-304, 1985.
23. Conzelman K.A., Mooseker M.S. The 110-kD protein-calmodulin complex of the intestinal microvillus in an actin-activated MgATPase. J. Cell Biol., 105, 313-324, 1987.
Mooseker M. S. Organization, chemistry, and assembly of the cytoskeletal apparatus of the intestinal brush border. Annu. Rev. Cell. Biol., 1, 209-241, 1985.
24. Burridae K. et al. Focal adhesions: transmembrane junctions between the extracellular matrix and cytoskleton. Annu. Rev. Cell Biol., 4, 487-525, 1988.
Horwitz A., Duyaan K., Buck C., Beckerle M.C., Bur ridge K. Interaction of plasma membrane fibronectin receptor with talin-a transmembrane linkage. Nature, 320, 531-533, 1986.
25. Bonder E. M., Fishkind D.J., Mooseker M.S. Direct measurement of critical concentrations and assembly rate constants at the two ends of an actin filament. Cell, 34, 491-501, 1983.
Korn E.D., Carlier M.-F., Pantaloni D. Actin polymerization and ATP hydrolysis. Science, 238, 638-644, 1987.
26. Abercrombie M. The crawling movement of metazoan cells. Proc. R. Soc. Lond. (Biol.), 207, 129-147, 1980.
Small J. V., Rinnerthaler G., Hinssen H. Organization of actin meshworks in cultured cells: the leading edge. Cold Spring Harbor Symp. Quant. Biol., 46, 599-611, 1982.
Wany Y. Exhange of actin subunits at the leading adge of living fibroblasts: possible role of treadmiling. J. Cell Biol., 101, 597 602, 1985.
27. Tilney L. G., Inoue S. Acrosomal reaction of Thyone sperm. II. The kinetics and possible mechanism of acrosomal process elongation. J. Cell Biol., 93, 820-827, 1982.
28. Carson M., Weber A., Zigmond S. H. An actin-nucleating activity in poly-morphonuclear leukocytes is modulated by chcrnotactic peptides, J. Cell Biol., 103, 2707-2714, 1986.
Devreotes P., Zigmond S. Chemotaxis in eukaryotic cells. Annu. Rev. Cell Biol., 4, 649-686, 1988.
Tilney L. G., Bonder E. M., DeRosier D.J. Actin filaments elongate from their membrane-associated ends. J. Cell Biol., 90, 485-494, 1981.
29. Cooper J.A. Effects of cytochalasin and phalloidin on actin. J. Cell Biol., 105, 1473-1478, 1987.
30. Dustin P. Microtubules, 2nd ed., pp. 127-164. New York, Springer-Verlag, 1984.
Gibbons I.R. Cilia and flagella of eukaryotes. J. Cell Biol., 91, 107s-124s, 1981.
Roberts K., Hyams J.S., eds. Microtubules. New York. Academic Press, 1979. Satir P. How cilia move. Sci. Am., 231(4), 44-63, 1974.
31. Amos L. A., Baker T.S. The three dimensional structure of tubulin protofilaments. Nature, 279, 607-612, 1979.
Mandelkow E.-M., Schultheiss R., Rapp R., Muller M., Mandelkow E. On the surface lattice of microtubules: helix starts, protofilament number, seam and handedness. J. Cell Biol., 102, 1067-1073, 1986.
Raff E.C. Genetics of microtubule systems. J. Cell Biol., 99, 1-10, 1984.
Sulivan К. F. Structure and utilization of tubulin isotypes. Annu. Rev. Cell Biol., 4, 687-716, 1988.
32. Linek R. W., Amos W. B. Localization of tektin filaments in microtubules of sea urchin sperm flagella by immunoelectron microscopy, J. Cell Biol., 100, 126-135, 1985.
33. Goodenough U. W., Heuser J. E. Substructure of inner dynein arms, radial spokes, and the central pair/projection complex of cilia and flagella.
J. Cell Biol., 100, 2008 2018, 1985.
34. Summers K. E., Gibbons 1. R. ATP-induced sliding of tubules in trypsin-treated flagella of sea urchin sperm. Proc. Natl. Acad. Sci. UDA, 68, 3092-3096, 1971. Warner F. D., Satir P. The structural basis of ciliary bend formation. J. Cell Biol., 63, 35-63, 1974.
35. Johnson K. A. Pathway of the microtubule-dynein ATPase and structure of dynein: a comparison with actomyosin. Annu. Rev. Biophys. Biophys. Chem., 14, 161-188, 1985.
36. Brokaw C.J. Future directions for studies of mechanisms for generating flagellar bending waves. J. Cell Sci., Suppl. 4, 103 113, 1986.
Brokaw C. J., Luck D. J. L., Huang B. Analysis of the movement of Chlamydomonas flagella: the function of the radial-spoke system is revealed by comparison of wild-type and mutant flagella. J. Cell Biol., 92, 722-732, 1982.
37. Afzelius B. A. The immotile-cilia syndrome: a microtubule-associated defect. CRC Crit. Rev. Biochem., 19, 63-87, 1985.
Huang B. Chlanydomonas reinhardtii: a model system for genetic analysis of flagellar structure and motility. Int. Rev. Cytol., 99, 181 215, 1986.
Luck D. J. L. Genetic and biochemical dissection of the eucaryotic flagellum. J. Cell Biol., 98, 789 794, 1984.
38. Lefebvre P. A., Rosenbaum J. L. Regulation of the synthesis and assembly of ciliary and flagellar proteins during regeneration. Annu. Rev. Cell Biol., 2, 517-546, 1986.
Wheatley D. N. The Centriole: A Central Enigma of Cell Biology. New York, Elsevier, 1982.
39. Karsenti E., Мого В. Centrosomes and the spatial distribution of microtubules in animal cells. Trends Biochem. Sci., 11, 460-463, 1986. Ramanis Z., Luck D. J. L. Loci affecting flagellar assembly and function map to an unusual linkage group in Chlamydomonas reinhardtii. Proc. Natl. Acad. Sci. USA, 83, 423 436, 1986.
Vorobjev LA., Chentsov Y.S. Centrioles in the cell cycle. 1. Epithelial cells. J. Cell Biol., 93, 938 949, 1982.
40. Dustin P. Microtubules, 2nd ed. Berlin, Springer-Verlag, 1984.
41. De Brabander M. et al. Microtubule dynamics during the cell cycle: the effects of taxol and nocodazole on the microtubule system of Ptk2 cells at different stages of the mitotic cycle. Int. Rev. Cytol., 101, 215-274, 1986.
Inoue S. Cell division and the mitotic spindle. J. Cell Biol., 91, 13Is-147s, 1981.
Salmon E. D., McKeel M., Hays T. Rapid rate of tubulin dissociation from microtubules in the mitotic spindle in vivo measured by blocking polymerization with colchicine. J. Cell Biol., 99, 1066-1075, 1984.
42. Farrell K. W., Jordan M.A., Miller H.P., Wilson L. Phase dynamics at microtubule ends: the coexistence of microtubule length changes and treadmilling. J. Cell Biol., 104, 1035-1046, 1987.
Mclntosh J. R., Euteneuer U. Tubulin hooks as probes for microtubule polarity: an analysis of the method and evaluation of data on microtubule polarity in the mitotic spindle. J. Cell Biol., 98, 525 533, 1984.
43. Carlier M.-F. Role of nucleotide hydrolysis in the polymerization of actin and tubulin. Cell Biophys., 12, 105-117, 1988.
Horio H. Hotani H. Visualization of the dynamic instability of individual microtubules by dark field microscopy. Nature, 321, 605-607, 1986. Mitchison Т., Kirschner M. Dynamic instability of microtubule growth. Nature, 312, 237-342, 1984.
44. Karsenti E., Maro B. Centrosomes and the spatial distribution of microtubules in animal cells. Trends Biochem. Sci., 11, 460-463, 1986. Mitchison Т., Kirschner M. Microtubule assembly nucleated by isolated Centrosomes. Nature, 312, 232-237, 1984.
45. Kirschner M., Mitchison T. Beyond self-assembly: from microtubules to morphogenesis. Cell, 45, 329-342, 1986.
Sammak P. J., Borisy G. G. Direct observation of microtubule dynamics in living cells. Nature, 332, 724-726, 1988.
46. Barra H. S., Arce C. A., Argarana С. Е. Posttranslational tyrosination and detyrosination of tubulin. Molec. Neurobiol., 2, 133-153, 1988. Gundersen G. G., Khawja S., Bulinski J. C. Postpolymerization detyrosination of [a]-tubulin: a mechanism for subcellular differentiation of microtubules. J. Cell Biol., 105, 251-264, 1987.
Maruta Н., Greer К., Rosenbaum J. L. The acetylation of a-tubulin and its relationships to the assembly and disassembly of microtubules. J. Cell Biol., 103, 571-579, 1986.
Schulze E., Asai D. J., Bulinski J. C., Kirschner M. Post-translational modification and microtubule stability. J. Cell Biol., 105, 2167-2177, 1987.
47. Olmstcd J. B. Microtubule-associated proteins. Annu. Rev. Cell Biol., 2, 421-457, 1986.
Vallee R.B., Bloom G. S., Theurkauf W. E. Microtutbule-associated proteins: subunits of the cytomatrix. J. Cell Biol., 99, 38s-44s, 1984.
48. Alien R.D. The microtubule as an intracellular engine. Sci. Am., 256(2), 42-49, 1987.
Alien R.D. ct al. Gliding movement of and bidirectional transport along single native microtubules from squid axoplasm: evidence for an active role of microtubules in cytoplasmic transport. J. Cell Biol., 100, 1736 1752, 1985.
49. Vale R. Intracellular transport using microtubule-based motors. Annu. Rev. Cell Biol., 3, 347-378, 1987.
Vale R.D., Reese T.S., Sheetz M.P. Identification of a novel force-generating protein, kinesin, involved in microtubule-based motility. Cell, 42, 39 50, 1985.
Vallee R. В., Wall J. S., Paschal B. M., Shpetner H. S. Microtubule-associated protein 1C from brain is a two-headed cytosolic dynein. Nature, 332, 561 563, 1988.
50. Allan V.J., Kreis Т.Е. A microtubule-binding protein associated with membranes of the Golgi apparatus. J. Cell Biol., 103, 2229-2239, 1986. Dabora S. L., Sheet- M. P. The microtubule-dependent formation of a tubulovesicular network with characteristics of the ER from cultured cell extracts. Cell, 54, 27-35, 1988.
Lee C., Chen L. B. Dynamic behavior of endoplasmic reticulum in living cells. Cell, 54, 37-46, 1988.
Lucocq J. M., Warren G. Fragmentation and partitioning of the Golgi apparatus during mitosis in HeLa cells. EMBO J., 6, 3239-3246, 1987.
51. Geiger B. Intermediate filaments: looking for a function. Nature, 329, 392-393, 1987. Steinert P. M., Roop D. R. Molecular and cellular biology of intermediate filaments. Annu. Rev. Biochem., 57, 593-626, 1988.
Traub P. Intermediate Filaments: A Review. New York, Springer-Verlag, 1985. Wang E., Fischman D., Liem B.K.H., Sun T.-T., eds. Intermediate Filaments. Ann. N.Y. Acad. Sci., 455, 1985.
52. Osborn M., Weber K. Tumor diagnosis by intermediate filament typing: a novel tool for surgical pathology. Lab. Invest., 48, 372-394, 1983.
53. Ip W., Hartzer M. K., Pang S. Y.-Y., Robson R. M. Assembly of vimentin in vitro and its implications concerning the structure of intermediate filaments. J. Mol. Biol., 183, 365-375, 1985.
Quintan R. A. ct al. Characterization of dimer subunits of intermediate filament proteins. J. Mol. Biol., 192, 337-349, 1986.
54. Geuens G., De Brabander M., Nuydens R., De Mey J. The interaction between microtubules and intermediate filaments in cultured cells treated with taxol and nocodazole. Cell Biol. Int. Rep., 7, 35-47, 1983.
Goldman R. et al. Intermediate filaments: possible functions as cytoskeletal connecting links between the nucleus and the cell surface. Ann. N. Y. Acad. Sci., 45, 1-17, 1985.
55. Geisler N., Weber K. Phosphorylation of desmin in vitro inhibits formation of intermediate filaments: identification of three kinase A sites in the aminoterminal head domain. EMBO J., 7, 15 20, 1988.
Inagaki M., Nishi Y., Nishizawa K., Matsuyama M., Sato C. Site-specific phosphorylation induces disassembly of vimentin filaments in vitro. Nature, 328, 649 652, 1987.
56. Aebi U., Cohn J., Buhle L., Gerace L. The nuclear lamina is a meshwork of intermediate-type filaments. Nature, 323, 560-564, 1986.
McKeon F.D., Kirschner M. W., Caput D. Homologies in both primary and secondary structure between nuclear envelope and intermediate filament proteins. Nature, 319, 463-468, 1986.
57. Abercrombie M. The crawling movement of metazoan cells. Proc. R. Soc. Lond. (Biol.), 207, 129-147, 1980.
Bridgman P. Structure of cytoplasm as revealed by modern electron microscopy techniques. Trends Neurosci., 10, 321-325, 1987.
Singer S. J., Kupfer A. The directed migration of eukaryotic cells. Annu. Rev. Cell Biol., 2, 337-365, 1986.
Trinkaus J. P. Cells into Organs: The Forces that Shape the Embryo. 2nd ed. Englewood Clifis, NJ, Prentice-Hall, 1984.
58. Bridgman P. C., Reese T. S. The structure of cytoplasm in directly frozen cultured cells. 1. Filamentous meshworks and the cytoplasmic ground substance. J. Cell Biol., 99, 1655-1668, 1984.
Heuser J., Kirschner M. W. Filament organization revealed in platinum replicas of freeze-dried cytoskeletons. J. Cell Biol., 86, 212-234, 1980.
59. Fulton A.B. How crowded is the cytoplasm? Cell, 30, 345-347, 1982.
Luby-Phelps K., Taylor D. L., Lanni F. Probing the structure of the cytoplasm. J. Cell Biol., 102, 2015-2022, 1986.
60. Kolega J. Effects of mechanical tension on protrusive activity and microfilament and intermediate filament organization in an epidermal epithelium moving in culture. J. Cell Biol., 102, 1400 1411, 1986.
Trinkam J. P. Cells into Organs: The Forces That Shape the Embryo, 2nd ed., pp. 157 244. Englewood Cliffs, NJ. Prentice-Hall, 1984.
61. Bray D., Hollcnbeck P.J. Growth cone motility and guidance. Annu. Rev. Cell Biol., 4, 43-62, 1988.
Euteneuer U., Schliwa M. Persistent, directional motility of cells and cytoplasmic fragments in the absence of microtubules. Nature, 310, 5861, 1984.
Malawista S. E., De Boisfleury Chevance A. The cytokinetoplast: purified, stabile, and functional motile machinery from human blood polymorphonuclear leukocytes. J. Cell Biol., 95, 960-973, 1982.
Marsh L., Letourneau P. C. Growth of neurites without filopodial or lamellipodial activity in the presence of cytochalasin B. J. Cell Biol., 99, 2041-2047, 1084.
Vasiliev J. M. et at. Effect of colcemid on the locomotion of fibroblasts. J. Embryol. Exp. Morphol., 24, 625-640, 1970.
62. Bray D., White J.G. Cortical flow in animal cells. Science, 239, 883-888, 1988.
De Lozannc A., Spudich J.A. Disruption of the Dictyostelium myosin heavy chain gene by homologous recombination. Science, 236, 10861091, 1987.
Knecht D. A., Loomis W. F. Antisense RNA inactivation of myosin heavy chain gene expression in Dictyostelium discoideum. Science, 236, 1081 1086, 1987.
63. Bergmann J.E., Kupfer A., Singer S.J. Membrane insertion at the leading edge of motile fibroblasts. Proc. Natl. Acad. Sci., USA, 80, 1367-1371, 1983.
Bretscher M.S. How animal cells move. Sci. Am., 257(6), 72 90, 1987.
64. Lackie J.M. Cell Movement and Cell Behaviour, pp. 253-275. London, Alien and Unwin, 1986.
Trinkaus J. P. Cells into Organs: The Forces That Shape the Embryo, 2nd ed., pp. 157 244. Englewood Cliffs, NJ. Prentice-Hall, 1984.
65. Ode/I G. M., Oster G., Alberch P., Burnside B. The mechanical basis of morphogenesis. 1. Epithelial folding and invagination. Dev. Biol., 85, 446-462, 1981.
66. Tilncy L. G., Tilney M. S., Cotanche D. A. Aclin filaments, stereocilia, and hair cells of the cochlea. V. How the staircase pattern of stereociliary lengths in generated. J. Cell Biol., 106, 355-365, 1988.
Tilney L. G., De Rosier D. J. Actin filaments, stereocilia, and hair cells of the bird cochlea. IV. How the actin filaments become organized in developing stereocilia and in the cuticular plate. Dev. Biol., 116, 119-129, 1986.