Молекулярная биология клетки - Том 2 - Албертс Б., Брей Д., Льюис Дж., Рэфф М., Робертс К., Уотсон Дж. 1993
Рост и деление клеток
Гены «социального контроля» клеточного деления
Как мы видели на примере дрожжей, генетика располагает большими возможностями для выяснения молекулярных основ регуляции клеточного деления, если имеются способы отбора мутаций соответствующих генов. У многоклеточных животных мутации генов, непосредственно участвующих в «социальном контроле» клеточного деления (мы будем называть их генами социального контроля), выделять нетрудно. Клетка, содержащая одну или несколько таких мутаций, будет продолжать делиться, игнорируя нужды организма как целого, и ее потомство образует макроскопически видимую опухоль.
Раковые опухоли - по определению злокачественные, т. е. их клетки не только делятся неконтролируемым образом, но и проникают в другие ткани, где появляются многочисленные вторичные опухоли, или метастазы. Для возникновения рака необходимо, чтобы в клетке сначала произошел ряд мутаций, освобождающих ее от воздействия различных регуляторов клеточного деления, а затем накопились дальнейшие изменения, делающие ее способной к инвазии и метастазированию. Эти аспекты рака будут обсуждаться в гл. 21. Здесь же мы не будем пытаться объяснить природу рака, а посмотрим, что можно узнать при изучении раковых клеток относительно тех генов, которые в норме контролируют клеточное деление.
13.4.1. Трансформация клетки в культуре позволяет выявлять гены, участвующие в социальном контроле клеточного деления
Как можно выявить мутантный ген (или гены), если имеется клон опухолевых клеток, возникший предположительно в результате мутации? Классические методы картирования генов здесь неприменимы, так как клетки не размножаются половым путем. Более прямой подход состоит в выделении генетического материала из опухолевых клеток и поиске таких его фрагментов, которые при введении в нормальные клетки вызвали бы у них поведение, сходное с поведением опухолевых клеток. Методы решения столь сложной задачи были впервые разработаны только в конце 1970-х гг., но основой для этого послужили более ранние исследования, касавшиеся очень сходных естественных явлений.
Некоторые виды опухолей вызываются вирусами. Выделенные из них вирусы инфицируют нормальные клетки и, внося в них свою РНК или. ДНК, трансформируют эти клетки в опухолевые. Первым из таких опухолеродных (онкогенных) вирусов был вирус саркомы Рауса, вызывающий соединительнотканные опухоли (саркомы) у птиц. Он стал важным объектом исследований, так же как и ряд других онкогенных вирусов, открытых позже.
Природу опухолевой трансформации легче всего изучать на клеточных культурах. Через несколько дней после добавления онкогенного вируса в культуре появляются небольшие колонии аномально пролиферирующих клеток. Каждая такая колония является клоном, происшедшим от одной клетки, инфицированной вирусом и включившей в свой геном вирусный генетический материал. Будучи избавлены от социального контроля клеточного деления, трансформированные клетки растут в культуральной чашке, как и в организме, быстрее нормальных клеток, и поэтому их легко выделить. У трансформированных клеток нередко обнаруживается целый комплекс аномалий (табл. 13-2): у них отсутствует контактное торможение клеточного деления (разд. 13.3.5) - вместо этого они наслаиваются друг на друга по мере роста культуры (рис. 13-31); для роста им часто не требуется прикрепление, и они способны делиться даже в суспензии; им свойственна более округленная форма, напоминающая форму нормальных клеток в митозе, и слабая адгезия к субстрату и друг к другу; они способны делиться даже в отсутствие факторов роста; они бессмертны и не подвержены старению в культуре; и наконец, если их инъецировать в организм подходящего хозяина, они могут давать начало опухолям.
Таблица 13-2. Некоторые изменения, часто наблюдаемые при трансформации нормальных клеток в культуре онкогенным вирусом
|
1. Аномалии, связанные с плазматической мембраной A. Усиленный транспорт метаболитов Б. Избыточное образование пузыревидных выступов B. Повышенная подвижность белков мембраны |
|
2. Изменения в механизмах адгезии A. Ослабленное прилипание к поверхностям; в результате клетки могут оставаться округленными Б. Актиновые филаменты не организуются в стрессовые волокна B. Уменьшение наружной каймы из фибронектина Г. Повышенная выработка активатора плазминогена, приводящая к усиленному внеклеточному протеолизу |
|
3. Аномалии роста и деления A. Рост до необычной плотности клеточной популяции Б. Пониженная потребность в факторах роста B. Меньшая зависимость от прикрепления (клетки могут расти, даже не прикрепившись к твердой поверхности) Г. «Бессмертие» (клетки способны делиться неопределенно долго) Д. Клетки могут вызывать образование опухолей при введении восприимчивым животным |
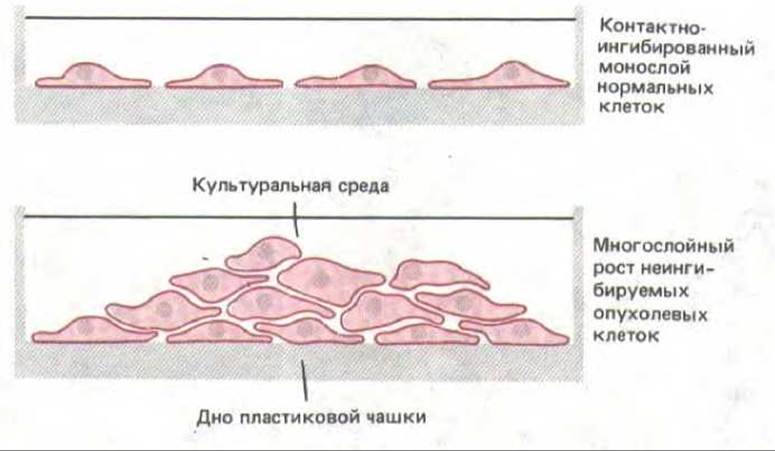
Рис. 13-31. Раковые клетки в отличие от большинства нормальных клеток продолжают расти и наползают друг на друга, после того как образуют непрерывный монослой.
13-20
13.4.2. Опухолеродные вирусы служат источником легко клонируемых онкогенов [28]
Опухолевый вирус разрушает нормальный контроль клеточного деления, необратимо изменяя генетическую конституцию клетки- хозяина; в результате этого клетка начинает вырабатывать белок, не подверженный воздействию нормальных регуляторных механизмов. Поэтому такие вирусы дают возможность выявлять механизмы, ответственные в норме за контроль клеточного деления. До сих пор наиболее важные результаты были получены при изучении РНК-содержащих опухолевых вирусов, называемых также ретровирусами. После заражения клетки ретровирусом на его РНК путем обратной транскрипции синтезируется ДНК, которая затем включается в геном клетки-хозяина. Жизненный цикл ретровируса представлен на рис. 5-75.
Когда ретровирус трансформирует нормальную клетку в опухолевую, аномальное поведение часто бывает обусловлено геном, который (привнесен вирусом, но для выживания и репродукции самого вируса фактически не нужен. Впервые это выяснилось, когда были открыты мутанты вируса саркомы Рауса, способные нормально размножаться, но не трансформирующие клетку. Оказалось, что некоторые из этих нетрансформирующих мутантов не имеют гена (или части гена), кодирующего белок с мол. массой 60000. В результате других мутаций этого гена трансформирующее действие вируса может становиться термочувствительным: зараженные клетки проявляют трансформированный фенотип при 34°С, но после повышения температуры до 39°С они быстро (через несколько часов) возвращаются к нормальному фенотипу (рис. 13-32). По-видимому, этот специфический ген в онкогенном вирусе ответствен за клеточную трансформацию (и этим привлекает наше внимание), но является ненужным балластом с точки зрения репродукции самого вируса.
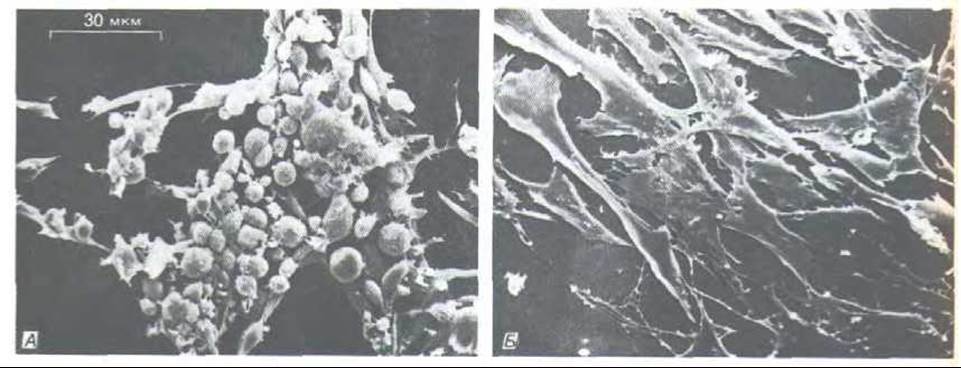
Рис. 13-32. Клетки, инфицированные вирусом саркомы Рауса, несущего термочувствительную мутацию гена, ответственного за трансформацию (онкогена v-src) (микрофотографии, полученные с помощью сканирующего электронного микроскопа). А. Клетки трансформированы и приобрели аномальную округлую форму при низкой температуре (34°С), при которой продукт онкогена активен. Б. Те же клетки, прочно прикрепленные к культуральной чашке и восстановившие свою нормальную уплощенную форму, после того как продукт онкогена инактивирован повышением температуры (до 39°С). (С любезного разрешения G. Steven Martin.)
Трансформирующий ген вируса саркомы Рауса, выявленный в этих экспериментах, был назван геном v-src. Он был отнесен к онкогенам (от греч. onkos-масса, опухоль), так как при введении в нормальную клетку он превращает ее в опухолевую. Каково происхождение этого гена и какова его нормальная функция? Когда радиоактивная ДНК-копия вирусного гена src была использована как зонд для поиска родственных последовательностей методом ДНК-ДНК-гибридизации (разд. 4.6.7), оказалось, что геномы нормальных клеток позвоночных содержат очень сходную, но не идентичную последовательность. Этот гомолог вирусного гена src в нормальной клетке обозначают c-src и относят к протоонкогенам. По-видимому, вирусный онкоген был когда-то захвачен из генома клетки-хозяина и подвергся мутации. Можно предполагать, что протоонкоген - это один из нормальных генов социального контроля, а ретровирус, по существу, клонировал его для нас. В настоящее время таким же способом выявлено и проанализировано много других онкогенов, и в каждом случае это привело к открытию соответствующего протоонкогена.
13-21
13.4.3. Опухоли, возникающие разными способами, содержат мутации одних и тех же протоонкогенов [26, 29]
Опухоли часто возникают не от вирусной инфекции, а в результате мутаций, происходящих случайно или же под действием химических канцерогенов или облучения. Из таких опухолевых клеток можно получить очищенную ДНК и проверить ее на наличие онкогенов путем введения в нетрансформированные клетки в культуре in vitro. Для такого теста часто используют клетки ЗТЗ, поскольку они неопределенно долго делятся в культуре и содержат мутации, благодаря которым их легко трансформировать добавлением всего лишь одного онкогена. Онкоген, ответственный за такую трансформацию, может быть выделен, клонирован и секвенирован с помощью метода рекомбинантной ДНК (рис. 13-33). Примечательно, что в большинстве случаев, когда это было сделано, онкоген оказывался мутантной формой одного из тех самых протоонкогенов, которые были выделены с использованием ретровируса, хотя при этом было открыто и несколько новых онкогенов. При помощи сходных методов было установлено, что трансформация может также происходить в результате перепроизводства некоторых нормальных генных продуктов. Часто опухоли содержат неизмененный протоонкоген, избыточная экспрессия которого обусловлена либо тем, что он представлен слишком большим числом копий, либо тем, что хромосомная перестройка поставила его под контроль несоответствующего промотора. Эти вопросы будут обсуждаться в гл. 21.
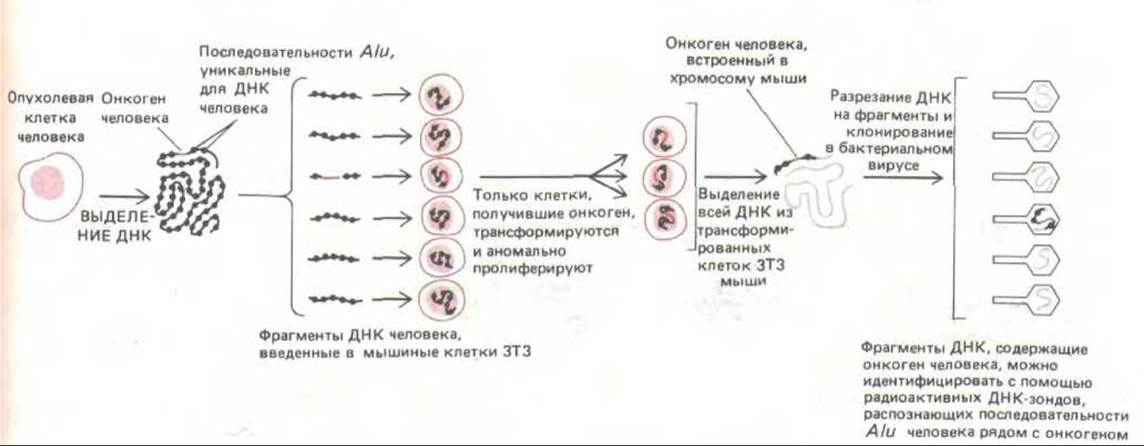
Рис. 13-33. Метод, позволяющий идентифицировать и клонировать онкогены человека. Онкогены, содержащиеся в образце ДНК, взятом из опухоли человека, выявляются по их способности трансформировать мышиные клетки ЗТЗ. Трансформированные клетки ЗТЗ безудержно делятся и распознаются по колониям, которые они образуют в культуральной чашке. Повторяющиеся последовательности семейства Alu (разд. 10.5.11) разбросаны по всему геному человека и служат удобным маркером, который можно использовать для идентификации ДНК человека в клетке другого организма. Используемые в качестве ДНК-зонда последовательности Alu позволяют клонировать онкоген человека, трансформирующий клетки ЗТЗ. При повторном тестировании этим же методом клонированная ДНК, содержащая онкоген, будет очень эффективно трансформировать клетки ЗТЗ.
До сих пор идентифицировано более 50 протоонкогенов (разд. 21.2.3, 21.2.4). Они, видимо, составляют значительную часть протоонкогенов нормальной клетки. Однако многие гены социального контроля, вероятно, еще не обнаружены. Фибробластоподобные клетки ЗТЗ, обычно используемые в тестах на трансформацию, могут не поддаваться действию того онкогена, который трансформировал какие-то другие виды дифференцированных клеток. Кроме того, тест на клеточную трансформацию позволяет выделять только доминантные мутации генов социального контроля, т. е. такие мутации, которые нарушают регуляцию клеточного деления даже при наличии в клетке копий нормального аллеля. Возможно, что в раковых клетках чаще встречаются рецессивные мутации генов социального контроля, обусловленные утратой генной функции, но их нельзя выявить в таком тесте. Поэтому гены, продукты которых в норме помогают стимулировать деление клеток, легче идентифицировать с помощью современных методов, чем те, продукты которых в норме тормозят деление. Тем не менее уже есть данные о том, что гены с тормозящим действием существуют и что их рецессивные мутации нередко бывают причиной клеточной трансформации и рака. Например, после слияния трансформированных клеток с нетрансформированными полученные гибридные клетки очень часто ведут себя как нормальные; по-видимому, контроль клеточного деления у них восстанавливается благодаря появлению белка, которого не было у трансформированной клетки. Поэтому, помня о том, что многие важные гены социального контроля еще не открыты, мы теперь рассмотрим функции уже известных генов.
13-16
13-22
13.4.4. Некоторые протоонкогены кодируют факторы роста или рецепторы факторов роста [26, 30]
Если онкоген клонирован и секвенирован, то указания на вероятную функцию соответствующего гена социального контроля (протоонкогена) часто можно найти, сравнивая последовательности нуклеотидов данного онкогена и уже известных генов. Именно таким путем было открыто, что один из протоонкогенов, c-sis, кодирует функционально активную субъединицу фактора роста PDGF. Клетка, содержащая соответствующий онкоген v-sis, непрерывно и без надобности вырабатывает эту субъединицу, и она, связываясь с клеточным рецептором для PDGF, все время побуждает клетку к пролиферации. По крайней мере три других протоонкогена - c-erbB, c-fms и c-erbA - тоже кодируют рецепторы для факторов роста или гормонов: c-erbB кодирует рецептор для фактора роста эпидермиса (разд. 12.3.13), c-fins-рецептор фактора, стимулирующего рост колоний макрофагов (M-CSF) (этот фактор способствует пролиферации предшественников макрофагов, разд. 17.5.8), a c-erb A-рецептор гормона щитовидной железы (разд. 12.2). Превратившись в результате мутаций в онкогены, эти гены будут кодировать измененные рецепторы, которые ведут себя так, как будто присоединили лиганд (даже если его нет), и поэтому стимулируют клетку, когда это не нужно (разд. 12.3.14).
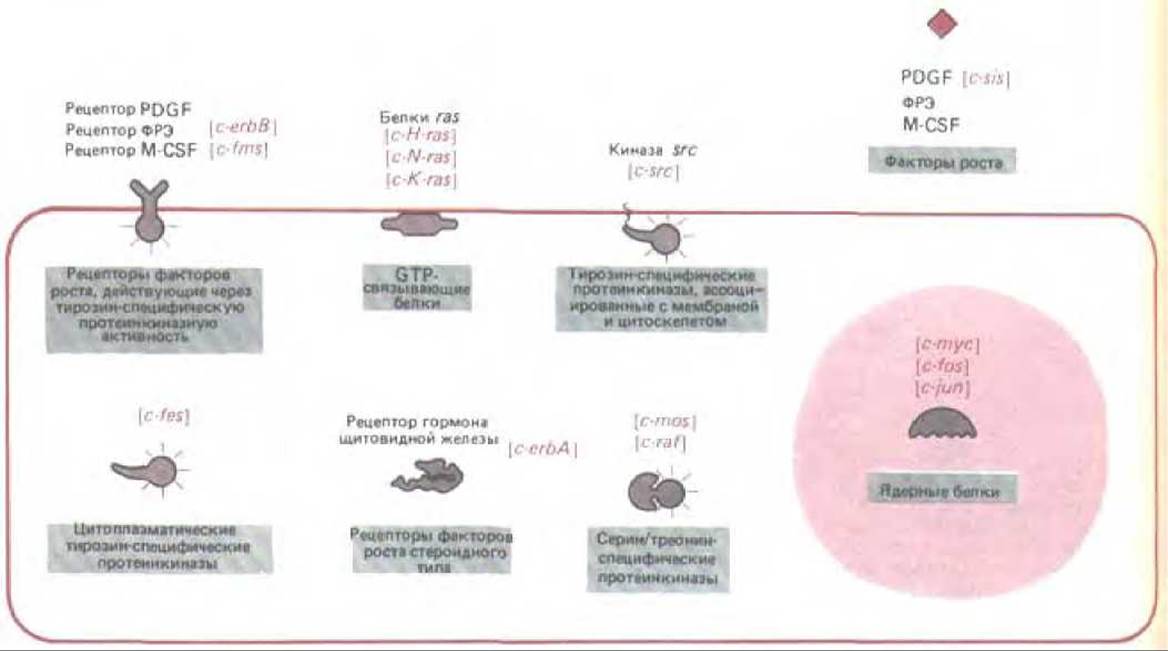
Рис. 13-34. Активность и локализация в клетке основных классов известных протоонкогенов. Названия некоторых типичных протоонкогенов каждого класса выделены цветом. См. также рис. 21-27.
Хотя функции большинства других протоонкогенов еще в точности не известны, можно предполагать, что большинство из них кодирует белки внутриклеточной сигнальной сети, дающей возможность факторам роста стимулировать клеточную пролиферацию. Теперь мы должны рассмотреть, насколько широкий диапазон функций могут осуществлять уже известные группы протоонкогенов, представленные на рис. 13-34.
13.4.5. Некоторые протоонкогены кодируют внутриклеточные медиаторы, участвующие в стимуляции деления клеток
Как уже говорилось в гл. 12, рецепторы для большинства факторов роста, в том числе и PDGF, - это тирозин-специфические протеинкиназы, которые при их активации фосфорилируют сами себя и различные другие белки. Одна группа онкогенов кодирует аномальные формы таких рецепторов, включая только что описанные измененные рецепторы для EGF и M-CSF (рис. 13-34). Другое небольшое семейство сходных протоонкогенов, гены c-ras, кодирует белки, которые связывают и гидролизуют GTP и, возможно, отдаленно родственны G-белкам, участвующим в передаче многих типов сигналов (разд. 12.3.11). Действие мутантных генов ras, обусловливающих трансформацию клеток, связано с повышенными концентрациями или повышенной эффективностью внутриклеточных медиаторов инозитолтрифосфата и диацилглицерола, и они делают клетку сверхчувствительной к некоторым факторам роста; эти факторы, как полагают, индуцируют выработку упомянутых медиаторов. Гены, гомологичные ras, имеются у почкующихся дрожжей, где они участвуют в регуляции цикла клеточного деления в зависимости от количества питательных веществ в среде.

Рис. 13-35. Эта электронная микрофотография показывает, что протеинкиназа, кодируемая онкогеном v-src вируса саркомы Рауса, прикреплена к внутренней поверхности плазматической мембраны; как полагают, белок src, образующийся под действием белка c-src, по- видимому, находится там же, но его труднее обнаружить, так как он обычно присутствует в очень малых количествах. Локализация белка src была определена на этом препарате по его реакции со специфическими антителами, к которым были присоединены электроноплотные частицы ферритина. (С любезного разрешения Ira Pastan; M. С. Willingham, G. Jay, I. Pastan, Cell 18: 125-134, 1979. Copyright Cell Press.)
Нормальный ответ животной клетки на стимуляцию факторами роста включает и многие другие внутриклеточные эффекты, в том числе изменения в рН, в концентрациях Са2+ и циклического AMP, в фосфорилировании белков, в транскрипции генов, в процессинге и распаде мРНК, в белковом синтезе и в цитоскелете. Многие из этих изменений происходят за несколько секунд, для других требуются часы. Большинство белковых продуктов протоонкогенов, участвующих в этой сложной сети управляющих систем, пока еще плохо поддаются классификации. Некоторые из них, например упоминавшиеся выше рецепторы для фактора роста, являются тирозин-специфическими протеин-киназами, связанными с мембраной. Другие, например продукт гена cdc/28 у дрожжей, - это серин/треонин-специфические протеинкиназы, содержащиеся в цитоплазме. Третью категорию составляют белки, находящиеся главным образом в ядре (см, рис. 13-34); один из них, белок c-jun, был идентифицирован как регулятор транскрипции АР-1 (разд. 10.2.8, табл. ЮЛ); он может комбинироваться с другим членом того же семейства - белком c-fos, образуя с ним комплекс, связывающийся с ДНК.
Другой белок ядерной группы, соответствующий протоонкогену с-mус, видимо, может служить показателем того, находится ли клетка в пролиферативном состоянии: в быстро делящихся клетках белок с-mус присутствует в постоянной низкой концентрации на протяжении всего цикла, но как только клетка переходит в состояние покоя Gq, он исчезает. Когда в среду с покоящимися клетками добавляют факторы роста, концентрация белка с-mус резко возрастает, достигая пика за несколько часов, а затем падает до более низкого ненулевого уровня. В отличие от с- mус подавляющее большинство других белков в клетке почти не изменяют своей концентрации при переходе из пролиферативного состояния в стадию покоя или обратно.
13.4.6. Влияние онкогенов на регуляцию клеточного деления тесно связано с воздействием на адгезию клеток [32, 33]
Одним из наиболее интенсивно изучаемых протоонкогенов является c-src, соответствующий онкогену v-src вируса саркомы Рауса. Он принадлежит к небольшому семейству гомологичных протоонкогенов и кодирует белок src - тирозин-специфическую протеинкиназу с мол. массой 60000 (поэтому иначе ее называют P60src), которая содержит ковалентно связанную жирную кислоту, прикрепляющую ее к внутренней стороне плазматической мембраны (разд. 8.2.3). В своей онкогенной форме эта киназа сверхактивна, и для того, чтобы она могла вызывать трансформацию клетки, необходимо ее прикрепление к мембране (рис. 13-35). Эксперименты с антителами показывают, что белок src концентрируется в фокальных контактах, т. е. в местах, где клетка прикреплена к субстрату при помощи соединений с матриксом, в которых участвуют внутриклеточные актиновые филаменты (рис. 13-36). По-видимому, белок src играет роль в прикреплении актина к мембране, поскольку активация термочувствительной разновидности белка v-src (путем понижения температуры) сразу же приводит к увеличению складчатости мембраны (в результате движения ламеллоподий при участии актина; см. разд. 11.2.11), а также к ослаблению клеточной адгезии, включающему разрушение фокальных контактов, так что клетка округляется (см. рис. 13-30). Наблюдаемое изменение адгезии объясняют по меньшей мере двумя независимыми воздействиями белка src. Первое из них состоит в том, что активная киназа v-src фосфорилирует остаток тирозина в находящемся внутри клетки «хвостє» рецептора фибронектина (разд. 11.2.8). Исследования in vitro позволяют предполагать, что это фосфорилирование уменьшает сродство рецептора как к талину (внутри клетки), так и к фибронектину (вне клетки). Кроме того, клетки, трансформированные v-src, выделяют большое количество протеолитического фермента, называемого активатором плазминогена. Это название связано с его способностью активировать другой протеолитический фермент, плазмин, путем расщепления предшественника - плазминогена; однако активатор плазминогена способен и непосредственно разрушать другие белки. Очевидно, и при прямом, и при косвенном воздействии он помогает клетке ослаблять ее прикрепление и мигрировать во внеклеточном матриксе. Когда в культуральную среду добавляют моноклональное антитело к активатору плазминогена, клетки становятся более адгезивными и проявляют тенденцию распластываться на субстрате. Таким образом, чрезмерная активность тирозинкиназы v-srct видимо, ослабляет клеточную адгезию двумя способами: она фосфорилирует рецепторы фибронектина (и другие трансмембранные молекулы из группы интегринов, участвующие в прикреплении клеток к матриксу - см. разд. 14.1.3) и вызывает секрецию протеинкиназы, которая разрушает фибронектин (и другие молекулы матрикса).
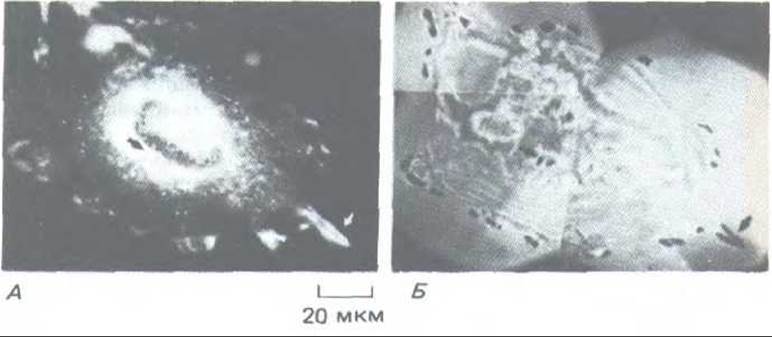
Рис. 13-36. Белок src присутствует во многих участках клетки, но особенно концентрируется, видимо. в фокальных контактах и других местах прикрепления клетки к внеклеточному матриксу. А. Иммуно-флуоресцентная фотография, выявляющая распределение белка src по связыванию src-специфических антител. Б. Вид той же клетки при использовании метода оптической интерференции, выявляющего места плотного прикрепления клетки к субстрату (темные участки). Распределение светлых пятен белка src на фото А соответствует распределению темных пятен прикрепления на фото Б (указано стрелками). Эти фотографии показывают распределение вирусного белка src в клетке, трансформированной вирусом саркомы Рауса. По-видимому, белок src, синтезируемый в нормальной клетке, распределяется сходным образом, но его труднее выявить, так как он присутствует в меньших количествах. (L. R. Rohrschneider, Proc. Natl. Acad. Sci. USA 77: 3514-3518, 1980.)
Какое отношение могут иметь эти факты к регуляции роста клеток? Если покоящийся фибробласт обработать PDGF, это сразу же вызовет складчатую деформацию и фокальные контакты клеток изменят свою структуру за несколько минут: из этих контактов ненадолго исчезнет винкулин, и прикреплявшиеся здесь пучки актиновых филаментов будут временно разрушены. Таким образом, в стимулируемой к делению покоящейся клетке PDGF вызывает много изменений того же типа, что возникают и под действием v-src. В самом деле, среди немедленных изменений, вызываемых PDGF, отмечается и усиленное фосфорилирование белка c-src, которое, повышая киназную активность src, могло бы прямо объяснить это сходство эффектов (рис. 13-37). С этой точки зрения трансформация клеток онкогеном v-src (и многими другими онкогенами с подобным же действием) - это как бы преувеличенный эффект нормального механизма стимуляции роста, который включает и ослабление клеточной адгезии. Опасность онкогенов для организма заключается в том, что в отличие от PDGF, стимулирующего клетку лишь кратковременно, белки, подобные v-src, стремятся необратимо вывести клетку из состояния G0 и таким образом удерживать ее в пролиферативном состоянии.
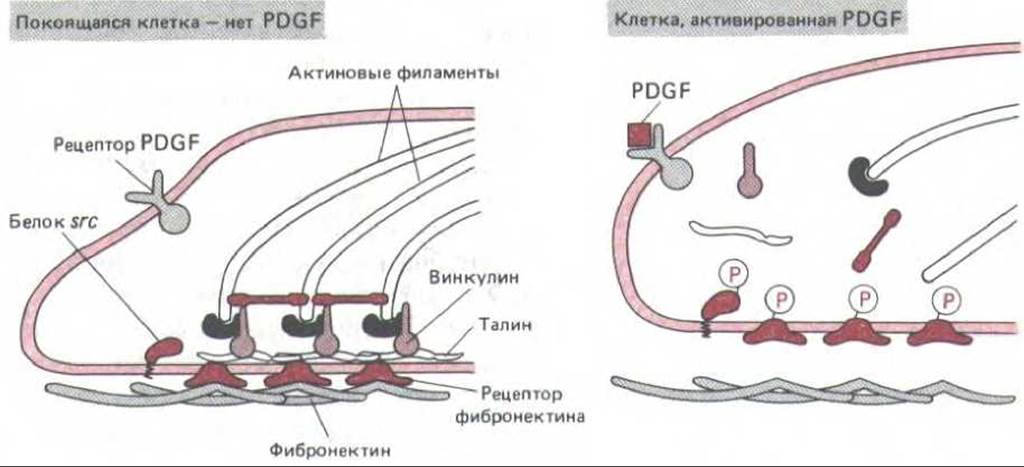
Рис. 13-37. Умозрительная модель, поясняющая, как могли бы происходить быстрые изменения клеточной адгезии при стимуляции клеток к делению фактором PDGF. Связывание PDGF с его рецептором приводит (пока не известным путем) к фосфорилированию белка c-src. В результате эта протеинкиназа, связанная с плазматической мембраной, активируется и в свою очередь фосфорилирует тирозиновые остатки соседних трансмембранных белков клеточной адгезии, в том числе рецептор фибронектина. Это приводит к тому, что фокальные контакты и другие участки клеточной адгезии частично разрушаются и связанные с ними актиновые филаменты теряют связь с мембраной. Частично эта модель основана на наблюдениях над клетками, трансформированными вирусом саркомы Рауса, которые содержат постоянно активный модифицированный белок src (v-src). Тирозин-протеинкиназы, кодируемые двумя другими протоонкогенами семейства src - c-abl и c- yes,- могли бы действовать таким же образом, как белок c-src в описанном выше механизме. Однако такими ферментами обычно фосфорилируется много белков, и не ясно, какие из них играют решающую роль в контроле клеточного деления. Некоторые важные мишени могут быть представлены в клетке одной или несколькими копиями (этого слишком мало для определения их обычными биохимическими методами), и у разных клеток мишени могут быть различными. Кроме того, трудно установить причинные взаимосвязи в сложной сети взаимодействующих компонентов, где многие факторы могут действовать параллельно и один и тот же эффект может достигаться разными способами.
13.4.7. Связь между клеточной пролиферацией и клеточной адгезией пока еще непонятна [33]
Наше обсуждение контроля нормальной пролиферации клеток позвоночных приводит к парадоксу. С одной стороны, ясно: чтобы выйти из состояния G0 и начать делиться, нормальные клетки должны формировать адгезивные контакты с субстратом (адгезия между клетками и матриксом). Это наводит на мысль, что трансмембранные белки, связывающие клетки с внеклеточным матриксом (включая рецептор фибронектина и другие белки группы интегринов), создают некий внутриклеточный сигнал, который облегчает деление клеток, находящихся в соответствующем состоянии. С другой же стороны, адгезия сама по себе еще не достаточна для запуска деления - необходимы еще факторы роста. Парадокс здесь в том, что факторы роста, по-видимому, частично действуют так, что временно ослабляют адгезию, от которой зависит пролиферация нормальных клеток (рис. 13-37). Такое действие заставляет вспомнить о втором наблюдении: во многих случаях недолгая обработка остановленных в росте нормальных клеток протеолитическим ферментом (например, трипсином), приводящая к потере прикрепленными клетками контакта с субстратом и к их округлению, дает еще побочный эффект - запуск одного цикла деления. Видимо, пролиферация клеток кратковременно стимулируется как внеклеточными протеазами, непосредственно ослабляющими адгезию между клетками и матриксом в результате переваривания адгезионных внеклеточных белков, так и факторами роста, которые нарушают эту адгезию косвенно, воздействуя на фокальные контакты через внутриклеточные медиаторы.
Исследования на раковых клетках усиливают этот парадокс. Большинство таких клеток, в том числе и трансформированные хорошо изученными онкогенами, представленными на рис. 13-34, отличаются от их нормальных двойников тем, что для деления им не нужно прикрепляться к субстрату. Поскольку такая независимость от прикрепления дает возможность трансформированным клеткам расти в новых условиях, где нормальные контакты клеток между собой и с матриксом установить нельзя (разд. 13.3.6), можно предполагать, что она явилась результатом естественного отбора клеток, формирующих опухоли. Но почему многие раковые клетки не просто делятся независимо от прикрепления, но не прикрепляются прочно к внеклеточному матриксу даже тогда, когда такая возможность существует? Намек на ответ следует из наблюдений над трансформированными клетками, которые искусственно заставляют прикрепиться к культуральной чашке. Как отмечалось выше, фибробласты куриного эмбриона, трансформированные с помощью v-src, выделяют в больших количествах активатор плазминогена, который ослабляет их прикрепление к чашке. Если такие клетки растут в присутствии антитела, блокирующего активность этой протеазы, то они более прочно прикрепляются к чашке и в то же время становятся более подверженными нормальному социальному контролю клеточного деления: вместо образования многослойной структуры они проявляют тенденцию прекращать деление при взаимном контакте. Таким образом, прочное сцепление с внеклеточным матриксом, видимо, тормозит рост этих трансформированных клеток.
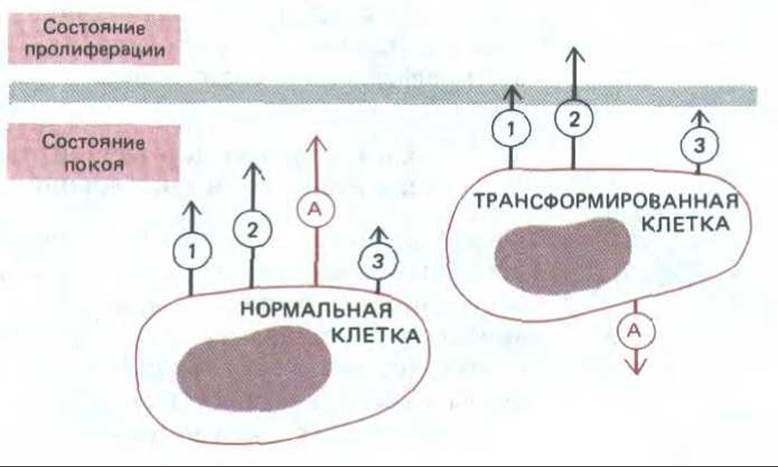
Рис. 13-38. Общая природа сигналов социального контроля, воздействующих на нормальные и трансформированные клетки. В обоих случаях различные факторы роста (обозначенные здесь цифрами 1, 2 и 3) действуют совместно, «поднимая» клетку из G0 в пролиферативное состояние. Поскольку трансформированная клетка поддерживается в положении, близком к границе перехода (цветная линия), она может часто стимулироваться к пролиферации только одним фактором роста (или очень низкой концентрацией смеси факторов роста). Однако, как отмечалось в тексте, есть существенная разница в эффекте прикрепления (обозначенном как А) между этими двумя типами клеток: для пролиферации нормальных клеток прикрепление необходимо, тогда как у трансформированных клеток оно скорее тормозит пролиферацию.
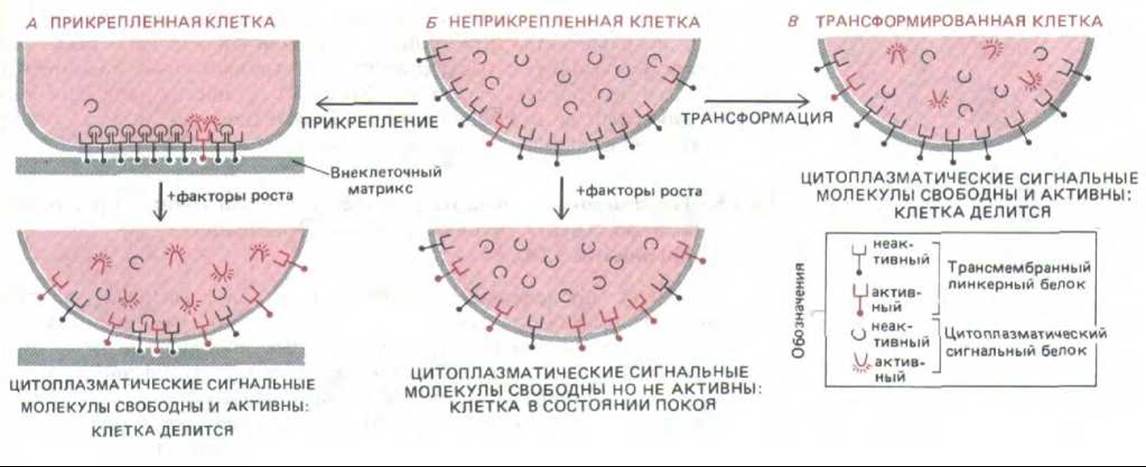
Рис. 13-39. Гипотетическая схема, объясняющая наблюдаемую зависимость пролиферации нормальных и трансформированных клеток от адгезии между клетками и матриксом. Главное внимание уделяется двум типам молекул: 1) цитоплазматическому белку, который служит внутриклеточным сигналом к делению, и 2) трансмембранному линкерному белку, который может связываться как с цитоплазматической сигнальной молекулой по одну сторону клеточной мембраны, так и с внеклеточным матриксом по другую сторону. Это связывание - кооперативный процесс, так что сигнальные молекулы, связавшиеся с линкерным белком внутри клетки, стабилизируют трансмембранную структуру и способствуют ее связыванию с внеклеточным матриксом; и наоборот, связывание с внеклеточным матриксом способствует связыванию сигнальных молекул с линкерным белком внутри клетки. Чтобы клетка получила сигнал к делению, сигнальные молекулы должны быть несвязанными в цитоплазме и находиться в активной конформации, в которой они менее прочно связываются с линкерным белком. Предполагается, что сигнальные молекулы активируются при их фосфорилировании, которое происходит благодаря киназной активности линкерного белка.
Когда прикрепленную клетку стимулируют факторы роста (А), включается киназная активность; сигнальные молекулы фосфорилируются и отсоединяются от линкерных белков, что служит для клетки сигналом к делению и ослаблению адгезии. Нормальные клетки в суспензии (Б) не делятся при воздействии факторов роста потому, что очень мало сигнальных молекул внутри клетки связывается с линкерными белками, которые могли бы их фосфорилировать. Трансформированные клетки (В) отличаются пониженной адгезивностью и могут делиться даже в суспензии, так как в их регуляторной системе имеется «шунт», благодаря которому сигнальные молекулы всегда находятся в фосфорилировать состоянии.
Различные условия, необходимые для роста нормальных и трансформированных клеток, и противоположное влияние на них адгезии к клеточному матриксу (рис. 13-38) могут иметь логическое объяснение. Сложная структура, формирующаяся в фокальном контакте между клеткой и субстратом, в каком-то отношении, вероятно, играет очень важную роль в возникновении внутриклеточных сигналов, регулирующих деление клеток. Наблюдаемые явления можно было бы объяснить, предположив, что для нормального запуска деления необходимы три шага: 1) прикрепление клетки к матриксу при участии упорядоченного комплекса цитоскелетных белков, образующегося внутри клетки (разд. 11.2.8); 2) активация этого комплекса, как правило, одним или несколькими факторами роста для создания сигнала к делению; и 3) частичное разрушение контактов клетки с матриксом, как этап, необходимый для подачи такого сигнала. Для трансформированной клетки первый шаг становится ненужным, и разъединенные внутриклеточные компоненты контактов с матриксом будут необходимы и достаточны для возникновения сигнала к пролиферации. Гипотетическая модель такого механизма регуляции роста представлена на рис. 13-39.
13.4.8. Позиционные сигналы и автономные клеточные программы контролируют деление клеток в растущем организме [20, 34]
Эксперименты, проведенные в упрощенных искусственных условиях клеточной культуры, дают нам многое из того, что мы знаем о молекулярных механизмах, контролирующих рост и деление клеток у многоклеточных животных. Пока эта работа, однако, выявила только некоторые из основных «болтов и гаек» значительно более сложной системы социального контроля, которая должна действовать в интактном организме для регулирования пролиферации каждой группы клеток в соответствии с ее пространственным положением и предшествующим ходом развития.
Обсуждая проблему клеточного старения, мы высказали мысль, что клетками часто управляют долговременные внутриклеточные программы, поэтому текущее пролиферативное поведение клетки зависит от предыстории воздействия определенных факторов за много клеточных поколений до этого (разд. 13.3.10). Хотя взаимоотношения между долговременными и кратковременными механизмами контроля все еще остаются загадкой, по-видимому, в тех и других участвует много одинаковых молекул, в том числе факторов роста и продуктов протоонкогенов. В процессе эмбрионального развития программы деления клеток могут быть удивительно сложными и четкими. Это ярко продемонстрировано, например, на нематоде Caenorhabditis elegans, оплодотворенное яйцо которой делится так, что производит в точности 959 ядер соматических клеток взрослого животного; уже начато изучение некоторых генных продуктов, участвующих в реализации этой программы (разд. 16.3.3).
Однако не следует предполагать, что рост зародыша регулируется простым подсчетом клеточных делений. Это стало ясно, например, при сравнении тритонов разной плоидности. Клетки пентаплоидного тритона примерно в пять раз крупнее клеток гаплоидного, но благодаря тому, что их в каждой ткани в пять раз меньше, чем у гаплоида, размеры тела и органов у обоих животных практически одинаковы (рис. 13-40 и 13-41). Очевидно, у позвоночных механизмы контроля клеточного деления, регулирующие размеры тела, основаны на измерении длин, а не на простом подсчете числа клеток или циклов деления. Такие механизмы нуждаются в сложном позиционном контроле, в котором важную роль могли бы играть диффундирующие факторы роста.
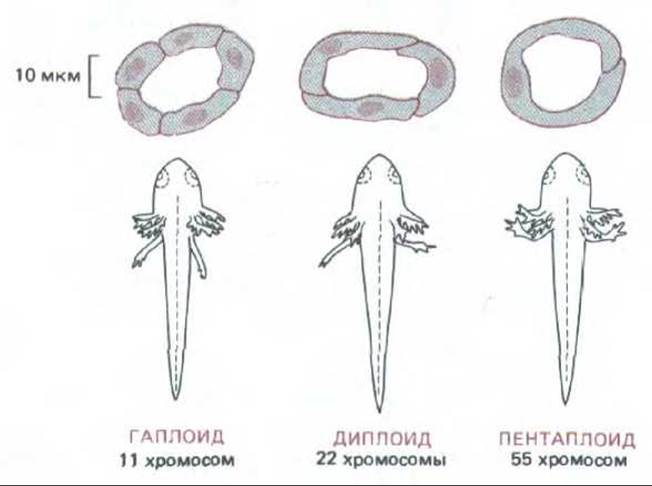
Рис. 13-40. Вверху изображены типичные срезы почечных канальцев аксолотлей разной плоидности. У пентаплоидных аксолотлей клетки крупнее, чем у гаплоидных, однако сами животные и их органы имеют одинаковые размеры, так как каждая ткань пентаплоидного животного состоит из меньшего числа клеток. Это указывает на то, что размеры клеток регулируются каким-то механизмом, в основе которого лежит учет размеров и расстояний, а не числа делений или числа клеток. [G. Frankhauser, In: Analysis of Development (В. H. Willier, P. A. Weiss, V. Hamburger, eds.), pp. 126-150. Philadelphia, Saunders, 1955.]
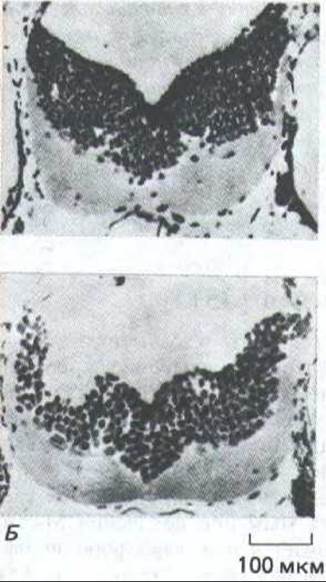
Рис. 13-41. Микрофотографии срезов мозга гаплоидного и тетраплоидного аксолотлей (см. также рис. 13-40). А. Поперечный срез заднего мозга гаплоидного аксолотля. Б. Соответствующий срез мозга тетраплоидного аксолотля; видно, что уменьшенное число клеток компенсируется увеличением их размеров. (G. Frankhauser, Int. Rev. Cytol. 1: 165-193, 1952.)
Позиционный контроль клеточного деления может работать с удивительной специфичностью. Когда часть эпителия ножки одного таракана пересаживают на гомологичный участок другому, она «вживляется» без заметного деления клеток. Однако если ее трансплантировать в негомологичное место, то и клетки трансплантата, и соседние клетки хозяина начинают делиться, а затем дифференцируются с образованием таких клеток, которые в норме лежали бы между участком, откуда был взят трансплантат, и участком, куда он был пересажен (разд. 16.4.9). Молекулярная основа такого поведения совершенно не известна.
Вообще деление клеток в процессе эмбрионального развития регулируется при совместном участии как автономных клеточных программ, так и межклеточных взаимодействий, но важность каждого из этих факторов меняется от вида к виду и от одной части тела к другой. В зрелых тканях клеточное деление тоже регулируется сложной сетью различных механизмов: при заживлении глубокой кожной раны у позвоночных, чтобы возместить потерю ткани, должны регенерировать в надлежащих количествах около 12 типов клеток, начиная с фибробластов и кончая шванновскими клетками. Кроме того, в системе социального контроля существует избыточность с многочисленными ограничителями, действующими параллельно так, чтобы утрата одного контролирующего компонента в одной клетке (обычно это результат соматической мутации) не повредила целому организму вследствие появления огромного клона интенсивно делящихся клеток. Исследования в области рака показывают, что в данной клеточной линии должно произойти от четырех до шести мутаций, прежде чем она даст начало злокачественной опухоли (разд. 21.1.4).
Изучение молекулярных деталей тщательно отлаженных механизмов социального контроля, позволяющих развиться и существовать во взрослом организме такому органу, как почка, видимо, потребует работы нескольких поколений клеточных биологов. Теперь, однако, стали доступными такие мощные средства, как антитела, блокирующие специфические факторы роста или рецепторы, и получение трансгенных животных, у которых вырабатываются сигнальные молекулы, несвойственные определенным типам клеток (разд. 5.6.10). Благодаря таким новым подходам задача, хотя и труднейшая, уже не кажется неразрешимой.
Заключение
Аномальные клетки, не повинующиеся социальным сдерживающим факторам, пролиферируют с образованием опухолей в организме; они также появляются при трансформации в культуре клеток. Хотя это часто приводит к гибели всего организма, как индивидуальные клетки они получают селективное преимущество, и поэтому их легко выделять. Трансформация клетки часто сопровождается мутацией или сверхэкспрессией специфических онкогенов, во многих случаях выявленных благодаря их наличию в РНК опухолевых вирусов (ретровирусов). Нормальные гомологи таких вирусных онкогенов в здоровых клетках, называемые протоонкогенами, по-видимому, кодируют ключевые компоненты нормальной системы социального контроля клеточного деления. Некоторые протоонкогены кодируют факторы роста, другие - рецепторы для этих факторов или внутриклеточные регуляторные белки, участвующие и клеточной адгезии, а третьи — белки, помогающие передавать сигналы клеточного деления в ядро клетки. Чтобы клетка превратилась в раковую, в ней должны подвергнуться изменению многие гены социального контроля, что указывает на избыточность сложных регуляторных систем, влияющих на клеточную пролиферацию в тканях.