Общая микробиология - Шлегель Г. 1987
Разложение природных веществ
Углеводороды
Даже химически столь устойчивые вещества, как парафины, нефть и каучук, подвергаются разложению под действием микробов. Заметного их распада не происходит только в отсутствие O2 (например, в нефтяных месторождениях или, при особых условиях, в пластах каменного угля). Большое практическое значение имеют следующие вопросы: подвергается ли биологическому окислению нефть, попадающая в почву или в воду? Существуют ли микроорганизмы, специфически использующие углеводороды? И наконец, можно ли по количеству микроорганизмов, окисляющих углеводороды, судить о вероятном наличии нефти или природного газа?
Еще недавно рост микроорганизмов на нефти считали явлением очень редким. Предполагалось, что бактерии, способные использовать нефть, встречаются только там, где имеется сама нефть (нефтяные промыслы, нефтехранилища). На этом основании был предложен и новый способ разведки нефти; нефтяные месторождения надеялись обнаружить, подсчитывая в пробах грунта число бактерий, способных использовать нефть. Однако, согласно современным данным, такие бактерии распространены очень широко и могут быть выделены из любой полевой, лесной или луговой почвы. Кроме того, способность использовать нефть в качестве источника энергии присуща не единичным специализированным формам, а многим грибам и бактериям. Эти сведения согласуются с новыми аналитическими данными о химическом составе бактериальных, растительных и животных клеток. Углеводороды содержатся во многих организмах и непрерывно синтезируются бактериями и растениями. К ним, по-видимому, относятся воскообразные вещества, покрывающие листья растений. Таким образом, углеводороды - это не только сохранившиеся до наших дней продукты жизнедеятельности древних растений; это также вторичные метаболиты, и ныне синтезируемые зелеными растениями в значительных количествах.
14.11.1 Метан
Среди углеводородов метан занимает особое положение. Его используют и окисляют бактерии, не способные расщеплять углеводороды с длинной цепью. Такого рода бактерии следует рассматривать не как микроорганизмы, окисляющие углеводороды, а скорее как группу бактерий, специализировавшихся на использовании С1-соединений. Поэтому бактерии, окисляющие метан, относят вместе со всеми бактериями (и дрожжами), способными использовать метанол, метилированные амины, диметиловый эфир, формальдегид и формиат, к метило- трофным организмам. В накопительных культурах с метаном как единственным источником углерода и энергии развиваются бактерии, относящиеся к различным родам: Methylomonas, Methylococcus, Methylosinus. Некоторые из них растут только на средах, содержащих метан, метанол или диметиловый эфир, и не могут использовать сахара, органические кислоты или иные спирты (кроме метанола).
Получение энергии. Восстановительные эквиваленты для получения энергии могут создаваться в результате окисления метана через этапы образования метанола, формальдегида и формиата до СO2. Окисление метана в метанол сопровождается включением в молекулу одного атома кислорода; эту реакцию катализирует метаноксигеназа.
![]()
Синтез клеточного вещества. Вещество клеток синтезируется, как правило, из формальдегида - промежуточного продукта окисления метана. Этот синтез может осуществляться разными путями, из которых наиболее изучены рибулозомонофосфатный цикл фиксации формальдегида и сериновый путь.
В рибулозомонофосфатном цикле формальдегид (продукт окисления метана) превращается в результате альдольной конденсации с рибулозо-5-фосфатом в арабино-3-гексулозо-6-фосфат; последний в ходе изо- меразной реакции превращается в фруктозо-6-фосфат (рис. 14.6). Из фруктозо-6-фосфата снова (подобно тому, как это происходит при фиксации СO2 в рибулозобисфосфатном цикле) образуется пентозофосфат. Цикл не включает реакцию, катализируемую седогептулозо-1,7-фосфатазой, и протекает, таким образом, согласно схеме, представленной на рис. 11.2 слева.
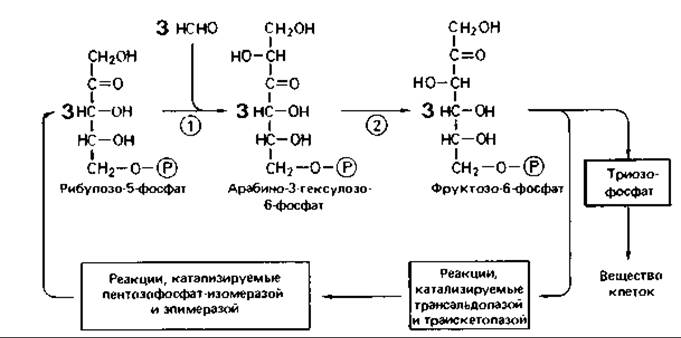
Рис. 14.6. Рибулозомонофосфатный цикл фиксации формальдегида. Ключевые ферменты (цифры в кружках): 1 -гексулозофосфатсинтаза; 2 - гексулозофосфатизомераза. (Ström et al., Biochem. J., 144 [1974], 465-476.)
Сериновый путь (рис. 14.7) был изучен на Pseudomonas MA и Нуphomicrobium X. Вероятно, у других микроорганизмов имеются модификации этого пути. Акцептором формальдегида служит глицин. Следует ожидать, что у организмов, ассимилирующих Отсоединения с помощью этого цикла, удается обычно обнаружить гидроксипируватредуктазу, малаттиокиназу, малил-СоА-лиазу и изоцитрат-лиазу.
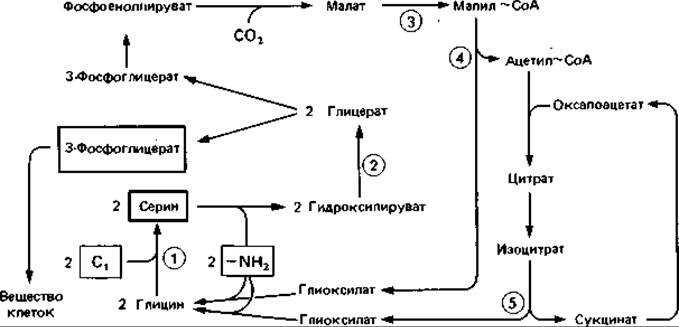
Рнс. 14.7. Ассимиляция C1-соединений по сериновому пути. C1-соединение включается в серин при участии тетрагидрофолиевой кислоты. Последующая цепь реакций приводит к синтезу промежуточных продуктов (фосфоенолпирувата и пирувата) и в конечном счете - клеточного материала, а также к регенерации глицина. Ключевые ферменты (цифры в кружках): 1 - серин-гидроксиметил- трансфераза; 2 - гидроксипируватредуктаза; 3 - малаттиокиназа; 4 - малил-СоА-лиаза; 5 - изоцитратлиаза. (Bollion, Hersh. Arch. Biochem. Biophys., 153 [1972], 368; Harder et al., J. gen. Microbiol., 78 [1973], 155.)
Дрожжи способны использовать только метанол, но не метан. У ряда дрожжей (Candida boidinii, Hansenula polymorphä) включение метанола в вещество клеток происходит тоже через формальдегид, однако через другой пентозофосфат, а именно ксилулозо-5-фосфат. В этом ксилулозо- монофосфатном цикле фиксации формальдегида последний вместе с кси- лулозо-5-фосфатом превращается с помощью специальной транскетолазы в глицеральдегидфосфат и дигидроксиацетон. Оба продукта (дигидроксиацетон - после фосфорилирования триокиназой) поступают на пути синтеза.
Использование метанола бактериями начинается при участии метанолдегидрогеназы. В этом ферменте была обнаружена ранее неизвестная простетическая группа - метоксатин, или пирролохинолинхинон. В настоящее время известно, что метоксатин входит в состав многих бактериальных мембраносвязанных алкогольдегидрогеназ.
14.11.2 Этан, пропан и бутан
В то время как в накопительных культурах, содержащих помимо СO2 и О2 только чистый метан, развивается главным образом Methylomonas methanica, в культурах на природном газе, в состав которого наряду с метаном входит и этан, растут одни только окислители этана. К окислению этана способно гораздо большее число видов, чем к окислению метана. Большинство микроорганизмов, окисляющих этан, принадлежит к родам Mycobacterium, Flavobacterium и Nocardia. Некоторые из бактерий, использующих этан, могут также окислять газообразный водород. Еще большее число видов бактерий развивается в накопительных культурах за счет использования пропана. Были выделены также бактерии, способные окислять бутан (Mycobacterium и Pseudomonas).
14.11.3 Алканы (алифатические углеводороды) с длинной цепью
Алканы с длинной цепью используются очень многими бактериями. Решающее значение при этом имеет длина цепи: по мере удлинения цепи парафинов растет число видов, способных использовать эти соединения, а также активность их использования. В их разложении участвуют микобактерии, нокардии и коринебактерии. Долгое время способность бактерий расти на средах с углеводородами рассматривалась как своего рода курьез. Интерес к микроорганизмам, окисляющим углеводороды, возник в связи с двумя наблюдениями. В 1950 г. в Институте бродильных производств в Берлине из накопительных культур, содержавших в качестве источника энергии различные фракции углеводородов, были выделены два вида дрожжей - Candida lipolytica и Candida tropicalis. Оказалось, что С. lipolytica использует все высшие гомологи углеводородов, начиная с С15-соединений. Вслед за этим было установлено, что большинство видов Candida окисляет углеводороды. Проведенная проверка штаммов из коллекции дрожжей показала, что способность использовать углеводороды присуща очень многим из них. Использование углеводородов протекает с необычайно высоким выходом полезных продуктов (У). Если при использовании углеводов коэффициент У составляет около 0,5, то для углеводородов он колеблется в пределах от 0,7 до 1,0.
Механизм. Многие псевдомонады окисляют углеводороды настолько полно, что накопления промежуточных продуктов не происходит. Только у Acinetobacter calcoaceticus продукты окисления выделяются в среду, а у Nocardia накапливаются в клетке. Характер продуктов зависит от природы субстрата. Если А. calcoaceticus растет на среде с гексадеканом, то из культуральной жидкости можно выделить цетилпальмитат. Цетилпальмитат представляет собой эфир пальмитиновой кислоты и цетилового спирта (гексадеканола)-двух продуктов окисления гексадекана. На приводимой схеме (рис. 14.8) показано, что расщепление парафина начинается с окисления концевого углерода.
В первичном воздействии на углеводородную цепь участвует кислород. Без молекулярного кислорода парафин не окисляется. Окисление катализирует монооксигеназа (алканоксигеназа):
Парафин + O2 + NADH2 → Алифатический спирт + NAD + Н2O
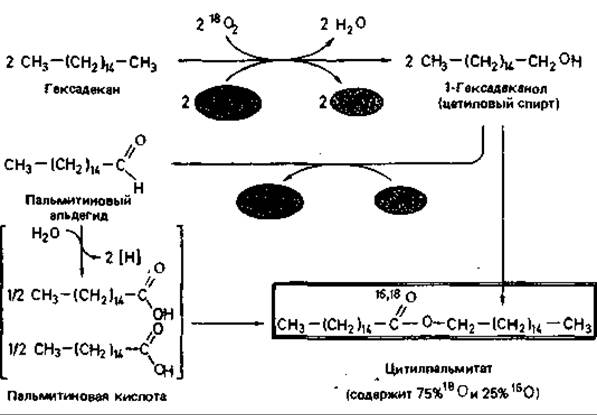
Рис. 14.8. Образование цетилпальмитата из гексадекана, осуществляемое Acinetobacter calcoaceticus. При росте на среде с обычной водой (Н216О) в атмосфере с тяжелым кислородом (18O2) образуется цетилпальмитат, кислород которого на 75% состоит из 18О. Это согласуется с представлением о том, что превращение гексадекана начинается с окисления концевого углерода при участии алканоксигеназы.
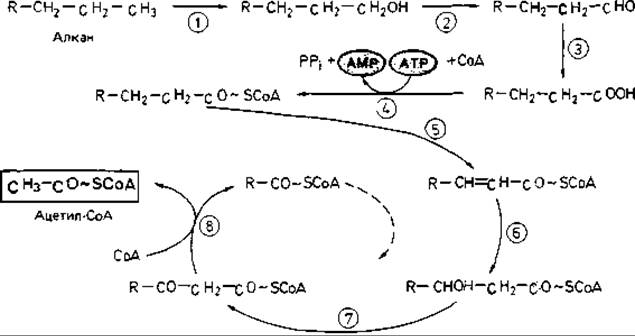
Рис. 14.9. Расщепление алканов (парафинов) путем терминального окисления при участии монооксигеназы и последующего ß-окисления до ацетил-СоА. Участвующие ферменты: 1 - монооксигеназа (алкан-1-гидроксилаза); 2-алкогольдегидрогеназа; 3 - альдегиддегидрогеназа; 4 - ацил-СоА-синтетаза; 5 - ацил-СоА-дегидрогеназа; 6 - 3-гидроксиацил-СоА-гидро-лиаза; 7 - 3-гидроксиацил-СоА-дегидрогеназа; 8- ß-кетотиолаза.
Дальнейшее окисление парафина протекает по пути, который известен как ß-окисление жирных кислот с длинной цепью (рис. 14.9). Если псевдомонады, окисляющие гептан, поместить в условия пониженного парциального давления кислорода, то в культуральной жидкости будут накапливаться С3-, С5- и С7-жирные кислоты. Вырастив клетки бактерий в присутствии гексана, а затем инкубируя их с гептаном, можно наблюдать накопление пропионовой кислоты. Это, видимо, объясняется тем, что клетки, выросшие в присутствии гексана, не содержат ферментов, необходимых для окисления пропионата через метилмалонил-СоА.
14.11.4 Ароматические углеводороды
Растения синтезируют много соединений, содержащих ароматические кольца. Из них в количественном отношении преобладает лигнин, составляющий 20% (по весу) древесины. Способность расщеплять такие соединения с разрывом ароматического кольца обладают многие бактерии и грибы. Некоторые псевдомонады растут на среде, содержащей бензоат, быстрее, чем на среде с сахарами. Для быстрого расщепления ароматических веществ необходимо присутствие молекулярного кислорода. Пути такого расщепления мы рассмотрим в этом разделе. Согласно новейшим данным, ароматические соединения могут подвергаться также анаэробному разложению, но мы не будем описывать его метаболические механизмы.
Подготовка к расщеплению кольца. Большинство природных ароматических соединений расщепляется бактериями сначала до пирокатехина (катехола) или протокатеховой кислоты. Расщеплению до пирокатехина подвергаются многие соединения, у которых в ароматическом кольце имеется либо один заместитель, либо два заместителя в положениях 1 и 2, т. е. такие вещества, как миндальная кислота, фенилаланин, толуол, бензол, фенол, бензойная и салициловая кислоты.
Ароматические вещества с двумя заместителями в положениях 1,3 или 1,4, а также с большим числом замещающих групп (например, 4-гидроксибензойная, хинная, ванильная и шикимовая кислоты) расщепляются с образованием протокатеховой кислоты. Во всех случаях в кольцо вводятся гидроксигруппы. Атомы кислорода для гидроксигрупп доставляет молекулярный кислород. В случае нефенольных ароматических веществ необходимая для разрыва кольца 1,2-дигидроксибензольная структура создается путем двойного гидроксилирования.
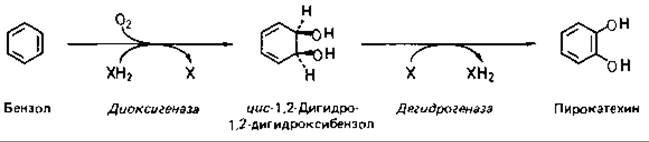
Например, незамещенное кольцо бензола подвергается гидроксилированию с помощью диоксигеназы (двойной гидроксилазы) до цис-1,2-дигидро-1,2-дигидроксибензола, а затем дегидрируется (реароматизируется) с образованием пирокатехина.
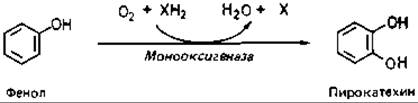
Фенольные ароматические соединения гидроксилируются монооксигеназами. Один атом О молекулярного кислорода включается в субстрат, а другой восстанавливается до воды. Донорами водорода могут служить пиридиннуклеотиды.
Заместители в ароматическом кольце часто (но не всегда) отщепляются до разрыва кольца. Например, атомы хлора, нитрогруппы и сульфогруппы могут быть заменены на гидроксильные группы. Алифатические боковые цепи могут изменяться и укорачиваться самым различным образом или же остаются без изменений.
Разрыв кольца. Разрыв ароматического кольца осуществляют диоксигеназы. При этом в субстрат включается молекулярный кислород. Разрыв происходит либо между двумя соседними гидроксильными группами, либо между гидроксилированным углеродом и соседним негидроксилированным. Из участвующих в процессе ферментов лучше всего изучены ферменты, выделенные из разных видов Pseudomonas. На рис. 14.10 показаны наиболее важные типы разрыва ароматического кольца.
Орто-расщепление. Разрыв кольца между двумя соседними гидроксилированными атомами С (орто-расщепление, или интрадиольное расщепление) приводит к образованйю дикарбоновой кислоты. По-видимому, сначала происходит присоединение молекулы О2 к гидроксильным группам соседних атомов углерода с образованием циклической перекиси, а затем в результате внутримолекулярной перегруппировки межуглеродная связь разрывается и образуется цис,цис-муконовая кислота:
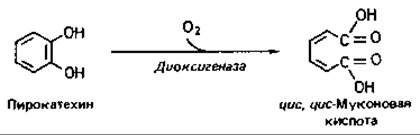
Пирокатехин расщепляется с помощью орто-пирокатехазы (кате- хол-1,2-диоксигеназы), а протокатеховая кислота - при участии протока- техат-3,4-диоксигеназы. Образующиеся при этом промежуточные продукты -цис,цис-муконовая кислота и 3-карбокси-цис,цис-муконовая кислота - в ходе дальнейшего катаболизма проходят через этап общего для них обоих продукта - 3-оксоадипиновой кислоты. Последняя активируется СоА-трансферазой и расщепляется с образованием сукцинил- СоА и ацетил-СоА, которые подвергаются дальнейшим превращениям в Ходе промежуточного обмена (рис. 14.10).
Мета-расщепление. Разрыв ароматического кольца между гидроксилированным и негидроксилированным атомами углерода (мета-расщепление, или экстрадиольное расщепление) тоже катализируется диоксигеназами. Продукты расщепления в этом случае - полуальдегиды 2-гидроксимуконовой кислоты (рис. 14.11), которые затем превращаются (в зависимости от замещений) в пируват, ацетальдегид, оксалоацетат, фумарат, ацетоацетат, сукцинат или иные промежуточные продукты, вовлекаемые в промежуточный метаболизм.
Проведенные исследования показали, что пути распада ароматических соединений чрезвычайно разнообразны. Варьировать могут и стадии, предшествующие их расщеплению, и характер самого расщепления. У некоторых бактерий даже от фазы и условий роста зависит, будут ли образовываться в клетках ферменты орто- или мета-расщепления. Некоторые псевдомонады расщепляют ароматические соединения, подвергшиеся распаду до пирокатехина, по opтo-пути, а расщепленные до протокатеховой кислоты - по мета-пути.
Конвергентные пути распада. В расщеплении ароматических соединений участвует достаточно большое число различных реакций. Разные пути распада в конце концов сходятся (конвергируют), приводя к образованию либо пирокатехина, либо протокатеховой кислоты (рис. 14.12 и 14.13). Поэтому на примере распада ароматических соединений можно изучать регуляцию конвергирующих путей катоболизма (разд. 16.1.1).
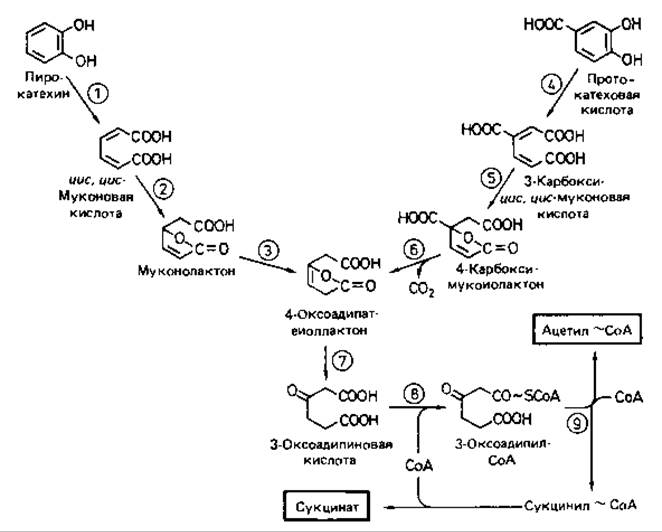
Рис. 14.10. Орто-расщепление ароматического кольца и путь 3-оксоадипиновой кислоты. Участвующие ферменты: 1 - пирокатехаза (катехол-1,2-диоксигеназа); 2 - муконатциклоизомераза; 3 - муконолактон-изомераза; 4 - протокатехат-3,4-диоксигеназа; 5 - 3-карбоксимуконат-циклоизомераза; 6 - 4-карбоксимуконолактон-декарбоксилаза; 7 - 4-оксоадипат-еноллактонгидролаза; 8 - 3-оксоадипат-сукцинил-СоА-трансфераза; 9 - 3-оксоадипил-СоА-тиолаза.
Нафталин, антрацен и другие полиароматические соединения. Некоторые бактерии способны расщеплять полициклические углеводороды, из которых мы упомянем лишь нафталин, антрацен и фенантрен. Если выращивать бактерии на среде, содержащей одно из этих соединений, то можно часто наблюдать выделение в культуральную жидкость салициловой кислоты; по-видимому, здесь происходят превращения, уже рассмотренные выше на примере расщепления моноциклических соединений (рис. 14.13).
Подводя итоги, можно сказать, что природные углеводороды частично или полностью окисляются микроорганизмами. При благоприятных условиях даже асфальт подвергается разложению, хотя и очень медленно. В почве, населенной микроорганизмами, окисляется даже графит.
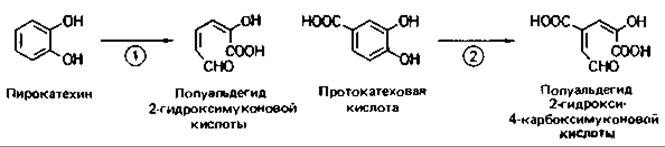
Рис. 14.11. Мета-расщепление ароматического кольца. Участвующие ферменты: 1 - метапирокатехаза (катехол-2,3-диоксигеназа); 2 - протокатехат-4,5-диоксигеназа.
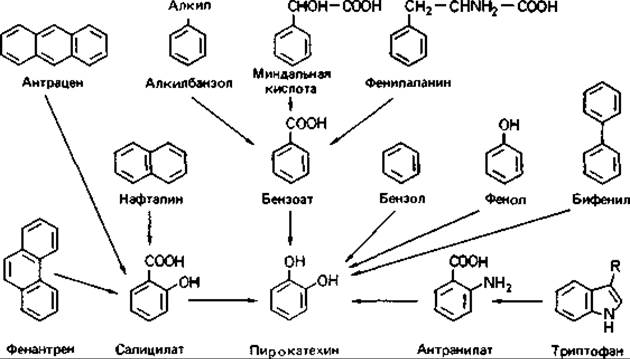
Рис. 14.12. Пути расщепления ароматических соединений, ведущие к образованию пирокатехина.
Загрязнение среды нефтью. В случае загрязнения почвы нефтью следует учесть, что в нестерильных аэрируемых почвах углеводороды быстро и полностью разлагаются. Только при сильном загрязнении и в отсутствие доступа воздуха или в тех случаях, когда нефть проникает в почву на большую глубину, возникает опасность, что она будет долго сохраняться здесь и в конце концов попадет в питьевую воду. Нефть, разлившаяся по поверхности моря, вначале представляет большую опасность для флоры и фауны, но затем тоже разлагается бактериями. При этом, однако, остаются алканы с длинной цепью, полиароматические углеводороды и смеси веществ, напоминающие асфальт; все эти вещества долгое время не поддаются биологическому воздействию.
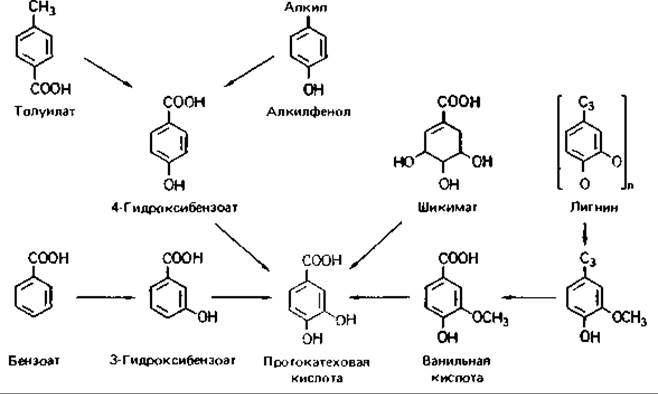
Рис. 14.13. Пути расщепления ароматических соединений, ведущие к образованию протокатеховой кислоты.
Чужеродные вещества. Чужеродные вещества (ксенобиотики), в особенности различные ядохимикаты (фунгициды, гербициды, инсектициды и нематоциды), после обработки ими почвы могут накапливаться в ней, так как при этом не развиваются микроорганизмы, способные разлагать и «обезвреживать» эти вещества.
Ароматические соединения с такими заместителями в кольце, как галогены, сульфогруппы и нитрогруппы, разлагаются крайне медленно и могут противостоять воздействию микробов на протяжении многих лет. Одно из самых стойких веществ - дихлордифенилтрихлорэтан (ДДТ). Неопасны, но, видимо, совершенно не поддаются микробному разложению пластмассы типа полиэтилена, полипропилена и т. п. Содержащиеся в них пластификаторы постепенно окисляются, но полимерный скелет остается.
Кометаболизм. По-видимому, некоторые соединения расщепляются микроорганизмами только совместно с хорошо утилизируемыми субстратами. Такое превращение какого-либо вещества, которое само по себе не может быть использовано, в присутствии так называемого косубстрата, т. е. вещества, используемого клетками для роста, получило название кометаболизма или соокисления. Явление кометаболизма может быть полезно, например, при очистке промышленных сточных вод, содержащих плохо поддающиеся разложению синтетические продукты, вместе со сточными водами из населенных пунктов в тех же самых водоочистных сооружениях.