ПІДРУЧНИК ІМУНОЛОГІЯ - Меркьюрі Поділля 2013
СТРУКТУРА І ПРИНЦИПИ ФУНКЦІОНУВАННЯ ІМУННОЇ СИСТЕМИ
У сучасній медицині імунологія зайняла значне місце як галузь, що розвивається, і на неї покладають надії лікарі різних спеціальностей. Клінічна імунологія - це клінічна і лабораторна дисципліна, яка займається обстеженням, діагностикою і лікуванням хворих з патологічними процесами, що розвиваються в результаті порушення імунних механізмів, а також тими випадками, коли імунологічні маніпуляції є важливою частиною терапії і (або) профілактики.
Порушення розвитку, диференціювання імунокомпетентних клітин, їх функціонування, синтезу їх продуктів або регуляції цих процесів ведуть до порушень імунологічних функцій. Ці порушення можуть залишатися безсимптомними або виявляються клінічно, і по тяжкості клінічні прояви коливаються від м'яких до фатальних. Такі порушення можуть стосуватися основних клітин імунної системи: Т- і В-лімфоцитів, фагоцитів, природних кілерів та їх продуктів: білків системи комплементу, імуноглобулінів, цитокінів.
Значна частина порушень пов'язана з природженими або придбаними дефектами продукції імунокомпетентних клітин або їх функцій. Інші випадки імунодефіцитів пов'язані з малігнизацією імунокомпетентних клітин та їх неконтрольованою проліферацією, надмірним накопиченням їх продуктів. Різноманітними можуть бути клінічні прояви порушень регуляції імунологічних функцій: нерегульованої активації системи комплементу, нерегульованої продукції і рецепції цитокінів.
Імунна система складається з таких органів: кістковий мозок, тимус, селезінка, лімфатичні вузли, скупчення лімфоїдної тканини. Розрізняють первинні - центральні (кістковий мозок і тимус) і вторинні - периферичні (селезінка, лімфатичні вузли, скупчення лімфоїдної тканини) органи імунної системи. Всі вони взаємозв'язані системою кровообігу, лімфотоку і єдиною системою імунорегуляції.
Імунітет - це еволюційно обумовлена сукупність реакцій взаємодії між системою імунітету і біологічно активними агентами (антигенами), що направлені на збереження фенотипічної постійності внутрішнього середовища (гомеостазу) організму.
Основні функції імунної системи: контроль за антигенним станом внутрішнього середовища організму, захист організму від патогенних мікроорганізмів і протипухлинний нагляд. У виконанні цих функцій беруть участь як механізми неспецифічного захисту, так і специфічна імунна відповідь на конкретні інфекційні або пухлинні антигени. Специфічна імунна відповідь підсилює механізми неспецифічного захисту, робить їх більш цілеспрямованими.
Органи імунної системи
Центральні органи імунної системи - кістковий мозок і тимус виконують найважливіші функції, забезпечуючи самооновлення імунної системи. У цих органах відбуваються процеси проліферації клітин-попередників, їх диференціювання і дозрівання, аж до виходу в циркуляцію і заселення периферичних органів імунної системи зрілими імунокомпетентними клітинами.
Кістковий мозок. Всі клітини крові, у тому числі імунокомпетентні клітини, походять з поліпотентної стволової клітини, яка дає початок різним паросткам кровотворення, зокрема, мієло-моноцитарному і лімфоцитарному. Напрям диференціювання ранніх попередників залежить від впливу їх мікрооточення, від впливу стромальних клітин кісткового мозку.
Дія окремих цитокінів на клітини-попередники в умовах in vitro проявляється стимуляцією зростання окремих колоній, що складаються з лейкоцитів певного типу. Звідси їх назва - колонієстимулюючі чинники: GM-CSF, G-CSF, M-CSF. Гранулоцитарно-моноцитарний чинник стимулює проліферацію ранніх загальних клітин-попередників мієло-моноцитопоезу, а також клітини-попередники кожного з паростків. Ще більш універсальним є так званий мульти-CSF (інтерлейкін-3), який стимулює всі паростки кровотворення. Продуцентами цих ростових чинників та інших цитокінів є стромальні клітини кісткового мозку, макрофаги і активовані лімфоцити. Інтерлейкін-1 і інтерлейкін-6 є синергістами колонієстимулюючих чинників в стимуляції, проліферації клітин-попередників та індукують продукцію ростових чинників.
Тимус (вилочкова залоза) є єдиним органом імунної системи, що піддається швидкій віковій інволюції. Протягом перших 50 років життя щорічно втрачається по 3% істинно тимічної тканини, яка поступово заміщається жировою і сполучною тканиною. Відповідно знижується і продукція Т-лімфоцитів. Найвища продукція Т-лімфоцитів зберігається до двох років життя, а потім швидко падає. Проте, слід зазначити, що кількість Т-лімфоцитів в циркуляції зберігається на досягнутому рівні. Річ у тому, що значну частину популяції Т-лімфоцитів складають клітини, які довго живуть і не потребують постійного оновлення. Тому чисельність Т-клітин може підтримуватися в дорослому організмі і у відсутності тимусу. Більш того, зрілі Т-лімфоцити піддаються, так званій «клональній експансії», тобто виборчій проліферації у відповідь на зустріч зі своїм антигеном, за рахунок чого їх чисельність зростає. Після створення пулу периферичних Т-лімфоцитів втрата тимусу вже не призводить до катастрофічного зниження імунітету. На користь цього говорять результати імунологічного обстеження дорослих людей, що перенесли тимектомію.
Периферичні органи імунної системи. Периферичні органи імунної системи - лімфатичні вузли, селезінка і лімфоїдна тканина, що асоціюється із слизовими оболонками, є місцем зустрічі антигенів з імунокомпетентними клітинами, місцем розпізнавання антигену і розвитку специфічної імунної відповіді, місцем взаємодії імунокомпетентних клітин, їх проліферації (клональної експансії), антиген-залежного диференціювання і місцем накопичення продуктів імунної відповіді.
Лімфатичні вузли функціонують як своєрідні фільтри лімфи, затримуючи мікроорганізми та інші частинки, що потрапили в лімфу. Разом з тим лімфовузли є місцем взаємодії імунокомпетентних клітин в ході специфічної імунної відповіді, місцем синтезу антитіл-імуноглобулінів, місцем, де розігруються події клітинно-опосередкованого імунітету.
Один лімфовузол має масу близько 1 грама, містить приблизно 2000 мільйонів лімфоцитів, що відповідає 25% всіх циркулюючих в крові лімфоцитів. Кожну годину з лімфовузла виходить в лімфу кількість лімфоцитів, еквівалентна його потрійній вазі. Велика частина (90%) клітин в цій еферентній лімфі є лімфоцитами, що покинули кров'яне русло на території цього лімфовузла. Мічені лімфоцити, введені в кров, знову опиняються в лімфі вже через декілька годин, досягаючи максимуму через 20 годин. Серед клітин лімфовузла близько 10% складають макрофаги і близько 1% - дендритні клітини.
Тканина лімфовузла складається із зовнішнього кортикального шару, в якому скупчення клітин утворюють фолікули, частково - із зародковими центрами, і внутрішнього мозкового шару з меншим вмістом лімфоцитів у поєднанні з макрофагами, які зосереджені по ходу лімфатичних і судинних синусів. Така структура лімфовузлів дає можливість вільної циркуляції і рециркуляції лімфоцитів між лімфою, кров'ю і тканинами. Певні зони лімфовузла заселяються строго певними клітинами.
Селезінка. В селезінці, як і в лімфовузлах, є Т-залежні і В-залежні зони. Періартеріолярними лімфоїдними скупченнями є Т-залежні зони. Селезінка є місцем розпізнавання антигену, антигензалежної проліферації і диференціювання Т- і В-лімфоцитів, їх активації, а також продукції і секреції специфічних антитіл імуноглобулінів. Основна відмінність селезінки від лімфовузлів полягає в тому, що селезінка є місцем специфічної імунної відповіді на антигени, які циркулюють в крові, а в лімфовузлах відбуваються процеси специфічної імунної відповіді на антигени, що потрапляють в лімфу. Крім того, селезінка з її багаточисельною мережею макрофагів в червоній пульпі виконує функції фільтру крові, що видаляє з крові чужорідні частинки і молекули, які потрапляють туди, а також постарілі еритроцити, або еритроцити, навантажені імунними комплексами .
Лімфоїдна тканина асоціюється із слизовими оболонками. Скупчення лімфоцитів, макрофагів та інших допоміжних клітин були виявлені у складі багатьох органів і тканин, особливо у складі слизових оболонок. Безпосередньо під мукозним епітелієм в тісному зв'язку з епітеліальними клітинами розташовуються лімфоцити Пейерових бляшок тонкого кишечнику, лімфоїдних фолікулів апендиксу, мигдалин глотки, лімфоїдних фолікулів підслизового шару верхніх дихальних шляхів і бронхів, сечостатевого тракту. Всі ці лімфоїдні скупчення отримали збірну назву - асоційована із слизовими оболонками лімфоїдна тканина (MALT від mucosal-associated lymphoid tissue).
Імунокомпетентні клітини. Імунокомпетентні клітини знаходяться в стані рециркуляції, тобто постійно відбувається обмін клітинами між кров'ю, лімфою і лімфоїдними органами. Це необхідно для реалізації специфічної імунної відповіді, оскільки імунна система повинна бути готова відповісти на будь-який з безлічі чужорідних антигенів, що потрапляє в будь-яку ділянку тіла. Оскільки кожен окремий антиген розпізнається лише дуже невеликою частиною популяції лімфоцитів, тільки постійна рециркуляція може створити умови для зустрічі кожного антигену з одиничними лімфоцитами, що несуть специфічні для нього антиген-розшукуючі рецептори. У органах імунної системи, де відбувається ця зустріч, відбувається взаємодія антиген-специфічних лімфоцитів з іншими клітинами, що виконують роль допоміжних, беруть участь в запуску імунної відповіді та в її ефекторній фазі. До допоміжних клітин відносяться дендритні клітини, мононуклеарні фагоцити, гранулоцити та ін.
В процесі диференціювання на мембранах клітин системи імунітету з'являються різні макромолекули - маркери, що відповідають певній стадії розвитку клітинних популяцій. У 1983 р. Перша міжнародна робоча нарада з антигенів диференціювання лейкоцитів ввела в практику клінічної імунології термін "clusters of differentiation" (кластери диференціювання, скорочено CD). З використанням моноклональних антитіл стало можливим провести кількісний аналіз популяцій клітин крові та класифікувати їх відповідно до наявності поверхневих CD-антигенів (від англ. - clusters of differentiation - кластери диференціювання).
У 1989 р. Четверта нарада прийняла робочу номенклатуру диференціровочних антигенів лімфоцитів людини. Моноклональні антитіла з фактично ідентичною специфічністю до даного мембранного антигену були згруповані і позначені відповідним номером кластера диференціювання (CD). Всі вони виконують функції рецепторів адгезинів, після взаємодії з якими всередину клітини поступає сигнал і відбувається її активація, супресія або навіть апоптоз.
CD3 - несуть зрілі (інтактні) Т-лімфоцити, забезпечує передачу сигналу від Т-клітинного антиген-специфічного рецептору (ТКР) в цитоплазму. Антигенспецифічний Т-клітинний рецептор, CD3 та інші корецептори складають комплекс, що розпізнає чужорідний антиген зв’язаний з молекулами головного комплекса гітосумісності I чи II класу (MHC I або II), в залежності від типу клітин (CD8 чи CD4).
CD4 - маркер Т-хелперів, корецепторна структура Т-клітинного рецептора; один з рецепторів вірусу імунодефіциту людини (ВІЛ); бере участь в розпізнаванні антигенів, що асоціюються з молекулами MHC II класу і є для них рецептором.
CD8 - маркер Т-супресорів і цитотоксичних лімфоцитів, його мають деякі NK-клітини; корецепторна структура Т-клітинного рецептора; залучається до розпізнавання антигенів за участю молекул MHC I класу, є рецептором для молекул MHC I класу.
CD14 - маркер моноцитів. CD14 розміщений на поверхні моноцитів і макрофагів і бере участь в активації цих клітин через Toll-подібний рецептор-4 (TLR4).
CD16 - маркер натуральних кілерів (NK-клітин), низькоафінний Fc-рецептор для IgG III типу. Ця молекула бере участь в антитілозалежній клітинній цитотоксичності, здійснюваною NK. Окрім NK-клітин ця молекула представлена в більшості нейтрофілів.
CD19 - мають пре-В-лімфоцити і В-лімфоцити, він є частиною їх рецепторного комплексу, залучається до їх активації (сигнал трансдукції, асоційований з CD21). CD19 не виявляється на лімфоїдних клітинах інших типів.
CD21 - рецептор для компонента комплементу C3d. Можливо ця молекула сприяє рецептор-опосередкованому поглинанню антигену В-клітиною. Молекула CD21 є також рецептором для вірусу Епштейн- Бара. Цей маркер експресований на всіх зрілих В-клітинах і фолікулярних дендритних клітинах. CD21 може бути використаний для кількісної оцінки В-лімфоцитів.
CD22 - експресований на зрілих В-лімфоцитах, молекулах адгезії, бере участь в негативній регуляції В-клітин.
CD25 - а-ланцюг рецептора IL2, з'являється тільки при активації клітини і в результаті формується високоафінний рецептор IL2. CD25 (маркер активації) експресують різні типи клітин периферичної крові: CD4+, CD8+, NK, CD4+NKT-клітини, В-лімфоцити, моноцити. CD25+ клітини в нормі можуть складати до 18% від загальної популяції лімфоцитів.
CD56 - адгезійна молекула NCAM (neural cell adhesion molecule). Окрім природних кілерів CD56 експресується на багатьох типах клітин, у тому числі на Т-лімфоцитах.
CD69 та CD95 є на клітинах з ознаками апоптозу.
CD45 - антиген, представлений на поверхні усіх лейкоцитів людини, за своєю природою є тирозинфосфатазою. Рівень експресії CD45 наростає у міру диференціювання гемопоетичних клітин від незрілих попередників до зрілих форм. Максимальний рівень CD45 виявлений на зрілих лімфоцитах, проміжний на клітинах мієлоїдного ряду. Існує 3 ізо-форми CD45:
- CD45RO - експресується на ефекторних Т-клітинах, Т-клітинах пам'яті, В-клітинах, моноцитах і макрофагах.
- CD45RA - експресується на наївних Т-клітинах, В-клітинах, моноцитах.
- CD45RB - представлений на Т, В-лімфоцитах, моноцитах, гранулоцитах.
У таблиці 1 представлені відомі на сьогоднішній день кластери диференціювання, що визначені в клітинах імунної системи за допомогою моноклональних антитіл.
Таблиця 1. Перелік кластерів диференціювання, визначених в клітинах імунної системи за допомогою моноклональних антитіл
Антиген |
Ліганд |
Клітини, що несуть антиген |
Функції антигену |
Маркери T-лімфоцитів |
|||
CD1 |
- |
T-лімфоцити коркового слою тимусу (тімоцити) та дендрітні клітини Лангерганца |
Пов'язаний з бета2-мікроглобуліном, бере участь в представленні антигену незрілим T-лімфоцитам |
CD2 |
LFA-3 |
T-лімфоцити та NK- клітини, Е-РОК |
Рецептор до еритроцитів барана, бере участь в активації T-лімфоцитів |
CD3 |
- |
зрілі T-лімфоцити, рецептор для антигену на Т-клітинах |
Пов'язаний з антиген-розпізнаючим рецептором T-лімфоцитів, бере участь в їх активації |
CD4 |
MHC II класу |
T-хелпери/індуктори, моноцити |
Присутній на T-хелперах, забезпечує їх взаємодію з макрофагами |
CD5 |
CD72 |
T- і B-лімфоцити |
Присутній на зрілих T-лімфоцитах і незначній частині B-лімфоцитів, з'являється на лейкозних B-лімфоцитах при хронічному лімфолейкозі |
CD6 |
зрілі Т-лімфоцити |
||
CD7 |
- |
T-лімфоцити, тімоцити, NK-клітини (частина) |
Присутній на кістково-мозкових попередниках T-лімфоцитів і зрілих T-лімфоцитах |
CD8 |
MHC I класу |
T-супресори/кілери та NK-клітини (частина) |
Присутній на цитотоксичних T-лімфо- цитах, забезпечує їх взаємодію з клітинами-мішенями |
CD16 |
NK-клітини |
||
CD19 |
незрілі та зрілі В-лімфоцити |
||
CD20 |
зрілі В-лімфоцити |
||
CD22, CD23 |
B-клітини мигдалин, 70% B-клітин крові |
||
CD25 |
Інтерлейкін-2 |
T-, B- і NK-лімфоцити, моноцити |
Альфа-ланцюг рецептора до інтерлейкіну-2 (p55), маркер активованих T- і B-лімфоцитів |
CD28 |
CD80 |
T-лімфоцити |
Бере участь в активації T-лімфоцитів |
CD29 |
Фібро-нектин |
T-лімфоцити |
Забезпечує адгезію до позаклітинного матриксу, маркер активованих Т-лімфоцитів |
CD38 |
- |
T- і B-лімфоцити, активовані В-лімфоцити |
Присутній на T-лімфоцитах кіркової речовини тимусу, активованих T-лімфоцитах, незрілих B-лімфоцитах і плазматичних клітинах, бере участь в регуляції функцій B-лімфоцитів |
CD43 |
ICAM-1 |
T- і B-лімфоцити, гранулоцити, моноцити |
Бере участь в активації T-лімфоцитів |
CD45 |
- |
Всі лейкоцити |
Бере участь в активації лімфоцитів, внутрішньоклітинна частина рецептора є тирозинкіназою |
CD45RO |
- |
T- і B-лімфоцити, гранулоцити, моноцити |
Маркер клітин пам'яті (лімфоцитів CD4), ефекторних клітин |
CD45RA |
- |
Всі лейкоцити |
Маркер Т і В-лімфоцитів та моноцитів |
CD45RB |
- |
Т- і В-лімфоцити, моноцити, гранулоцити |
Маркер зрілих Т і В-лімфоцитів та моноцитів |
CD71 |
Трансферин |
T-лімфоцити, моноцити |
Рецептор трансферину, маркер активованих T-лімфоцитів |
Маркери B-лімфоцитів |
|||
Поверхневі імуноглобуліни |
Антиген |
B-лімфоцити |
Присутні тільки на зрілих B-лімфоцитах |
CD10 |
- |
B-лімфоцити |
Присутній на незрілих B-лімфоцитах, з'являється на лейкозних клітках при гострому лімфолейкозі |
CD19 |
- |
B-лімфоцити |
Присутній на пре-П-лімфоцитах і на всіх зрілих B-лімфоцитах, бере участь в активації B-лімфоцитів |
CD20 |
- |
B-лімфоцити |
Присутній на всіх B-лімфоцитах |
CD21 |
C3d, CD23 |
B-лімфоцити |
Рецептор до комплементу і вірусу Епштейн-Бара |
CD23 |
IgE |
B- і T-лімфоцити, моноцити, еозинофіли |
Низькоафінний рецептор до Fc-фрагменту IgE |
CD32 |
IgG |
B-лімфоцити, гранулоцити |
Нізькоафінний рецептор до Fc-фрагменту IgG |
CD40 |
gр39 |
B-лімфоцити |
Стимулює проліферацію B-лімфоцитів, за будовою схожий з CD27 і рецептором чинника некрозу пухлин |
CD72 |
CD5 |
B-лімфоцити |
З’являється на кістково-мозкових попередниках B-лімфоцитів, бере участь в їх диференціюванні |
HLA-DR |
Антиген, CD4 |
B- і T-лімфоцити, моноцити |
Антиген MHC II класу, бере участь в представленні антигену T-хелперам і їх активації, маркер активованих T-лімфоцитів |
Маркери моноцитів і макрофагів |
|||
CD11a |
ICAM-1 |
Всі лейкоцити |
Альфа-ланцюг LFA-1, бере участь в міжклітинній адгезії |
CD11b |
C3bi, фібронектин |
Моноцити, гранулоцити, NK-лімфоцити |
Альфа-ланцюг CR3, бере участь в міжклітинній адгезії |
CD11c |
C3bi |
Моноцити, гранулоцити, B- і NK-лімфоцити |
Альфа-ланцюг CR4, бере участь в міжклітинній адгезії |
CD14 |
TLR4 |
Моноцити, макрофаги |
Приймає участь в активації цих клітин через Toll-подібний рецептор-4 |
CD18 |
- |
Всі лейкоцити |
Бета-ланцюг рецепторів CD11a/CD18, CD11b/CD18, CD11c/CD18, бере участь в міжклітинній адгезії |
Маркери NK-лімфоцитів |
|||
CD3 |
- |
Зрілі NK- і Т-лімфоцити |
|
CD16 |
Fc-фрагмент IgG |
NK-лімфоцити, моноцити і гранулоцити |
Низькоафінний рецептор IGG |
CD56 |
- |
NK- і T-лімфоцити |
Присутній на частині T-лімфоцитів, бере участь в міжклітинній адгезії, NCAM (neural cell adhesionmolecule) |
CD57 |
- |
NK- і T-лімфоцити |
Присутній на частині лімфоцитів CD8, при деяких вірусних інфекціях збільшується число лімфоцитів, що несуть одночасно CD8 і CD57 |
Примітка: (-) - невідомий або відсутній; CR - рецептор до компонентів комплементу; ICAM - молекули міжклітинної адгезії (Inter Cellular Adhesion Molecule); LFA - лімфоцитарний функціональний антиген (Lymphocyte Function-associated Antigen).
Лімфоцити - це єдині клітини організму, здатні специфічно розпізнавати і розрізняти різні антигени і відповідати активацією на контакт з певним антигеном. При схожій морфології малі лімфоцити діляться на дві популяції, що мають різні функції і продукують різні білки.
В-лімфоцити. Одна з популяцій лімфоцитів отримала назву В-лімфоцити, від назви органу "бурса Фабріциуса", де було вперше виявлено дозрівання цих клітин у птахів. Маркер CD20 представлений на В-клітинах всіх стадій розвитку В-лімфоцитів. У людини В-лімфоцити дозрівають в кістковому мозку. В-лімфоцити розпізнають антигени специфічними рецепторами імуноглобулінової природи (CD19-22), які у міру дозрівання експресуються на їх мембранах. Взаємодія антигену з такими рецепторами є сигналом активації В-лімфоцитів, та їх антиген- залежного диференціювання в плазматичні клітини, що активно продукують і секретують специфічні для даного антигену антитіла - імуноглобуліни.
При дозріванні В-лімфоцити змінюють клас імуноглобулінів, які синтезуються ними. Спочатку В-лімфоцити синтезують імуноглобуліни класу М (IgM), при дозріванні 10 % В-лімфоцитів продовжують синтезувати IgM, 70 % перемикаються на синтез IgG, а 20 % - на синтез IgA. Наступна експресія поверхневого IgD означає, що клітина готова до стимуляції антигеном. Деякі клітини, таким чином, несуть поверхневі Ig трьох різних класів: M, G і D або M, A і D, але усі молекули Ig на одній клітині мають однаковий ідіотип і, отже, кодуються одними і тими ж генами V(H) і V(L). Після стимуляції антигеном поверхневий IgD втрачається і у клітин пам'яті не виявляється. Антигенна структура зрілого В-лімфоциту: CD19, CD20, CD21, CD45R, CD40, MHC II кл., IgM, IgD. Окрім молекул рецепторного комплексу на поверхні В-клітин експресуються молекули гістосумісності MHC II кл., оскільки В-лімфоцити є антиген-презентуючими клітинами.
В-лімфоцити складаються з декількох субпопуляцій:
1) В1 - лімфоцити - попередники плазмоцитів, несуть на мембрані диференційований антиген CD5+, синтезують антитіла IgM після контакту з антигеном без взаємодії з Т-лімфоцитами;
2) В2 - лімфоцити - попередники плазмоцитів, проходять диференціювання в кістковому мозку від стовбурової клітини до попередників В- лімфоцитів під впливом ростових чинників, інтерлейкінів (IL-1, 4, 6) синтезують імуноглобуліни усіх класів після контакту з антигеном у відповідь на взаємодію з Т-хелперами. Ці клітини забезпечують гуморальний імунітет на антигени, розпізнавані Т-хелперами;
3) В3-лімфоцити (К-клітини), або В-кілери, вбивають клітини-антигени, покриті антитілами. Відносяться до великих гранулярних лімфоцитів, здатних розпізнавати (як і T-клітини) зміни клітинної поверхні, які виникають при злоякісному переродженні чи вірусній інфекції. Крім того, на відміну від цитотоксичних T-лімфоцитів, вони ефективно розпізнають клітини, поверхня яких не має молекул MHC або частково їх втратила;
4) В-супресори гальмують функцію Т-хелперів, а В-лімфоцити пам'яті, зберігаючи і передаючи пам'ять про антигени, активно синтезують певні імуноглобуліни при повторній зустрічі з антигеном.
Особливістю В-лімфоцитів є те, що вони спеціалізуються на конкретних антигенах. При реакції В-лімфоцитів з антигеном, що зустрічається уперше, утворюються плазмоцити, які виділяють антитіла саме проти цього антигену. Утворюються клони В-лімфоцитів, відповідальні за реакцію з цим конкретним антигеном. При повторній реакції розмножуються і синтезують антитіла тільки В-лімфоцити, а точніше - плазмоцити, спрямовані проти цього антигену. Інші клони В-лімфоцитів не беруть участь в реакції. В-лімфоцити безпосередньо не приймають участь в боротьбі з антигенами. Під впливом стимулів від фагоцитів і Т-хелперів вони трансформуються в плазмоцити, які і синтезують антитіла імуноглобуліни, які знешкоджують антигени.
Т-лімфоцити отримали свою назву у зв'язку з їх диференціюванням у тимусі. Зрілі Т-лімфоцити (CD2, CD3) на відміну від незрілих (тимоцитів - CD2) здатні відповідати проліферацією на Т-клітинні мітогени. За функціями серед Т-лімфоцитів розрізняють ефекторні (CD8 цитотоксичні лімфоцити - CTL, T-кілери) і регуляторні (CD4+ Т-хелпери-Th) субпопуляції.
Т-хелпери стимулюють проліферацію і диференціювання цитотоксичних лімфоцитів, В-клітин і утворення антитіл. Тобто, Т-хелпери мають хелперну функцію (стимулюють В-лімфоцити для продукції імуноглобулінів) і індукторну функцію (стимулюють проліферацію і диференціювання цитотоксичних лімфоцитів, що відповідають на розчинні антигени проліферацією і продукцією лімфокінів).
Внутрішньоклітинні паразити, здатні вижити усередині макрофагів, руйнують механізми знищення, властиві цим клітинам. Проте такі мікроорганізми не здатні перешкодити макрофагам переробити невеликі фрагменти антигенів (неповний фагоцитоз) і експонувати їх на своїй поверхні (процесінг). T-хелпери, відзначені цими антигенами, здатні впізнавати комбінацію з антигену і молекули MHC II класу на поверхні макрофага і зв'язуватися з нею (антигенпредставлення), а потім продукувати цитокіни (інтерферон-у), які активують макрофаги, запускаючи пошкоджені раніше мікробіцидні механізми макрофагів, і викликають загибель внутрішньоклітинних мікроорганізмів - повний фагоцитоз (рис. 1).
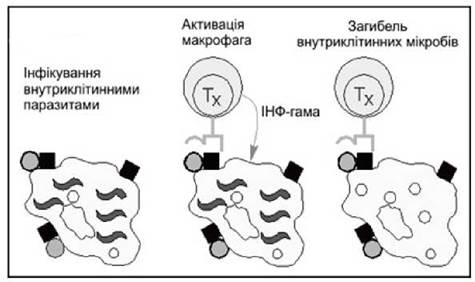
Рис. 1. Активація макрофагів Т-хелперами.
Примітка: кружки - поверхневий мікробний антиген; квадрати - молекули MHC класу II, хвилясті лінії - внутрішньоклітинні паразити.
Існує дві субпопуляції CD4+ Т-хелперів - Т-хелпери 1 і 2 типів, що не мають відмінностей за антигенною структурою, але розрізняються за набором (профілем) цитокінів, які вони здатні синтезувати у відповідь на антигенну стимуляцію, і від цього профілю залежить, який з двох основних типів імунної відповіді буде реалізований (клітинний або гуморальний).
Т-хелпери 1 типу (Th1) мають диференційні антигени CD3, CD4, CD29, CD45Ra. Це - активатори клітинного імунітету, натуральних кілерів і моноцитів. Якщо наївна Т-клітина розпізнає антиген, що презентується макрофагом, то вона трансформується в T-хелпер 1 типу. На цій клітині з’являються маркери диференціювання CD25 та CD45RB. Функція таких клітин - посилення активності макрофагів, спрямованої на знищення захопленого антигену, або приведення його в імуногенну форму.
Продукуючи інтерлейкіни-2, 3, 12, ІФН-γ і ФНО-β, ГМ-КСФ, вони викликають активацію цитотоксичних Т-лімфоцитів, натуральних кілерів, макрофагів та Т-ефектори гіперчутливості уповільненого типу. Thl забезпечують імунітет проти вірусів, внутріклітинних бактерій і онкогенних клітин. Активність Thl подавляє інтерлейкін-10.
Т-хелпери 2 типу (Th2) мають диференційовочні антигени CD3, CD4, CD29, CD45Ra і відповідають за кооперацію з В-клітинами. Якщо Т-клітина розпізнає антиген, що розміщений на поверхні В-лімфоцитів, то це розпізнавання є сигналом до трансформації в Т-хелпери 2 типу, які забезпечують посилення продукції антитіл. На цій клітині з’являються маркери диференціювання CD25 та CD45RB. Продукуючи інтерлейкіни 4, 5, 6, 10 та 13, вони активують гуморальну імунну відповідь, В-лімфоцити і алергічне запалення. Стимулюючи продукцію плазматичними клітинами імуноглобулінів IgM, IgG4 і IgA, Th2, забезпечують імунітет проти звичайних (позаклітинних) бактерій і їх токсинів. Активація еозинофілів, тучних клітин і стимуляція синтезу імуноглобуліну Е (IgE) веде до розвитку алергії. Активність Th2 подавляє ІФН-γ.
T-лімфоцити, що несуть на своїй поверхні антигени CD8, мають супресорну (щодо В-лімфоцитів і продукції ними імуноглобулінів) і цитотоксичну активність.
CD8 Т-супресори гальмують розвиток імунної відповіді як на власні, так і на чужі антигени, забезпечуючи імунологічну толерантність.
Цитотоксичні CD8 Т-лімфоцити (CD8+ CTL, T-кілери) - це ефектори клітинної імунної відповіді, що забезпечують руйнування чужорідних клітин.
Особливість Т-клітинного рецептору - здатність розпізнавати чужорідний антиген тільки в комплексі з власними клітинними антигенами на поверхні допоміжних антиген-представлених клітин (дендритних або макрофагів). На відміну від В-лімфоцитів, здатних розпізнавати антигени в розчині і зв'язувати білкові, полісахаридні і ліпопротеїдні розчинні антигени, Т-лімфоцити можуть розпізнати тільки короткі пептидні фрагменти білкових антигенів, представлені на мембрані інших клітин в комплексі з власними антигенами головного комплексу гістосумісності. CD4 Т-лімфоцити здатні розпізнавати антигенні пептиди в комплексі з антигенами гістосумісності (mane compartable complex) MHC II класу, а CD8 Т-лімфоцити здатні розпізнавати антигенні пептиди в комплексі з антигенами гістосумісності MHC I класу.
Натуральні кілери (CD3-CD16+CD56+, NK-клітини) є субпопуляцією лімфоцитів, відрізняються від Т-лімфоцитів відсутністю Т-клітинного рецептора (ТКР-). Активовані NK можуть нести на своїй поверхні CD25, HLA - DR, інтегріни, CD69, трансфериновий рецептор CD71, NK-рецептори. Їх морфологічні ознаки - крупні розміри і наявність гранул в цитоплазмі є підставою для їх другої назви - великі гранулярні лімфоцити (ВГЛ). На відміну від Т-клітин літична активність NK-клітин проявляється при первинному контакті без попередньої сенсибілізації. Їх основна функціональна характеристика - здатність вбивати деякі пухлинні клітки. В периферичній крові NK-клітини складають від 5 до 20% циркулюючих лімфоцитів.
NK-клітини розвиваються незалежно від Т- і В-лімфоцитів і не несуть характерних для Т- і В-лімфоцитів поверхневих маркерів. Їх поверхневий фенотип: ТКР-, CD3-CD16+CD56+, але вони мають деякі загальні з Т-лімфоцитами сигнальні молекули: CD2, окремі компоненти CD3, α-ланцюг CD 8.
Природні регуляторні Т-клітини - Treg (CD3+CD4+CD25+) Treg - підклас CD4+ Т-лімфоцитів, які можуть антигенспецифічно пригнічувати Т-клітинну імунну відповідь. Ці клітини контролюють імунну відповідь при трансплантації органів і тканин. Природні Treg здатні відповідати як на власні, так і на мікробні агенти.
Специфічних поверхневих маркерів Treg не описано. Від звичайних активованих Т-лімфоцитів Treg можна відрізнити за додатковими фенотипічними ознаками. На активованих Т-клітинах з'являється CD40L (CD154) - молекула, яка необхідна для контакту з антиген-пред ставленими клітинами, відсутня ізоформа CD45RO. Природні Treg в периферичній крові мають наступний фенотип: CD4+, CD25+, CD45RO+, CD62L+, CD122, CD152+, GITR - glucocorticoid - induced TNF - R family.
Мононуклеарні фагоцити (CD14, CD64). Система мононуклеарних фагоцитів, яка включає кістково-мозкові попередники, що походять з єдиної стволової клітини, - монобласт і промоноцит, циркулюючий в крові моноцит і зрілі тканинні макрофаги. Мононуклеарні фагоцити забезпечують природжений неспецифічний захист організму за рахунок своєї фагоцитарної функції.
Основні функції макрофагів: фагоцитоз корпускулярних часток, мікроорганізмів (важливий клітинний фактор природного резистентності - «професійні сміттярі»), секреція біологічно активних речовин, презентація антигену. Біологічна функція макрофагів полягає в тому, що вони фагоцитують антиген і представляють його лімфоцитам, беруть участь в індукції запалення, в цитотоксичної протипухлинному імунітеті, в процесах регенерації і інволюції, в гуморальній і клітинному імунітеті.
Молекули, що секретуються макрофагами, виконують ефекторні і регуляторні функції. При формуванні специфічної імунної відповіді макрофаги виконують функцію презентації антигену.
Для цього захоплений макрофагами антиген піддається переробці у фаголізосомах. Пептидні фрагменти антигену, що утворюються в результаті обмеженого протеолізу, комплексуються з молекулами антигенів головного комплексу гістосумісності класу 2 і виставляються на мембрані макрофага у формі, доступній для розпізнавання Т-лімфоцитами.
Макрофаги постійно дозрівають з циркулюючих в крові моноцитів, що мають кістково-мозкове походження. Покидаючи кров'яне русло, дозріваючі макрофаги мігрують в різні тканини організму. У легенів вони представлені альвеолярними макрофагами. Велика кількість макрофагів знаходиться в сполучній тканині, в лімфовузлах і лімфоїдній тканині, що асоціюється із слизовими оболонками, зокрема із слизовими оболонками повітряносних шляхів. Оновлення тканинних макрофагів відбувається в основному за рахунок рекрутування моноцитів з крові.
Дендритні клітини і клітини Лангерганса мають кістково-мозкове походження. Розрізняють фолікулярні й інтердигітальні дендритні клітини. Перші виявляють у В-зонах лімфатичних вузлів і селезінки, вони мають на своїй поверхні рецептор до Fc-фрагмента імуноглобулінів, але позбавлені антигенів МНС класу II, вони презентують антиген В-лімфоцитам. Інтердигітальні дендритні клітини містяться в Т-клітинних ділянках лімфатичних вузлів і селезінки, мають на своїй поверхні антигени МНС класу II, але не містять рецептори до Fc-фрагмента, беруть участь у презентації антигену для Т-лімфоцитів.
Гранулоцити. В ефекторній фазі специфічної імунної відповіді можуть брати участь й інші лейкоцити крові: гранулоцити або поліморфноядерні лейкоцити. Ці клітини складають першу лінію неспецифічного протимікробного захисту. Вони першими мобілізуються у вогнище запалення або інфекції і від їх фагоцитарної активності залежить елімінація збудників. Їх мобілізація з кров'яного русла різко підвищується під впливом цитокінів макрофагального походження (інтерлейкін-8) або С5а-фракції активованої системи комплементу. Інші продукти макрофагів активують функції гранулоцитів (туморнекротизуючий фактор).