Клінічна імунологія та алергологія - О.М. Біловол 2011
Вторинні імунодефіцитні стани
Актуальність теми: Здатність імунної системи організму протистояти різним інфекційним чинникам (бактерії, віруси, грибки) є невід’ємною частиною процесу виживання людини. Здатність організму людини протидіяти різним мікроорганізмам обумовлена двома механізмами: неспецифічною протиінфекційною резистентністю, яка направлена на безліч інфекційних агентів, і розвитком специфічного набутого імунітету до конкретних мікроорганізмів.
Набута резистентність популяції виникає через адаптивний імунітет у більшої частини населення після вакцинації або перенесеної інфекції. Сприйнятливість для всіх інфекцій є індивідуальною і завжди обумовлена недостатністю імунітету до інфекту. Якщо є резистентність - імунітет, то не виникають навіть особливо небезпечні інфекції.
Умовно-патогенні бактерії і грибки індукують інфекційний процес в організмі з нормальними захисними механізмами лише тоді, коли співвідношення інфікуючої дози на одиницю захисного чинника, наприклад, на один фагоцит, перевищуватиме якийсь критичний рівень, тобто при відносному імунодефіциті. У такій ситуації фагоцит не в змозі поглинути і перетравити дане число мікробів. Зазвичай інфекції, що реалізовуються умовно-патогенними мікробами, виникають у людей з дефіцитами у системі імунітету, і для цього достатньо невеликої дози мікроорганізмів, котрі не інфікують людей з нормальною системою імунітету, - тобто йдеться про абсолютний імунодефіцит.
У зв’язку з цим з’ясування причин ослаблення імунологічного захисту організму, імунологічна характеристика станів, що супроводжуються порушенням імунної відповіді, і розробка методів їх імунологічної корекції є важливим завданням діагностики і лікування вторинний імунодефіцитів.
Загальна мета: Навчитися діагностувати, розуміти причини виникнення і механізми розвитку, методи імунологічної діагностики і імунотерапії вторинних імунодефіцитів.
Конкретні цілі: |
Початковий рівень знань-умінь: |
1. Визначення, причини, механізми розвитку, діагностика вторинних імунодефіцитів. 2. Скласти програму обстеження хворого. 3. Знайомство з класифікацією вторинних імунодефіцитів. 4. Визначити тяжкість клінічних проявів і навчитися диференціювати симптоматику того або іншого вторинного імунодефіциту. 5. Поставити діагноз і визначити ускладнення первинних імунодефіцитів. 6. Характеристика основних видів вторинних імунодефіцитів. 7. Роль вторинних імунодефіцитів у патогенезі різних захворювань. 8. Раннє виявлення в організмі вторинної імунної недостатності. 9. Визначити тактику лікування і профілактики вторинного імунодефіциту з урахуванням клінічних проявів і особливостей перебігу. 10. Синдром підвищеної втоми; синдром хронічної втоми. |
1. Збір скарг, анамнезу, проведення об’єктивного обстеження пацієнтів з вторинними імунодефіцитними станами. 2. Інтерпретація результатів лабораторних досліджень (гемограми й імунограми). 3. Виявлення в анамнезі, об’єктивних даних та імунограмі ознак, що вказують на можливість наявності вторинного імунодефіциту. 4. Визначати імунопатогенетичні чинники у розвитку вторинного імунодефіциту (ВІЛ; герпес-вірусній, хламідійній інфекції, інфекційному мононуклеозі). 5. Уявлення про методи лікування вторинних імунодефіцитів 6. Розуміння динаміки основних показників лейкограми та імунограми при вторинних імунодефіцитах. 7. Демонструвати володіння морально-деонтологічними принципами медичного фахівця і принципами професійної субординації. |
Завдання для перевірки початкового рівня знань
1. Які фактори можуть бути причиною розвитку вторинного імунодефіциту?
A. Недостатність харчування.
B. Важкі інфекційні захворювання.
C. Тривалі хронічні рецидивуючі інфекції.
D. Опромінення.
E. Введення великої кількості кортикостероїдних препаратів.
F. Введення цитотоксичних агентів.
G. Жоден з перерахованих факторів.
2. Розвиток вторинного імунодефіциту може бути обумовленим:
A. Ферментопатіями, у тому числі обумовленими недостатнім надходженням в організм або порушенням зв'язування в організмі іонів заліза.
B. Імунодепресивною дією вірусів та їх токсинів.
C. Зниженням функціональної активності макрофагів при хронічних інфекціях.
D. Ураженням лімфатичних судин у результаті впливу мікробів та їх токсинів.
E. Появою у плазмі крові факторів, що блокують бласттрансформацію лімфоцитів.
F. Розвитком лімфопроліферативних захворювань.
G. Жодна з перерахованих причин не може призвести до розвитку вторинного імунодефіциту.
3. Які клінічні ознаки характерні для хворих з недостатністю Т-клітинного імунітету?
A. Підвищена чутливість до вірусних інфекцій.
B. Схильність до новоутворень лімфоїдного або епітеліального походження.
C. Зміна показників Т-клітинного імунітету.
D. Зміна показників гуморального імунітету.
4. З якими патологічними станами і захворюваннями, пов'язаними з імунодепресією, необхідно диференціювати СНІД?
A. З уродженим імунодефіцитом
B. Із злоякісною пухлиною лімфоретикулярної системи.
C. З важкою білково-енергетичною недостатністю.
D. З жодним із перерахованих патологічних станів.
5. У чому полягає системна відповідь на інфект при сепсисі?
A. У неконтрольованому викиді цілого комплексу медіаторів.
B. У зменшенні кількості лімфоцитів.
C. У викиді цілого комплексу прозапальних та протизапальних цитокінів.
D. В інактивації системи комплементу.
E. В активації системи макрофагів, лімфоцитів та ендотелію.
6. Які фактори захисту частіше всього можуть бути порушені при вторинному імунодефіциті?
A. Механічний захист від проникнення інфекційного збудника в організм.
B. Гуморальні фактори, які руйнують збудник, що потрапив в організм.
C. Фактори фагоцитозу.
D. Жоден з перерахованих варіантів.
7. При обстеженні хворих для оцінки імунного статусу необхідно:
A. Дослідження клітинного імунітету.
B. Дослідження гуморального імунітету.
C. Дослідження системи комплементу.
D. Дослідження всіх параметрів.
8. Імунологічне обстеження хворих здійснюється як:
A. Одноразове обстеження хворого під час вступу до клініки.
B. Двократне обстеження хворого.
C. Імунологічний моніторинг за перебігом захворювання.
D. Імунологічне обстеження у динаміці при використанні імунотропної терапії.
9. Завдання імунологічного обстеження хворих у клініці:
A. Імунодіагностика.
B. Прогнозування перебігу захворювання.
C. Контроль за якістю лікування.
D. Призначення імунорегулюючої терапії за показаннями.
10. Які чинники зовнішнього середовища сприяють розвитку вторинних імунодефіцитів:
A. Тривалі стреси.
B. Несприятливі кліматичні чинники.
C. Бактерії.
D. Віруси.
Вірні відповіді на питання: 1 - ABCDEF; 2 - ABCDEF; 3 - ABC; 4 - ABC; 5 - A; 6 - ABC; 7 - D; 8 - CD; 9 - ABCD; 10 - ABCD.
Джерела учбової інформації
1. Клінічна імунологія та алергологія: Підручник / [Г. М. Дранік, О. С. Прилуцький, Ю. І. Бажора та ін.]; за ред. проф. Г. М. Драніка. - К.: Здоров’я, 2006. - 888 с.
2. Казмірчук В. Є. Клінічна імунологія і алергологія / В. Є. Казмірчук, Л. В. Ковальчук. - Вінниця: Нова книга, 2006. - 504 с.
3. Андрєйчин М. А. Клінічна імунологія та алергологія: Підручник/Андрєйчин М. А., Чоп’як В. В., Господарський І.Я. - Тернопіль: Укрмедкнига, 2005. - 372 с.
4. Клиническая иммунология и аллергология: Учебное пособие / под ред. А. В. Караулова. - М.: Медицинское информационное агентство, 2002. - 651 с.
5. Никулин Б. А. Оценка и коррекция иммунного статуса / Никулин Б. А. - М.: ГЭОТАР-Медиа, 2007. - 376 с.
6. Бурместер Г. Р. Наглядная иммунология, пер с англ. / Бурместер Г. Р. - М.: БИНОМ. Лаборатория знаний, 2007. - 329 с.
7. Змушко Е. И. Клиническая иммунология: руководство для врачей / Змушко Е. И. - СПб: "Питер", 2001. - 576 с.
8. Бобкова М. Р. Иммунитет и ВИЧ-инфекция / Бобкова М. Р. - М.: Олимпия Пресс, 2006. - 240 с.
9. Шувалова Е. П. Инфекционные болезни / Шувалова Е. П. - М.: Медицина, 2001. - 324 с.
Недостатність імунітету та інфекції
Інфекція (інфекційний процес) - патологічний процес в організмі, що виникає внаслідок взаємодії між патогенним мікроорганізмом і клітинами та тканинами неімунного, чутливого макроорганізму, супроводжується розмноженням мікроорганізму, зміною реактивності макроорганізму, пошкодженням тканин. Інфекція - це один з можливих результатів взаємодії мікро- і макроорганізму. Іншим, ймовірно, частішим, є природна резистентність, виникнення імунітету або його посилення (за наявності).
Для виникнення інфекційного процесу необхідно три основні умови: патогенний збудник, проникнення його у внутрішні середовища організму, сприйнятливість макроорганізму. Причому розвиток інфекційного процесу визначається ступенем вираженості трьох названих умов. За першої умови, воно залежить від дози і вірулентності збудника, за другої - від стану природних бар’єрів макроорганізму і місця проникнення збудника, за третьої - від резистентності - імунітету макроорганізму.
Хоча індукція та інтенсивність інфекційного процесу і залежать від дози, вірулентності, шляху проникнення збудника, проте головним є ступінь недостатності природного або набутого імунітету макроорганізму. Саме недостатність імунітету - відносний (до даного збудника) або абсолютний імунодефіцит, у кожній конкретній ситуації служить визначальним чинником розвитку інфекції.
Тому інфекційна хвороба - це, перш за все, імунодефіцитна хвороба в індивіда, у якого патогенність інфекту, що проник, більше його "імунітетних можливостей" у момент зараження.
Здатність організму людини протистояти різним мікроорганізмам обумовлена двома механізмами: неспецифічною протиінфекційною резистентністю, яка відразу спрямована на безліч інфекційних агентів, і розвитком специфічного набутого імунітету до конкретних мікроорганізмів.
Облігатно-патогенні бактерії (особливо небезпечних інфекцій - чуми, сибірської виразки та ін.) мають високу вірулентність, чинники знешкодження і подолання природних бар’єрів імунітету нормального, але не імунного до них організму (відносний імунодефіцит). Для захисту від них необхідна попередня активація систему імунітету, індукція антитіл і/або імунних Т-клітин, тобто створення імунітету, тоді і ці бактерії не можуть його подолати.
Багато вірусів здатні долати бар’єри природного вродженого імунітету, проте після індукції набутого імунітету шляхом вакцинації (кір, поліомієліт, грип та ін.) інфекція не виникає.
Набуті (вторинні) імунодефіцити
Придбаний (вторинний) імунодефіцит - це порушення імунної системи, що розвиваються у постнеонатальному періоді або у дорослих і не є результатом генетичних дефектів.
Таким чином, під терміном "вторинний імунодефіцит" слід розуміти порушення імунітету, що виникають у результаті соматичних та інших хвороб, а також інших чинників, і мають клінічні прояви (Міжнародна класифікація хвороб, X перегляд).
Придбаний (вторинний) імунодефіцит - це клініко-імунологічний синдром:
а) що розвинувся на фоні раніше нормально функціонуючої імунної системи; б) що характеризується стійким значним зниженням кількісних і функціональних показників імунного статусу; в) є зоною ризику розвитку хронічних інфекційних захворювань, автоімунної патології, алергічних хвороб і пухлинних новоутворень.
З такого визначення поняття придбаного (вторинного) імунодефіциту виходять наступні його особливості.
1. Порушення у системі імунітету дійсно вторинні і з’являються на фоні раніше нормального здоров’я які у клінічному, так і в імуно-лабораторному відношенні. Це можна з’ясувати шляхом бесіди з хворим.
2. Порушення в імунній системі повинні носити стійкий і виражений характер. Це важлива умова, оскільки відомо, що показники імунної системи лабільні, рухомі, що дозволяє різним її ланкам взаємодоповнювати й "підстраховувати" одне одного. Тому транзиторні, тимчасові зміни параметрів імунітету можуть бути обумовлені особливостями ситуативного реагування.
3. Порушення в імунній системі повинні носити не тільки кількісний характер. Слід оцінювати також функцію тих або інших клітин. Відомі випадки, коли зниження кількості, наприклад NK-клітин, компенсувалося їх підвищеною функціональною активністю. Якщо ж зниження кількості тих або інших клітин імунної системи супроводжується одночасним порушенням їх функції - це безумовно найважливіша лабораторна ознака імунодефіциту.
4. Порушення у системі імунітету можуть зачіпати показники як специфічного (адаптивного) імунітету, так і неспецифічної резистентності, тобто вродженого (природного) імунітету.
5. Порушення у системі імунітету характеризуються переважним ураженням однієї з ланок імунітету (клітинного, гуморального, комплементарного чи фагоцитарного), інші зміни імунологічних показників носять вторинний, як правило, компенсаторний характер. Можливі комбіновані порушення імунітету.
6. Важливо розуміти наступне: як правило, на прийом до лікаря потрапляє хворий, у якого вже є клінічні ознаки вторинного імунодефіциту, наприклад хронічна, резистентна до традиційної терапії, інфекційно-запальна патологія. У цьому випадку потрібне активне втручання клінічного імунолога. Проте, важливо націлити лікаря на те, що у деяких так званих практично здорових осіб можуть бути виявлені імуно-лабораторні ознаки вторинного імунодефіциту, що супроводжуються лише непрямими клінічними ознаками, наприклад підвищеною втомлюваністю, яка ще не набула хронічного характеру. У цьому випадку краще говорити про транзиторні зміни в імунограмі, що не підкріплені клінікою і, в багатьох випадках, не вимагають призначення імунотропних препаратів. Для уточнення ситуації такі хворі потребують повторного спостереження. У такому разі слід пам’ятати, що дана людина знаходиться у зоні ризику розвитку тієї або іншої патології, пов’язаної з вторинним імунодефіцитом: інфекційної, автоімунної, алергічної, онкологічної тощо. Разом з тим, приналежність до "зони ризику" - це ще, на щастя, оборотна ситуація, і такій людині можна допомогти шляхом проведення імунореабілітаційних заходів.
Нижче наведені причини, які можуть викликати розвиток вторинного імунодефіциту.
Причини розвитку вторинних імунодефіцитів
I. Інфекційні
1. Вірусні інфекції:
а) гострі - кір, краснуха, грип, вірусна паротитна хвороба (епідемічний паротит), вітряна віспа, гепатити, герпес та ін.;
б) персистуючі - хронічний гепатит В, підгострий склерозуючий паненцефаліт, СНІД та ін.;
в) уроджені - цитомегалія, краснуха (TORCH-комплекс).
2. Бактеріальні інфекції: стафілококова, пневмококова, менінгококова, туберкульоз та ін.
3. Протозойні інвазії і гельмінтози (малярія, токсоплазмоз, лейшманіоз, трихінільоз, аскаридоз та ін.).
II. Аліментарні (порушення харчування)
1. Білково-енергетична недостатність.
2. Дефіцит мікроелементів (Zn, Cu, Fe), вітамінів - ретинолу (А), аскорбінової кислоти (С), альфа-токоферолу (Е), фолієвої кислоти.
3. Виснаження, кахексія, втрата білка через кишечник, нирки.
4. Вроджені порушення метаболізму.
5. Зайве харчування, ожиріння.
6. Синдром порушення всмоктування у кишечнику.
III. Метаболічні
1. Хронічна ниркова недостатність, уремія, нефротичний синдром.
2. Хронічні захворювання печінки.
3. Цукровий діабет.
4. Гіперкатаболізм імуноглобулінів.
IV. Стани, що призводять до втрати імунокомпетентних клітин і імуноглобулінів (кровотечі, лімфорея, опіки, нефрит).
V. Злоякісні новоутворення, особливо лімфопроліферативні.
VI. Автоімунні захворювання.
VII. Екзогенні й ендогенні інтоксикації (отруєння, тиреотоксикоз, декомпенсований цукровий діабет).
VIII. Імунодефіцит після різних впливів
1. Фізичних (іонізуюче випромінювання, ЗВЧ та ін.).
2. Хімічних (імуносупресори, цитостатики, кортикостероїди, наркотики, гербіциди, пестициди та ін.).
3. Несприятливі екологічні чинники.
4. Імунодепресивні заходи лікування: лікувальні препарати (імунодепресанти, глюкокортикостероїди, цитостатики, антибіотики, нестероїдні протизапальні препарати).
4. Професійні шкідливості, у тому числі рентгенологічне випромінювання, радіоактивний вплив, біологічно активні та хімічно агресивні речовини.
5. Різні види стресу (емоційний, психічні травми, фізичний, спортивні перевантаження та ін.).
IX. Різні важкі захворювання, хірургічне втручання, наркоз, опіки.
X. Порушення нейрогормональної регуляції.
XI. Вікові фактори: ранній дитячий вік, старечий вік, вагітність.
Слід ще раз підкреслити, що за клінічними ознаками і лабораторними даними вторинні і первинні імунодефіцити вельми схожі, аж до існування взаємозв’язку між характером імунних порушень і типом збудника. Принциповою відмінністю залишається причина, що лежить в основі імунних порушень: при первинних це вроджений дефект, при вторинних - набутий.
Так само, як і первинні, вторинні імунодефіцити можуть бути обумовлені порушенням функції однієї з основних систем імунітету: гуморальної (В-системи), клітинної (Т-системи), системи фагоцитів, системи комплементу або декількох (комбіновані дефекти).
Серед вторинних імунодефіцитів виділені три форми:
- набута;
- індукована;
- спонтанна (код МКХ-10 D.84.9).
Набута форма вторинного імунодефіциту є синдром набутого імунодефіциту (СНІД), що розвивається у результаті ураження імунної системи вірусом імунодефіциту людини (ВІЛ).
Індукована форма (код МКХ-10 D.84.8) вторинного імунодефіциту виникає у результаті конкретних причин, що викликали її появу: рентгенівське випромінювання, цитостатична терапія, застосування кортикостероїдів, травми і хірургічні втручання, а також порушення імунітету, що розвиваються повторно по відношенню до основного захворювання (діабет, захворювання печінки, нирок, злоякісні новоутворення).
Спонтанна форма (код МКХ-10 D.84.9) вторинного імунодефіциту характеризується відсутністю явної причини, що викликала порушення імунної реактивності. Клінічно вона виявляється у вигляді хронічних, часто рецидивуючих інфекційно-запальних процесів бронхо-легеневого апарату, додаткових пазух носа, урогенітального і шлунково-кишкового тракту, очей, шкіри, м’яких тканин, викликаних опортуністичними (умовно-патогенними) мікроорганізмами. Тому хронічні, часто рецидивуючі, уповільнені, такі, що важко піддаються лікуванню традиційними засобами, запальні процеси будь-якої локалізації у дорослих розглядаються як клінічні прояви вторинного імунодефіциту.
У кількісному відношенні спонтанна форма є домінуючою формою вторинного імунодефіциту.
Види вторинних імунодефіцитів (залежно від етіологічного чинника):
- уточнений (інфекційний, токсичний, метаболічний, фізичний, психогенний, посттравматичний, з вказівкою конкретного діагнозу - захворювання, яке його викликало) (код МКХ-10 D.84.8);
- неуточнений (криптогенний, або есенціальний, або ідіопатичний, або спонтанний - виставляється за відсутності будь-якого етіологічного чинника) (код МКХ-10 D.84.9).
Види уточнених імунодефіцитів
Інфекційний імунодефіцит формується у результаті дії інфекційного збудника, у т. ч. умовно-патогенного (вірусний, бактеріальний, протозойний, грибковий, гельмінтний).
Токсичний імунодефіцит розвивається за умов тривалого впливу екзо- та ендотоксинів, ксенобіотиків тощо (екзогенний, медикаментозний, професійний, ендогенний, опіковий тощо).
Метаболічний імунодефіцит розвивається за умов тривалого порушення обміну речовин, у т.ч. порушення кислотно-лужної рівноваги (харчовий, обмінний, через дефіцит білків, порушення всмоктування тощо).
Фізичний імунодефіцит розвивається у результаті тривалої дії на організм людини іонізуючого та ультрафіолетового опромінення, дії високих частот і полів тощо.
Психогенний імунодефіцит розвивається за умов тривалої дії психоемоційного перевантаження, стресів, захворювань ЦНС тощо.
Посттравматичний імунодефіцит (у т.ч. операційний) розвивається за умов важких обширних травм, опіків, об’ємних і тривалих оперативних втручань, крововтрат, лімфореї тощо.
Типи дефектів імунної системи
Лімфоцитарний імунодефіцит характеризується стійкими кількісними і/або функціональними змінами Т-клітинної ланки імунної системи.
Гуморальний імунодефіцит характеризується стійкими кількісними і/або функціональними змінами В-клітинної ланки імунної системи, у тому числі продукції імуноглобулінів.
Фагоцитарний імунодефіцит характеризується стійкими кількісними і/або функціональними змінами фагоцитуючих клітин (моноцити/макрофаги, гранулоцити) імунної системи.
Комплементарний імунодефіцит характеризується стійкими змінами рівня та активності компонентів комплементу.
Комбінований імунодефіцит характеризується стійкими кількісними і/або функціональними змінами показників декількох (двох чи більше) ланок імунної системи. Доцільно виділяти провідний дефект імунної системи (наприклад, комбінований дефект з перевантаженням лімфоцитарного).
Класифікація вторинних імунодефіцитів за клінічною формою
Автоімунна форма характеризується відповідними клінічними та лабораторними даними (гіпергаммаглобулінемія, підвищений рівень ЦІК тощо).
Алергічна форма (у т.ч. IgE-залежний, реагіновий) характеризується відповідними клінічними (гіперчутливість шкіри та слизових оболонок, у першу чергу дихальної системи і шлунково-кишкового тракту) та лабораторними даними (еозинофілія, підвищений рівень IgE тощо).
Імуно-проліферативна форма характеризується формуванням пухлин у різних органах та системах з нагромадженням пухлинної маси лімфоїдно-моноцитарно-клітинного складу, збільшенням розмірів селезінки, мигдаликів, аденоїдів, тимусу, пейєрових бляшок тощо.
Паранеопластична форма характеризується порушенням функціонування імунної системи в онкологічних хворих внаслідок дії пухлини на організм та ураження імунної системи після використання протибластомних засобів (цитостатична терапія, опромінення тощо).
Нейрогенна форма (синдром хронічної втоми, нейроімуноендокринний синдром, імунодефіцит при психічних хворобах тощо).
Змішана форма - характеризується наявністю у хворого двох чи більше форм; доцільно виділяти провідну форму (наприклад, змішана форма з переважанням автоімунної).
Варіанти перебігу вторинних імунодефіцитів
Гострий - клініко-лабораторні ознаки імунодефіциту розвиваються та зберігаються протягом 1 місяця.
Підгострий - клініко-лабораторні ознаки імунодефіциту розвиваються та зберігаються протягом 3 місяців.
Хронічний - клініко-лабораторні ознаки імунодефіциту розвиваються та зберігаються протягом 6 місяців.
Рецидивуючий - клініко-лабораторні ознаки імунодефіциту повторно формуються раніше, ніж через 6 місяців після успішно проведеного лікування.
Ступені імунної недостатності
(в залежності від абсолютної кількості лімфоцитів; норма абсолютної кількості лімфоцитів - 1,4-3,2 х 109/л)
1- й ступінь імунної недостатності - мінімальний (ІН-1) - абсолютна кількість лімфоцитів становить 1,4-1,2 х 109/л; лабораторні показники знижені на 15-30% від середньої нормальної величини. Клінічно імунодефіцит може не проявлятися (компенсована форма).
2- й ступінь імунної недостатності - середній (ІН-2) - абсолютна кількість лімфоцитів становить 1,1-0,9 х 109/л; лабораторні показники знижені на 35-55% від середньої нормальної величини. Клінічно імунодефіцит може проявлятися одним чи комбінацією кількох клінічних синдромів, підгострим чи хронічним варіантом перебігу.
3- й ступінь імунної недостатності - високий (ІН-3) - абсолютна кількість лімфоцитів становить менше 0,9 х 109/л; лабораторні показники знижені більш ніж на 55% від середньої нормальної величини. Клінічно імунодефіцит проявляється вираженими клінічними симптомами.
Класифікація вторинних імунодефіцитів за функціональною недостатністю
ФН І - хворий зберігає працездатність, потребує амбулаторного лікування без видачі листка непрацездатності.
ФН ІІ - хворий тимчасово втрачає працездатність або його працездатність обмежена, потребує амбулаторного лікування з видачею листка непрацездатності.
ФН ІІІ - хворий втрачає працездатність тимчасово або має стійку втрату працездатності, потребує стаціонарного лікуваннята/або експертизи працездатності.
Основні види, форми, типи імунодефіцитів, ступені компенсації та недостатності імунної системи, варіанти перебігу та імунопатологічні синдроми представлені у табл. 1.
Таблиця 1
Класифікація вторинних імунодефіцитів
Етіологічний чинник |
Клінічна форма |
Тип за дефектом імунної системи |
Варіанти перебігу |
Ступінь імунної недостатності |
Ступінь функціональної недостатності |
1. Імунодефіцит з встановленою етіологією (уточнений імунодефіцит), наводиться етіологічний варіант (код МКХ- 10 D.84.8). 2. Імунодефіцит неуточнений (код МКХ-10 D.84.9). |
1. Інфекційна. 2. Автоімунна. 3. Алергічна. 4. Імунопроліферативна. 5. Паранеопластична. 6. Нейрогенна. 7. Змішана. |
1. Клітинний. 2. Гуморальний. 3. Фагоцитарний. 4. Гранулоцитарний. 5. Комплементарний. 6. Комбінований. |
1. Гострий. 2. Підгострий. 3. Хронічний. 4. Рецидивуючий. |
ІН-1 ІН-2 ІН-3 |
ФН І ФН ІІ ФН ІІІ |
Основною клінічною ознакою вторинних імунодефіцитів є наявність і конкретні клінічні форми інфекційного синдрому - рецидивів і загострень інфекцій, що викликаються умовно-патогенними мікроорганізмами - вірусами, бактеріями, грибками, паразитами.
Головна умова виникнення інфекційного процесу - сприйнятливість макроорганізму, тобто недостатність його імунітету (імунодефіцит), коли навіть умовно-патогенний мікроорганізм може викликати інфекцію. Зв’язок інфекцій, що викликаються умовно-патогенними мікроорганізмами, з імунодефіцитом очевидна, оскільки лише при його наявності можлива їх експансія.
Імунодефіцит - відносний або абсолютний - головна причина інфекцій, оскільки при підвищенні, стимуляції імунітету після вакцинації виникає резистентність до багатьох високовірулентних збудників. Так, шляхом вакцинації населення була ліквідована віспа, що загубила мільйони людей, зараз індукується несприйнятність до кору, поліомієліту, грипу, гепатиту В, кліщового енцефаліту, жовтої лихоманки та інших інфекцій. Це доводить, що навіть високовірулентні збудники не можуть подолати заздалегідь мобілізовані імунні бар’єри організму. Отже, вірулентність збудників інфекцій не абсолютна, і організм з достатньо високим ступенем специфічної і неспецифічної активності імунітету - тобто імунний - в змозі протистояти їй.
Діагностика вторинних імунодефіцитів
Першим етапом діагностики є збір анамнезу і з’ясування скарг хворого, які, залежно від виду імунопатології, можуть істотно розрізнятися.
При наявності вторинного імунодефіциту в анамнезі зазвичай виявляються рецидивуючі інфекції, характер і локалізація яких може указувати на вид імунодефіциту. Алергічний процес має свої особливості, і вже тільки на підставі анамнезу можна іноді встановити правильний діагноз.
Характерні риси має анамнез при автоімунних захворюваннях, що дозволяє відрізнити їх від інших видів патології. Лімфопроліферативні і онкологічні процеси також мають властиві їм ознаки. Наступним етапом є проведення імунологічнихдосліджень, що дозволяють оцінити імунний статус хворого з передбачуваним імунодефіцитом.
"Імунний статус" - це стан системи імунітету здорового або хворого у певний момент часу за конкретних умов навколишнього середовища.
Імунологічний, або імунний статус (ІС), характеризується комплексом інформативних показників, що відображають стан різних ланок системи імунітету в момент дослідження при конкретному процесі або захворюванні. Оцінка імунного статусу - це процес отримання комплексу неспецифічних і специфічних кількісних і функціональних показників, що відображають стан системи імунітету. Відображаючи форму і варіант захворювання, показники ІС служать основою для створення імунологічного "образу" хвороби, тобто її імунологічної характеристики, виявлення дефектної ланки імунітету.
Імунодіагностика - це застосування сукупності імунологічних методів для виявлення захворювання або визначення збудника хвороби у досліджуваному матеріалі. Всі методи імунодіагностики діляться на 2 групи:
Загальні неспецифічні методи, що характеризують стан різних ланок системи імунітету: лімфоцитів, гранулоцитів, макрофагів, комплементу. Зазвичай їх застосовують для виявлення дефекту в системі імунітету, тобто при імунодефіцитах.
Специфічні методи, що дозволяють виявити антитіла, імунні Т-лімфоцити, антигени збудника в організмі людини або у зовнішньому середовищі. Ці методи використовують для діагностики інфекцій, алергії, автоімунних захворювань.
Стандарт діагностики при вторинних імунодефіцитних станах представлений наступними дослідженнями.
1. Обов’язкове лабораторне обстеження:
а) дослідження імунного статусу (визначення загальної кількості лейкоцитів, лімфоцитів, субпопуляцій Т-лімфоцитів, В-лімфоцитів, рівня імуноглобулінів А, М, G, фагоцитозу);
б) контроль виявлених порушень після курсу проведеної терапії.
2. Додаткові методи дослідження: спеціальні імунологічні дослідження залежно від клінічних проявів і дефектів, що виявляються, при первинній оцінці імунного статусу, такі як дослідження функціональної активності класів і субкласів лімфоцитів, гемолітичної активності системи комплементу, неспецифічних гострофазових показників, інтерферонового статусу, імунного контролю умовнопатогенних інфекцій та ін.
3. Інструментальна діагностика.
4. Консультації фахівців.
Основні ознаки вторинних імунодефіцитів:
- відсутність зв’язку із спадковістю і генетичною обумовленістю;
- виникнення на фоні нормальної реактивності у зв’язку із захворюванням, дією несприятливих фізичних і біологічних чинників, способів або засобів лікування;
- збереження дефіциту при лікуванні основного захворювання і усуненні чинників, що індукують його;
- відсутність або тривала сповільнена нормалізація імунного статусу.
Характеристика порушень імунного статусу при вторинних імунодефіцитах представлена у табл. 2.
Таблиця 2
Характеристика вторинних імунодефіцитів
Показники |
Індуктори |
|||
Бактеріальні інфекції |
Стрес |
Неспецифічні хронічні захворювання |
Лікарські препарати, опромінювання |
|
Лімфоцити |
+, рідко - |
- |
+/- |
- |
Т-лімфоцити |
- |
- |
- |
- |
CD-4 |
+/- |
- |
+/- |
- |
CD-8 |
+ |
+ |
+ |
+ |
В-лімфоцити |
+ |
+/- |
+ |
+/- |
Імуноглобуліни |
Дисімуноглобулінемія |
Дисімуноглобулінемія |
Дисімуноглобулінемія |
Дисімуноглобулінемія |
NK-клітини |
+/- |
- |
+/- |
- |
Фагоцитоз |
+/- |
+ |
+/- |
- |
Примітка: (+) - підвищення, (-) - зниження показника
Клініко-імунологічна характеристика вторинних імунодефіцитів
Переважно Т-клітинні імунодефіцити
1. Т-лімфоцитопенічний синдром
Паракортикальні зони лімфовузлів запустівають, лімфоїдна тканина атрофується. Знижена кількість Т-лімфоцитів на 15% і більше. Діагноз встановлюється при повторному підтвердженні на фоні ремісії основного захворювання.
Варіанти: автоімунний (з наявністю анти-Т-клітинних антитіл), стресовий, токсичний (лікарський), вірусний, дисметаболічний, при саркоїдозі, лімфограгулематозі, Т-лейкозі та ін.
Клінічна картина: рецидивуючі вірусні інфекції з тривалим перебігом у поєднанні з бактеріальними інфекціями.
2. Синдром Т-клітинного імунорегуляторного дисбалансу
Імунний статус: відношення Th-CD4/Ts-CD8 менше 1,4 (чим менше, тим сильніше виражений вторинний імунодефіцит). Діагноз встановлюється при виявленні і підтвердженні цих порушень у період ремісії основного захворювання.
Клінічна картина: поліморфні рецидивуючі інфекції різної локалізації.
3. Синдром Т-клітинного імунорегуляторного дисбалансу з підвищеною цитотоксичною реактивністю
Імунний статус: відносний лімфоцитоз. Імунорегуляторний індекс Th- CD4/Ts-CD8 менше 1,4 (чим менше, тим сильніше виражений вторинний імунодефіцит). Різко підвищені рівні NK-клітин (CD 16), IgM, IgG, збільшений НСТ-тест. Є ознаки розвитку цитотоксичної реакції на фоні внутрішньоклітинної інфекції, наприклад герпес-вірусна, цитомегаловірусна інфекції.
Клінічна картина: поліморфні рецидивуючі інфекції різної локалізації.
4. Синдром дефіциту лімфокінів та їх рецепторів
Встановлюється при неодноразовому підтвердженні.
Переважно В-клітинні імунодефіцити
5. Пангіпогаммаглобулінемія
Гіпоплазія лімфоїдних фолікулів, атрофічні лімфовузли.
Імунний статус: зменшення концентрації гаммаглобулінів у сироватці крові, зниження рівня природних антитіл, зменшення у крові та інших біологічних рідинах (слина, секрети) IgA, М, G при нормальному або помірно зниженому рівні і функціональній активності Т-лімфоцитів.
Клінічна картина: переважають рецидивуючі бактерійні інфекції дихальних шляхів, легень, сепсис.
6. Дисімуноглобулінемія
Імунний статус: зміна співвідношення між імуноглобулінами при обов’язковому зниженні концентрації одного з них на фоні нормального і підвищеного рівня інших.
7. Синдром дефіциту антитіл
Імунний статус: відсутність антитіл проти виявлених збудників інфекцій (наприклад, до стафілококу, стрептококу).
Клінічна картина: рецидивуючі інфекції.
8. Дефіцит секреторного IgA
Імунний статус: у слині, трахеобронхіальному, кишковому й інших секретах відсутній (понижений) рівень секреторного IgA.
Клінічна картина: хронічні бронхіти, запалення слизової оболонки ротової порожнини (парадонтози), хронічні тонзиліти, отити та ін.
9. Вторинний імунодефіцит при В-клітинних пухлинах (плазмоцитома Вальденстрема, лімфоми, В-клітинний лейкоз)
10. Вторинний імунодефіцит з явищами дисімуноглобулінемії і автоімунним компонентом.
Імунний статус: характерні нейтрофільний лейкоцитоз, збільшення рівня плазмоцитів, В-лімфоцитів, збільшення Th2 (CD4+), CD8+, рівня IgM, ЦІК, комплементу, ШОЕ, СРБ і підвищення (рідше зниження) активності фагоцитів.
Дефіцити макрофагів і гранулоцитів
11. Синдром гіперактиваціїмакрофагів-моноцитів
Імунний статус: моноцитоз, збільшення ІЛ-1 у біологічних рідинах.
Клінічна картина: лихоманковий синдром, артрити і запалення різної локалізації.
12. Пангранулоцитопенія, дефіцит гранулоцитів
Імунний статус: агранулоцитоз і нейтрофілопенія.
Варіанти - автоімунний, алергічний, токсичний, інфекційний.
Клінічна картина: гнійно-септичні захворювання, виразка слизових оболонок.
13. Синдром гіпереозинофілії
Імунний статус: підвищення кількості еозинофілів у крові, секретах, тканинах.
Клінічна картина: автоімунні, алергічні, паразитарні захворювання.
14. Дефіцит рецепторів нейтрофілів і молекул адгезії
Імунний статус: відсутність або зниження кількості нейтрофілів з відповідними рецепторами і молекулами. Зниження їх адгезії до поверхні клітин.
Клінічна картина: гнійно-септичні захворювання.
15. Дефіцит хемотаксичної активності нейтрофілів
Імунний статус: зниження спонтанної й індукованої рухливості нейтрофілів.
Клінічна картина: гнійно-септичні захворювання.
16. Дефіцит метаболічної активності нейтрофілів
Імунний статус: зниження показників стимулюючого НСТ-тесту, активності мієлопероксидази, інших ферментів.
Клінічна картина: гнійно-септичні захворювання.
17. Дефіцит поглинальної функції нейтрофілів
Імунний статус: зниження фагоцитарного числа і фагоцитарного індексу.
Клінічна картина: гнійно-септичні захворювання.
18. Дефіцит перетравлюючої активності нейтрофілів
Імунний статус: відсутнє або знижене перетравлювання мікроорганізмів.
Клінічна картина: рецидивуючі запальні процеси, частіше - шкірних покривів.
19. Панлейкопенічний синдром
Варіанти: токсичний, автоімунний, інфекційний, радіаційний. Зменшення кількості всіх лейкоцитів, спустошення кісткового мозку, пригнічення утворення колоній.
Клінічна картина: важкі форми інфекцій, сепсис.
20. Загальний лімфоцитопенічний синдром
Варіанти: автоімунний з антилімфоцитарними антитілами; лімфоцитолітичний як наслідок руйнування лімфоцитів екзогенними чинниками; вірусна лімфоцитопенія.
Імунний статус: лімфоцитопенія (кількість лімфоцитів на 15% і більше нижче за норму, синдром "недостатності лімфоцитів").
Клінічна картина: стійко рецидивуючі локалізовані або генералізовані бактерійні та вірусні інфекції, іноді спленомегалія.
21. Синдром поліклональної активації лімфоцитів
Імунний статус: у крові присутні антитіла різної специфічності до автоантигенів, наростає їх титр до інших антигенів, гіперплазія фолікулів лімфатичних вузлів, підвищення рівня імуноглобулінів IgG, збільшення Т-хелперів CD4 і зниження рівня Т-супресорів CD8, В-лімфоцитів, при близькому до норми рівні загальних Т-лімфоцитів.
Клінічна картина: інфекційні, автоімунні і алергічні процеси.
22. Лімфоаденопатія (локалізована або генералізована)
Варіанти: з нормальним рівнем лімфоцитів у крові; з Т-лімфопенією.
Клінічна картина: гіперплазія лімфатичних вузлів, тривалий субфебрилітет, вегетативна дисфункція (дистонія, кардіалгія та ін.).
23. Синдром гипертрофії та гіперплазії мигдаликів і аденоїдів. Хронічний тонзиліт, аденоїди; кількісна і функціональна дисфункція лімфоцитів і цитокінів.
24. Посттонзилектомічний синдром
Клінічна картина: рецидивуючі захворювання верхніх дихальних шляхів після видалення мигдаликів у зв’язку з хронічним тонзилітом. Рецидивуючі інфекції носоглотки і у ділянці дужок мигдаликів.
Імунний статус: можливе помірне зниження Т-лімфоцитів, дисбаланс їх субпопуляцій, дисімуноглобулінемія.
25. Постспленектомічний синдром. Пригнічення продукції антитіл на тимуснезалежні антигени (стрептококи, стафілококи та ін.), можлива Т-клітинна лимфопенія, підвищена чутливість до інфекцій.
26. Тиміко-лімфатичний синдром. Характеризується поєднанням тимомегалії, недостатності надниркових залоз і функціональної активності лімфоцитів.
Клінічна картина: адинамія, бліда мармурова шкіра, задишка у спокої, мікролімфоаденопатія, гіперсимпатикотонія.
27. Синдром патології імунних комплексів
Імунний статус: високі рівні імунних комплексів у крові, відкладення їх в тканинах, зниження активності фагоцитів, пригнічення активності Fc-рецепторів лімфоцитів.
Клінічна картина: васкуліти при імунних, алергічних, інфекційних захворюваннях; гепатоспленомегалія, телеангіоектазії.
Метаболічні вторинні імунодефіцити
28. Дефіцити мікроелементів
Дефіцит цинку - атрофія лімфоїдної тканини, пригнічення функції Т-хелперів і нейтрофілів, ентеропатичний акродерматит.
Дефіцит міді - нейтропенія, порушення функції фагоцитів і Т-лімфоцитів.
29. Імунодефіцит при гіповітамінозі
Дефіцит вітаміну С - порушення функції фагоцитів, пригнічення синтезу антитіл.
30. Імунодефіцити при недостатності білка (аліментарної та ін.) і дисліпопротеїнеміях, порушеннях вуглеводного обміну.
Дефекти системи компліменту
31. Синдром гіпокомплементемії
Імунний статус: зниження гемолітичної активності комплементу, збільшення числа імунних комплексів в крові.
Клінічна картина: автоімунні, алергічні й інфекційні захворювання.
Дефіцит тромбоцитів.
32. Тромбоцитопенічний синдром з антитромбоцитарними антитілами (імунна тромбоцитопенія)
Варіанти: автоімунний, алергічний, токсичний, інфекційний.
Імунний статус: порушення адгезії і функції тромбоцитів.
Клінічна картина: тромбоцитопенічна пурпура.
Вторинні імунодефіцити в дитячому віці
Сприяючими чинниками вторинної імунологічної недостатності у дітей є відхилення в антенальному періоді розвитку плоду, такі, як гестози I і II половини вагітності, перенесені жінкою різні захворювання, особливо у 1-му триместрі вагітності, професійні шкідливості у батьків, шкідливі звички (алкоголь, нікотин, наркотики, токсичні речовини), психоемоційні стреси. Чітким моментом індукції вторинного імунодефіциту є патологія пологів, частіше це пологи передчасні, з великою кількістю причинно-значущих чинників, відшарування плаценти під час пологів, фармакологічне знеболення, післяродові кровотечі, інфікування геніталій тощо. Переважна більшість дітей з набутими імунодефіцитами мають ознаки і симптоми наслідків перинатального пошкодження мозку з відхиленням за шкалою Апгар і розвитком неврологічної симптоматики; у періоді новонародженості часті гнійничкові захворювання, порушення функції шлунково-кишкового тракту і респіраторної системи. Частота останніх клінічних симптомів корелює з штучним і раннім змішаним вигодовуванням. Внутрішньоутробна інфекція також вносить свій внесок до формування імунодефіцитних хвороб у дітей. У періоді раннього дитинства при недостатності імунної системи посилюється схильність до харчової алергії, незвичайних реакцій на вакцинацію і лікарські сполуки. До певного часу така дитина залишається клінічно здоровою, а наявність у неї вторинного імунодефіциту маскується різними нетиповими симптомокомплексами.
Діти, що підлягають імунологічному обстеженню для виявлення вторинних імунодефіцитів, повинні виділятися у першу чергу з групи тих, що часто і тривало хворіють на різні захворювання. Так, важкий перебіг гнійно-септичних інфекцій, особливо у клінічній формі сепсису, супроводжується у дітей комбінованою імунологічною недостатністю.
Вторинні імунодефіцити у дітей можуть клінічно виявлятися будь-якою інфекцією, наприклад, пневмонією, резистентною до традиційної терапії, хронічними осередками інфекції. Типовою клінічною маскою вторинного імунодефіциту є тривалий субфебрилітет, коли його причини не вдається клінічно і лабораторно ідентифікувати. При вторинних імунодефіцитах за Т-системою лімфоцитів клінічним еквівалентом можуть бути рецидивуючі грибкові захворювання слизових оболонок респіраторної системи, шлунково-кишкового тракту, сечовивідних шляхів, а також кандидоз шкірних покривів. Лімфоаденопатія, що не є симптомом певної нозології, теж може служити проявом імунодефіциту і клінічним показанням для імунологічного обстеження.
Зміни у периферичній крові типу лімфопенії, нейтропенії, тромбоцитопенії, гіпогаммаглобулінемії, що тривало залишаються після одужання, указують на наявність вторинного імунодефіциту і вимагають імунотерапії та імунореабілітації.
Дефіцити системи імунітету можуть виникати у будь-яких ланках імунологічного реагування, бути ізольованими по одному компоненту або по одній функції, поєднаними або багатокомпонентними, комбінованими.
Порушення імунітету при вторинних імунодефіцитах у дітей можуть значно варіювати:
а) підвищення активності неспецифічних і специфічних клітин супресорів, яке може виявитися пригніченням функцій Т- і В-лімфоцитів (повинне бути достовірне зниження у порівнянні з нормою);
б) гіперстимуляція однієї або декількох популяцій Т-, В-лімфоцитів, а також нейтрофілів з різними рецепторами (відносно нейтрофілів варіантом вторинного імунодефіциту може бути зниження кількості або функції одної або декількох їх субпопуляцій);
в) дисімуноглобулінемія з переважним зниженням або підвищенням одного, декількох або всіх класів;
г) зміни функціонального стану нейтрофілів периферичної крові, які характеризуються дисоціацією процесів поглинання і перетравлювання, що призводить до незавершеного фагоцитозу на фоні підвищеної метаболічної активності у клітинах;
д) порушення у системі цитокінів.
Клінічні прояви вторинних імунодефіцитів у дітей теж можуть бути різноманітні, але характерні інфекційні синдроми:
1. Рецидивуючі гострі респіраторні вірусні інфекції.
2. Бактерійні, грибкові інфекції слизових оболонок і шкірних покривів.
3. Пневмонії та бронхіти бактеріальної етіології.
4. Захворювання, резистентні до традиційної бактеріальної терапії.
5. Реакції на введення лікарських препаратів і вакцин.
6. Тривалий субфебрилітет, фебрильна лихоманка неясного походження.
7. Хронічні осередки інфекції з явищами інтоксикації і порушенням психоневрологічного і фізичного розвитку.
8. Рецидивуючі гнійничкові захворювання, стан після перенесеного сепсису.
9. Лімфоаденопатія, гепато-спленомегалія.
10. Синдром гіперплазії вилочкової залози.
11. Тиміко-лімфатичний синдром.
12. Хронічна діарея.
13. Перинатальні пошкодження нервової системи, що ускладнені інфекцією.
14. Стани після внутрішньоутробної інфекції.
15. Гіпотрофія, резистентна до традиційно прийнятої терапії, що супроводжується інфекцією.
16. Модуляція показників периферичної крові на фоні клінічного здоров’я, диспротеїнемія.
17. Гнійно-септичні захворювання.
18. Інфекційні риніти, фарингіти, тонзиліти, посттонзилоектомічний синдром.
Принципи лікування вторинних імунодефіцитів
Етапи лікування і імунореабілітації хворих з вторинними імунодефіцитами:
1. Усунення етіологічного чинника.
2. Антимікробна терапія.
3. Замісна імунотерапія.
4. Профілактика інфікування.
5. Імунокоригуюча терапія.
6. Протирецидивна імунокорекція та імунореабілітація.
Орієнтирами лікування вторинних імунодефіцитів служать відповідні протоколи.
Застосування імуномодуляторів при вторинних імунодефіцитах
Основним показанням для призначення імуномодуляторів служить наявність вторинного імунодефіциту, діагноз якого встановлюють за клінічними і лабораторними даними. Початково виділяють 3 групи людей: 1) особи (хворі), що мають клінічні ознаки порушень імунітету в поєднанні із змінами його параметрів, виявлених імунологічними методами; 2) хворі, що мають тільки клінічні ознаки порушень імунітету, без лабораторних даних; 3) особи з відхиленнями імунологічних показників, але клінічно здорові. Імуномодулятори рекомендується призначати тільки хворим. Коригувати зміни (ймовірно, компенсаторні) імунного статусу у клінічно здорових осіб не рекомендується (Манько В.М. та ін., 2002).
При складанні комплексу імунокоригуючої терапії перше призначення у комплексі, як правило, повинне бути таким, що визначає і відповідає основному дефекту імунітету, потім підбираються засоби однонаправленої дії, але опосередкований подібний ефект терапії через інший механізм. Після проведення основної схеми лікування вторинного імунодефіциту проводиться фонова терапія, комплекс якої, у свою чергу, визначається характеристикою клінічної маски імунодефіцитного стану. Основна мета фонової терапії - подальша імунореабілітація. Таким чином, імунокоригуюча терапія має етапність свого проведення
I. Етап імунокоригуючої терапії (гострий період)
1. Т-клітинні вторинні імунодефіцити вірус-індуковані
- Противірусні препарати (ацикловир);
- інтерферони а, у, лейкінферон, віферон-1 (150 000 МО) дітям до 7 років і віферон-2 (500 000 МО у свічці) дітям старше 7 років;
- Т-міметики - тактивін 0,01% 1 мл, тимоптин у дозі 100 мкг, тимоген 0,01% - 1 мл в/м, тималін 10 мг п/ш чи в/м протягом 3 днів і далі через день 10 ін’єкцій;
- імунофан 1 мл 0,005% розчину в/м 1 раз на день № 10;
- галавіт 200 мг 1 раз на день в/м № 10;
- Т-цитокіни (ІЛ-2 - ронколейкін та ін.);
- поліоксидоній у дозі від 6 до 12 мг;
- метилурацил у віковій терапевтичній дозі протягом 10 діб, контроль периферичної крові провести на 7-му добу лікування;
- вітамін А всередину, 10-14 діб; вітамін Е 7-10 діб (вікові дози, ін’єкції);
- УВЧ-терапія на ділянку сонячного сплетіння 3-5 сеансів;
- ультразвукова дія на ділянку вилочкової залози 3 сеанси в дітей до 3 років, 5-6 сеансів у дітей, старших за 3 роки.
Вищезгадана імунотерапія підходить також для дітей з рецидивуючими гострими респіраторними вірусними інфекціями, з тривалим субфебрилітетом і фебрильною лихоманкою неясного генезу, а також з хронічною небактеріальною діареєю; ефективна також при перинатальних пошкодженнях нервової системи.
Для дітей, що перенесли внутрішньоутробні інфекції у генералізованій формі, а також страждаючих повторними вірусними інфекціями респіраторного тракту в поєднанні з рецидивуючими грибковими інфекціями слизових оболонок і шкіри можна рекомендувати наступну схему:
- аміксин, курс 2 тижні; для дітей раннього віку 1 раз на добу 0,03 per os, до 6-7 років у разовій дозі 0,06; до 12 років 0,1, старше 12 років по 0,125; або арбідол курсом 3 тижні (у ранньому віці 0,05 кожні 3 дні per os, до 6 років - 0,08, старше 6-7 років - 0,1); у окремих випадках можна використовувати лікувальну дозу 3 рази на добу протягом 5-7 діб; при необхідності арбідол добре використовувати у поєднанні з флуконазолом або дифлюканом (терапевтичні вікові дози);
- тактивін або тималін у терапевтичній віковій дозі, курсом 10 діб;
- імунофан підшкірно, 5 ін’єкцій 0,005% розчину через 2 доби, дітям раннього віку по 0,3 мл, іншим по 0,4-0,7 мл;
- мембраностабілізація може бути досягнута прийомом кетотифену (задитену) протягом 1-1,5 міс. (терапевтична вікова доза).
Ще приклад схеми імунокоригуючої терапії при неуточненому імунодефіцитному стані з Т-лімфоцитопенічним синдромом:
- поліоксидоній дітям старше 6 міс. внутрішньом’язово по 0,1-0,15 мг/кг через 48-72 години (курс 5-7 ін’єкцій), при хронічних процесах - 2 рази на тиждень по 0,1-0,5 мг/кг (7-10 ін’єкцій), для підтримуючого курсу можна застосовувати свічки поліоксидонію після очищення кишечника (0,1-0,2 мг/кг доба 3 доби, потім через 48 годин, курс - 10 свічок);
- ронколейкін, 4 ін’єкції з інтервалом у 3 доби в/в на фізіологічному розчині (швидкість введення - див. анотацію до препарату), в ранньому віці від 25 000 до 100 000 МО, більш старшим дітям по 100 000-500 000 МО на ін’єкцію;
- віферон курсом 5 діб, дітям до 7 років - віферон-1 у свічках (150 000 МО), дітям старше 7 років віферон-2 (500 000 МО);
- УВЧ на ділянку сонячного сплетення, чергуючи з ультразвуком на надниркову ділянку, дітям раннього віку курс лікування по 3 процедури, решті - по 5-7 діб кожного виду;
- гепарин підшкірно або внутрішньошкірно, курсом у 4 дні (доза від 100 од. у ранньому віці до 200-350 од. більш старшим дітям). При внутрішньошкірному введенні використовується декілька точок.
Приклад імунокоригуючої терапії у дітей, що мають неуточнений вторинний імунодефіцит з лімфоцитопенією, що стабілізувалася після перенесених внутрішньоутробних інфекцій у генералізованій формі:
- лейкінферон по 3-10 тис. ОД в/м 3 рази на тиждень, курс 3 тижні (дітям до року 3000 Од, до 3-х років 5000 Од, з 3-х років 7-10 тис. Од на ін’єкцію);
- тактивін в/м №10 через добу;
- кетотифен 1/8-1/2 таб. 2 рази (залежно від віку) - 1 міс;
- вітамін А по 3-6 тис. Од. 1 раз на добу 10 діб;
- препарати цинку протягом 3 тижнів у дозі 10-15-20 мг всередину.
Після імунологічного контролю можна повторити курс один-два місяці, якщо є нормалізація кількості субпопуляцій лімфоцитів і відзначається позитивний клінічний ефект.
2. В-клітинні вторинні імунодефіцити, що асоціюються з бактеріальними інфекціями
- Антибактеріальні (протигрибкові) препарати;
- імуноглобуліни (антитіла) при важкому перебігу внутрішньовенно:
IgG-вмісні: сандоглобулін 1,0; 3,0; 6,0; 12 г у флаконі; октагам 50, 100, 200 мл у флаконі; інтраглобін 2,5 г; 5,0 г; імуноглобулін нормальний людський для в/в введення біавен 1,0; 2,5;
IgM-вмісні: пентаглобін 5% - 10,0 мл; 20,0 мл, 50,0 мл.
Замісна терапія проводиться у режимі насичення (рівень імуноглобуліну G не менше 400 мкг/мл), підтримуюча терапія - під контролем лікаря-імунолога.
- Внутрішньом’язові імуноглобуліни;
- В-міметики (мієлопід 0,003 г, поліоксидоній у дозі від 6 мг до 12 мг);
- циклоферон у дозуванні, відповідному віку, на 10-14 діб;
- вітамін А всередину протягом 10-12 діб;
- лікопід у таблетках по 1-5 мг 1 раз на добу протягом 10 діб або гумізоль методом електрофорезу.
Інший варіант при стабільній В-лімфоцитопенії, що характеризується клінічними масками вторинного імунодефіциту (повторні пневмонії і бронхіти, хронічні осередки інфекції та ін.) може включати:
- циклоферон по 0,07-0,15 на добу 10 прийомів через 1-2 дні (або в ін’єкціях);
- ликопід по 1-2 мг, курс 10 діб (у періоді новонародженості 0,25 мг);
- тактивін по 0,5 мкг/кг у ранньому віці, курс 5 ін’єкцій, більш старшим дітям 1 мкг/кг; слід проводити підтримуючі щомісячні курси по 2-3 ін’єкції;
- дріжджовий напій протягом 2 тижнів для дітей раннього віку, 3-4 тижнів для більш старших дітей (5 г дріжджів на 40 мл води з цукром) або алое курсом №7-10 у ін’єкціях або електрофорезом.
Окрім вищезгаданих добре зарекомендував себе комплекс імунотерапії:
- лікопід 1-2,5-5 мг 1 раз на добу 10 діб (доза залежить від віку);
- кетотифен від 1/8 до 1/3 табл. 2 рази на добу 1,5 міс;
- рібомуніл дітям раннього віку по 0,5 табл. 2 рази на добу 4 доби на тиждень, курсом 5 тижнів, більш старшим дітям - по анотації. Можливе використання підтримуючої терапії під імунологічним моніторингом;
- повторно кетотифен через 1 міс;
- імунофан у 5 введень через 3 доби від 0,3 до 0,7 мл на ін’єкцію, залежно від віку;
- димексид - аплікації 30% розчину на ділянку сонячного сплетення через добу або на проекцію шокового органу.
3. Імунодефіцит з комбінованим Т-, В-лімфоцитопенічним синдромом
Схема імунокоригуючої терапії:
- тактивін підшкірно з розрахунку 10 мкг/м поверхні тіла 1 раз на добу протягом 10 діб і далі 5 ін’єкцій через 2-3 дні; курс слід повторити через 2-3 міс.;
- метилурацил у терапевтичному дозуванні на 15-17 діб;
- лікопід по 1-2,5-5 мг 1 раз на добу, курсом 10 діб;
- вітамін Е у терапевтичній віковій дозі (краще в ін’єкціях).
Стабільна Т, В-лімфоцитопенія може бути коригована також наступним комплексом:
- тималін в/м у 5-6 ін’єкцій по 3-10 мг залежно від віку;
- IRS-19 (дозований аерозоль) по 1-2 інсоляції на добу протягом 10 діб у поєднанні з прийомом кетотифену.
Ще одна схема імунокоригуючої терапії при комбінованій Т-, В-лімфопенії:
- один з препаратів внутрішньовенного імуноглобуліну (вибір ґрунтується переважною гіпоімуноглобулінемією);
- рекомбінантний гранулоцитарно-макрофагальний чинник (лейкомакс) підшкірно по 1-3 мкг/кг на добу під контролем компенсації лейкопенії;
- настій родіоли рожевої (золотого кореня), разова доза - по краплі на рік життя, три рази на добу 3-4 тижні.
Імунодефіцит з рецидивами вірусних інфекцій
Схема імунокоригуючої терапії:
- гропрінозин (ізопріназин) всередину по 50 мг/кг у 6 прийомів, тривалість курсу 7 діб;
- імунний (гамма) інтерферон 3 тис. Од/кг на ін’єкцію курсом до 7 діб (або лейкінферон);
- аплікації 15% димексиду (від 8 до 20 мл на 1 процедуру) протягом 8-10 діб. Місце для дії димексиду залежить від клінічної локальної симптоматики. Це може бути грудна клітка, ділянка печінки, передня поверхня живота, проекція підщелепних та інших лімфатичних вузлів і т. п.;
- при загостренні - ацикловір у вікових дозах (або гевіран).
4. Фагоцитарні імунодефіцити
Антибактеріальні (протигрибкові препарати).
Імуностимулятори широкого спектру:
- поліоксидоній в дозі від 6 до 12 мг;
- лікопід у дозі 1-10 мг 10 днів.
Препарати гранулоцитарно-макрофагальних колонієстимулюючих чинників:
- молграмостим (лейкомакс) 150 мкг, 300 мкг, 400 мкг;
- філграстим (нейпоген) 300 мкг, 480 мкг (1-5 мкг/кг/добу) підшкірно через день, 8-10 ін’єкцій;
- граноцит (ленограстим) 105, 265 і 365 мкг;
- мікроелементи у послідовності: цинк, мідь, селен;
- вітаміни А, Е, В;
- рибомуніл двома курсами по 4 тижні з інтервалом у місяць.
Замісна терапія
- Лейкоцитарна маса 3 мл/кг маси, курс 1-2-3 ін’єкції (за потреби);
- цитокіни - ронколейкін вводять по 0,25-1 мг (25 000-1 000 000 МО) у 200400 мл 0,9% розчину хлориду натрію в/в краплинно.
Додаткова терапія
Екстракорпоральні методи імунокорекції:
- екстракорпоральна імунофармакотерапія (ЕІФТ);
- плазмаферез;
- імуносорбція.
II. Етап протирецидивної імунореабілітації (при ремісії)
- Адаптогени (женьшень, елеутерокок та ін.);
- імуностимулятори рослинного походження (імунофан та ін.);
- санаторно-курортне лікування;
- фізіотерапія;
- імуностимулюючі вакцини широкого спектру (рібомунил, респіброн).
Вид імунотерапії (загальна і місцева) та її конкретний метод (фізичний, хімічний, біологічний) визначається природою дефіциту і його належністю до того або іншого варіанту порушення імунної системи.
Поєднання місцевої і загальної імунокоригуючої терапії дозволяє досягти найбільшого клінічного ефекту. Комбінована імунокорекція може включати сукупність 3-4 засобів і способів різної дії, що переважно впливають на різні ланки імунітету.
Тривалість амбулаторного або стаціонарного лікування залежить від характеру і тяжкості хвороби і складає від 3-х тижнів до 2-х місяців.
Терапія інфекційних ускладнень. Для зменшення контактів хворого з мікроорганізмами застосовують різні способи ізоляції. До простих методів профілактичної ізоляції відносяться: виділення окремої палати з санітарним вузлом (боксу) для хворого; використання персоналом змінюваних халатів, масок, рукавичок, ретельного миття рук; хворим забороняють сирі фрукти, овочі, молочні продукти - можливі джерела грамнегативних бактерій. Складніші технології направлені на очищення повітря навколо хворого.
Усунення етіологічного чинника можливе, коли відома причина вторинного імунодефіциту - імунодепресивна дія, професійні агенти та ін., які необхідно усунути.
Оскільки вторинні імунодефіцити виявляються інфекційними ускладненнями, то протимікробна терапія займає ключове місце у їх лікуванні. Вибір препаратів залежить від виду мікрофлори і особливостей вторинного імунодефіциту. Проте часто необхідна комплексна терапія через наявність асоціацій мікроорганізмів. Противірусні препарати, перешкоджаючи реплікації вірусів, звільняють їх нуклеїнові кислоти для індукції інтерферонів, а капсидні білки для активації антитілогенезу.
Антибактеріальна терапія. При вторинних імунодефіцитах бактеріальні інфекції часто рецидивують. Лікування включає основний курс і підтримуючу терапію. Використовуються принципи раціональної антибактеріальної терапії. Тривалість антибіотикотерапії перевищує у 2-3 рази період лікування звичайних хворих. Застосовуються високі дози антибіотиків широкого спектру дії, їх комбінації, тривалі курси кожного препарату (до 10-14 днів при його ефективності). Лікування загострень бактеріальних інфекцій досягається, як правило, послідовним проведенням 2-3 і більш курсів антибіотикотерапії, загальною тривалістю не менше 4-5 тижнів. Тривалість лікування одним препаратом складає 10-21 добу.
Для активної неспецифічної і напівспецифічної терапії використовують умовно-патогенні мікроорганізми у вигляді гетеровакцин, що складаються з мікробів, які колонізують дихальні шляхи (рібомуніл, ІРС-19, респіброн), або використовують імуностимулятори (лікопід, поліоксидоній).
Схожий з вакцинами ефект надають препарати нуклеїнових кислот, зокрема, нуклеїнат натрію, що отримується з дріжджів. Він зменшує дефіцит Т- і В-клітин, IgM, підвищує стійкість до зараження багатьма бактеріями, позитивно зарекомендував себе при хронічному паротиті, хронічному бронхіті, виразковій хворобі, а також у лікуванні ускладнень радіо- і хіміотерапії.
Серед засобів імуномодулюючої терапії показані препарати з органів імунітету (тактивін, тималін, мієлопід та ін.). Вибір засобів визначається варіантом імунодефіциту, порушенням певних ланок імунітету.
Протигрибкова терапія. Протигрибкові препарати у хворих з вторинними імунодефіцитами застосовують з лікувальною і профілактичною метою. Хворі з різними формами імунодефіцитів неоднаково чутливі до грибкової інфекції. У хворих з гуморальними і багатьма комбінованими дефектами грибкова інфекція зустрічається не часто, тому протигрибкові препарати (флуконазол, кетоконазол, клотримазол, інтраконазол) застосовуються у профілактичних дозах при повторних курсах антибіотиків.
Провідного значення протигрибкова терапія набуває при лікуванні генералізованних форм грибкової інфекції. У таких хворих можуть бути ураження шкіри і слизових оболонок грибками Candida і Aspergillus, але можливі і важкі інфекції, особливо при СНІДі і раку, високопатогенними Histoplasma capsulatum, Coccidiodes immitis; рідко зустрічаються феогіфомікози (Curerelaria spp., Alternaria spp. і ін.), зигомікози (Rhizopus spp., Mucor spp.), гіалогіфомікози (Fusarium spp. та ін.) у зв’язку з ендогенною колонізацією. У цих хворих навіть непатогенні дріжджі можуть викликати летальні інфекції.
Безпечні для життя поверхневі кандида-інфекції, зокрема рецидивуючий шкірно-слизовий кандидоз, ефективно усуваються препаратами імідазольної групи. Для профілактики пневмоцистної пневмонії застосовують флуконазол або інтраназол (5-10 мг/кг/добу). Для профілактики пневмоцистних пневмоній при ВІЛ-інфекції, а також для лікування використовують пентамідин (аерозолі і внутрішньовенно), а при його непереносимості - дапсон.
Противірусна терапія показана при Т-клітинних та інтерферонових вторинних імунодефіцитах. Профілактика деяких вірусних інфекцій досягається завдяки вакцинації при збереженні у хворого синтезу антитіл. Їх дефіцит супроводжується вірусним енцефалітом і менінгітами, ECHO-вірусними інфекціями.
При лікуванні вірусних респіраторних інфекцій у хворих з вторинними імунодефіцитами використовуються всі загальноприйняті засоби, а також додаткові лікувальні або профілактичні заходи, що запобігають розвитку ускладнень з урахуванням конкретного дефекту імунітету (антибіотики, позачергове переливання плазми або введення гамма-глобуліну).
Ефективним засобом терапії гострих герпетичних інфекцій (генітальних, проктитів, пневмоній) є препарат ацикловір (зовіракс) (400 мг всередину через 8 год., протирецидивно - 200-400 мг через 12 год.), дія якого заснована на блокуванні специфічних ферментів вірусу, при герпесі та цитомегаловірусній інфекції (ЦМВ) використовують також фоскарнет (60 мг/кг в/в кожні 8 год.), ганцикловір по 5 мг/кг в/в через 12 год., потім фамцикловір (250 мг всередину через 8 год.). При тяжкій герпес-zoster інфекції - ацикловір по 10 мг/кг в/в через кожних 8 год. 7-14 діб; у легких випадках - по 800 мг всередину через 4 год., або фамцикловір по 500 мг всередину через 8 год.; або валацикловір по 1 г всередину через 8 год.
За показаннями призначають препарати інтерферонів у різних дозуваннях залежно від виду імунного дефекту. Інтерферон має противірусну, імуномодулюючу, антипроліферативну і радіопротекторну дію. Сформульовано поняття "інтерфероновий статус", в основу оцінки якого покладено визначення сироваткового інтерферону, здатності до продукції а-інтерферону та у-інтерферону.
При цьому більш значущим є взаємозв’язок компонентів, а не окремо взяті значення (у фізіологічних умовах рівень сироваткового інтерферону не перевищує 4 МО, і він представлений сумішшю інтерферонів різних типів). у-інтерферон здатний викликати як стимулюючий, так і супресорний вплив на запальний процес. а-інтерферон успішно застосовують у лікуванні сепсису, активно стимулюючи Т-клітини і нейтрофіли. Людський рекомбінантний а2-інтерферон у поєднанні з антиоксидантами (віферон) рекомендований для лікування вірусних і бактеріальних інфекцій у новонароджених і дітей молодшого віку (група ризику імунодефіцитів), дозволяє зменшити введення препаратів крові і скоротити тривалість антибіотикотерапії при важких формах інфекції у неонатальному періоді. Індуктори інтерферону - циклоферон, аміксин, неовір - призначають у добовій дозі 5-8 мг/кг повторними курсами протягом 5-10 діб при тривало перебігаючих інфекціях - гепатитах, герпесі, хламідіях, кампілобактеріозі.
Противірусну дію має ізопринозин.
Лінкоміцин пригнічує багато вірусів (герпесу 1-го типу, енцефаломієліту та ін.).
Протипаразитарна терапія. У лікуванні паразитарних інфекцій у хворих з недостатністю імунітету використовують загальноприйняті препарати і дозування.
Токсоплазмоз найчастіше спостерігається при ВІЛ-інфекції. Оскільки Toxoplasma gondii - внутріклітинний паразит, то застосовують пиріметамін (100 мг всередину в 1-шу добу, потім 75 мг), сульфадіазин (25 мг/кг через 6 год.) або кліндаміцин (600 мг всередину через 6 год.).
Лікування і профілактика імуноглобулінами. При дефіцитах антитіл і вторинних гіпогаммаглобулінеміях застосування препаратів плазми крові і внутрішньовенних імуноглобулінів є провідним методом лікування і профілактики інфекцій.
При недостатності імуноглобулінів (Ig) (агаммаглобулінемія) Ig вводять в/в у режимі насичення по 400-800 мг/кг ваги. Октагам по 400-800 мг/кг болюсно, курс: одне введення (200 мг/кг) з інтервалом 3-4 тижні. Пентаглобін вводять дорослим від 0,4 мл/кг/год. і до 15 мл/кг/год. протягом 3 діб. Нативну свіжозаморожену плазму застосовують по 10-40 мл/кг. Курс 1000-2400 мл 2 рази на тиждень. Для профілактики інфекції рівні Ig при вторинних імунодефіцитах повинні підтримуватися не нижче за 4-6 г/л (200-800 мг/кг/місяць октагаму). Нативну плазму з цією ж метою вводять 1 раз на місяць по 15-20 мл/кг.
Профілактична імунізація. Згідно меморандуму ВООЗ (1995), живі вакцини не повинні вводитися у важких випадках недостатності імунітету:
при вторинній гіпогаммаглобулінемії;
при набутих імунодефіцитах у зв’язку з лімфомами, лімфогранулематозом, лейкозом та іншими онкозахворюваннями системи імунітету;
при лікуванні імунодепресантами і променевою терапією.
Ефективність вакцинації у дітей з вторинними імунодефіцитами невисока через кількісний дефіцит антитіл при недостатності імуноглобулінів, але імунізація анатоксинами безпечна.
Імунотерапія при вторинних імунодефіцитах у деяких клінічних випадках
Вторинні імунодефіцити при гнійно-септичній інфекції
Вторинні імунодефіцити з клінікою гнійно-септичної (хірургічної) інфекції зазвичай викликаються умовно-патогенними ендогенними мікроорганізмами, що часто проникають в осередок ураження у результаті транслокації з кишечника. Імунодефіцит, що індукований оперативним втручанням, наркозом, носить, як правило, комбінований характер. Розвиток інфекції залежить від маси інфекції, що поступає у чутливий організм, а співвідношення її маси і сили захисної реакції визначає терміни і характер розвитку хвороби.
Імунологічні механізми. Механізми пригнічення імунітету при гнійно-септичній інфекції можуть бути наступними: конкуренція антигенів, посилення активації Т-супресорів (при багатьох інфекціях), модуляція ланок імунної відповіді різними токсинами і антигенами бактерій. У розпал сепсису відмічається дисбаланс у складі популяцій Т- і В-лімфоцитів, порушується диференціювання лімфоцитів, що веде до недостатності їх функцій. Збільшується кількість недиференційованих "нульових" лімфоцитів, зростає співвідношення Ts/Th, виникає дисімуно- глобулінемія, знижується рівень природних і специфічних антитіл. Отже, при гнійно-септичному процесі розвивається полівалентний ефект інфекції у вигляді порушення різних ланок імунної відповіді, виражена недостатність яких служить діагностичним і прогностичним критерієм при сепсисі. У період клінічного одужання спостерігається нормалізація показників імуноглобулінів, але не складу субпопуляцій Т-лімфоцитів. Така відсутність нормалізації рецепторного складу лімфоцитів приховує у собі можливість рецидивів інфекції і є вторинним імунодефіцитом.
Тому разом з хірургічним видаленням гнійних вогнищ і антибактеріальною терапією, імунотерапія є невід’ємною частиною лікування як в гострий період захворювання, так і при реконвалесценції, а у ряді випадків необхідна протирецидивна імунореабілітація.
Схема і види імунотерапії залежать від форми і тяжкості процесу. При сепсисі та генералізованних формах інфекції застосовують препарати внутрішньовенних імуноглобулінів, а також плазмаферез, гемосорбцію, інші види дезінтоксикаційної терапії, одночасно сприяючи видаленню, нейтралізації надлишку прозапальних цитокінів, що з’явилися на першому етапі процесу. Імуноглобуліни, що збагачені IgM (пентаглобін), краще нейтралізують ендотоксини і мають переваги перед іншими при лікуванні сепсису і септичного шоку. Введення антитіл, що блокують ці цитокіни (анти-ФНП, анти-ІЛ-1 та ін.) може поліпшити клінічний перебіг захворювання. У подальшому гіперпродукція прозапальних цитокінів на фоні дії ендотоксинів бактерій індукує імуносупресію і розвиток імунологічного паралічу з поліорганною недостатністю - другий етап септичного процесу, коли видалення або пригнічення цитокінів запалення не ефективне.
Тимоміметики - тактивін, тималін - знижують частоту інфекційних післяопераційних ускладнень і, нормалізуючи імунний статус, прискорюють одужання.
Лікопід по 10 мг у таблетках або в ін’єкціях в/м по 0,125 мг щодоби протягом 10 діб призначають при гнійно-септичних ускладненнях.
Мієлопід призначають після операцій на серці, при переломах щелепи та іншій патології, коли виникає комбінований загальний варіабельний імунодефіцит.
Імунофан вводять підшкірно або в/м по 1 мл на добу 0,009% розчин 7-10 діб хворим з септичним ендокардитом, важкими гнійно-септичними післяопераційними ускладненнями, септичною пневмонією, перитонітом.
Поліоксидоній застосовують при сепсисі, перитоніті, абсцесах та інших гнійно-запальних захворюваннях, на курс лікування від 15 до 45 мг препарату.
Плазмаферез при гнійно-септичних процесах видаляє прозапальні цитокіни, а замісна імунотерапія екзогенними імуностимулюючими цитокінами сприятливо впливає на спектр цитокінів.
Ронколейкін - рекомбінантний ІЛ-2 вводять по 0,25-1 мг (250 0001 000 000 MО) у 200-400 мл 0,9% розчину хлориду натрію в/в крапельно із швидкістю 1-2 мл/хв протягом 4-6 год. щодоби. Курс лікування 3-8 внутрішньовенних інфузій.
Беталейкін (рекомбінантний ІЛ-lß) стимулює Т- і В-лімфоцити, кістково-мозкове кровотворення. Він виявився корисним при гнійно-деструктивних процесах, перитонітах, абсцесах. Вводять п/к або в/в крапельно для стимуляції лейкопоезу в дозі 15-20 нг/кг і імунітету - 5-8 нг/кг 1 раз на день протягом 5 днів, при необхідності курс повторюють через 2 тижні.
Лейкінферон - комплексний препарат цитокінів з високим вмістом інтерферонів (ІФН-а), нормалізує рівні Т-лімфоцитів і Т-хелперів-1 (різко знижені), підвищує фагоцитоз. Лейкінферон застосовують в/м по 10 000 МО (1 ампула) через добу 3-5 разів при важких грипі, перитоніті, сепсисі, ускладненому синдромом поліорганної недостатності. Застосування лейкінферону за 1-2 доби до операції прискорює терміни нормалізації температури і формули крові хворих, покращує антибактеріальний і противірусний імунітет.
Комбінована імунокорекція є переважною при хронічних гнійних захворюваннях, оскільки їх основою служить набутий комбінований імунодефіцит. Засоби імуностимуляції повинні використовуватися разом з антибактеріальною терапією вже під час передопераційної підготовки. У разі лейкопеній необхідні препарати, стимулюючі лейкопоез: метилурацил, цитокіни (лейкінферон), гранулоцитарно-моноцитарний колонієстимулюючий чинник - лейкомакс (молгра-мостім) у дозі 1-10 мкг/кг/добу або граноцит (ленограстім) по 2-10 мкг/кг/добу протягом 6 діб, тактивін (1,0 мл/добу) в/м, лейкінферон по 1 амп. через добу в/м, за показаннями - ронколейкін по 1 мг (1 000 000 Од) у 400 мл 0,9% розчину хлориду натрію в/в крапельно із швидкістю 1-2 мл/хв протягом 4-6 год., цитопротектор глутоксим 1% 2 мл в/м 1 раз на добу, 10 введень.
Новиков Д.К. і співавтори (2005) запропонували поєднувати левамізол, димексид і гепарин при імунодефіцитах з клінікою гнійно-запальних захворювань, оскільки димексид нівелює негативний ефект левамізолу на нейтрофіли, а гепарин, введений внутрішньошкірно, підсилює лімфопоез. Введення 30% розчину димексиду здійснювали електрофорезом по загальній методиці до 7 діб післяопераційного періоду, а потім димексид вводили місцево в осередок запалення, до виписки хворого із стаціонару. Левамізол призначали по 25-50 мг через добу протягом 15 діб. Замість левамізолу можна використовувати тактивін (тималін), поліоксидоній та інші імуномодулятори. За наявності бактеріальної інфекції їх слід комбінувати з антибактеріальними препаратами, які теж підсилюють імунні реакції. Такі ефекти виявлені у метронідазола, який стимулює синтез антитіл, фагоцитоз, інтерферони.
Пасивна імунотерапія людським антистафілококовим глобуліном (10 Од на 1 кг маси тіла протягом 10 діб), гомологічною імунною антистафілококовою плазмою (внутрішньовенно крапельно щодня по 30 Од на кг маси тіла), гетерогенним антистафілококовим глобуліном, який вводиться за Безредком (внутрішньом’язово 10 мл щоденно, N10), а також стафілококовим інтравенозним фагом (по 40 мл внутрішньовенно, N10). При важких процесах - в/в імуно-глобуліни, що містять IgG і IgM.
Активна імунотерапія за наявності резервних можливостей організму стафілококовим анатоксином, введенням автовакцини, введенням лейко-суспензії хворому.
Підвищення активності неспецифічного імунітету методом ультрафіолетового опромінювання крові.
Як приклад імунодефіциту за гранулоцитарним і В-клітинним типом наводимо історію хвороби хворого В., 54 років, що знаходився на лікуванні у хірургічному відділенні з діагнозом: хроніосепсис (стафілококовий), міжпетельні абсцеси черевної порожнини, септикопіємія. В анамнезі у хворого оперативне лікування з приводу гнійно-деструктивного апендициту, проведене 6 місяців тому, погіршення стану протягом 2-х тижнів (приклад 9).
Заключення імунограми (приклад 9): лейкопенія. Нейтропенія, відносний Th-цитоз. Зниження рівня В-лімфоцитів, продукції імуноглобулінів IgG, IgM. Зниження поглинальної здатності нейтрофілів (ФІ, ФЧ). Зниження спонтанної бактерицидності (НСТ-тест сп.), функціонального резерву окислювально-відновлювального потенціалу фагоцитів (НСТ-тест рез.), підвищення вмісту комплементу (CH-50). Ознаки інтоксикації (ТЗН).
Висновок: ознаки формування імунодефіцитного стану по гранулоцитарній і В-клітинній ланці із зниженням фагоцитарної активності внаслідок хронічного перебігу запального процесу, можливо, септичного характеру, що супроводжується важкою інтоксикацією з низькою реактивністю імунної системи.
В аналізі крові хворого був висіяний золотистий стафілокок з високою гемолітичною активністю.
Приклад 9
Хворий В., 54 роки. Діагноз: хроніосепсис, міжпетельні абсцеси черевної порожнини, септикопіємія, імунодефіцит за гранулоцитарним і В-клітинним типом (D 84.9).
Показник |
Результат |
Норма |
Вираженний анізоцитоз, анізохромія, ТЗН-68% |
|||||
Гемоглобін |
110 |
Ж - 115-145, Ч - 132-164 г/л |
||||||
Еритроцити |
2,9 |
Ж - 3,7-4,7, Ч - 4,0-5,1 ∙ 1012 /л |
||||||
Тромбоцити |
210 |
150-320 ∙ 109/л |
||||||
ШОЕ |
45 |
2-15 мм /год |
||||||
Лейкоцити |
3,8 |
4-9 Г/л |
||||||
Нейтр. |
П/я |
Еоз. |
Баз. |
Мон. |
Лімф. |
БГЛ |
Плаз. |
|
43-71% |
1-4% |
С/я |
0,5-5% |
0-1% |
3-9% |
25-37% |
1-5% |
0-1% |
2000-6500 |
80-400 |
80-370 |
20-80 |
90-720 |
1600-3000 |
80-500 |
20-80 |
|
49 |
6 |
43 |
2 |
0 |
2 |
44 |
0 |
0 |
1860 |
220 |
1640 |
80 |
80 |
1670 |
|||
Імунологічні показники |
Результат |
Норма (ОД СІ) |
Імунологічні показники |
Результат |
Норма (ОД СІ) |
||
Т-лімф. |
% |
72 |
50-80 |
IgG |
7,6 |
8,0-18,0 г/л |
|
CD-3 |
Абс. число |
1360 |
1000-2200 |
||||
Т-хелп. |
% |
40 |
33-46 |
IgM |
0,15 |
0,2-2,0 г/л |
|
CD-4 |
Абс. число |
795 |
309-1571 |
||||
Т-цитотокс. CD-8 |
% |
30 |
17-30 |
IgA |
1,8 |
0,3-3,0 г/л |
|
Абс. число |
501 |
282-999 |
|||||
ІРІ |
CD-4 /CD-8 |
5,05 |
1,4-2,0 |
ЦІК |
72 |
30-50 од. опт. щільн. |
|
NK-клітини CD-16 |
% |
20 |
12-23 |
Поглинальна активність |
ФІ |
45 |
60-80% |
Абс. число |
400 |
72-543 |
ФЧ |
1,4 |
1,5-3,5 |
||
В-лімф. |
% |
8 |
17-31 |
Сп |
3 |
До 10% |
|
CD-22 |
Абс. число |
133 |
109-532 |
НСТ-тест |
Інд |
6 |
- |
Сп. |
15 |
До 10% |
рез |
3 |
>16% |
||
РБТЛ |
Інд. |
60 |
50-70% |
Комплемент |
СН-50 |
70 |
30-60 гем. од/мл |
Заключний діагноз: хроніосепсис, міжпетельні абсцеси черевної порожнини, септикопіємія, імунодефіцит за гранулоцитарним і В-клітинним типом (D 84.9).
Хворому проведено оперативне лікування, дренована черевна порожнина. Виходячи з особливостей імунологічного статусу хворого В., для лікування хроніосепсису призначили наступну схему імунотропної терапії:
I етап терапії (стаціонарний)
1) специфічна антибактеріальна терапія (імунотерапія людським антистафілококовим глобуліном 10 мл в/м протягом 10 діб);
2) етіотропна антибактеріальна терапія - сульперазон по 1,0 г на 200 мл 0,9% розчину хлориду натрію в/в крапельно 2 рази на добу; зівокс (лінезолід) 0,6 г в/в крапельно 2 рази на добу;
3) дезінтоксикація - реополіглюкін 400 мл в/в крапельно; 400 мл 0,9% розчину хлориду натрію в/в крапельно, глюкоза 5% 400 мл + інсулін 4 ОД в/в крапельно;
4) плазмаферез 400 мл плазми 2 рази на тиждень 6 сеансів;
5) прямі антикоагулянти - клексан 40 мг 2 рази на добу підшкірно;
6) рекомбінантний ІЛ-2 ронколейкін 1 мг (1 000 000 Од) у 400 мл 0,9% розчину хлориду натрію в/в крапельно 1 раз на добу, 5 інфузій;
7) гранулоцитарний колонієстимулюючий чинник філграстім (нейпоген) по 60 млн ОД (2 мл, 10 мкг/кг/доба) п/ш 1 раз на добу. Якщо число нейтрофілів стає вище 1х109/л 3 дні поспіль, то дозу препарату знижують до 30 млн ОД (1 мл, 5 мкг/кг/доба). Відміну препарату проводять після того, як число нейтрофілів перевищує 1х109/л ще на протязі 3 днів;
8) цитопротектор глутоксим 1% 2 мл в/м 1 раз на добу, 10 введень;
9) пробіотик лінекс по 2 капс. 3 рази на добу.
II етап терапії (амбулаторний)
10) поліоксидоній по 6 мг в/м 2 рази на тиждень № 10;
11) лікопід 1 мг, по 1 табл. 1 раз на добу, 10 діб;
12) лінекс по 2 капс. 3 рази на добу, 20 діб.
Імунореабілітація
13) віферон 150 тис. Од, через добу в свічках, 10 введень;
14) натрію нуклеїнат по 0,1 г 3 рази на добу, 20 діб.
Вторинний імунодефіцит при хронічному рецидивуючому фурункульозі
Хронічний рецидивуючий фурункульоз (ХРФ) характеризується безперервно рецидивуючим перебігом і малою ефективністю антибактеріальної і симптоматичної терапії.
Фурункул розвивається у результаті гострого гнійно-некротичного запалення волосяного фолікула і тканин, що оточують його, і є ускладненням остеофолікуліту стафілококової етіології. Фурункули можуть виникати як одиночно, так і кількісно (фурункульоз). У разі рецидивування фурункульозу діагностується хронічний рецидивуючий фурункульоз.
Імунологічні механізми. При ХРФ виявляються порушення практично всіх ланок імунної системи. У 50-70% хворих ХРФ є порушення фагоцитарної ланки імунітету, що виражається у зниженні внутрішньоклітинної бактерицидності нейтрофілів, дефектах утворення активних форм кисню. Дефекти, що призводять до порушення міграції гранулоцитів, можуть призводити до хронічних бактеріальних інфекцій. Дефекти утилізації патогенів усередині фагоцитів, такі, як дефект НАДФН-оксидази, призводять до незавершеного фагоцитозу і розвитку важкої клінічної картини.
Низькі показники рівня сироваткового заліза можуть обумовлювати зниження ефективності оксидативного кілінгу патогенних мікроорганізмів нейтрофілами. При ХРФ виявлено зниження загальної кількості Т-лімфоцитів периферичної крові. У 20-50% хворих ХРФ понижена кількість СD4-лімфоцитів, а у 10-60% - підвищена кількість СD8-лімфоцитів.
У 30-40% хворих ХРФ понижена кількість В-лімфоцитів. При оцінці компонентів гуморального імунітету у хворих фурункульозом виявляються різні дисімуноглобулінемії. Найчастіше зустрічаються зниження рівнів IgG і IgM, відмічено зниження аффінності імуноглобулінів.
З вищесказаного виходить, що зміни показників імунного статусу в хворих на ХРФ носять різноплановий характер: у 30-50% відмічена зміна складу субпопуляції лімфоцитів, у 50-70% - фагоцитарної і у 30-60% - гуморальної ланки імунної системи. Залежно від вираженості змін у показниках імунного статусу, хворих на ХРФ можна розділити на три групи: легкої, середньої і важкої тяжкості, що корелює з клінічним перебігом захворювання. При легкому перебігу фурункульозу у більшості хворих (70%) показники імунного статусу знаходяться у межах норми. При середньому і важкому ступені переважно виявляються зміни фагоцитарної і гуморальної ланок імунної системи.
Схема і види імунотерапії. У стадії загострення ХРФ потрібне проведення місцевої терапії у вигляді обробки фурункулів антисептичними розчинами, антибактеріальними мазями, гіпертонічним розчином; у разі локалізації фурункулів у ділянці голови і шиї або наявності множинних фурункулів - проведення антибактеріальної терапії з урахуванням чутливості збудника. У будь-якій стадії захворювання необхідна корекція виявленої патології (санація осередків хронічної інфекції, лікування патології ШКТ, ендокринної патології тощо).
При виявленні у хворих на ХРФ латентної сенсибілізації або за наявності клінічних проявів алергії необхідно додавати до лікування антигістамінні препарати, призначати гіпоалергенну дієту, проводити хірургічне втручання з премедикацією гормональними і антигістамінними препаратами.
У стадії загострення ХРФ рекомендовано застосування наступних імуномодуляторів.
За наявності змін фагоцитарної ланки імунітету доцільне призначення поліоксидонія по 6-12 мг в/м протягом 6-12 діб.
При зниженні аффінности імуноглобулінів - галавіт 100 мг через добу в/м № 15.
При зниженні рівня В-лімфоцитів, порушенні співвідношення CD4/CD8 у бік зменшення ІРІ показане застосування міелопіду по 3 мг в/м щодня або через добу протягом 5-7 діб.
При зниженні рівня IgG на фоні важкого загострення ХРФ при клінічній неефективності застосування галавіту використовуються препарати імуноглобуліну для внутрішньовенного введення (октагам, габріглобін, інтраглобін).
Імунореабілітація
У період ремісії можливе призначення наступних імуномодуляторів.
Поліоксидоній 6-12 мг в/м протягом 6-12 діб - за наявності змін фагоцитарної ланки імунітету.
Лікопід 10 мг протягом 10 діб перорально щоденно 7 діб, потім через добу протягом 2-3 тижнів - за наявності дефектів утворення активних форм кисню.
Галавіт 100 мг № 15 в/м - при зниженні афінності імуноглобулінів, при уповільненому, безперервно рецидивуючому фурункульозі.
Препарати імуноглобуліну для внутрішньовенного введення (октагам, габріглобін, інтраглобін) при стійкому рецидивуванні ХРФ на фоні змін гуморальної ланки імунітету.
Комбінована імуномодулююча терапія
При загостренні фурункульозу можливе призначення поліоксидонію, надалі, при виявленні дефекту аффінності імуноглобулінів, додається галавіт.
При рецидивах фурункульозу - тактивін, міелопід (по 1 мл) 7 днів; далі тактивін через 3 дні протягом 2-3 тижнів.
Місцево на осередки ураження - аплікації 33% дімексиду з 0,1% йодом або 0,05% хлоргексидином. Медикаментозну імунокорекцію корисно поєднувати із застосуванням немедикаментозних методів, що надають корисної імуномодуляції: ультрафіолетовим і лазерним опромінюванням крові, плазмаферезом, УВЧ-терапією.
Як приклад імунодефіциту за фагоцитарним типом (приклад 10) наводимо історію хвороби хворої Р., 28 років, що знаходилась на лікуванні у хірургічному відділенні з діагнозом: хронічний рецидивуючий (стрептококовий) фурункульоз.
Хвора Р., 28 років (приклад 10), скаржиться на наявність гнійників на тулубі та кінцівках. Указані гнійники вперше з’явилися 3 роки тому, загострення спостерігаються 3-4 рази на рік, останнє загострення 2 тижні, хвора приймала доксициклін 100 мг/добу протягом 10 днів, динаміка висипань слабо позитивна. Хворій виставлений діагноз: хронічний рецидивуючий фурункульоз.
При бактеріологічному дослідженні вмісту фурункула висіяний гемолітичний стрептокок.
Заключення імунограми: на імунограмі мають місце ознаки дисрегуляції T-клітинної ланки з відносним зниженням T-хелперної популяції, ІРІ 0,94. Функція В-лімфоцитів і продукція імуноглобулінів не порушені. NK-клітини у нормі. Спостерігається зниження активності гранулоцитарної ланки. Значне зниження поглинальної здатності нейтрофілів (ФЕ, ФЧ), спонтанної бактерицидності (НСТ-тест сп. < 10), функціонального резерву окислювально-відновлювального потенціалу фагоцитів (НСТ-тест рез. < 16), підвищення вмісту комплементу (CH-50). Ознаки інтоксикації (ТЗН).
Висновок: імунодефіцитний стан по фагоцитарній ланці - дефіцит поглинальної функції і перетравлюючої активності нейтрофілів. Ознаки хронічного перебігу запального процесу, що супроводжується інтоксикацією зі зниженою реактивністю імунної системи.
Приклад 10
Імунограма хворої Р., 28 років. Діагноз: хронічний рецидивуючий (стрептококовий) фурункульоз, імунодефіцит за фагоцитарним типом (D 84.9)
Показник |
Результат |
Норма |
ТЗН=45% |
|||||
Гемоглобін |
117 |
Ж - 115-145, Ч - 132-164 г/л |
||||||
Еритроцити |
3,7 |
Ж - 3,7-4,7, Ч - 4,0-5,1 ∙ 1012 /л |
||||||
Тромбоцити |
230 |
150-320 ∙ 109 /л |
||||||
ШОЕ |
14 |
2-15 мм /год |
||||||
Лейкоцити |
6,1 |
4-9 Г/л |
||||||
Нейтр. 43-71% 2000-6500 |
П/я 1-4% 80-400 |
С/я |
Еоз. 0,5-5% 80-370 |
Баз. 0-1% 20-80 |
Мон. 3-9% 90-720 |
Лімф. 25-37% 1600-3000 |
БГЛ 1-5% 80-500 |
Плаз. 0-1% 20-80 |
59 |
6 |
53 |
2 |
1 |
7 |
31 |
0 |
0 |
3600 |
370 |
3230 |
120 |
60 |
430 |
1890 |
||
Імунологічні показники |
Результат |
Норма (ОД СІ) |
Імунологічні показники |
Результат |
Норма (ОД СІ) |
||
Т-лімф. CD-3 |
% |
37 |
50 - 80 |
Ig G |
12,6 |
8,0-18,0 г/л |
|
Абс. Число |
699 |
1000-2200 |
|||||
Т-хелп. CD-4 |
% |
17 |
33-46 |
Ig M |
3,06 |
0,2-2,0 г/л |
|
Абс. число |
321 |
309-1571 |
|||||
Т- цитотокс. CD-8 |
% |
18 |
17-30 |
Ig A |
1,8 |
0,3-3,0 г/л |
|
Абс. число |
340 |
282-999 |
|||||
ІРІ |
CD-4/CD-8 |
0,94 |
1,4-2,0 |
ЦІК |
76 |
30-50 од. опт. щільн. |
|
NK- клітини CD-16 |
% |
19 |
12-23 |
Поглинальна активність |
ФІ |
42 |
60-80% |
Абс. число |
359 |
72-543 |
ФЧ |
1,2 |
1,5-3,5 |
||
В-лімф. CD-22 |
% |
23 |
17-31 |
НСТ-тест |
Сп |
4 |
До 10% |
Абс. число |
435 |
109-532 |
Інд |
8 |
- |
||
РБТЛ |
Сп. |
10 |
До 10% |
рез |
4 |
>16% |
|
Інд. |
60 |
50-70% |
Комплемент |
СН-50 |
75 |
30-60 гем. од/мл |
|
Заключний діагноз: хронічний рецидивуючий (стрептококовий) фурункульоз. Імунодефіцит за фагоцитарним типом (D 84.9).
Імунотропна терапія:
1) специфічна антибактеріальна терапія (імунотерапія нормальним людським імуноглобуліном 4,5 мл в/м через день протягом 10 днів);
2) етіотропна антибактеріальна терапія - спіраміцин 500 мг 2 рази на день;
3) місцево - трідерм на ділянки ураження 2 рази на добу - 2 тижні;
4) поліоксидоній по 6 мг в/м 2 рази на тиждень, 20 діб, або галавіт 100 мг через добу в/м, 20 діб;
5) пробіотик лінекс по 2 капс. 3 рази на добу, 20 діб.
Імунореабілітація
6) віферон 150 тис МОд, через добу в свічках, 10 введень;
7) натрію нуклеїнат по 0,1 г 3 рази на добу 30 діб.
Вторинні імунодефіцити при хронічних запальних процесах бронхолегеневої системи
У хворих хронічним бронхітом і з різними змінами імунного статусу ремісія отримана при лікуванні поліоксидонієм або лікопідом. Поліоксидоній краще призначати у фазу загострення у поєднанні з антибактеріальною терапією при змінах у лімфоїдній системі та фагоцитозі. Отримані позитивні результати у лікуванні загострень інфекції у хворих з бронхіальною астмою на фоні цих імуномодуляторів.
Як приклад порушень T-клітинної ланки та фагоцитозу при патології бронхолегеневої системи (приклад 11) наводимо історію хвороби хворого С., 52 років, що знаходився на лікуванні у терапевтичному відділенні з діагнозом: хронічний бронхіт, загострення.
Хворий С., 52 років, (приклад 11) скаржиться на кашель з виділенням невеликої кількості харкотиння слизисто-гнійного характеру, задишку змішаного характеру при фізичному навантаженні. Хворіє 5 років, останнє загострення на протязі 1 тижня. При огляді відмічається незначний дифузний цианоз. Перкуторно-коробчастий відтінок перкуторного звуку у нижніх відділах легень, аускультативно - над всією поверхнєю легень на фоні жорсткого дихання відмічаютья сухі, розсіяні хрипи.
Аналіз харкотиння хворого С., 52 років: кількість 15 мл, слизово-гнійного характеру, без сторонніх домішок, лейкоцити - 30-40 у п/з, нейтрофіли 20-30 у п/з, макрофаги - 8-10 у п/з, еритроцити - 1-2 у п/з, епітел. клітини (циліндричний) - 1-2 у п/з, змішана флора - St. pneumoniae, Н. Influenzae. БК не виявлено.
Спірометрія хворого С., 52 років.
Графік потік-час
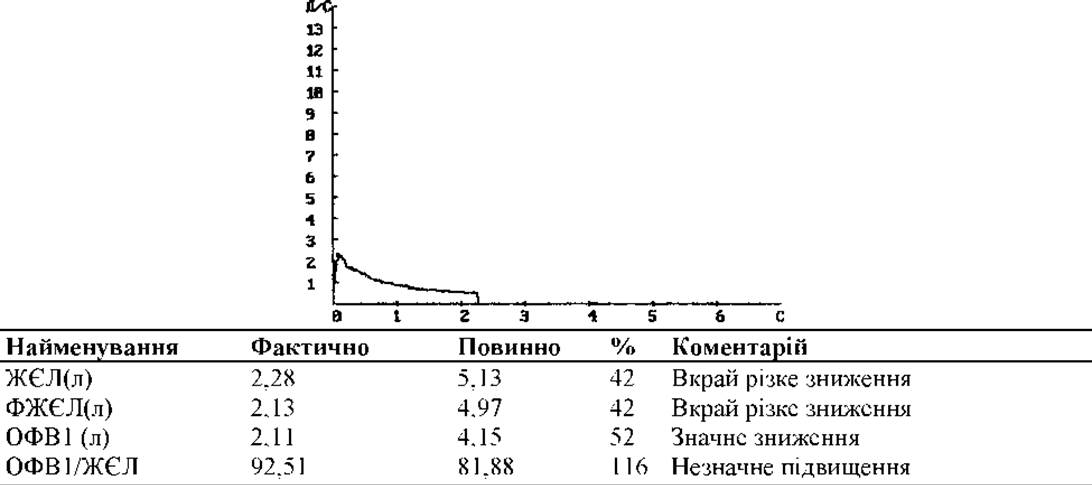
Рентгенограма хворого С., 52 років. Рентгенографія ОГП в прямій проекції. Виявляється посилення бронхолегеневого рисунку, ущільнення коренів легень. Емфізематозні зміни обох легень.
Приклад 11
Імунограма хворого С., 52 років. Діагноз: хронічний бронхіт, загострення з переважними порушеннями T-клітинної ланки та фагоцитозу
Показник |
Результат |
Норма |
||||||||
Гемоглобін |
142 |
Ж - 115-145, Ч - 132-164 г/л |
||||||||
Еритроцити |
5,1 |
Ж - 3,7-4,7, Ч - 4,0-5,1 ∙ 1012 /л |
||||||||
Тромбоцити |
250 |
150-320 ∙ 109 /л |
||||||||
ШОЕ |
25 |
2-15 мм /год |
||||||||
Лейкоцити |
10,3 |
4-9 Г/л |
||||||||
Нейтр. 43-71% 2000-6500 |
П/я 1-4% 80-400 |
С/я |
Еоз. 0,5-5% 80-370 |
Баз. 0-1% 20-80 |
Мон. 3-9% 90-720 |
Лімф. 25-37% 1600-3000 |
БГЛ 1-5% 80-500 |
Плаз. 0-1% 20-80 |
||
76 |
10 |
66 |
4 |
1 |
3 |
16 |
0 |
0 |
||
7830 |
100 |
7730 |
4 |
И0 |
100 |
300 |
164 |
8 |
||
Імунологічні показники |
Результат |
Норма (ОД СІ) |
Імунологічні показники |
Результат |
Норма (ОД СІ ) |
||
Т-лімф. CD-3 |
% |
40 |
50-80 |
IgG |
18,5 |
8,0-18,0 г/л |
|
Абс. число |
656 |
1100-2200 |
|||||
Т-хелп. CD-4 |
% |
20 |
33-46 |
IgM |
2,2 |
0,2-2,0 г/л |
|
Абс. число |
328 |
309-1571 |
|||||
Т- цитотокс. CD-8 |
% |
16 |
20-33 |
IgA |
4,0 |
0,3-3,0 г/л |
|
Абс. число |
262 |
282-999 |
|||||
ІРІ |
CD-4 /CD-8 |
1,25 |
1,4-2,0 |
ЦІК |
90 |
30-50 од. опт.щільн. |
|
NK-клітини CD-16 |
% |
20 |
16-22 |
Поглинальна активність |
ФІ |
85 |
60-80% |
Абс. число |
328 |
72-543 |
ФЧ |
3,82 |
1,5-3,5 |
||
В-лімф. CD-22 |
% |
32 |
10-20 |
НСТ-тест |
Сп |
5 |
До 10% |
Абс. число |
525 |
109-532 |
Інд |
9 |
- |
||
РБТЛ |
Сп. |
9 |
До 10% |
рез |
4 |
>16% |
|
Інд. |
45 |
50-70% |
Комплемент |
СН-50 |
45 |
30-60 гем. од/мл |
|
Заключення аналізу харкотиння: мокрота слизово-гнійного характеру з підвищеним вмістом нейтрофілів та наявністю бактерій.
Заключення рентгенографії ОГП: ознаки хронічного бронхіту.
Заключення спірометрії: виражені порушення вентиляційної функції легень переважно по рестриктивному типу. Різке зниження життєвої ємкості легень.
Заключення імунограми: нейтрофільний лейкоцитоз з помірним здвигом формули вліво. Відносна лімфоцитопенія за рахунок зниження T-хелперів CD-4 та цитотоксичних T-лімфоцитів CD-8, ІРІ 1,25. Підвищення рівня В-лімфоцитів і продукції імуноглобулінів IgM, IgG та IgA. NK- клітини у нормі. Незначне підвищення поглинальної здатності нейтрофілів (ФЕ, ФЧ), при різкому зниженні функціонального резерву окислювально-відновлювального потенціалу фагоцитів (НСТ- тест рез. < 16), що свідчить про незавершеність фагоцитозу.
Висновок: дисфункція Т-клітинної ланки у поєданні з неефективним фагоцитозом. Ознаки загострення хронічного запального процесу (підвищення IgG, IgM) у ділянці слизових оболонок (збільшення IgA).
Заключний діагноз: хронічний бронхіт, загострення. Дисфункція імунної системи з переважними порушеннями T-клітинної ланки та фагоцитозу.
Виходячи з особливостей імунологічного статусу хворого С., для лікування хронічного бронхіту призначили наступну схему імунотропної терапії:
1) етіотропна антибактеріальна терапія - амоксиклав 500/125 мг 3 рази на день в/м 7 днів;
2) галавіт 0,1 г в/м через день, 10 ін’єкцій;
3) імунофан 0,005% по 0,4-0,7 мл п/ш 2 рази на тиждень, 10 ін’єкцій;
4) АЦЦ-лонг 600 мг по 1 табл. 1 раз на день, 10 днів.
Імунореабілітація
5) респіброн по 1 табл. на день під язик, курс - 10 днів. З метою профілактики по 1 табл. на день, курс - по 10 днів протягом 3 місяців.;
6) тималін 1 мл підшкірно через добу, 10 діб.
При імунодефіцитах, що виявляються на фоні ХОЗЛ, позитивний ефект спостерігається при призначенні: левамізолу, тактивіну, нуклеїнату натрію, діуцифону та інших. У ряді випадків при ХОЗЛ переважним є інгаляційний шлях введення імуномодуляторів (поєднання розчинів димексиду і левамізолу).
Як приклад імунодефіциту за B-клітинним типом при патології бронхо-легеневої системи (приклад 12) наводимо історію хвороби хворого Т., 58 років, що знаходився на лікуванні у терапевтичному відділенні з діагнозом: хронічне обструктивне захворювання легень II ст., загострення. ЛН II ст.
Хворий Т., 58 років (приклад 12), страждає на ХОЗЛ протягом останніх 5 років, загострення спостерігаються 2-3 рази на рік. Хворий постійно знаходиться на базисній терапії спиріва (тіотропія бромид) 18 мкг 1 інгаляція 1 раз на день, теофілін 150 мг 1 раз на день.
Заключення імунограми: відносна лімфоцитопенія. Дисрегуляція T-клітинної ланки з відносним підвищенням T-хелперної популяції, ІРІ 2,5. Зниження рівня В-лімфоцитів. Продукція IgM знижена, а IgA - підвищена. NK-клітини у нормі. Значне підвищення поглинальної здатності нейтрофілів (ФІ, ФЧ), при зниженні функціонального резерву окислювально-відновлювального потенціалу фагоцитів (НСТ-тест рез. < 16), що свідчить про незавершеність фагоцитозу.
Висновок: імунодефіцитний стан по B-клітинній ланці, дисрегуляція продукції імуноглобулінів, що свідчить про загострення хронічного запального процесу (підвищення IgM) у ділянці слизових оболонок (збільшення IgA). Активація фагоцитозу з ознаками його неефективності.
Приклад 12
Імунограма хворого Т., 58 років. Діагноз: хронічне обструктивне захворювання легень, II ст., загострення. ЛН II ст.
Імунодефіцит за B-клітинним типом (D 84.9)
Показник |
Результат |
Норма |
Незначний анізоцитоз, анізохромія |
|||||
Гемоглобін |
122 |
Ж - 115-145, Ч - 132-164 г/л |
||||||
Еритроцити |
3,8 |
Ж - 3,7-4,7, Ч - 4,0-5,1 ∙ 1012 /л |
||||||
Тромбоцити |
220 |
150-320 ∙ 109 /л |
||||||
ШОЕ |
11 |
2-15 мм /год |
||||||
Лейкоцити |
6,6 |
4-ж9 Г/л |
||||||
Нейтр. 43-71% 2000-6500 |
П/я 1-4% 80-400 |
С/я |
Еоз. 0,5-5% 80-370 |
Баз. 0-1% 20-80 |
Мон. 3-9% 90-720 |
Лімф. 25-37% 1600-3000 |
БГЛ 1-5% 80-500 |
Плаз. 0-1% 20-80 |
66 |
3 |
63 |
6 |
1 |
3 |
23 |
0 |
0 |
4360 |
200 |
4160 |
400 |
70 |
200 |
1518 |
||
Імунологічні показники |
Результат |
Норма (ОД СІ) |
Імунологічні показники |
Результат |
Норма (ОД СІ ) |
||
Т- лімф. CD-3 |
% |
72 |
50-80 |
IgG |
11,9 |
8,0-18,0 г/л |
|
Абс. число |
1092 |
1100-2200 |
|||||
Т- хелп. CD-4 |
% |
53 |
33-46 |
IgM |
0,18 |
0,2-2,0 г/л |
|
Абс. число |
804 |
309-1571 |
|||||
Т- цитотокс. CD-8 |
% |
21 |
20-33 |
IgA |
4,8 |
0,3-3,0 г/л |
|
Абс. число |
319 |
282-999 |
|||||
ІРІ |
CD-4 /CD-8 |
2,5 |
1,4-2,0 |
ЦІК |
59 |
30-50 од. опт.щільн. |
|
NK- клітини CD-16 |
% |
23 |
16-22 |
Поглинальна активність |
ФІ |
91 |
60-80% |
Абс. число |
349 |
72-543 |
ФЧ |
4,45 |
1,5-3,5 |
||
В-лімф. CD-22 |
% |
8 |
10-20 |
НСТ-тест |
Сп |
21 |
До 10% |
Абс. число |
121 |
109-532 |
Інд |
26 |
- |
||
РБТЛ |
Сп. |
10 |
До 10% |
рез |
5 |
>16% |
|
Інд. |
40 |
50-70% |
Комплемент |
СН-50 |
55 |
30-60 гем. од/мл |
|
Заключний діагноз: хронічне обструктивне захворювання легень II ст., загострення. ЛН II ст. Імунодефіцит за B-клітинним типом (D 84.9).
Виходячи з особливостей імунологічного статусу хворого Т., для лікування ХОЗЛ призначили наступну схему імунотропної терапії:
1) етіотропна антибактеріальна терапія - левофлоксацин 500 мг в/в крапельно 1 раз на день 7 днів, димексид 5 мл на 200 мл 0,9% розчину хлориду натрію в/в крапельно 1 раз на день 5 днів; азитроміцин 500 мг 1 раз на день 3 дні;
2) поліоксидоній по 6 мг в/м 2 рази на тиждень, протягом 10 діб;
3) галавіт 100 мг 1 раз на добу в/м, 10 діб;
4) лактофільтрум по 2 капс. 2 рази на добу, 14 діб;
5) флуконазол 100 мг через добу, 10 діб.
Імунореабілітація
6) ІРС-19 інгаляції 1 раз на добу, 20 діб;
7) тималін 1 мл підшкірно через добу, 10 діб.
Вторинні імунодефіцити при внутриклітинних інфекціях Хламідійна інфекція
Хламідійна інфекція супроводжується наявністю антитіл у крові, але недостатністю уродженого і набутого імунітету. У хворих знижений рівень NK, HLA-DR-лімфоцитів, субпопуляцій Т- і В-лімфоцитів, порушений цитокіновий та інтерфероновий статус.
Схема і види імунотерапії. При персистуючій формі хламідійної інфекції позитивні ефекти відмічені після включення у схему лікування поліоксидонію, глутоксиму, препаратів інтерферонів, лейкінферону, що призначаються звичайним чином і у свічках. Високоефективне послідовне застосування ронколейкіну і беталейкіну. У хворих з сечостатевим хламідіозом ефективні ронколейкін і бестім на фоні макролідів (вільпрафен та ін.).
Місцеве, внутрішньо-уретральне застосування препаратів (беталейкін, ронколейкін) може бути ефективнішим; курс - 15-20 щоденних інстилляцій по 5-6 мл (5 нг/мл беталейкіна).
Корисні індуктори інтерферонів (циклоферон, неовір, арбідол, аміксин). Аміксин призначають по 0,25 г/добу 2 доби, потім по 0,125 мг через 48 год. протягом 4-х тижнів; антибіотики призначають на 3-й день.
При ознаках Т-клітинної недостатності застосовують тимічні препарати (тактивін, тималін).
Активація імунітету може бути отримана при призначенні специфічних вакцин, а при їх відсутності - універсальних вакциноподібних препаратів (лікопід та ін.).
Туберкульоз
Туберкульоз - інфекція з внутрішньоклітинним паразитуванням мікобактерій, обумовленим недостатністю у сприйнятливих індивідів чинників уродженого, зокрема фагоцитарного (кілінг, перетравлення), імунітету на фоні високої алергічної реактивності негайного і сповільненого типу на антигени мікобактерій.
При туберкульозі виявляються IgG-антитіла і сенсибілізовані Т-лімфоцити, що не забезпечують імунітет. Вакцина БЦЖ не індукує стійкого імунітету в чутливих до мікобактерій осіб. Зростаюча резистентність мікобактерій до основних лікарських препаратів створює проблеми лікування хворих. Імунокоригуюча терапія, направлена на стимуляцію специфічної і неспецифічної резистентності хворих, може поліпшити ситуацію.
Схема і види імунотерапії. Для активації фагоцитарної ланки імунітету в хворих на туберкульоз легень апробований лікопід. Доведена його активуюча дія на моноцитарно-макрофагальну систему вродженого імунітету - утворення активних форм кисню, синтез ІЛ-1 і ФНП-а. Лікопід застосовують по 10 мг 10 днів на фоні етіотропної терапії або по 1 табл. (10 мг) 1 раз під язик, 3 цикли по 7 днів з інтервалами 2 тижні. Припинення виділення бактерій спостерігали у 80% хворих; зменшувалися гнійна мокрота, інтоксикація, підвищувалися число Т-лімфоцитів і бактерицидність фагоцитів.
Глутоксим призначають хворим на туберкульоз легень (інфільтративна, казеозна і диссемінована форми) протягом 50 днів внутрішньовенно і внутрішньом’язово по 1 мл 3% розчину двічі на день. Препарат зменшує інтоксикацію, запалення у легенях, попереджає загострення хронічного гепатиту, лейкопенію.
Галавіт зменшує генералізацію туберкульозу в легенях. У хворих диссемінованим та інфільтративним туберкульозом підсилює клінічну ефективність протитуберкульозних препаратів, зменшує їх побічні ефекти. Препарат знижує лімфоцитоз, збільшує знижений рівень СD19+ В-лімфоцитів, знижує збільшений рівень IgA.
Поліоксидоній у комплексній терапії туберкульозу покращує клініко-рентгенологічну картину захворювання, стимулює закриття порожнин розпаду легеневої тканини, розсмоктування вогнищ запалення. Він нормалізує показники імунного статусу і стимулює активність фагоцитозу.
Лейкінферон у хворих на туберкульоз терапевтичного профілю застосовують по 1 ампулі 3 рази на тиждень, курс 12-15 ін’ єкцій. У хірургічних хворих його призначають до операції по 1 ампулі внутрішньом’язово 3 рази на тиждень, курс 6-36 ампул. На 2-й день після операції препарат вводять внутрішньом’язово по 1-2 ампули через день і внутрішньоплеврально по 1 ампулі з хіміопрепаратами. Він зменшує інтоксикацію, в 2-4 рази прискорює припинення бациловиділення, зменшує деструктивні зміни у легенях, прискорює закриття порожнин розпаду.
Ронколейкін (рекомбінантний ІЛ-2) на фоні застосування протитуберкульозних препаратів вводять внутрішньовенно хворим туберкульозом легень по 500 тис. МОд через день - 3 ін’єкції. Безпосередні результати лікування поліпшувалися на 30%, зменшувалася частота постопераційних ускладнень, поліпшувалися показники імунітету
Отже, випробувані імуномодулятори на фоні базисної терапії туберкульозу істотно покращують її ефективність, нормалізують показники імунного статусу.
Вторинні імунодефіцити при вірусних інфекціях
Віруси здатні індукувати вторинні імунодефіцити двома шляхами - безпосередньо руйнуючи імунокомпетентні клітини (ВІЛ) і змінюючи їх рецептори, активність взаємодії, модифікуючи імунореактивність (CMV, HSV, EBV).
Віруси можуть служити індукторами вторинних імунодефіцитів і провокувати ускладнення будь-якого запального процесу. Так, вірус EBV може вражати В- лімфоцити і викликати гіпо- і агаммаглобулінемію. Віруси кору, грипу, паротиту, краснухи, CMV змінюють співвідношення між популяціями клітин, порушують кооперацію цих клітин, пригнічують імунні реакції і підвищують чутливість до бактеріальних агентів. Хронічна персистенція вірусу герпесу в лейкоцитах і нервових гангліях, вірусу гепатитів В і С у гепатоцитах створює всі умови для розвитку вторинних імунодефіцитів. Вірус імунодефіциту сам руйнує Т-хелпери, викликаючи дисбаланс в імунній системі.
Як приклад імунодефіциту по T-лімфоцитопенічному типу при хронічному вірусному захворюванні (приклад 13) наводимо історію хвороби хворої Д., 37 років, що знаходилася на лікуванні у терапевтичному відділенні з діагнозом: інфекція у ділянці обличчя і губ.
Хвора Д., 37 років, скаржиться на висип на слизовій оболонці верхньої губи та на шкірі носо-губного трикутника, що свербить. Указані прояви спостерігаються на протязі останніх 2 років, носять рецидивуючий характер. Загострення відбуваються після переохолодження та ОРЗ. При огляді на верхній губі та на шкірі носо-губного трикутника виявляється локальний висип везикуло-папульозного характеру, в порожнині рота у хворої виявлені ерозійні зміни на язику, кваліфіковані як кандидоз.
Приклад 13
Імунограма хворої Д., 37 років. Діагноз: хронічна рецидивуюча герпес-вірусна інфекція у ділянці обличчя і губ, оро-фарінгеальний кандидоз, імунодефіцит за T-лімфоцитопенічним типом (D 84.9)
Показник |
Результат |
Норма |
||||||
Гемоглобін |
112 |
Ж - 115-145, Ч - 132-164 г/л |
||||||
Ерітроцити |
3,4 |
Ж - 3,7-4 ,7, Ч - 4,0-5,1 ∙ 1012 /л |
||||||
Тромбоцити |
260 |
150-320 ∙ 109 /л |
||||||
ШОЕ |
18 |
2-15 мм /год |
||||||
Лейкоцити |
3,8 |
4-9 Г/л |
||||||
Нейтр. 43-71% 2000-6500 |
П/я 1-4% 80-400 |
С/я |
Еоз. 0,5-5% 80-370 |
Баз. 0-1% 20-80 |
Мон. 3-9% 90-720 |
Лімф. 25-37% 1600-3000 |
БГЛ 1-5% 80-500 |
Плаз. 0-1% 20-80 |
67 |
3 |
64 |
4 |
0 |
8 |
21 |
0 |
0 |
2550 |
110 |
2440 |
150 |
300 |
800 |
|||
Імун. показники |
Результат |
Норма (ОД СІ) |
Імун. показники |
Результат |
Норма (ОД СІ ) |
||
Т- лімф. CD-3 |
% |
45 |
50-80 |
Ig G |
15,1 |
8,0-18,0 г/л |
|
Абс. число |
360 |
1000-2200 |
|||||
Т-хелп. CD-4 |
% |
27 |
33-46 |
Ig M |
4,08 |
0,2-2,0 г/л |
|
Абс. число |
216 |
309-1571 |
|||||
Т- цитотокс. CD-8 |
% |
39 |
17-30 |
Ig A |
1,62 |
0,3-3,0 г/л |
|
Абс. число |
312 |
282-999 |
|||||
ІРІ |
CD-4/CD-8 |
0,69 |
1,4-2,0 |
ЦІК |
62 |
30-50 од. опт. щільн. |
|
NK-клітиниCD-16 |
% |
15 |
12-23 |
Поглинальна активність |
ФІ |
93 |
60-80% |
Абс. число |
120 |
72-543 |
ФЧ |
4,57 |
1,5-3,5 |
||
В-лімф. CD-22 |
% |
28 |
17-31 |
НСТ-тест |
Сп |
11 |
До 10% |
Абс. число |
224 |
109-532 |
Інд |
19 |
- |
||
РБТЛ |
Сп. |
14 |
До 10% |
рез |
8 |
>16% |
|
Інд. |
71 |
50-70% |
Комплемент |
СН-50 |
74 |
30-60 гем. од/мл |
|
Заключення по імунограмі: дані імунологічного дослідження дозволили встановити, що перебіг вірусної інфекції (герпес) у даної хворої характеризується лімфопенією, з відносним Т-цитозом (СБ-8), зниженням імуно-регуляторного індексу (ІРІ=0,59), незначним підвищенням ШОЕ, активацією гуморальної ланки імунітету за рахунок підвищення продукції IgM, активацією фагоцитозу (поглинальної активності нейтрофілів, спонтанної бактерицидності), зниження функціонального резерву окислювально-відновлювального потенціалу фагоцитів (НСТ-тест рез. < 16). Підвищення вмісту комплементу (CH-50).
Лімфопенія у поєднанні з підвищенням рівня цитотоксичних лімфоцитів і зниженням ІРІ, а також зниження функціонального резерву окислювально-відновлювального потенціалу фагоцитів (НСТ-тест рез.) свідчать на користь наявності у хворого хронічної вірусної інфекції (супресований варіант імунної відповіді). У хворої імунодефіцитний стан за T-лімфоцитопенічним типом (D 84.9).
Заключний діагноз: хронічна рецидивуюча герпес-вірусна інфекція у ділянці обличчя і губ. Оро-фарінгеальний кандидоз. Імунодефіцит за T-лімфоцитопенічним типом (D 84.9).
Етіотропна та імунотропна терапія:
1) етіотропна противірусна терапія - зовіракс (ацикловір) 400 мг всередину 4 рази на день протягом 1 місяця; герпевір (мазь) - змащувати уражені ділянки шкіри і слизової оболонки губ 4 рази на день 7 діб;
3) неспецифічна противірусна терапія:
- віферон по 500 000 МО 1 раз на день у свічках протягом 1 місяця; вірогель - змащувати уражені ділянки шкіри і слизової оболонки губ 2 рази на добу 5-7 діб;
- індуктор інтерферону - циклоферон - 12,5% розчин для ін'єкцій - 2 мл, разова доза 0,25 г в/м на 1, 2, 4, 6, 8, 11, 14, 17, 20, 23, 26, 29-ту добу. Призначають після інтерферонотерапії;
4) імунофан по 1 мл в/м через добу № 10;
5) поліоксидоній 12 мг (свічки) 1 раз на 3 дні № 10;
6) аміксин по 125 мг (1 капс.) через добу після сніданку № 20;
7) інтраконазол (інтрунгар) 100 мг 1 раз на добу 2 тижні.
Імунореабілітація
8) тималін по 1 мл підшкірно через добу № 10;
9) циклоферон 12,5 мг підшкірно 2 рази на тиждень № 10;
10) галавіт 0,1 г (свічки) через день, протягом 20 днів.
Вторинні імунодефіцити при паразитарних інвазіях
Паразитуючі гельмінти виділяють речовини, що пригнічують імунну відповідь і активують Т-супресори. Паразитуючи у макрофагах та інших клітинах крові, тріпаносоми, токсоплазми позбавляють їх можливості участі в імунній відповіді. У діагностиці вторинних імунодефіцитів при інвазіях найбільше значення має виявлення паразитів, їх яєць або личинок і виявлення алергії до їх антигенів у шкірних пробах і в тестах in vitro.
Синдром хронічної втоми (код МКХ-10 D86.9)
Синдром хронічної втоми (СХВ) є постінфекційним (ОРВІ) хронічним захворюванням, основний прояв якого - немотивована виражена загальна слабкість, що на тривалий час виводить людину з активного повсякденного життя. Головними мішенями хвороби є ЦНС і імунна система.
Частота СХВ складає 10-37 випадків на 100 тис. населення.
Діагностичні критерії СХВ
Великі діагностичні критерії: 1) втома, що не проходить, і зниження працездатності (не менш ніж на 50%) у раніше здорових людей протягом останніх шести місяців; 2) виключення інших причин або хвороб, які можуть викликати хронічну втому.
Малі симптоматичні критерії: 1) раптовий початок; 2) підвищення температури до 38 °С; 3) болі у горлі, першіння; 4) невелике збільшення (до 0,30,5 см) і болісність шийних, потиличних і пахових лімфатичних вузлів; 5) нез’ясована генералізована м’язова слабкість; 6) болісність окремих груп м’язів (міалгії); 7) мігруючі болі у суглобах (артралгії); 8) періодичний головний біль; 9) швидка фізична втомлюваність з подальшою тривалою (понад 24 год.) втомою; 10) розлади сну (гіпо- або гіперсомнія); 11) нейропсихологічні розлади (фотофобія, зниження пам’яті, підвищена дратівливість, сплутана свідомість, зниження інтелекту, неможливість концентрації уваги, депресія); 12) швидкий розвиток (протягом годин або днів) всього симптомокомплексу.
Об’єктивні (фізикальні) критерії: 1) субфебрильна температура; 2) неексудативний фарингіт; 3) пальповані шийні або пахвові лімфовузли (менше 2 см у діаметрі).
Діагноз СХВ встановлюється за наявності 1 і 2 великих критеріїв, а також малих симптоматичних критеріїв: 6 (або більше) з 11 симптоматичних критеріїв і 2 (або більше) з 3 фізикальних критеріїв; або 8 (або більше) з 11 симптоматичних критеріїв.
До захворювання схильні люди будь-якого віку, проте відмічено, що жінки у віці 25-49 років хворіють частіше, ніж чоловіки. В окремих випадках захворювання розвивається через 2 роки після першої атаки. У більшості пацієнтів хронічна втома та інші супутні симптоми, почавшись у період грипоподібного захворювання, після одного-двох тижнів дещо зменшуються, але одужання не наступає. У найбільш важких випадках може початися сильна депресія, наступає втрата концентрації уваги і різка фізична слабкість. Описані випадки спонтанного одужання. Проте велика частина хворих продовжує страждати від циклічних захворювань протягом багатьох місяців або років.
Етіологія і патогенез. Найбільш вірогідною причиною СХВ є вірусна інфекція, конкретний представник якої у даний час не встановлений. Це може бути один з герпес-вірусів (Епштейна-Барр (EBV), цитомегаловірус (CMV), вірус герпесу 1 і 2-го типу (HSV-1, 2), вірус герпесу 6-го типу (HSV-6)), varisella zoster (HSV-4), віруси Коксакі А або В, ентеровіруси та ін. СХВ, вочевидь, є мультипричинним розладом нейроімунних механізмів, який виявляється у генетично схильних осіб у результаті активації імунної системи інфекційними агентами і дисрегуляції ЦНС. Латентна інфекція може призводити до хвороби (тобто включатися) при дії ряду можливих стимулів: важкий емоційний стрес, несприятливі чинники зовнішнього середовища, інтоксикації, травми, хірургічні втручання, вагітність, пологи та ін.
Інша теорія відводить головну роль нейропсихічним чинникам з переважанням імунодисрегуляції.
Імунна дисфункція. Існує велика кількість "пускових механізмів", що викликають імунологічні реакції, які залучають різні типи клітин крові та молекул, таких як інтерферон та інтерлейкіни. Можна вважати, що у хворих на СХВ ці механізми порушені, причому може спостерігатися як збільшення, так і зменшення значень імунологічних показників. Наприклад, у 20% хворих з СХВ спостерігається лейкоцитоз і у такої ж кількості - лейкопенія. Відносний лімфоцитоз відмічається у 20% випадків, лімфопенія - у 30% пацієнтів. У 30% пацієнтів відмічено зниження рівня сироваткових імуноглобулінів класів A, D, G і M, у 30% хворих СХВ рівень імуноглобулінів, навпаки, збільшений. 50% пацієнтів мають низькі рівні циркулюючих імунних комплексів, у 25% відмічається знижена активність комплементу.
Прояв дисфункції імунної системи у хворих СХВ виражається також у зниженні цитотоксичної активності природних кілерів; підвищенні рівнів ІЛ-1-a, 2 і 6; зниженні мітоген-стимульованих лімфоцитів, підвищенні вмісту альфа- інтерферону та інших цитокинів; зміні числа і функції Т- і В-лімфоцитів.
Серологічні дослідження зазвичай не виявляють значних відхилень. Є відомості про присутність у низьких концентраціях антиядерних антитіл і ревматоїдного чинника, але без клінічних проявів системного вовчаку або ревматоїдного артриту. Збільшення вмісту кріоглобулінів і холодових аглютинінів було знайдене у невеликого числа (8%) пацієнтів.
З урахуванням виду етіологічного чинника виділяють наступні варіанти СХВ:
1. Інтоксикаційний вариант - дія біологічно-активних чинників навколишнього середовища призводить до зміни функціонування імунної та центральної нервової системи. Характерними порушеннями імунної системи є зниження фагоцитарної активності лейкоцитів, збільшення значень ТЗН (токсична зернистість нейтрофілів), знижується НСТ-тест, збільшується рівень IgG і кількість циркулюючих імунних комплексів, тобто спостерігається активація антитоксичної функції імунітету.
2. Ендокринний варіант СХВ - порушуються співвідношення рівнів гормонів як у крові, так і у тканинах, що призводить до погіршення функціонування центральної нервової системи. Найбільш значущими є зниження рівнів гормонів щитоподібної залози, дисбаланс статевих гормонів (при клімаксі), дисфункція кори надниркових залоз.
3. Інфекційний варіант - персистування "повільних" вірусних інфекцій, таких як герпес-, ЦМВ- і Епштейн-Бар-вірусна інфекція, призводить до дисфункції імунної системи. Слід звернути увагу на той факт, що ряд змін імунологічних параметрів, а саме, зниження функціональної активності природних кілерів (NK- клітин) і макрофагів, зниження відповіді лімфоцитів на мітогени і активації CD4+ лімфоцитів, є загальними для СХВ і різних вірусних інфекцій.
Основні принципи лікування СХВ. На даний час специфічне лікування СХВ не розроблене. Є тактика лікування, яка дозволяє продовжити ремісії захворювання і повернути пацієнтів до роботи. Застосовуються трициклічні антидепресанти, інгібітори зворотного захоплення серотоніну (флуоксетин-прозак), які підвищують енергетичні можливості пацієнта, коригують сон, знижують болісність і напруженість у м’язах. Проводиться комплексна терапія імунотропними препаратами з урахуванням результатів імунологічного обстеження. Основні напрями терапії СХВ можна сформулювати таким чином:
1. Повноцінна, збалансована по білках, вітамінах і мікроелементах (Zn, Se, Cu, Co) дієта.
2. Режим антигенного щадіння: гіпоалергенна дієта; санація вогнищ хронічних інфекції; відмова від вакцинації під час проведення курсу комплексної терапії; відновлення мікробіоценозу шкіри, відкритих і закритих слизових оболонок.
3. Терапія антиоксидантами.
4. Імуномодулююча терапія.
5. Адекватна раціональна антибактеріальна, противірусна, протигрибкова терапія.
Принципи імунотропної (імуномодулюючої) терапії СХВ (по точках додатку):
1. Відновлення Т-клітинного імунітету з використанням тимічних чинників (тактивін, тималін, тимоген, імунофан, гепон).
2. Відновлення інтерферонового статусу (віферон, лаферон).
3. Відновлення активності NK-клітин (імуномакс, гепон, лікопід, поліоксидоній).
4. Відновлення гуморального імунітету (мієлопід).
При виявленні у хворого з СХВ імунодефіциту лімфоцитарного типу призначають:
1) стимулятори синтезу ІЛ-2 (ізопрінозин, гропрінозин);
2) тимічні пептиди: старі (тималін, тактивін, тимоптин) і нові (задоксин, імунофан);
3) галавіт.
Імунологічні критерії ефективності терапії:
1. Зниження вмісту CD3, CD4, CD25.
2. Зниження імунорегуляторного індексу CD4/CD8.
3. Зниження продукції ІЛ-2, гамма-інтерферону.
4. Збільшення продукції ІЛ-4, 5, 6.
При виявленні у хворого з СХВ імунодефіциту інтерферонового типу призначають:
1) інтерферони (віферон, лаферон);
2) індуктори ендогенного інтерферону і NK-клітин: акрідони (неовір, циклоферон); аміксин; антиагреганти (курантил); нові (з тривалим ефектом) - кагоцел.
Імунологічні критерії ефективності терапії:
1. Зниження продукції альфа- і гамма-інтерферонів.
2. Зниження рівня CD4, CD 16.
3. Зниження імунорегуляторного індексу CD4/CD8.
4. Збільшення продукції ІЛ-4, 5, 6.
При виявленні у хворого з СХВ імунодефіциту гуморального типу призначають специфічні імуноглобуліни: антигерпетичний (тип 1 або 2), антицитомегаловірусний, антихламідійний, а у разі невстановленого виду вірусної інфекції - нормальний людський.
Імунологічні критерії ефективності терапії:
1. Зменшення кількості CD19.
2. Зниження рівнів специфічних IgМ, IgG і нормалізція полімеразної ланцюгової реакції (ПЛР).
3. При серонегативній формі інфекції - нормалізація титрів IgA, IgM, IgG, зменшення рівня В-лімфоцитів і плазмоцитів, зниження рівня ЦІК і комплементу.
При виявленні у хворого з СХВ імунодефіциту фагоцитарного типу призначають:
1) поліоксидоній - 6 мг препарату перед ін’єкцією розчиняють в 1-1,5 мл фізрозчину, дистильованій воді або 0,25% розчину новокаїну, вводять в/м або підшкірно через день, курс - 5 ін’єкцій; потім 2 рази на тиждень курсом 10-15 ін’єкцій;
2) метілурацил - застосовується у таблетках по 0,5 г 3 рази на день протягом 3-4 тижнів або тривалішими курсами.
Імунологічні критерії ефективності терапії:
1. Зниження фагоцитарного числа та індексу.
2. Зниження показника НСТ-тесту.
Етіотропна терапія - призначають препарати ацикловіру (зовіракс, гевіран, ацик, герпівір), валацикловір (вальтрекс), ганцикловір (цимевін), панцикловір (денавір), фамцикловір (фамвір). Препарати призначаються:
1) обов’язково - у период загострення (VHS-1, 2, 4, 6, CMV, EBV IgM+, DNA+);
2) бажано - при виявлені специфічних органних уражень при умові наростання концентрації специфичних IgG (VHS-1, 2, 4, 6, CMV, EBV) у динаміці; 3) як варіант вірус-супресивної терапії (підтримка ремісії) - у меншій дозі і протягом більш тривалого часу. При рецидивуванні у хворого ГРЗ, частих загостреннях хронічного бронхіту, інших інфекцій показана антибіотикотерапія препаратами широкого спектру дії, ефективними у відношенні внутрішньоклітинної інфекції: 1) макроліди (спіраміцин, рокситроміцин, кларитроміцин, дирітроміцин, азитроміцин, джозаміцин, пристинаміцин, миноциклін); 2) фторхінолони (2, 4-го покоління - "нереспіраторні": ципрофлоксацин або гатифлоксацин).
Критерії ефективності терапії: обов’язкове виявлення інфекції (наприклад, Chl-IgM+, Chl-DNA+, зростання концентрації Chl-IgG у динаміці).
Клінічні ефекти терапії СХВ:
1) регресія проявів СХВ, регресія хронічної втоми, відновлення працездатності, розумових здібностей, пам’яті, поліпшення настрою;
2) регресія симптомів хронічної інтоксикації;
3) регресія ознак хронічного фарингіту і тонзиліту;
4) скорочення кількості ОРВІ з 15-24 на рік до 1-3 на рік;
5) зменшення епізодів VHS-1,2 з 15-24 на рік до 1-2 на рік.
6) елімінація EBV, CMV, HV-6, Chl (полімеразна ланцюгова реакція - додіагностичний рівень).
Прогноз при СХВ у більшості випадків сприятливий. Пацієнти в основному видужують протягом 2-4 років, проте повного відновлення фізичної активності не відбувається. Приблизно у 15-20% хворих відмічається прогресивне посилення симптоматики.
Як приклад імунодефіциту по T-лімфоцитопенічному типу при хронічному вірусному захворюванні (приклад 14) наводимо історію хвороби хворої О., 48 років, що знаходилася на лікуванні у терапевтичному відділенні з діагнозом: синдром хронічної втоми, хронічна рецидивуюча герпес-вірусна інфекція з локалізацією у ділянці губ, ВПГ-1, загострення.
Хвора О., 48 років, скаржиться на виражену втому впродовж останніх 6 місяців. В анамнезі у хворої часті стресові ситуації на роботі, хронічна рецидивуюча герпетична інфекція з висипаннями в ділянці губ. Останнє загострення спостерігалося після переохолодження 2 тижні тому, супроводжувалося посиленням загальної слабкості, "розбитості", депресії, що змусило хвору звернутися до психоневролога, який направив її до клінічного імунолога.
Заключення імунограми: відносний ЦТЛ-цитоз. Підвищення поглинальної активності нейтрофілів (Ф1, Ф4), спонтанна бактерицидність (НСТ-тест сп.). Знижений функціональний резерв окислювально-відновлювального потенціалу фагоцитів (НСТ-тест рез.), підвищений вміст комплементу.
Знижений відносний і абсолютний вміст T-лімфоцитів (CD-3 із зниженням імунорегуляторного індексу (ІРІ) убік T-цитотоксичних лімфоцитів (хелперів) CD8. Підвищення рівня всіх класів імуноглобулінів (IgG, IgM, IgA), трохи підвищений вміст імунних комплексів (ЦІК).
Висновок: ознаки формування імунодефіцитного стану по T-клітинній ланці на фоні високого антигенного навантаження (активація фагоцитозу, підвищення вмісту імуноглобулінів).
Методом ІФА у хворої були визначені підвищені титри IgG HSV-1 1:550, IgM HSV-1 1:600, IgG CMV 1:550 (норма до 1:400).
Хворій поставлений діагноз: синдром хронічної втоми. Хронічна рецидивуюча герпес- вірусна інфекція з локалізацією у ділянці губ, ВПГ-1, загострення. Імунодефіцит (D84.9), лімфоцитарний тип, хронічний перебіг, ІН-1, ФН II стадії.
Приклад 14
Імунограма пацієнтки О., 48 років. Діагноз: синдром хронічної втоми.
Хронічна рецидивуюча герпес-вірусна інфекція з локалізацією у ділянці губ, ВПГ-1, загострення. Імунодефіцитний стан по T-клітинній ланці на фоні високого антигенного навантаження
Показник |
Результат |
Норма |
|||||||
Гемоглобин |
145 |
Ж - 115-145, Ч - 132-164 г/л |
СЛГ=21% |
||||||
Ерітроцити |
4,3 |
Ж - 3,7-4 ,7, Ч - 4,0-5,1 ∙ 1012 /л |
|||||||
Тромбоцити |
200 |
150-320 ∙ 109 /л |
|||||||
ШОЕ |
12 |
2-15 мм /год |
|||||||
Лейкоцити |
7,3 |
4-9 Г/л |
|||||||
Нейтр. 43-71% 2000-6500 |
П/я 1-4% 80-400 |
С/я |
Еоз. 0,5-5% 80-370 |
Баз. 0-1% 20-80 |
Мон. 3-9% 90-720 |
Лімф. 25-37% 1600-3000 |
БГЛ 1-5% 80-500 |
Плаз. 0-1% 20-80 |
|
64 |
1 |
63 |
6 |
0 |
7 |
19 |
2 |
||
4570 |
70 |
4600 |
44 |
0 |
510 |
1390 |
150 |
||
Імунолог. показники |
Результат |
Норма (ОД СІ) |
Імунолог. показники |
Результат |
Норма (ОД СІ ) |
||
Т- лімф. CD-3 |
% |
46 |
50-80 |
IgG |
18,8 |
8,0-18,0 г/л |
|
Абс. число |
639 |
1000-2200 |
|||||
Т- хелп. CD-4 |
% |
28 |
33-46 |
IgM |
2,6 |
0,2-2,0 г/л |
|
Абс. число |
389 |
309-1571 |
|||||
Т- цитотокс. CD-8 |
% |
29 |
20-33 |
IgA |
3,2 |
0,3-3,0 г/л |
|
Абс. число |
305 |
282-999 |
|||||
ІРІ |
CD-4/CD-8 |
1,27 |
1,4-2,0 |
ЦІК |
60 |
30-50 од. опт. щільн. |
|
NK-кл. CD-16 |
% |
26 |
17-22 |
Поглинальна активність |
ФІ |
89 |
60-80% |
Абс. число |
361 |
72-543 |
ФЧ |
3,7 |
1,5-3,5 |
||
В-лімф. CD-22 |
% |
23 |
10-20 |
НСТ-тест |
Сп |
11 |
До 10% |
Абс. число |
319 |
109-532 |
Інд |
22 |
- |
||
РБТЛ |
Сп. |
15 |
До 10% |
Рез |
11 |
>16% |
|
Інд. |
60 |
50-70% |
Комплемент |
СН-50 |
70 |
30-60 гем. од/мл |
|
Виходячи з особливостей імунологічного статусу у хворої О., для лікування синдрому хронічної втоми призначили наступну схему імунотропної терапії:
1) специфічна противірусна терапія (замісна - протигерпетичний імуноглобулін типу 1 по 1,5 мл в/м, всього 5 ін'єкцій 2 рази на тиждень; протицитомегаловірусний імуноглобулін (цитотект) по 1,5 мл в/м, всього 5 ін'єкцій 2 рази на тиждень;
2) етіотропна противірусна терапія - ацикловір 2 табл. 3 рази на добу протягом 7 діб;
3) неспецифічна противірусна терапія:
- лаферон по 1 млн МОд через добу в/м протягом 10 діб;
- індуктор інтерферону - циклоферон - 12,5% розчин для ін'єкцій - 2 мл, разова доза 0,25 г в/м на 1, 2, 4, 6, 8, 11, 14, 17, 20, 23, 26, 29-ту добу. Призначають після інтерферонотерапії;
4) галавіт 0,2 г на 5 мл фізрозчину в/м через добу, 3 ін'єкції.
Імунореабілітація
5) галавіт 0,1 г ректальні свічки через добу, 20 днів;
6) нуклеїнат натрію 0,1 г 2 рази на день, 40 діб;
7) луцетам 1,2 г 2 рази на день (вранці та в обід) протягом місяця.
Профілактика й імунореабілітація при вторинних імунодефіцитах
Профілактика вторинних імунодефіцитів може бути як запобіжною, так і протирецидивною. Перша полягає у своєчасній і повноцінній терапії захворювань, які можуть бути причиною цих дефектів; ранній діагностиці дисбалансу в системі імунітету; своєчасній корекції цього дисбалансу.
Протирецидивна імунопрофілактика базується на диспансеризації хворих і імунореабілітації тих, у кого виявлений вторинний імунодефіцит. Такі хворі повинні регулярно обстежуватися, і при виявленні у них в динаміці негативних зрушень в системі імунітету необхідна імунокорекція. Так, наприклад, дітям, які перенесли гнійно-септичні захворювання, необхідна імунореабілітація, оскільки, не зважаючи на клінічне одужання, показники клітинного і гуморального імунітету у них повністю не відновлюється: IgG ще знижений; IgM і IgA - на субнормальному рівні, а у деяких дітей вище за норму, що відображає готовність організму до реінфекції. При збереженні у період ремісії понижених показників імунологічної реактивності проводять комплекс активних реабілітаційних заходів.
Неспецифічна імунореабілітація й імунопрофілактика є важливим етапом у лікуванні хворих з вторинними імунодефіцитами в період ремісії. Застосування "м’яких" імуностимуляторів у випадках достатньо збереженої реактивності імунітету попереджає рецидиви захворювання, тобто забезпечує імунореабілітацію. З цією метою в період ремісії призначають перорально адаптогени, імуностимулятори рослинного походження (ехінацея, женьшень елеутерокок, аралія, заманиха, лимонник, золотий корінь та ін.), а також вітаміни і мікроелементи. Використовують курси фізіоімунотерапії (КВЧ, магнітотерапію та ін.), гартуючі заходи, раціональне харчування відповідно клінічним проявам імунодефіциту, раціональне використання природних чинників своєї місцевості і курортотерапії.
На диспансерному обліку діти з вторинними імунодефіцитами знаходяться до повної імунологічної реабілітації і припинення клінічних проявів, що маскують її. Здійснює диспансеризацію дільничний лікар, консультує і проводить корекцію лікування фахівець-імунолог. Кратність спостережень залежить від клінічної симптоматики згідно інструктивно-методичних рекомендацій з диспансеризації дитячого населення; імунологічний контроль проводиться по ходу лікування, потім рекомендується обстежувати дитину 2 рази з інтервалом у 6 місяців, після чого дитина може бути знята з обліку з оформленням етапного епікризу.
Імунопрофілактика професійних вторинних імунодефіцитів. Апробовано дві схеми: 1-ша схема включає нуклеїнат натрію, полівітаміни (вітрум, мультитабс, юнікап) і адаптогени (екстракт елеутерокока, настойка женшеню); 2-га - антиоксиданти (а-токоферол, убихінон), препарати з позитивними метаболичними властивостями (рібоксин, предуктал МР), полівітаміни адаптогени, які призначають протягом 20-45 діб.
Імунореабілітація хворих з рецидивуючими вірусними інфекціями респіраторного тракту
У гострому періоді призначають лікування, відповідне етіології і патогенезу вірусної інфекції із застосуванням антивірусних і антибактеріальних препаратів на фоні дезінтоксикації та вітамінотерапії. У ремісії (краще відразу ж після імунокоригуючої терапії) доцільно призначити:
1. Екстракт або настій елеутерококу або женьшеню у терапевтичній дозі протягом 1-2 місяців (імунологічний адаптоген).
2. Кисневий коктейль з настоєм з плодів брусниці і шипшини, 2-3 курси на рік по 10 сеансів.
3. Дібазол (всередину) у терапевтичній дозі на 10-12 діб.
4. Антиоксидантні комплекси (вітаміни С, А, Е, мікроелементи - цинк, селен, мідь).
При контакті з ОРВІ профілактично і з метою імуномодуляції призначається
інтерферон у ніс і гепарин підшкірно у терапевтичній дозі (100 Од/кг) на 5-6 діб з контролем показників первинного гемостазу через тиждень.
Якщо клінічна маска вторинного імунодефіциту характеризується ще і субфебрилітетом, то у комплекс фонової терапії доцільно після дибазолу ввести циннарізин, нікотинову і глютамінову кислоти. Після цього на 4-6 місяців призначається комплекс вітамінних трав і рослин з підвищеним вмістом біоелементів у вигляді настоїв. Хороший клінічний ефект може бути отриманий при призначенні гліцину, особливо дітям з підвищеною нервово-м’язовою збудливістю, по 0,5-1 табл. 2 р. на добу протягом 10-12 діб.
Імунореабілітація хворих імунодефіцитом з клінікою хронічного бронхіту, резистентного до традиційної терапії
Після завершення основного курсу імунокоригуючої терапії, яку слід почати у гострий період, рекомендуємо провести наступну диспансерну імунореабілітацію:
1. Лізоцим (лісобакт) по 1 табл. 3 рази на день по одному тижню кожного місяця, 3-4 курси (дозування терапевтичне, розводити краще молоком, при непереносимості яєць не призначати).
2. Екстракт елеутерококу (або лимонніка) - 30 діб.
3. Кисневі коктейлі з вітамінізованими сиропами кожні 10 діб 2 місяці.
4. Гліцирам по 25 мг по 1-2 табл. 2-3 рази на день за 30 хв перед їдою, протягом 10 днів кожного третього місяця 1 рік, або ультразвуковий вплив на надниркову ділянку (3 сеанси).
5. Фітотерапія з настоїв трав: м’яти, звіробою, кропиви (3-4 рази на добу протягом місяця по черзі по 10 діб кожної трави), за рік такі курси повторити 2-3 рази.
6. Закінчується фонова реабілітація короткою схемою (двократно) імунізації стафілококовим анатоксином або курсом бронхомунала протягом 10-30 діб.
За наявності абсцедувань, що ускладнюють пневмонії, доцільно паралельно з лізоцимом включити у схему терапії аплікації з 25-30% розчином димексиду (можна вводити методом електрофорезу) на проекцію ділянки ураження до 8-10 сеансів.
Схема імунореабілітації при рецидивуючих бактеріальних бронхітах:
1. Фітонцидні антибактеріальні препарати по черзі: настійка часнику, хлорофіліпт, настійка календули по 10 діб всередину у віковій дозі (1 крапля на рік життя, але не більше 20 крапель).
2. Лізоцим по 1 табл. 3 рази на день по одному тижню кожного місяця, 3-4 курси.
3. Гліцирам по 25 мг по 1-2 табл. 2-3 рази на день за 30 хв перед їдою, протягом 10 днів кожного третього місяця 1 рік для припинення процесів інфекційної алергізації.
4. УВЧ на ділянку сонячного сплетення по 5 сеансів на курс 2 рази на рік.
5. Пробіотики (біфідум-бактерин, лактобактерин, лактив-ратіофарм та ін.) при тенденції розвитку бактерійного дисбактеріозу і після лікування антибіотиками під контролем складу біфідофлори кишечника. Можна використовувати лінекс, хілак-форте.
Курси фітонцидних антибактеріальних препаратів можна повторювати 2-3 рази на рік.
Обов’язкова умова проведення імунореабілітації - імунологічний контроль за її ефектом. Виконуючи її, слід пам’ятати про терміни настання цього ефекту у кожного використовуваного препарату і не поспішати відміняти препарат, замінюючи його іншим, навіть якщо вони відносяться до однієї і тієї ж групи за імунологічною дією. Відновлення імунологічної компетентності організму - це тривалий процес, що вимагає вдумливого і обов’язково науково обґрунтованого підходу до питань терапії з урахуванням особливостей клінічних проявів у даний час і причинно-значущої патології.
Імунокорекція при аденоідиті, хронічному тонзиліті та риніті
Комплексні схеми лікування гіперплазії мигдаликів і аденоїдів:
- пропасол 10 діб;
- календула 10 діб + естифан 3 тижні;
- хлорофіліпт 2 тижні всередину;
- IRS-19 - спрей, 2 рази на день зрошувати мигдалики, курс 2 тижні.
Мигдалики стискаються і зменшуються.
Комплексна схема лікування хронічного тонзиліту (загострення). Критерії - спайки з дужками і ознаки хронічної інтоксикації:
- амоксіцилін або амоксіклав - 7 діб у вікових дозах;
- лейкінферон 5 ін’єкцій або віферон 5-7 свічок по 500 000 Од через добу;
- пропасол 10 діб + плазмол №5;
- лікопід 10 діб по 1 мг для дітей і 10 мг - дорослим;
- естифан + люголь;
- УФО мигдаликів №5;
- димексид 30% - аплікації на підщелепні та шийні лімфатичні вузли;
- рібомуніл 6 тижнів по 1 табл. 2 рази 4 доби на тиждень.
Комплексна схема лікування хронічного риніту, асоційованого з ГРЗ:
- рібомуніл 1 табл. 2 рази 4 доби на тиждень 6 тижнів або IRS-19 - 10 днів (спрей у ніс);
- аплікації з 30% димексидом на спинку носа і проекції гайморових пазух №10 через добу;
- алое - електрофорез носа;
- судинозвужувальні - краще санорин, менше підсушується слизова оболонка.
Комплекс імунореабілітації для групи дітей, що часто і тривало хворіють
Комплексна імуномодулююча терапія переважно направлена на стимуляцію як Т-, так і В-клітинного імунітету, а також безпосередньо фагоцитарної ланки. Про вид імунного дисбалансу можна заздалегідь судити за клінікою епізодів повторної захворюваності - за етіологією: вірус, бактерія, грибки або їх асоціації; за патогенетичною реакцією крові: лейкоцитоз, лейкопенія, лімфоцитоз/лімфо- пенія; нейтрофільоз/нейтропенія, за клінікою - типові симптоми вірусної або грибкової, або бактерійної інфекції та інфікованості тощо.
Без побоювання ефекту гіперстимуляції і посилення дисбалансу між окремими ланками в системі імунітету можна призначити:
- тималін 10 мг, курс 5 ін’єкцій;
- рібомуніл або лікопід за загальноприйнятою схемою;
- мікроелементно-вітамінний комплекс і біопрепарати з профілактики і лікування дисбактеріозу на фоні підвищеної уваги до дитини з боку батьків - адекватного віку харчування, гартуючих фізичних заходів. За відсутності бажаного результату дитина повинна бути обстежена у спеціалізованому центрі або відділенні для складання індивідуальної програми імунореабілітації, а іноді навіть для підбору препаратів in vitro.
У тих випадках, коли немає реальної можливості провести імунологічне обстеження хворого для ідентифікації імунного дефекту і підбору коригуючої терапії (наприклад, в умовах сільського регіону), можна рекомендувати до практичного використання терапевтичні комплекси реабілітації, засновані на клінічних даних про хворого.
Такі схеми лікування можуть включати:
а) препарати з групи біогенних стимуляторів, які сприяють поліпшенню презентації різних антигенів (бактеріальних, вірусних, грибкових і змішаних) через системи фагоцитозу;
б) засоби, стимулюючі процеси анаболізму;
в) препарати, що активують окислювально-відновлювальні реакції у тканинах (у тому числі і в імунокомпетентних органах);
г) мікроелементи і їх сполуки;
д) медикаментозні засоби, що поліпшують обмін речовин у нервовій системі з непрямим впливом на систему імунітету (препарати амінокислот для стимуляції білкового обміну і енергетичних процесів у тканинах мозку, підвищення їх дихальної активності, ноотропні засоби для формування асоціативних зв’язків між клітинами головного мозку; препарати, що компенсують гіпоксію в ЦНС і поліпшують обмін ліпідів, наприклад, пангамат кальцію.
Клінічними показаннями у таких випадках можуть бути:
1. Рецидивування запальних захворювань з ризиком розвитку хронічних форм і формуванням хронічного осередку інфекції.
2. Схильність до генералізованого гнійно-септичного захворювання (за клінічними даними).
3. Наявність побічних незвичайних або псевдоалергічних реакцій на традиційні препарати.
4. Тривала астено-вегетативна дисфункція нервової системи, зміни у периферичній крові типу нейтропенії, лейкопенії, тромбоцитопенії, лімфоцитопенії тощо.
Для профілактики розвитку хронічного захворювання рекомендується наступне профілактичне лікування з елементами імунореабілітації:
1. На фоні затихання гострої фази запалення призначаються ін’єкції екстракту алое підшкірно, дітям дошкільного віку по 0,3-0,5 мл, дорослим по 1 мл курсом 15-20 введень через добу.
2. Внутрішньовенне введення тіосульфату натрію (можна і всередину, але клінічний ефект при цьому дещо слабший) з метою м’якої десенсибілізації, дезинтоксикації і протизапальної дії. Клінічні ефекти опосередковують нівеляцією сірчистими сполуками надлишку медіаторів підвищеної чутливості негайного і сповільненого типів, які в сукупності обумовлюють морфологічний еквівалент хронічного процесу. При призначенні всередину використовується 10% розчин тіосульфату натрію залежно від віку по 1 чайній, десертній або столовій ложці 3 рази на день; при внутрішньовенному способі застосовується 30% розчин по 1-1,5 мл до 5 років; по 2-3 мл дітям старше 5 років, дорослим по 5 мл 1 раз на добу, курс лікування складає зазвичай 10-14 діб.
3. Гліцерофосфат кальцію (стимуляція анаболізму в тканинах імунокомпетентних органів) всередину на 5-7 діб.
При тенденції інфекційного процесу до генералізації (основні клінічні ознаки: загальна біологічна ареактивність, астенізація, тривале порушення у системі мікроциркуляції, лейкоцитоз з нейтрофільозом за відсутності локалізованого гнійного вогнища або, навпаки, лейкопенія при маніфестному гнійно-запальному процесі, невідповідність температурної реакції клінічним проявам, особливо на фоні перинатального ураження головного мозку) рекомендується:
1. При лейкопенічній реакції крові слід починати профілактику вторинного імунодефіциту з плазмолу підшкірно дітям дошкільного віку по 0,2-0,3 мл, дорослим по 1 мл розчину 1 раз на добу протягом 10-14 діб. При лейкоцитозі слід почати з дибазолу в ін’єкціях курсом до 2 тижнів у віковому терапевтичному дозуванні.
2. Паралельно призначається курс вітаміну Р (у формі аскорутину) всередину, але краще у формі урутину - в ін’єкціях по 0,2-0,3 мл дітям раннього віку, по 0,3-0,4 мл - дошкільникам, дорослим по 1 мл підшкірно 1 раз на добу протягом 20-30 діб. Вітамін Р стимулює функціональну активність імунокомпетентних клітин, що пояснюється, ймовірно, його активуючою дією на окислювально-відновлювальні процеси у тканинах.
3. Для поповнення бактерицидних чинників наступним призначенням може бути лісобакт (лізоцим, попередня біологічна проба на переносимість обов’язкова). Лізоцим призначається в ін’єкціях або всередину курсом 7-10 діб один раз на добу. Також призначається ехінацея.
4. Закінчити профілактичну схему рекомендується призначенням УВЧ- терапії на ділянку сонячного сплетіння, курсом з 5 сеансів, можна чергувати з ультразвуковою дією на зону проекції надниркових залоз.
За наявності незвичайних реакцій на лікарські препарати, які стимулюють явища непереносимості, рекомендується застосувати комплекс засобів, які стабілізують клітинні мембрани, що сприяє адаптації рецепторного апарату клітин імунної системи:
1. Вітамін Е парентерально у вигляді внутрішньом’язових ін’єкцій курсом до 7-10 діб.
2. Ентерально призначається окис цинку для стимуляції хемотаксису поліморфноядерних лейкоцитів і моноцитів, а також для стабілізації мембран цих клітин. Окис цинку призначається у дозі добової потреби від 4-6 мг у дітей грудного віку до 10-20 мг у старших дітей і дорослих у 2 прийоми.
3. Паралельно - ультразвукова дія на зону проекції надниркових залоз щодня курсом №5.
Завдання для заключного контролю знань
11. Інфекції при вторинних імунодефіцитах В-клітинного типу:
A. Вірусні.
B. Грибкові.
C. Бактеріальні.
D. Паразитарні.
12. Час появи перших клінічних ознак вторинних імунодефіцитів:
A. З першого місяця життя.
B. З 4-6 міс. життя.
C. У підлітковому періоді.
D. У будь-якому віці.
13. Клінічними маркерами вторинного Т-клітинного імунодефіциту є:
A. Рецидивуючі піогенні інфекції.
B. Рецидивуючі вірусні інфекції.
C. Гіпоплазія тимусу.
D. Патологія паращитоподібних залоз.
14. Інфекції, що часто зустрічаються при дефектах фагоцитозу у хворих вторинним імунодефіцитом:
A. Бактерійні.
B. Вірусні.
C. Паразитарні.
D. Грибкові.
15. Причини вторинних імунодефіцитів:
A. Хромосомні порушення.
B. Імуносупресивна терапія.
C. Онкологічні захворювання.
D. Хронічні інфекції.
16. Вторинний імунодефіцит може бути наслідком:
A. Порушення харчування.
B. Променевої терапії.
C. Множинних трансфузій.
D. Опікової хвороби.
17. Вторинний імунодефіцит характеризується підвищеною чутливістю хворого до вірусних і грибкових інфекцій. Основний дефект імунної системи визначається порушенням функції:
A. Макрофагів.
B. Т-лімфоцитів.
C. В-лімфоцитів.
D. Системи комплементу.
E. Нейтрофілів.
18. Вторинний імунодефіцит розвинувся на фоні опікової хвороби. Основний дефект імунної системи характеризується порушенням:
A. Т-лімфоцитів.
B. В-лімфоцитів.
C. Системи комплементу.
D. Фагоцитозу.
19. Показання для в/в введення імуноглобулінів:
A. Уроджені імунодефіцити.
B. Вторинні імунодефіцити.
C. Бактерійна інфекція.
D. Вірусна інфекція.
E. Алергія.
F. Ендотоксичний шок.
20. Які імуномодулятори найбільш ефективні при вторинних імунодефіцитах, викликаних персистенцією вірусів?
A. Тималін.
B. Поліоксидоній.
C. Мієлопід.
D. Галавіт.
E. Нуклєїнат натрію.
Вірні відповіді на питання: 11 - CD; 12 - D; 13 - B; 14 - AD; 15 - BCD; 16 - ABCD; 17 - B; 18 - CD; 19 - ABCD; 20 - ABD.