МІКРОБІОЛОГІЯ - М.Г. Сергійчук - 2008
Розділ 8. МІКРООРГАНІЗМИ І ДОВКІЛЛЯ
Взаємовідносини мікроорганізмів у природі
У процесі еволюції кожна група організмів мала пристосуватися не лише до умов неживої природи (довкілля), але й до інших живих організмів. Адаптація при тривалому тісному співіснуванні різних організмів привела до набуття ними нових метаболічних особливостей, які дозволяють організмам або отримувати користь від свого співіснування, або витримувати конкуренцію одного з одним. Явище співіснування організмів називають симбіозом (грец. symbiosis - сумісне життя).
Симбіотичні асоціації, які утворюють мікроорганізми з рослинами і тваринами, а також іншими мікроорганізмами, розділили за ступенем їхньої взаємної близькості на ектосимбіоз та ендосимбіоз. При екто- симбіозі мікроорганізми зберігають зовнішнє положення щодо свого хазяїна, тоді як при ендосимбіозі мікроорганізм розвивається всередині клітини хазяїна.
Залежно від впливу, який здійснюють симбіонти один на одного, він може розглядатись як позитивний та негативний. Серед позитивних взаємовідносин виділяють:
- мутуалізм (лат. mutuus - взаємний) - форма симбіозу, при якому обидва партнери отримують користь від свого існування. Часто цей зв'язок є нерозривним;
- синтрофія (грец. syn - разом, trophe - харчування) - ріст одного або декількох видів мікроорганізмів на середовищі, яке для кожного з них окремо є недоступним;
- коменсалізм (лат. com - разом, mensa - стіл, трапеза) - форма симбіозу, при якій один із партнерів покладає на іншого регуляцію своїх відносин з довкіллям. Існування коменсала для хазяїна залишається непомітним, тобто спостерігається однобічна синтрофія;
- синергізм - форма співіснування, коли в асоціантів відбувається підсилення фізіологічних функцій.
При негативних взаємовідносинах говорять про конкуренцію (лат. concurrere - стикатися) або антагонізм (грец. antagonisma - суперечка, боротьба). Конкуренція може бути пасивною (різні організми використовують однакові поживні речовини; перевага за швидкорослими формами) та активною (зумовлена виділенням бактерицидних речовин). Жорстким прикладом конкурентних взаємовідносин може бути також паразитизм (грец. parasitos - нахлібник, дармоїд), коли один із симбіонтів використовує іншого як середовище існування, та хижацтво - один використовує іншого як поживу.
Природні взаємовідносини між різними організмами настільки складні і багатогранні, що досить часто їх неможливо віднести до якогось конкретного типу.
Взаємовідносини мікроорганізмів. На відміну від лабораторних умов, де для мікроорганізмів штучно створюють умови чистої культури, у природі бактерії змушені витримувати боротьбу за існування. Неконкурентоспроможні мікроорганізми неминуче зникнуть із спільноти.
При пасивному антагонізмі спостерігають витіснення одного мікроорганізму іншим, якщо збільшення чисельності обох видів лімітовано одним і тим самим життєво важливим ресурсом, кількість та (або) доступність якого обмежені. Так, при вирощуванні на штучному поживному середовищі туберкульозних бактерій та сапрофітної мікрофлори переважно розвиваються сапрофіти через їхню більшу швидкість росту. Експериментально було доведено, що при зміні умов досліду можна змінити кінцевий результат конкурентних взаємовідносин, що в багатьох випадках може бути реальним відображенням сезонних змін. Наприклад, при сумісному культивуванні Spirillum sp. та Pseudomonassp. за температури 16о С і вище перевага була за Spirillum sp., тоді як за зниження температури до 2о С на тому самому субстраті швидше розвиваються Pseudomonas sp.
Активний антагонізм зумовлений виділенням бактерицидних речовин. Такими речовинами можуть бути неспецифічні продукти обміну (органічні кислоти, спирти, аміак, феноли, пероксид водню та ін.) або специфічні (антибіотики).
Такі продукти обміну, як кислоти та спирти, токсичні для будь-якої клітини. Так, при розвитку бактеріальних популяцій у молоці спочатку спостерігається незалежний розвиток різних видів мікроорганізмів. Але за наявності бактерій, які здійснюють молочнокисле бродіння, молоко поступово підкислюється і перевага залишається за кислотостійкими молочнокислими коками та паличками. З часом молочнокислі палички, які є більш кислотостійкими, витісняють і коки.
Оцтовокислі бактерії можна підтримувати в чистій культурі, не здійснюючи особливих заходів проти їхньої контамінації. Висока концентрація оцтової кислоти в середовищі запобігає розвитку інших мікроорганізмів.
Уролітичні бактерії у процесі гідролізу сечовини сприяють накопиченню аміаку, за рахунок якого середовище стає сильно лужним. Висока лужність та висока концентрація аміаку в середовищі запобігають розвитку інших мікроорганізмів.
Дія специфічних продуктів обміну (антибіотиків) спрямована на пригнічення чутливих до них мікроорганізмів. Проте остаточної думки з приводу значення для мікроорганізму антибіотиків не існує. У природних умовах антибіотики, як правило, не можуть бути накопичені в достатній кількості, щоб здійснити нейтралізуючий вплив на інші мікроорганізми. Так, Streptomyces olivocinereus - продуцент геліоміцину - пригнічує в нестерильному ґрунті популяцію Arthrobacter crystallopoietes, але ефект пригнічення спостерігається при щільності продуцента не менш як 106 колонієутворювальних одиниць в 1 г ґрунту. В іншому випадку одночасно проводили культивування кишкової палички та стрептоміцету, який продукує антибіотик, що пригнічує ріст Escherichia coli. При їх сумісному вирощуванні з'являються стійкі до дії цього антибіотика мутанти кишкової палички. З часом швидкорослі кишкові палички повністю витісняють клітини стрепто- міцету, які характеризуються більш повільним ростом.
Існує припущення, що деякі антибіотики можуть здійснювати регуляцію певних процесів у їхніх продуцентів. Синтез поліпептидних антибіотиків ендоспороутворювальними бактеріями, наприклад, збігається з інтенсивним спороутворенням. Розглядаються антибіотики і як випадкові продукти метаболізму, які не мають значення для організмів, що їх продукують. Хоча питання про біологічне значення антибіотиків остаточно не вирішене, проте в деяких випадках виявлено, що їх накопичення сприяє виживанню мікроорганізму у природному середовищі.
Найбільш яскраво конкуренція проявляється у формі паразитизму та хижацтва. Між цими типами взаємовідносин важко провести чітку межу, оскільки і паразити, і хижаки задовольняють свої харчові потреби за рахунок жертви. Різниця між ними полягає в тому, що хижаки вбивають свою жертву досить швидко, тоді як паразити живляться за рахунок живого організму.
Паразитизм мікроорганізмів на мікроорганізмах спостерігається досить рідко. Так, Vampirovibrio chlorellavorus є облігатним паразитом одноклітинної водорості Chlorella. Цей вібріон не здатний розвиватись на органічних середовищах і навіть на мертвих клітинах хлорели. Бактерії прикріплюються до оболонки водорості. До однієї клітини може прикріпитись декілька десятків вібріонів. Прикріплені вібріони збільшують проникність оболонки водорості і ростуть за рахунок речовин, що надходять у її клітину. З часом клітина водорості припиняє ріст і гине. Проте за допомогою антибіотиків, наприклад пеніциліну, можна вбити бактерії-паразити, не зашкодивши водорості. Вилікува- ні клітини хлорели здатні далі нормально розвиватись.
Інший вібріон (Bdellovibrio) може розглядатись як справжній хижак. Клітини бделовібріона можуть прикріплюватися до клітин інших бактерій і проникати в них. Після проникнення хижак росте, використовуючи вміст клітини-жертви як поживний субстрат, і ділиться. З часом клітина-жертва лізується, а хижак знаходить нову жертву. Коло можливих жертв досить широке, але найчастіше це представники кишкових бактерій.
Позитивні взаємовідносини між різними видами мікроорганізмів можна характеризувати як синтрофію. Синтрофія - це здатність двох або декількох видів бактерій здійснювати сумісно такий процес, який жоден з них не здатен здійснити самостійно. Основою таких взаємовідносин може бути передача факторів росту, утворення одним організмом субстрату, придатного для розвитку іншого, видалення одним організмом продуктів, токсичних для іншого. Декілька механізмів можуть діяти одночасно.
Синтрофія, основою якої є обмін субстратом, спостерігається, наприклад, при руйнуванні мікроорганізмами целюлози в середовищі, яке не містить зв'язаного азоту. Целюлозоруйнівні бактерії не здатні до фіксації молекулярного азоту. Вони отримують продукти фіксації азоту від азотофіксувальних бактерій. У той же час азотофіксувальні бактерії не можуть використовувати клітковину як джерело енергії та вуглецю. Вони використовують продукти їхнього гідролізу від целюлозоруйнівних бактерій. Для цієї спільноти, що розвивається в аеробних умовах, важливим є також поглинання кисню целюлозоруйнівними аеробами, оскільки знижений вміст кисню в середовищі є сприятливим для азотофіксації.
Синтрофію, основою якої є видалення з середовища токсичних продуктів, можна спостерігати в асоціаціях, де відбувається окиснення метану. Метилобактерії мають малоспецифічну монооксигеназу, яка крім метану частково окиснює інші вищі вуглеводні, у результаті чого утворюються високотоксичні для метилобактерій продукти. Якщо метилобактерії розвиваються в асоціаціях з мікроорганізмами, які здатні окиснювати ці токсичні сполуки, то метаноокиснювальні асоціації стабільні, тоді як чисті культури можуть бути швидко втрачені.
У деяких випадках симбіотичні взаємовідносини приводять до формування консорціуму (лат. consortium - співучасть, співтовариство), в якому клітини двох видів об'єднані нібито в один організм. Такий консорціум утворюють бактерії роду Desulfotomaculum та клітини Chlorobium phaeobacteroidus. У центрі асоціації містяться сульфатредуктори Desulfotomaculum, а на поверхні - фотосинтезуючі сіркобактерії. Перебуваючи у світлій зоні водойм в анаеробних умовах, фотосинтезуючі бактерії забезпечують сульфатредукуючі бактерії органічними речовинами та окисненою сіркою, а Desulfotomaculum виділяє сірководень і забезпечує фотосинтезуючі бактерії відновником. У результаті таких взаємовідносин консорціум може розвиватись у таких водоймах, де в анаеробній зоні присутні лише сліди сірководню. Консорціум проявляє фото- і хемотаксис. Ділення організмів, які входять у консорціум, відбувається синхронно, що свідчить про високий ступінь їхньої інтеграції.
Якщо наявність симбіонта необхідна лише одному з партнерів, то говорять про коменсалізм. Наприклад, навколо колонії мікроорганізмів, що активно синтезують ціанкобаламін, можуть розвиватись мікроорганізми, які не здатні синтезувати його самостійно, але потребують для свого розвитку. Існування симбіонта для мікроорганізму - продуцента вітамінів залишається непомітним. Або інший приклад: руйнування пеніциліну пеніциліназою аеробних спороутворювальних бактерій дає можливість розвиватись чутливим до пеніциліну мікроорганізмам.
Механізми "взаємодопомоги" у бактерій можуть бути пов'язані не лише з живленням. Так, патогенні для людини нерухомі Veillonella parvula та Actinomyces viscosus у ротовій порожнині прикріплюються до поверхні представників нормальної мікрофлори рота, здатних до ковзного типу руху, і таким чином направляються до ділянок сприятливих для їхнього розвитку.
Явище синергізму (в асоціантів відбувається підсилення фізіологічних функцій) знайшло застосування в біотехнології при проведенні мікробіологічного синтезу біологічно активних сполук. Сумісне культивування двох культур актиноміцетів - Streptomyces nmosus (продуцент протеаз) і S. violocinereus (не синтезує ферменти) - супроводжується збільшенням виходу ферменту в шість разів. Виявилося, що S. violocinereus продукує стимулятор, який впливає на розвиток продуцента ферменту.
Прикладами синтрофічних взаємовідносин можуть бути також полімікробні інфекції, зокрема газова гангрена, зумовлена дією декількох видів роду Clostridium в асоціації зі стафілококами та стрептококами.
Таким чином, між мікроорганізмами у природних асоціаціях встановлюються певні динамічні взаємовідносини, які часто не мають чітких меж. Причини, які сприяють прояву тих або інших форм взаємовідносин, зумовлені конкретними умовами існування, а також особливостями обміну речовин самих мікроорганізмів.
Взаємовідносини мікроорганізмів з рослинами. Мікроорганізми утворюють цілий ряд симбіотичних угруповань з вищими росли-
нами. Як ектосимбіонти або епіфіти (грец. ері - на, phyton - рослина) вони заселяють поверхню листків - філосферу (грец. phyllon - лист, sphaire - куля, шар), та ґрунт, що безпосередньо оточує корені рослини - ризосферу (грец. rhiza - корінь). Як ендосимбіонти мікроорганізми проникають у корінь і утворюють мікоризи (якщо проникає гриб) або бульбочки (при проникненні бактерій).
Мікроорганізми, що утворюють філосферу рослин, не лише перебувають на їхній поверхні, а й активно там розвиваються. Розвиток філосфери забезпечується поживними речовинами, вимитими з листків водою. Роса і змиви з листків містять амінокислоти, вуглеводи, вуглеводні, органічні кислоти, фітогормони, неорганічні сполуки. Поживні речовини можуть також міститися в пилюці, що осідає на поверхні листків.
Систематичний склад філосфери досить різноманітний. На різних рослинах можуть переважати певні види, але строгу специфічність філосфери не доведено. До 80 % від загальної кількості епіфітів становлять клітини Erwinia herbicola. Зустрічаються також деякі молочнокислі бактерії, наприклад Lactobacillus plantarum. Завжди виявляються бактерії, здатні до фіксації молекулярного азоту, їм належить певна роль у накопиченні азоту. У філосфері фіксується ~15 % від загальної кількості молекулярного азоту. Бацил та актиноміцетів мало, частіше виявляються спори та проростки грибів (Penicillium, Fusarium, Mucor та ін.). Особливістю більшості бактерій філосфери є здатність до утворення меланінових і/або каротинових пігментів, які захищають клітини від згубної дії сонячної радіації. Синтез позаклітинних полісахаридів захищає мікробні клітини як від радіації, так і від висихання. Крім того, слиз підсилює адгезію клітин, так що навіть під сильним дощем бактерії не змиваються з листків.
Крім того, що епіфітні мікроорганізми отримують від рослин поживні речовини, вони продукують речовини, які рослини здатні використовувати як стимулятори росту. Проте у складі філосфери можуть зберігатись і фітопатогенні мікроорганізми, які за певних умов здатні викликати захворювання рослини.
Завжди щільно заселена бактеріями коренева система рослин. Мікроорганізми містяться безпосередньо на поверхні коренів, а також у ґрунті, що оточує корені рослин. Кількість бактерій ризосфери у 10100 разів перевищує їх кількість у зоні, віддаленій від коренів.
Підсилене розмноження бактерій у ризосфері зумовлене надходженням у прикореневу зону кореневих виділень та кореневого опаду (відмерлих коренів), які містять різні органічні речовини.
Популяція численних видів мікроорганізмів ризосфери не є облігат- ною мікрофлорою коренів, але вона здійснює суттєвий вплив на найважливіші процеси життєдіяльності рослин: дихання, фотосинтез, запліднення, фосфатний, азотний обміни та ін. Так, бактерії ризосфери продукують тіамін та інші вітаміни, руйнують складні органічні сполуки і роблять їх придатними для використання рослинами, синтезують стимулятори росту - гіберелін та гетероауксин. Розвиток у складі ризосферної мікрофлори різноманітних бактерій створює умови для конкуренції між ними за поживні субстрати, що запобігає розвитку випадкових форм, у тому числі і фітопатогенних. У ризосфері переважають гетеротрофні грацилікутні палички. Склад ризосферної мікрофлори біля різних рослин відрізняється, але суворої приуроченості певних бактерій до конкретних рослин не спостерігають. Наприклад, у складі мікробних спільнот ризосфери різних сільськогосподарських культур на фоні загальних представників виявляють характерні види: у люцерни - Rhizobium meliloti, Pseudomonas ocawthe, P. liquida та P. carnea; у кукурудзи - P sinuosa, P. caudatus, Aerobacterium Uquefaciens.
Найбільш інтенсивне розмноження бактерій у ризосфері спостерігається в період інтенсивного росту та перед цвітінням. Після завершення розвитку однорічних рослин або відмирання багаторічних корені починають використовуватись як джерело живлення. У цей період склад ризосфери змінюється: розвиваються бактерії, що використовують пектин, клітковину, збільшується кількість грампозитивних форм.
Корені більшості вищих рослин перебувають у тісному симбіотичному зв'язку з грибами. При такій формі симбіозу, як і при багатьох інших, створюються динамічні умови взаємної експлуатації, з якої обидва партнери отримують користь. У результаті цього зв'язку структура кореня рослини змінюється специфічним чином. Така складна структура, що складається з коренів вищої рослини і гіф гриба, називається мікоризою.
Наявність чи відсутність мікориз, а також особливості їхньої будови визначаються насамперед систематичним положенням рослини- хазяїна. У вищих спорових рослин не мають мікориз спорофіти плавунів і хвощів. Голонасінні - всі мікотрофи. Серед покритонасінних в осокових, ситникових, хрестоцвітих, макових, гвоздичних, гречаних та маревих мікориза зустрічається рідше, ніж серед рослин інших родин. Бобові рослини, які перебувають у симбіозі з бульбочковими бактеріями, мають і мікоризу. Відомо, що майже 90 % судинних вищих рослин мають мікоризоване коріння. У мікоризованих рослин корені більш розгалужені і товщі. Виявлено, що при мікоризації корінь змінюється як морфологічно, так і цитологічно (рис. 8.6).
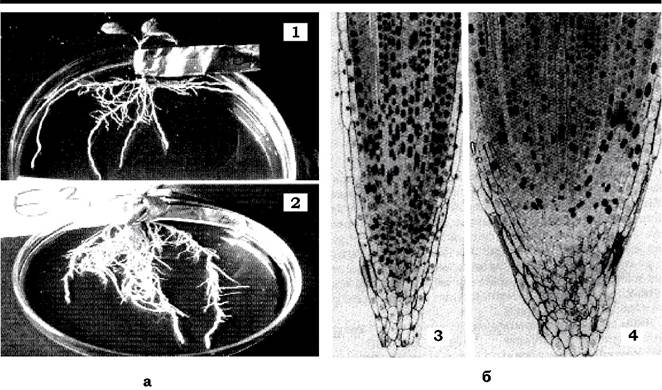
Рис. 8.6. Мікоризація коріння:
а - морфологічні зміни: 1 - Prunus cerasifera мікоризований грибом Glomus sp.;
2 - немікоризоване коріння; б - цитолітичні зміни: 3 - зріз апекса кореня Allumporum немікоризованого;
4 - мікоризований грибом Glomus sp.
На думку В. Вільямса, "мікотрофізм - це спосіб засвоєння вищими зеленими рослинами зольних елементів і азоту із середовища, яке містить ці елементи живлення у формі органічної речовини, що зберігається в умовах анаеробіозу. При цьому живлення здійснюється за рахунок симбіотичного співіснування зелених рослин з міцелієм грибів. Мікотрофний тип живлення рослин поширений у природі чи не більше, ніж автотрофний".
Зовнішній вигляд і будова мікориз може значно варіювати. Розрізняють ектотрофну, ендотрофну і перехідну (ектоендотрофну) мікоризи.
Ектотрофна мікориза (рис. 8.7) притаманна переважній більшості лісових деревних рослин. При цьому корінь щільно обплітається грибним чохлом, від якого відходить густа сітка гіф. Гіфи гриба проникають у корінь на невелику глибину, не торкаючись центрального циліндра (переважно до міжклітинників ектодерми, де, переплітаючись, утворюють так звану сітку Гартінга). Грибний чохол настільки сильно огортає корінь, що кореневі волоски зникають, а вода і поживні речовини поглинаються міцелієм гриба. Лише головні закінчення коренів залишаються імунними щодо гриба. Мікоризи цього типу можуть
утворюватися за участю різних грибів, індивідуальні особливості яких визначають колір чохла та його зовнішній вигляд. Грибний чохол найчастіше буває білуватим, рожевим і навіть чорним. Ектотрофна мікориза - це однорічний утвір, який поновлюється щорічно.
Види, що утворюють ектомікоризу, мають різний ступінь специфічності щодо рослини-хазяїна. Типові мікоризоутворювальні види реалізують мутуалістичний спосіб живлення (здатні доставляти рослині необхідні їй джерела фосфору та азоту й отримувати від неї джерела вуглецю). Неспецифічні ектомікоризні гриби можуть вступати в симбіоз з вищими рослинами, а за відсутності останніх живуть як типові гетеротрофи. За даними палеомікології, ектомікоризні гриби належать до найдавніших. Вік коренів з ектомікоризою становить ~ 50 млн років.
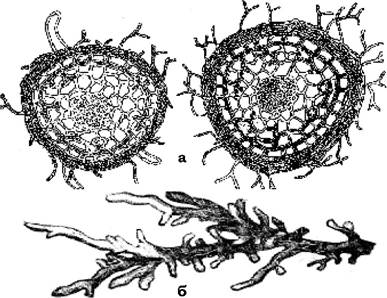
Рис. 8.7. Ектотрофна мікориза:
а - поперечний розріз корінця горобини, огорнутої оболонкою грибного міцелію; б - коренева мочка зрілого дуба, яка є коралоподібною мікоризою
Ендотрофний тип мікоризи (рис. 8.8) виявляється в орхідей, верескових рослин і багаторічних трав, на кореневій системі багатьох дерев і кущів. Вона відрізняється від ектотрофної тим, що грибний міцелій поширюється не лише між клітинами корової паренхіми, але й проникає в них. При цьому клітини корової паренхіми залишаються життєздатними і можуть навіть перетравлювати міцелій, що проник у них. Під впливом вмісту клітини рослини внутрішньоклітинний грибний міцелій може утворювати клубки (пелетони), інколи деревоподібні розгалуження (арбускули) або здуття на кінцівках гіф (спорангіоли і везикули). Центральний циліндр кореня рослини завжди залишається
вільним від інфекції. Частина міцеліальних закінчень виходить у ґрунт, не утворюючи грибного чохла. На відміну від ектотрофної, при ендотрофній мікоризі кореневі волоски рослини завжди зберігаються і можуть виконувати свої фізіологічні функції.
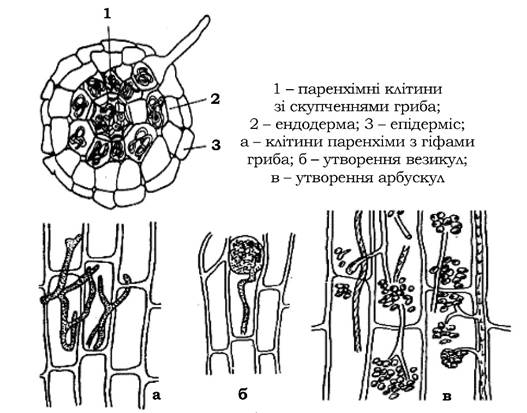
Рис. 8.8. Ендотрофна мікориза пшениці
У створенні ендотрофної мікоризи беруть участь види роду Glomus (відділ Zygomycota). Вони доставляють рослині легко доступні сполуки фосфору, засвоюючи вуглецеві сполуки рослини. Поряд з цим наявність екто- та ендомікоризних видів сприяє збільшенню життєздатності та резистентності рослини завдяки підвищеній адсорбційній здатності грибного міцелію щодо токсинів, важких металів, радіонуклідів. Останні залишаються в міцелії і не потрапляють у рослину. Наявність грибів-симбіонтів захищає рослину від кореневих фітопатогенів, зокрема видів родів FusaHum, Phoma, Rhizoctonia та ін.
Мікориза перехідного типу має властивості обох попередніх.
Інколи виявляється перитрофна мікориза, при якій гриб- мікоризоутворювач не вступає в тісний зв'язок із рослиною. Вони поселяються в ризосфері, огортаючи корінь. У деяких випадках утворюються псевдомікоризи, які формуються паразитичними грибами.
За відносинами з грибами-мікоризоутворювачами вищі рослини поділяють на групи:
- облігатно-мікотрофні рослини, які не можуть розвиватися без гриба (під'ялинник, орхідея);
- рослини, які покращують свій ріст і розвиток за наявності мікоризи. До цієї групи належать деревні (граб, дуб, хвойні тощо), чагарникові породи та трав'янисті рослини;
- рослини, які розвиваються без мікориз. Це, як правило, водні і невеличка група наземних рослин.
Мікоризу в однієї й тієї ж рослини можуть утворювати різні гриби, які здатні до симбіозу з нею. Один і той же гриб може утворювати мікоризу з різними рослинами, але деякі гриби виявляють певну специфічність щодо рослини-хазяїна. Цим можна пояснити досить характерний склад шапинкових грибів у різних деревних порід лісів.
Істинні мікоризи значно покращують розвиток як кореневої системи, так і наземної части рослини.
Ще один вид ендосимбіотичних взаємовідносин виникає між бульбочковими бактеріями та бобовими рослинами (утворення бульбочок). Відомо два шляхи проникнення бульбочкових бактерій у корінь рослини: через кореневі волоски та "розщілини", які утворюються в основі бокових відростків кореня. Рослини, які інфікуються через бокові волоски, мають більшу специфічність до рослини-симбіонта.
У кореневому волоску бактерії утворюють так звану інфекційну гіфу - слизову масу з бактеріальними клітинами, що інтенсивно розмножуються. З кореневого волоска ця гіфа проникає через клітини кори в паренхіму. Інфекційна гіфа в процесі росту вкривається целюлозною оболонкою, яку синтезує рослина.
Бульбочкові бактерії здатні розмножуватись лише в тетраплоїдних клітинах рослини. Коли інфекційна гіфа пронизує тетраплоїдні клітини, частина бактерій переходить з гіфи в цитоплазму рослинних клітин і там починає розмножуватись. Ці клітині, у свою чергу, стимулюють ділення сусідніх клітин. Таким чином формується тканина бульбочки. Бактерії, що перейшли в цитоплазму клітини рослини, ростуть, діляться, але потім перетворюються на бактероїди - не здатні до ділення клітини. У клітинах рослин бактероїди найчастіше містяться у вакуолях. Бактероїди мають більше полі-β-оксимасляної кислоти, глікогену та поліфосфатів, ніж вільноживучі клітини, але менше ДНК. Бактероїди стають чимось подібним до азотофіксуваль- них органел рослини-хазяїна.
Бульбочки, що активно фіксують азот, зазвичай червоного кольору через наявність леггемоглобіну, який виявляють вже на другий день після появи бульбочки. Фіксація азоту розпочинається на четвертий день. У синтезі леггемоглобіну, найважливішого продукту симбіозу, беруть участь обидва симбіонти - рослина і бактерії. Якщо культивувати бактерії і рослини окремо, то леггемоглобін не утворюється ні в тих, ні в інших. Леггемоглобін має дві особливості: він може окиснюватись і стійко зв'язувати кисень. Леггемоглобін міститься у вакуолях рослинної клітини і легко видаляється з них водою. Вважається, що він сприяє процесу засвоєння азоту, підтримуючи окисно-відновний стан на певному рівні.
Симбіотичні системи типу бульбочкові бактерії - бобові рослини це приклад складного, але чітко організованого симбіозу (в якому спостерігається прямий обмін генами) організмів, які належать до різних царств.
Крім позитивних взаємовідносин, між бактеріями та рослинами можуть виникати й негативні. Бактерії, що паразитують на рослинах, називають фітопатогенами. Види фітопатогенних бактерій є серед аеробних та факультативно-аеробних грамнегативних паличок (Pseudomonas, Xanthamonas, Erwinia, Agrobacterium та ін.), а також серед грампозитивних корінеформних бактерій і мікоплазм. Як і патогени тварин, патогени рослин мають фактори патогенності, що дозволяють їм перемагати захисні бар'єри рослин. До факторів патогенності належать ферменти пектиназа та целюлаза, а також фітотоксини та фактори адгезії.
Бактерії заражують рослини при проникненні крізь продихи сочевиці, нектарники, інколи можуть передаватися з насінням. Деякі бактерії можуть проникати в рослину лише через свіжі механічні пошкодження (ранки). Наприклад, збудник бактеріального раку томатів заражує рослину при поломці волосків на стеблі або плодах. Зараженню рослин часто сприяють комахи. Erwinia amylovora переноситься бджолами і проникає в рослину крізь нектарники. Erwinia stewarti, патоген кукурудзи, розноситься жуками і заражує рослину через погризи. Клітини бактерій містяться у слині та шлунку комах і навіть можуть перезимовувати там.
Фітопатогенні бактерії, що проникли в рослину, зазвичай розмножуються в міжклітинному просторі та судинах. Вони викликають різноманітні гнилі, опіки, плямистості, пухлиноподібні вирости.
Між фітопатогенними бактеріями та рослинами склались певні взаємовідносини, які передбачають процеси взаємного пізнавання і наступних за ним фізіологічних та регуляторних реакцій. Пізнавання бактеріями рослини може стимулювати її захисні функції. Суттєву роль у цьому відіграють лектини рослин.
Важливим фактором стійкості рослин до фітопатогенних бактерій є утворення ними фітоалексинів - низькомолекулярних сполук, які мають бактерицидні властивості. Фітоалексини не утворюються в здорових рослинах. Індукторами синтезу фітоалексинів можуть бути різні сполуки, в тому числі елементи клітинної стінки бактерій.
Взаємовідносини мікроорганізмів із безхребетними тваринами. Мікробні ендосимбіонти значно поширені серед найпростіших, черв'яків, комах та інших безхребетних тварин.
Бактеріальні клітини неодноразово виявляли в цитоплазмі, вакуолях, ядрах клітин амеб. Функції такого симбіозу вивчені недостатньо. Вважають, що у клітинах амеб, у яких відсутні мітохондрії, їхні функції виконують саме бактерії.
При досліджені анаеробних мікроорганізмів було відкрито їхні симбіотичні взаємовідносини з морськими амебами та інфузоріями. У клітинах цих тварин виявлено метаногенні архебактерії, асоційовані з мікро- тілами-гідрогеносомами, в яких відбувається утворення з пірувату водню, СО2 та ацетату. Метаногени використовують ці продукти у своєму метаболізмі й утворюють метан. Для хазяїна симбіонти є кінцевими акцепторами електронів, а самі архебактерії знаходять у клітині найпростіших захист і джерело харчування.
Цікавим є потрійний симбіоз між бактеріями, найпростішими та комахами. Так, таргани і терміти, які живляться деревиною, містять у своєму кишечнику велику кількість джгутикових найпростіших. Джгутиконосці щільно заповнюють мішкоподібне потовщення задньої кишки комахи. У свою чергу джгутиконосці є хазяїнами для позаклітинних спірохет та внутрішньоклітинних бактерій. При тісному співіснуванні мікроорганізмів та найпростіших відбувається продукування ферменту целюлази, яка забезпечує засвоєння комахами деревини. Однією з дивовижних особливостей циклу передачі симбіонтів у комах є те, що цистоутворення у джгутиконосців регулюється гормонами комахи.
За допомогою антибіотиків можна звільнити комах від симбіонтів. Таргани без симбіонтів слабо пігментовані, менш активні, розвиваються повільно, не уникають світла, на відміну від нормальних особин, і врешті-решт дегенерують. Припускають, що симбіонт постачає хазяїну деякі ферменти азотного обміну, які особливо необхідні комасі на стадії личинки.
Симбіоз з бактеріями є особливістю й у цикад. Описано понад 50 типів їхніх симбіонтів, до того ж цикади можуть мати від одного до шести симбіонтів одночасно. Крім бактерій, у цикад нерідко сим-
біонтами є гриби. Симбіонти передаються нащадкам через яйця. Клітини симбіонтів мають неправильну форму і на ультратонких зрізах виглядають дещо незвично. Вони оточені трьома мембранами: дві власні, а третя утворена хазяїном. ДНК-вмісні зони не виявляються. Слід зазначити, що життєздатні особини цикад розвиваються лише з яєць інфікованих симбіонтами.
Ще одним цікавим прикладом симбіотичних взаємовідносин є симбіоз погонофора і бактерії. Один вид таких симбіонтів мешкає на глибині 2500 м біля Галапагоських островів. Особливістю цієї форми життя є її повна незалежність від енергії сонця, оскільки використовується виключно геотермальна енергія. Травний тракт у погонофор повністю відсутній і обмін речовин здійснюється безпосередньо через епідерміс. Живлення організму забезпечується процесами, які відбуваються у трофалосомах - спеціалізованих ділянках тканини тварини, що включає клітини бактеріоцити. Бактеріоцити щільно заповнені клітинами грамнегативних бактерій. У воді, де живе погонофора, міститься значна кількість сірководню, який і окиснюють бактерії- симбіонти. Трофалосоми мають сильно розгалужену систему судин. Через кров здійснюється постачання бактеріям О2 та СО2. У клітинах, які мають симбіонтів, міститься цитоплазматичний гемоглобін, який забезпечує перенесення кисню до симбіонтів через цитоплазму. Автотрофні бактерії здійснюють синтез органічних речовин за рахунок енергії від окиснення сірководню. Продукти хемосинтезу - єдине джерело харчування як для мікроорганізмів, так і для їхнього хазяїна.
Будь-які бактерії можуть виявитись жертвою безхребетних - від амеби до молюсків та кліщів, для яких вони є їжею. Доля бактеріальних клітин, які проковтнув безхребетний, може бути різною. За наявності у тварини відповідних гідролітичних ферментів, які руйнують клітинні стінки бактерій, останні перетравлюються. Якщо ж такі ферменти відсутні, то мікроорганізми зберігають життєздатність, а інколи й інтенсивно розмножуються в тілі безхребетних.
Взаємовідносини мікроорганізмів з організмом людини. Унаслідок взаємного пристосування мікро- і макроорганізму, яке склалося у процесі еволюції, сформувалася так звана нормальна мікрофлора організму людини. Деякі мікроорганізми потрапляють в організм людини з водою, повітрям та продуктами харчування і перебувають у ньому недовго. Значна частина бактерій пристосувалася до існування в певних частинах тіла, тому, обговорюючи питання нормальної мікрофлори, виділяють мікрофлору шкіри, порожнини рота, шлунково- кишкового тракту, дихальних та сечовивідних шляхів, слизової оболонки ока і піхви.
Мікроорганізми шкіри. Шкірні покриви тіла людини мають свої ділянки, свій рельєф. Клітини епідермісу шкіри постійно відмирають і оновлюються. На поверхню шкіри виділяються продукти потових та сальних залоз. Усі ці виділення є поживним середовищем для мікроорганізмів. Потові залози забезпечують бактерії солями та органічними сполуками, у тому числі азотовмісними. Виділення сальних залоз багаті жирами.
Потових залоз багато (~300/см2) на ступнях, долонях, під пахвами і менше (до 100/см2) на спині. Мікроорганізми заселяють головним чином ділянки шкіри, вкриті волоссям і зволожені потом. Так, під пахвами мешкає 105-106 клітин бактерій на см2. На ділянках шкіри, що вкрита волоссям, міститься ~1,5 ·106 кл/см2, і лише кілька сотень бактерій живе на 1 см2 спини.
Зазвичай на шкірі переважають грампозитивні бактерії: Staphylococcus (S. epidermidis, S. hominis), Micrococcus, Propionibacterium, Corynebactenum, Brevibactenum, Acinetobacter.
Представники роду Corynebactenum інколи становлять до 70 % всієї мікрофлори шкіри. Деякі види утворюють ліпази, які розщеплюють жири (виділення жирових залоз). Стерильний піт не має запаху, запах йому надають продукти метаболізму бактерій, і насамперед Corynebacterium.
Для шкіри ніг властива наявність великої кількості клітин Brevibacterium, які при засвоєнні сірковмісних амінокислот утворюють газ метантіол, що має специфічний запах.
Шкіру людини постійно контамінують мікроорганізми ґрунту і повітря, серед яких можуть бути умовно-патогенні та патогенні мікроорганізми (стафілококи, збудники правцю, газової гангрени, ботулізму). Але у здорової людини нормальна мікрофлора шкіри та інші захисні фактори перешкоджають виникненню інфекційного процесу.
Кон’юнктива представлена незначною кількістю мікроорганізмів, що зумовлено вмістом лізоциму у сльозових виділеннях. Серед мікроорганізмів на кон'юнктиві є стафілококи та коринебактерії. У деяких випадках виявляються мікоплазми, аденовірус та вірус герпесу, які при послабленні захисних функцій організму можуть бути причиною інфекції У значного відсотка людей (~47 %о) мікрофлора кон'юнктиви повністю відсутня.
Мікрофлора вуха. У внутрішньому та середньому вусі в нормі мікроорганізмів не повинно бути. У зовнішньому слуховому проході часто виявляється факультативна мікрофлора, яка містить непатогенні стафілококи та коринебактерії; рідше - бактерії роду Pseudomonas, дріжджеподібні гриби роду Candida, цвілеві гриби (Aspergillus та ін.), які за певних умов можуть бути збудниками патологічних процесів.
Мікрофлора сечостатевої системи. Нирки, сечові канали і сеча в сечовому міхурі в нормі стерильні. На зовнішніх статевих органах локалізуються мікобактерії (Mycobacteriumsmegmatis), коринебактерії, мікоплазми та стафілококи. Мікрофлора піхви характеризується закономірними змінами на різних етапах статевого віку. У дівчат перші мікроорганізми з'являються через добу після народження. У перший місяць життя домінують лактобактерії (Lactobacillus acidophilus, L. fermentum), які передаються від матері під час пологів. Для розвитку в немовлят молочнокислих бактерій у цей період є оптимальні умови, оскільки їхній організм насичений естрогенними гормонами, а секрет піхви містить глікоген і має кислу реакцію. У цей же час у піхві виявляються стафілококи (S. saprophyticus), стрептококи (S. faecalis), коринебактерії (С. xerosis) та ін.
Наступні десять років у піхві мікроорганізми практично не виявляються. У цей період зникають гормони, отримані від матері під час пологів, а pH секрету піхви підвищується до нейтрального та слабо- лужного значення, зникає глікоген. Під час статевої зрілості знову з'являються молочнокислі бактерії. Це пов'язано з естрогенізацією організму власними гормонами і зниженням pH секрету піхви до кислої реакції. У періоди менструальних циклів секрет має лужну реакцію, внаслідок чого поряд з молочнокислими бактеріями і коринебактеріями виявляються стафілококи, негемолітичні стрептококи, мікоплазми, дріжджеподібні гриби та найпростіші.
Мікроорганізми дихальних шляхів. Протягом доби доросла людина вдихає близько 12 000-14 000 л повітря, з яким в її організм проникають частинки пилу й адсорбовані на них мікроорганізми. Повітря, яке видихається, містить у 250-500 разів менше мікробних клітин, ніж те, яке вдихується. Основна маса мікроорганізмів затримується на слизових оболонках верхніх дихальних шляхів, де вони зазнають бактерицидного впливу лізоциму та муцину, або при чханні частина мікроорганізмів знову виділяється в повітря.
У носовій порожнині визначається декілька постійних видів непато генних стафілококів (Staphylococcus epidermidis, S. saprophyticus), деякі коринебактерії, стрептококи, дифтероїди. Факультативна мікрофлора представлена Staphylococcus aureus, Streptococcus pyogenes, S. pneumoniae, нейсеріями (Moraxella locunata), гемоглобінофільними бактеріями (Haemophillus influenzae) та ін.
На слизових оболонках носоглотки визначається Streptococcus mitis, деякі непатогенні нейсерії та вейлонели. Факультативна мікрофлора носоглотки представлена Neissedameningitidis, Streptococcus pneumoniae та мікобактеріями.
Потенційно мікроорганізми з носоглотки здатні проникати в легені. Але цілий ряд захисних механізмів запобігає проникненню мікроорганізмів у трахеї, бронхи, легені. По-перше, більшість бактерій прилипає до слизової оболонки носоглотки і не може вільно пересуватись до легень, оскільки війчасті клітини епітелію, що вистеляють трахею, постійно женуть слиз вгору. По-друге, легені є місцем дуже активного фагоцитозу - механізму, завдяки якому чужорідні клітини захоплюються та інактивуються.
Мікроорганізми травного тракту. Коменсалами ротової порожнини є майже 100 видів мікроорганізмів, а в 1 мл слини міститься понад 108 мікробних клітин. Тут складаються ідеальні умови для розвитку як сапрофітних, так і патогенних чи умовно-патогенних видів. Головну роль у підтримці кількісного та якісного різноманіття мікроорганізмів порожнини рота відіграє слина. Вона містить необхідні поживні речовини, тут підтримується постійна температура, pH, вологість та інші необхідні для розвитку мікроорганізмів умови. Але в той же час слина виявляє певні антибактеріальні властивості, зумовлені наявністю таких ферментів, як птиалін, лізоцим, лактоферин, пероксидаза і нуклеа- за; вона містить специфічні секреторні імуноглобуліни.
Кількісний та якісний склад мікрофлори порожнини рота дитини залежить від її віку та дієти. Через декілька днів після народження в ротовій порожнині виявляються стрептококи (Streptococcus salivarius, S. mitis), лактобактерії, деякі види нейсерій та актиноміцети. З віком якісний та кількісний склад мікрофлори змінюється.
Основна маса мікрофлори ротової порожнини локалізується в зубному нальоті та на спинці язика. Майже 70 % об'єму зубного нальоту становлять мікроорганізми, в 1 мг його сухої маси визначається близько 2,5 х 108 мікробних клітин.
Найтиповішими для ротової порожнини дорослої людини є стрептококи (Streptococcus salivarius, S. mitis, S. mutans, S. sanguis, інколи S. faecalis), гемолітичні стрептококи, лактобактерії, вейлонели, сапрофітні нейсерії, бактероїди та коринебактерії.
У ротовій порожнині виявляються гемофільні бактерії (Haemophilus influenzae), трепонеми (Treponema denticola., T. macrodentium, T. oralis), дріжджеподібні грибки (Candidaalbicans), актиноміцети, мікоплазми (Mycoplasma oral, M. salivarium) та ін.
Серед факультативних мешканців порожнини рота зустрічаються ентеробактерії (представники родів Escherichia, Enterobacter, Klebsiella, Proteus), а також синьогнійна паличка (Pseudomonas aeruginosa), ендо- спороутворювальні бактерії родів Bacillus, Clostridium та ін.
Захворювання зубів і ясен можуть бути спричинені зміною кількісного та якісного складу представників нормальної мікрофлори, а також недотриманням гігієни ротової порожнини. Streptococcus mitis (представник нормофлори), локалізуючись у щілинах між яснами і поверхнею зуба, може викликати запалення зубної пульпи. S. salivarius міститься переважно в слині і на спинці язика, продукує в значних кількостях слизоподібні речовини декстранової й леванової природи і може бути причиною карієсу. S. sanguis локалізується в зубному нальоті, продукує слизоподібну речовину декстранової природи і також може бути однією з причин карієсу.
Потрапивши до шлунку більшість транзиторних мікроорганізмів тут гине. Цьому сприяють низькі значення pH та висока активність гідролітичних ферментів, які виявляють бактерицидну дію і є надійним бар'єром на шляху проникнення мікроорганізмів у кишечник. Проте рівень кислотності шлункового соку не завжди постійний, він змінюється залежно від характеру їжі та кількості води. У шлунку визначаються в невеликих кількостях (до 103 в 1 мл) молочнокислі бактерії, сарцини (Sarcina ventriculi), спори бактерій, дріжджі. У деяких випадках можливе потрапляння в шлунок, а потім і в кишечник дизентерійних, черевнотифозних, паратифозних бактерій, холерних вібріонів та інших патогенних чи умовно-патогенних мікроорганізмів.
У тонкій кишці, особливо у верхніх її відділах, виявляється невелика кількість мікроорганізмів, переважно аеробів, кількість яких не перевишує 102-103 клітин, незважаючи на те, що тут лужна реакція середовища. Бурному розвитку мікроорганізмів запобігають ферменти тонкої кишки, які мають бактерицидні властивості. У нижньому відділі тонкої кишки мікрофлора більш численна і за своїм складом близька до мікрофлори товстої кишки.
У товстій кишці найбільш сприятливі умови для розвитку багатьох видів мікроорганізмів. Склад мікрофлори кишок змінюється з віком людини. Кишечник новонароджених у перші години життя стерильний. З часом у ньому формується специфічна мікрофлора, яка на 8595 % складається з біфідо- та лактобактерій. Ці бактерії виявляють антагоністичні властивості щодо патогенних та умовно-патогенних мікроорганізмів, які здатні викликати кишкові розлади в немовлят. На 3-5-ту добу в кишечнику немовлят з'являються E. coli та ентерококи, вміст яких збільшується з переходом на змішане харчування. Бактероїди не виявляються в дітей першого півріччя життя.
Товста кишка дорослої людини містить понад 400 видів різних факультативних та облігатних анаеробів (~109 мікробних клітин в 1 г вмісту). Домінуючою групою, яка властива еубіозу дорослої людини, є аспорогенні анаеробні бактерії - біфідобактерії та бактероїди. З факультативних анаеробів у кишечнику домінують кишкова паличка, лактобацили та ентерококи. У незначних кількостях (до 103 на 1 г вмісту) виявляються представники роду Clostridium (C. perfringens, C. sporogenes), Proteus, Staphylococcus, Pseudomonas та дріжджеподібні грибки (Candida albicans).
Нормальні мікробіоценози людини і тварин прийнято розглядати як своєрідну мікроекологічну систему, яка виконує і регулює ряд життєво важливих функцій хазяїна. Однією з важливих функцій нормальної мікрофлори є запобігання колонізації макроорганізму патогенними бактеріями. Це забезпечується як за рахунок високих адгезивних властивостей нормобіоти (тобто більш високої конкурентоспроможності до колонізації епітеліальних тканин), так і за рахунок продукування речовин, які інгібують ріст патогенів, та створення несприятливих для їхнього росту значень pH. Доведена також участь нормофлори у формуванні захисно-адаптаційних механізмів макроорганізму. Так, мікроорганізми нормальної мікрофлори беруть участь у регуляції синтезу імуноглобулінів, стимулюють активність клітин фагоцитарного ряду, локалізованих у стінці кишечнику, та їх бактерицидну активність. Мікроорганізми кишкової флори беруть участь у метаболічних перетвореннях деяких речовин, наприклад, первинні жовчні кислоти трансформуються у вторинні під впливом бактероїдів. Інактивація деяких ферментів та токсинів відбувається також за участю представників нормофлори. Відомо, що нормофлора бере участь у метаболічних процесах макроорганізму. Так, біфідобактерії, синтезують амінокислоти, білки, вітаміни B1, B2, K, тіамін, рибофлавін, нікотинову, пантотенову та фолієву кислоти, піридоксин, ціанкобала мін, а також сприяють всмоктуванню кальцію, заліза та вітаміну D.
Таким чином, нормальна мікрофлора перебуває в безпосередньому зв'язку з макроорганізмом. Разом з тим вона є високочутливою індикаторною системою, яка реагує кількісними та якісними порушеннями на зміни в макроорганізмі.
Еволюційно сформована система макроорганізм - нормальна мікрофлора перебуває під постійним впливом різноманітних факторів довкілля, а саме: харчування, сезон, професія, хірургічне втручання, рентгено-, радіо- та хіміотерапія тощо. Усі ці фактори (кожен окремо або в комплексі) можуть негативно впливати на динамічну рівновагу між макроорганізмом та його мікробіоценозом. Зміни в мікробіоценозі загальної кількості мікроорганізмів і/або співвідношенні окремих видів та їхніх властивостей називають дисбактеріозом. Найпоширенішим є дисбактеріоз кишечнику.
До факторів, які призводять до змін у складі нормальної мікрофлори, можна віднести вік людини, характер харчування, зміну екологічних та кліматичних умов, емоційний стан (стреси). Це буде так званий первинний дисбактеріоз. Зміни у складі мікрофлори можуть бути наслідком певних захворювань або їхньої терапії. Такий дисбактеріоз називають вторинним.
Зі старінням організму практично в усіх людей похилого віку спостерігається віковий дисбактеріоз, який супроводжується порушенням моторики кишечнику, посиленням всмоктування продуктів метаболізму мікроорганізммів, що впливає на обмін холестерину і жовчних кислот. Продукти, які мають виводитися з організму через кишечник, затримуються, внаслідок чого збільшується кількість мікроорганізмів у нестерильних ділянках організму, змінюється їхній склад та властивості (з'являються ферментативно дефективні штами кишкової палички, її гемолітичні та капсульні форми).
Харчовий дисбактеріоз спостерігається в разі зміни режиму та характеру харчування. При харчуванні переважно молочними продуктами збільшується кількість ацидофільних бактерій, цитробактера, грибів і зменшується кількість кишкової палички та спороутворювальних мікроорганізмів. При м'ясній дієті, навпаки, збільшується кількість клітин кишкової палички і спороутворювальних аеробів, а кількість ацидофільної мікрофлори зменшується. Причинами зміни складу і властивостей мікрофлори при різних харчових режимах є зміни біохімічних процесів у товстій кишці.
Сезонний дисбактеріоз пов'язують з коливаннями температурного режиму і зміною харчування. Залежно від температури можуть змінюватись біологічні властивості мікроорганізмів. З підвищенням зовнішньої температури популяція мікроорганізмів може зазнавати фазової перебудови, переходячи з латентного стану в активний, що супроводжується інтенсифікацією епідемічного процесу. Зокрема, збільшення кишкових захворювань збігається з підвищенням температури. При цьому активуються як самі збудники захворювань, так і шляхи їх передачі. У більшості випадків зимовий дисбактеріоз супроводжується запором, а літній, навпаки, - проносом.
До первинного дисбактеріозу відносять також дисбіотичні зміни, які виникають у практично здорових людей під впливом стресових ситуацій.
При стресовому стані мікробна відповідь у кишечнику супроводжується видовою перебудовою, порушенням екологічного бар'єру та створенням умов для колонізації умовно-патогенними мікроорганізмами. Стресові зміни найбільше відбиваються на травному апараті та імунологічному статусі людини. Так, зміни у травному тракті визначаються ослабленням перистальтики кишок, порушенням їхньої бар'єрної функції через морфофункціональні зміни слизової оболонки. До того ж стресова ситуація зумовлює зміни як адгезивних властивостей бактерій, так і адгезивності макроорганізму. Поверхневий шар слизу слизової оболонки кишок, який складається з муцину, відіграє суттєву роль у багатофакторному процесі адгезії бактерій на її поверхні. Фізико- хімічний стан муцину легко може бути порушений жовчними кислотами, протеолітичними ензимами, коливаннями pH. При стрес-реакції відмічають різке зменшення муцину і зниження кислих мукополісахаридів на поверхні слизової оболонки кишок та в її покривних клітинах. Як фактор, що зумовлює зміни адгезії у стресових ситуаціях, слід розглядати і порушення гормонального гомеостазу, оскільки гормони індукують зміни синтезу рецепторів для бактерій і модифікують здатність відповідних клітин макроорганізму зв'язувати бактеріальні клітини. При стресовому стані змінюється імунореактивність, яка характеризується зниженням кількості lgА, значення якого в захисті від патогенних збудників пов'язують з пригніченням адгезії та колонізації.
Зниження імунологічної резистентності макроорганізму може суттєво вплинути і на топографічний розподіл окремих груп мікроорганізмів у шлунково-кишковому тракті, що є важливим з погляду ендогенної контамінації і метаболічних наслідків підвищеного бактеріального росту в тонкій кишці. Слід відзначити, що при стресових реакціях у людини порушуються практично всі види обміну.
У більшості випадків до первинного дисбактеріозу відносять зміни у складі мікрофлори кишок, які не супроводжуються вираженими клінічними ознаками, не потребують спеціального лікування і здебільшого зникають самостійно при усуненні фактора, який спровокував ці зміни.
До окремо виділеної форми дисбактеріозу слід віднести зміни у складі нормальної мікрофлори, які виникають під впливом іонізуючого опромінення.
З другої половини ХХ ст. внаслідок розвитку атомної промисловості і енергетики, медичної та побутової радіаційної апаратури безперервно зростає надходження в довкілля радіоактивних речовин. Випробовування ядерної зброї, аварії на ядерних установках, недбале користування радіаційним обладнанням - усе це призводить до появи великих та малих регіонів з підвищеним рівнем радіації. Вплив іонізуючого опромінення на організм людини не залишається непоміченим, причому ймовірність виникнення патологічних змін зростає з підвищенням дози опромінення.
Реакція травного тракту на опромінення - це сукупність складних змін, які вражають слизову оболонку кишок, порушують кровообіг у судинах, змінюють секрецію, моторику і процеси всмоктування. У клітинах слизової оболонки різко пригнічується синтез білків та ферментативна активність, спостерігається масова загибель епітеліальних клітин, знижується їх поділ. При малих дозах опромінення в кишечнику збільшується кількість кишкової палички, стафілококів, протеїв, клостридій і знижується вміст лактобацил. Кількість дріжджів та бактероїдів залишається незмінною.
Після опромінення суттєво зростає ступінь проникності стінок кишок, що полегшує надходження з травного тракту у кров токсичних продуктів, які виробляють шкідливі мікроорганізми. У мікробній інтоксикації при променевій хворобі певну роль відіграють токсини клост- ридій, стафілококів, стрептококів та інших бактерій, тобто токсини всіх мікроорганізмів, які містяться на слизовій оболонці. Важливо, що ці бактерії здатні вступати в асоціативний зв'язок із слизовою оболонкою кишок, і, напевно, діарея, яка виникає при гострій променевій хворобі, пов'язана з проникненням у слизову оболонку штамів, що синтезують ентеротоксини. Вважається, що зниження в кишечнику кількості ешерихій, які виявляють коліциногенну активність, корелює зі збільшенням кількості патогенних і антибіотикостійких штамів.
При дії високих доз радіації тварини гинуть на 3-4-ту добу, і постпроменевий дисбактеріоз не встигає розвинутись. Він розвивається поступово, через 6-8 діб після опромінення.
Під впливом іонізуючого опромінення значно знижується резистентність макроорганізму до зараження різноманітними інфекційними агентами. Перебіг інфекційних захворювань характеризується генералізацією процесу, накопиченням значних кількостей мікроорганізмів, переходом хронічного захворювання з латентним перебігом у маніфестуючі гострі форми хвороби, розвитком деструктивно- некротичного запального процесу в тканинах, скороченням тривалості життя та збільшенням летальності.
Щодо впливу іонізуючої радіації на мікрофлору організму людини можна зробити декілька узагальнень, а саме:
- опромінення викликає загибель мікроорганізмів, причому життєздатних клітин буде тим менше, чим вища доза опромінення. У цьому проявляється його летальна дія;
- опромінення виявляє мутагенну дію, що зумовлює появу спадково-змінених форм. До певної міри кількість мутагенів зростає з підвищенням дози;
- мінливість, зумовлена опроміненням, має ненаправлений, стохастичний характер (серед тих форм, що вижили, зустрічаються мікроорганізми з різними змінами морфологічних, фізіологічних і біохімічних властивостей);
- серед мутантних мікроорганізмів можна виділити форми з негативними (менш життєздатні) і позитивними (більш життєздатні) змінами.
До вторинних форм дисбактеріозу відносять дисбіотичні зміни, які супроводжують основне захворювання або є наслідком його терапії. Про те, що ці зміни вторинні, свідчить той факт, що в перші дні захворювання мікрофлора кишок є якісно різноманітною з фіксованим співвідношенням представників нормофлори на фоні зростання певних видів умовно-патогенних і патогенних мікроорганізмів. Лише з часом відбувається зниження питомої ваги біфідо- та лактобактерій, порушується рівновага між анаеробною та аеробною мікрофлорою. Оскільки колонізаційну резистентність кишок забезпечують анаеробні мікроорганізми, при зниженні їхньої кількості полегшується проникнення патогенних мікроорганізмів крізь слизові оболонки кишок. Крім того, при різних патологічних станах органів травлення відбувається заселення мікроорганізмами верхніх відділів тонких кишок, що є важливою ознакою дисбактеріозу.
Функціонально-морфологічні зміни у стінках кишок (наприклад, при ентероколіті) сприяють проникненню мікроорганізмів. До того ж при запальних процесах у тонкій кишці та наявності в ній мікроорганізмів гальмується інтенсивність регенерації епітелію, розвивається атрофія слизової оболонки, що супроводжується зниженням адсорбуючої здатності епітеліальних клітин. Унаслідок порушення мембранного травлення в порожнині кишки накопичуються не повністю гідролізовані продукти, порушується всмоктування, підвищується осмотичний тиск, що призводить до появи ентерального синдрому (пронос, бурчання в кишечнику, здуття живота). Одночасно настає дисфункція товстої кишки. Мікробні метаболіти і токсини справляють місцевий та загальний вплив на організм людини. Мікроорганізми втрачають здатність інактивувати травні ферменти, які потрапляють з верхніх відділів травного тракту, тому при дисбактеріозі кишкові ферменти (ентерокіназа та лужна фосфатаза) фекалій виділяються у великих кількостях.
Не менш важливим наслідком дисбактеріозу є порушення інтенсивності ендогенного синтезу і засвоєння вітамінів. Порушується також засвоєння заліза, кальцію, біологічно активних сполук, всмоктування вуглеводів, жирних кислот, амінокислот та сполук азоту.
Сенсибілізація й алергізація макроорганізму при дисбактеріозі призводить до тривалого перебігу основного захворювання, збільшення рівня гістаміну, неспроможності ушкодженої слизової оболонки кишки продукувати гістаміназу в достатній кількості для інактивації гістаміногенної мікрофлори.
Лікування цих змін антибіотиками у свою чергу призводить до порушень у складі нормального мікробіоценозу.
Динаміка змін мікрофлори кишок залежить від дози антимікробного препарату. При використанні малих та середніх терапевтичних доз антибіотиків кількість умовно-патогенних мікроорганізмів збільшується безпосередньо під час антибіотикотерапії. Застосування антибіотиків широкого спектра дії у високих терапевтичних дозах супроводжується порушенням цілісності біоплівки, аж до її повного зникнення зі значної частини поверхні кишок. Стійкий і виражений дисбактеріоз розвивається одразу після відміни антибіотиків. Звільнені місця на слизовій кишок займають мікроорганізми довкілля. Ці мікроорганізми відрізняються від представників нормофлори тим, що вони не здатні виконувати ряд важливих фізіологічних функцій, тому в кишечнику порушуються метаболічні процеси.
Використання антибіотиків призводить до зростання резистентних до них мікроорганізмів. Підвищення рівня антибіотикорезистентних бактерій зумовлено як процесом селективного розмноження, так і передачею R-фактора (фактор резистентності) спорідненим бактеріям.
Слід зазначити, що глобальні зміни складу нормофлори кишок відбуваються не лише при шлунково-кишкових інфекціях (сальмонельозі, стафілококовому гастроентероколіті, кампілобактеріозі тощо), а й при інфекційних захворюваннях, не локалізованих у шлунково-кишковому тракті, наприклад при гострих захворюваннях органів дихання. При цьому відмічають зниження кількості біфідофлори, збільшення кількості E. coli зі зміненими ферментативними властивостями та появу її гемолітичних форм. На більш пізніх етапах захворювання в мікробіоценозі кишок переважають Staphylococcus aureus, Pseudomonas aeruginosa та P. alcaligenes. Слід підкреслити, що мікрофлора травного тракту людей відновлюється значно пізніше, ніж настає клінічне одужання.
Усі зміни, що виникають під впливом на макроорганізм тих чи інших факторів, можуть бути більш чи менш виражені, тому в клінічній практиці прийнято визначати ступінь вираження дисбактеріозу.
Найбільш вдалою схемою визначення ступеня дисбактеріозу вважають запропоновану в 1986 р. Н. Грачовою. Згідно з цією схемою розрізняють чотири ступеня дисбактеріозу:
- дисбактеріоз 1-го ступеня (латентна, компенсована форма) характеризується незначними змінами аеробної частини мікробіоценозу (збільшення або зменшення кількості кишкової палички). Біфідо- та лактофлора залишаються незмінними. Кишкові дисфункції, як правило, не реєструються;
- дисбактеріоз 2-го ступеня (субкомпенсована форма). На фоні незначного зниження вмісту біфідофлори виявляються кількісні та якісні
зміни кишкової палички або інших умовно-патогенних мікроорганізмів. Така форма дисбактеріозу є граничним станом і свідчить про те, що досліджувані особи можуть бути віднесені до групи ризику;
- дисбактеріоз 3-го ступеня характеризується значним зниженням рівня біфідобактерій разом із лактобактеріями і різкими змінами кількості кишкової палички. Створюються умови для прояву патогенних властивостей умовно-патогенних мікроорганізмів. Виникають кишкові дисфункції;
- дисбактеріоз 4-го ступеня характеризується відсутністю біфідобактерій, значним зменшенням лактобактерій і суттєвими змінами кишкової палички. Зростає кількість факультативної та невластивої здоровій людині умовно-патогенної мікробіоти.
Своєчасне виявлення дисбактеріозу та визначення ступеня його вираження дозволяє вчасно та коректно підібрати методи і засоби для відновлення нормального мікробіоценозу людини.