МІКРОБІОЛОГІЯ - М.Г. Сергійчук - 2008
Розділ 12. ВИКОРИСТАННЯ МІКРООРГАНІЗМІВ ЛЮДИНОЮ
Мікробний синтез
Мікробний синтез - це синтез структурних елементів або продуктів обміну речовин за рахунок ферментних систем мікроорганізмів. Мікроорганізми використовують для отримання:
- антибіотиків;
- ферментів;
- органічних кислот;
- вітамінів.
Мікробний синтез складається з ряду технологічних етапів, які є спільними при отриманні різних речовин:
1. Підготовка мікроорганізму-продуцента.
2. Підготовка поживного середовища.
3. Проведення ферментації - культивування мікроорганізмів- продуцентів.
4. Відділення біомаси від культуральної рідини.
5. Виділення та очищення необхідного продукту з культуральної рідини або мікробної біомаси.
Синтез антибіотиків. Антибіотики відносять до вторинних метаболітів - речовин, які синтезуються після закінчення поділу клітин і не мають безпосереднього значення для росту мікроорганізму. Синтез антибіотиків проходить у культурах мікроорганізмів, які досягли стаціонарної фази росту. Саме ця фаза характеризується інтенсивним накопиченням антибіотика при низькій швидкості росту.
Для забезпечення максимального біосинтезу антибіотика здійснюють ретельний підбір середовищ і умов культивування для кожного продуцента.
Етапи промислового отримання антибіотиків наведено на рис. 12.5. Підготовка посівного матеріалу - це багатоступеневе вирощування культури - продуцента з постійним збільшенням її об'єму. Продуцент культивують на багатих середовищах, які забезпечують високу фізіологічну активність мікроорганізмів.
Промислову ферментацію здійснюють на середовищах, які забезпечують добрий ріст продуцента та максимальне накопичення антибіотика; містять доступні та дешеві компоненти; є однорідними і гарно фільтруються. Для кожного продуцента розробляють відповідне середовище. Забезпечують оптимальні умови культивування, температуру, рН, аерацію. Процес росту продуцента у ферментері ретельно контролюється.
Синтез ряду антибіотиків потребує додаткового внесення в середовище певних елементів або попередників антибіотиків - речовин, які
близькі за будовою до певної частини антибіотика та стимулюють його синтез. Наприклад, для синтезу пеніциліну в середовище вносять фенілоцтову кислоту. ЇЇ використовує гриб для побудови бічного ланцюга молекули бензилпеніциліну.
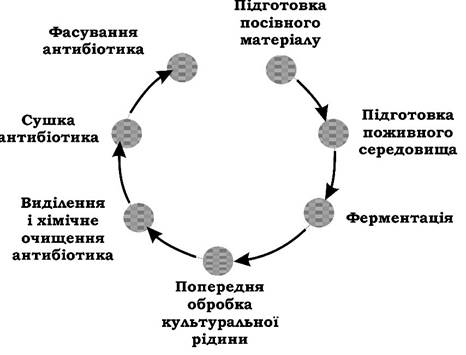
Рис. 12.5. Основні етапи отримання антибіотиків
Після завершення культивування застосовують певні методи вилучення антибіотика. Спочатку відокремлюють біомасу від культураль- ної рідини, використовуючи фільтрацію або сепарацію. Якщо антибіотик міститься в культуральній рідині, його виділяють методами екстракції розчинниками або осаджують у вигляді нерозчинних сполук, або сорбують іонообмінними смолами.
Наступною стадією отримання антибіотичних препаратів є очистка їх від різних домішок. Оскільки антибіотики застосовують у медичній практиці, то особливу увагу приділяють ступеню очистки та стерильності препаратів.
Залежно від властивостей антибіотика, його стабільності використовують два види сушки: ліофільну або розпилювальну.
Ліофільна сушка полягає у висушуванні антибіотика із замороженого стану у вакуумі. При розпилювальній сушці розчин антибіотика розпилюється до дрібних часточок (5-25 мкм) у потоці нагрітого до 160 0С повітря. Такий процес висушування триває декілька секунд, при цьому навіть термолабільні препарати не втрачають свої властивості. Готовий антибіотик підлягає контролю на стерильність і біологічну активність.
Напівсинтетичні антибіотики отримують шляхом модифікації вже існуючих антибіотичних речовин. Вони мають більш цінні властивості порівняно з вихідними препаратами. В основі напівсинтетичного способу отримання антибіотиків покладений наступний принцип. У результаті мікробного синтезу отримують вихідні антибіотики (пеніцилін, цефалоспорин, тетрациклін), які потім хімічно модифікують.
Іноді використовують не всю молекулу антибіотика, а лише основне ядро. Наприклад, для отримання напівсинтетичних пеніцилінів і цефалоспоринів використовують відповідно 6-амінопеніціланову кислоту, 7-аміноцефалоспоранову та 7-амінодезацетоксицефалоспора- нову кислоти, які хімічно модифікують.
Отримання ферментних препаратів. Ферменти знайшли широке використання в промисловості, сільському господарстві, медицині, дослідницькій роботі. Так, амілази застосовують для гідролізу крохмалю при виробництві спирту, пива, для отримання декстрину і патоки, для видалення клею з тканини.
У промисловості використовують, як правило, неочищені чи напівочищені ферменти, які називають ферментними препаратами.
Мікроорганізми є активними продуцентами ферментних препаратів, оскільки мають ряд особливостей:
- високу інтенсивність метаболізму (сумарна інтенсивність ферментних реакцій щодо поглинання молекулярного кисню у вигляді коефіцієнта QO2 (см3 кисню, який споживається 1 мг сухої біомаси за 1 год), для клітин печінки становить 2-5; нирки - 10-20; дріжджів - 50-100; у бактерій роду Acetobacter - 1800; у Azotobacter - 2000;
- високу швидкість приросту біомаси;
- високий вміст деяких ферментів у клітинах мікроорганізмів. Кількість рибулозобіфосфаткарбоксилази у фототрофних бактерій іноді сягає 40-60 % від усіх розчинних білків;
- наявність позаклітинних ферментів, які легко виділити з культуральної рідини, наприклад гідролази, які розщеплюють білки, крохмаль, целюлозу, жири та інші нерозчинні у воді речовини;
- ряд ферментів знайдено тільки в мікроорганізмів. До таких ферментів належать: таназа (розщеплює дигалат до галової кислоти), рацема- зи багатьох амінокислот; кератинази (гідролізують сірковмісні білки - кератини, що входять до складу волосся, пір'я, рогів і копит); пеніци- ліназа (розщеплює пеніцилін до пеніцилінової кислоти і води). Основними продуцентами ферментів до недавнього часу були гриби. Проте нині широке використання знаходять ферменти актиноміцетів, деяких бактерій (табл. 12.4).
Таблиця 12.4. Мікроорганізми — продуценти ферментів
Ферменти |
Гриби |
Бактерії |
Альфа-Амілаза |
Aspergillus oryzae, Aspergillus niger |
Bacillus amyloliquefaciens, Bacillus licheniformis |
Глюкоамілаза |
Aspergillus niger, Rhizopus niveus, Endomycopsis sp. |
|
Декстраназа |
Penicillium sp. |
|
Бета-Глюконаза |
Aspergillus niger |
Bacillus amyloliquefaciens |
Глюкозоізомераза |
Rhizopus formosaensis |
Actinoplanes missouriensis, Streptomyces olivaceus |
Інвертаза |
Aspergillus sp., Saccharomyces cerevisiae |
|
Целюлази |
Aspergillus niger, Trichoderma roseum, Trichoderma viride |
|
Пектинази |
Aspergillus niger, Trichoderma avamori |
|
Протеїнази |
Aspergillus niger, Aspergillus oryzae, Mucor mihei, Mucor rouxii, Mucor pusillus, Endothia parasitica |
Bacillus subtilis, B. amyloliquefaciens, B. licheniformis, B. staerothermophilus |
Ліпази |
Aspergillus oryzae, Aspergillus avamori, Candida cylindrica, Mucor mihei, Rhizopus sp. |
|
Глюкозооксидаза |
Aspergillus niger, Penicilium amagaskiense, Penicilium vitale, Penicilium notatum |
|
Каталаза |
Aspergillus sp. |
|
Деацетілаза |
Aspergillus sp. |
|
Аспартаза |
Escherichia coli |
|
Фумараза |
Escherichia coli |
Процес утворення того чи іншого ферменту залежить як від мікроорганізму, так і від складу середовища.
Для отримання ферментів використовують переважно комплексні, напівсинтетичні середовища, які містять синтетичну основу (мінеральні солі, органічні сполуки) і природні компоненти.
Деякі ферменти є індуктивними і потребують присутності індуктора в середовищі. Так, для синтезу ліпази необхідна наявність олії, рибонуклеази - нуклеїнові кислоти, протеїназ - глюкоза, органічний азот.
Найширшого використання набули ферменти, що належать до гідролаз, - глікозидази, пептидази та ін. Вони розщеплюють глікозидні, пептидні та деякі інші зв'язки за участю води.
Серед гідролаз багато позаклітинних ферментів. Вони накопичуються в культуральному середовищі. Отримання таких ферментів простіше і дешевше, ніж виділення із клітин. Максимальне накопичення ферментів відбувається у стаціонарній фазі росту.
Мікроорганізми культивують поверхневим або глибинним способом. Поверхневий спосіб використовують, як правило, для культивування цвілевих грибів. Їх вирощують на поверхні рідкого поживного середовища в кюветах при вологості повітря 70-95 %, температурі 28-32 0С та постійній циркуляції повітря. Один і той же продуцент може утворювати різні ферменти в певний період культивування. Наприклад, для Aspergillus oryzae амілази синтезуються на 21-30- ту годину культивування, протеолітичні - 48 год, пектолітичні - 3 доби, целюлозолітичні - 10 діб. Глибинне культивування здійснюється у великих ферментерах з інтенсивною аерацією.
Методи виділення та очистки ферментів різні і визначаються локалізацією ферменту (у клітинах чи культуральній рідині) і метою застосування.
Розрізняють неочищені та очищені ферментні препарати.
Неочищені ферментні препарати - це висушений і подрібнений міцелій гриба разом із щільним субстратом або культуральною рідиною. Ферментативна активність таких препаратів невелика, але вони дешеві і добре зберігаються. Таким способом отримують амілази, протеази, целюлази для сільського господарства та деяких галузей промисловості. При виділенні ферменту в культуральну рідину можливе її згущення та отримання сиропу.
Очищені препарати застосовують як терапевтичні засоби. Очищення проводять за допомогою гельфільтрації, діалізу, іонообмінних смол.
Окрім ферментів, отриманих у виробничих умовах і промисловому масштабі, є ряд ферментів, що використовуються поки що в обмеженій кількості, але деякі з них дуже важливі. До їх числа належать рестриктази (ендонуклеази), які розщеплюють нуклеїнові кислоти, і лігази, які беруть участь в їх синтезі. І ті і інші необхідні для генетичної інженерії.
Отримання органічних кислот. Промислове отримання органічних кислот методом мікробного синтезу розпочалося у 20-30-ті роки ХХ ст. До цього часу в харчовій промисловості використовували кислоти, отримані
з природних джерел: лимонну з лимонів, винну - з винного каменю. Оцтову кислоту отримували з вина, залишаючи його відкритим.
На сьогодні у промисловості за допомогою мікроорганізмів виробляють 18 видів органічних кислот (можливо отримати 50) з максимальним виходом від 35 % (ізолимонна) до 100 % (галова) (табл. 12.5).
Таблиця 12.5. Органічні кислоти та їх продуценти
Кислота |
Мікроорганізм |
Джерело вуглецю |
Молочна |
Lactobacillus delbrueckii Rhizopus oryzae |
Глюкоза Глюкоза |
Масляна |
Clostridium butyricum |
Крохмаль |
Пропіонова |
Propionibacterium shermanii |
Глюкоза |
Койева |
Aspergillus oryzae |
Глюкоза |
Глюконова |
Aspergillus niger |
Глюкоза |
2-Кетоглюконова |
Pseudomonas fluoreseens |
Глюкоза |
5-Кетоглюконова |
Gluconobacter suboxydans |
Глюкоза |
Винна |
Gluconobacter suboxydans |
Глюкоза |
Піровиноградна |
Pseudomonas aeruginosa |
Глюкоза |
Оцтова |
Acetobacter aceti Acetobacter sp. |
Етанол |
Лимонна |
Aspergillus niger Candida lipolytica |
Сахароза Парафін |
Ітаконова |
Aspergillus terreus |
Глюкоза |
Трео-О-ізолимонна |
Candida brumptii Candida lipolytica |
Глюкоза Алкани Етанол |
Аллоізолимонна |
Penicillium purpurogenum |
Глюкоза |
2-Кетоглутарова |
Pseudomonas fluoreseens Candida lipolytica |
Глюкоза Парафін |
Янтарна |
Bacterium succinicum |
Яблучна кислота |
Фумарова |
Rhizopus delemar Candida hydrocarbofumarica |
Глюкоза Парафін |
Яблучна |
Schizophyllum commune C. hydracarbofumarica + Pichia membranaefaciens |
Глюкоза Парафін |
Тетрадекандикарбонова |
Candida cloacea |
Гексадекан |
Отримання молочної кислоти. Молочну кислоту використовують у харчовій промисловості для виробництва сиропів, напоїв, мармеладу тощо. Молочна кислота має антимікробні властивості, тому
додається як консервант в деякі продукти (рибу, оливи тощо). Лактат кальцію застосовують у фармацевтиці як джерело кальцію.
Перевага мікробіологічного способу отримання молочної кислоти полягає в можливості спрямованого синтезу певного ізомеру, наприклад L+.
Розділення ізомерів молочної кислоти, отриманої шляхом хімічного синтезу, є технічно складним. Щорічно мікробіологічним шляхом отримують понад 20 тис. т молочної кислоти.
Продуцентами молочної кислоти можуть бути різні види молочнокислих бактерій (Lactobacillus delbrueckii, Lactobacillus bulgaricus). Перевагу віддають термофільним бактеріям для запобігання розвитку сторонньої мікрофлори. Як сировину використовують молочну сироватку, відходи цукрового виробництва - мелясу.
Ферментацію здійснюють у великих ферментерах. Для нейтралізації кислоти, що утворилась, періодично вносять Ca(OH)2, СаСО3 чи MgCO3. Кристалізації лактату Са у ферментері перешкоджає активне перемішування. Процес відбувається при температурі 49-50 0С. Цикл бродіння завершується за 7-10 діб залежно від складу середовища.
Після закінчення процесу ферментації культуральну рідину нейтралізують, фільтрують для відокремлення клітин. Фільтрат (містить 1213 % молочної кислоти) очищують багатоступенево і згущують до певної концентрації.
Отримання оцтової кислоти. Виробництво оцтової кислоти із спиртових розчинів відомо більш ніж 10 тис. років. Греки та римляни отримували цей напій, лишаючи вино відкритим.
Утворення оцтової кислоти здійснюють оцтовокислі бактерії. Вони характеризуються здатністю до окиснювальної трансформації первинних спиртів, гліколей, альдо і кетоцукрів та їх похідних (близько 80 трансформацій).
Продуцентами оцтової кислоти є аеробні грамнегативні бактерії Acetobacter aceti. Продуценти ростуть при рН 4,0, оптимум рН 5,0-6,0, витримують високу концентрацію оцтової кислоти, не здійснюючи її переокиснення.
Культивування здійснюють у струменевих генераторах, які заповнені дерев'яними ошурками. На ошурках адсорбують оцтовокислі бактерії, розпилюючи їх по поверхні ошурок. Поживне середовище повільно пропускають крізь ошурки з культурою. Середовище містить 3-5 % спирту, 5-6 % - оцтової кислоти, мінеральні солі. У міру протікання середовища бактерії окиснюють спирт до оцтової кислоти. У результаті 88-90 % спирту перетворюється в оцтову кислоту, що становить близько 1,4 кг/м3/добу.
При глибинному культивуванні швидкість утворення оцтової кислоти майже у 10 разів більша, ніж при поверхневому. Процес проводять у серії з шести ферментерів, які з'єднані послідовно. Кожний ферментер інтенсивно аерують та підтримують оптимальну температуру. У перший ферментер вносять середовище, що містить 4,05 % спирту і 1,4-1,5 % оцтової кислоти. У всі інші додатково додають спирт. Концентрація оцтової кислоти поступово зростає, а спирту - знижується. У першому ферментері культура активно розмножується, далі - лише накопичується оцтова кислота -30 кг/м3/добу.
Крім 6-9 % оцтової кислоти, розчин містить невелику кількість складних ефірів, які надають продукту приємного смаку.
Виробництво ряду органічних кислот здійснюють за допомогою мікроскопічних грибів - продуцентів. Метаболізм цих грибів через брак заліза, мангану, міді, магнію, калію чи кальцію порушується. Гриби починають виділяти в середовище глюконову, щавлеву, цитринову, ітаконову, фумарову, яблучну, бурштинову, мурашину кислоти.
Отримання лимонної кислоти. З усіх органічних кислот за обсягом виробництва лимонна кислота займає перше місце у світі - 350 тис. т/рік.
Близько 70 % кислоти використовується в харчовій промисловості, 18 % - у фармацевтичній, 12 % - для технічних цілей: як антивспінювач, як комплексоутворювальний агент, при обробці текстилю, у виробництві чистих металів, детергентів, для поглинання SO2. Застосування знаходять і побічні продукти ферментації: міцелій грибів і культуральна рідина.
Здатність утворювати лимонну кислоту характерна для міцеліальних грибів. Сьогодні перевага надається різним штамам Aspergillus niger. Штами, які використовуються у виробництві, відрізняються високою швидкістю росту, легкістю культивування і великим виходом лимонної кислоти.
Коли ріст гриба завершений, залишкова глюкоза за певних умов може перероблятись у лимонну чи інші кислоти.
Для синтезу лимонної кислоти грибом-продуцентом необхідні такі умови:
- висока концентрація вуглецю (15-20 %);
- наявність амонійних солей як джерела азоту;
- лімітування за фосфором та металами (особливо Zn, Fe, Mn);
- значення рН має бути нижче 2,0, щоб пригнітити утворення щавлевої і глюконової кислот;
- активна аерація.
У виробництві органічних кислот мікроскопічними грибами застосовують три способи ферментації: культивування на поверхні твердого поживного середовища (твердофазна ферментація); поверхневе культивування на рідкому середовищі; глибинне культивування.
При культивуванні на поверхні щільного середовища гриб- продуцент вирощують у неглибоких лотках на поверхні вологих висівок рису або пшениці. Під час ферментації рН становить 1,8-2,0. По закінченні процесу лимонна кислота разом із невеликою кількістю глюконової, щавлевої кислот, що утворилися одночасно, екстрагується водою, а потім осаджується у вигляді солі кальцію. Процес триває 5-8 діб. Такий найпростіший метод отримання лимонної кислоти застосовується в Японії.
Метод поверхневого культивування на рідкому середовищі широко використовується для виробництва лимонної кислоти у країнах Європи та Америки.
Поверхню рідкого середовища, яке розливають у неглибокі кювети, засівають конідіями гриба-продуцента. Кювети розміщують на стелажах у термостатованих кімнатах. Гриб розвивається у вигляді тонкої плівки на поверхні поживного середовища, яке містить високі концентрації цукру. Лимонна кислота, що утворюється, переходить з клітин міцелію в розчин, з якого по закінченні процесу її осаджують у вигляді кальцієвої солі, а потім переводять у форму вільної кислоти і кристалізують. Активність кислотоутворення грибної плівки досягає максимуму на 5-6-ту добу культивування (100-105 г лимонної кислоти/м2 плівки/год-1) і далі утримується на високому рівні (60-50 г кислоти/м2 плівки/год-1). Ферментацію можна продовжити, підводячи під плівку свіже середовище.
При отриманні лимонної кислоти поверхневим способом одним із найважливіших факторів є повітряний режим у камерах, тобто аерація, температура і вологість.
Глибинний спосіб культивування має ряд переваг порівняно з методом поверхневого культивування. Процес ферментації здійснюють у ферментері при інтенсивній аерації, використовуючи спеціально селекціоновані штами.
Амінокислоти. Амінокислоти знаходять застосування в різних галузях народного господарства. Дуже важливою є роль амінокислот у збалансуванні білкового харчування. Найбільше виробляють таких амінокислот, як L-лізин, L-глутамінова кислота, DL-метіонін, L-аспарагінова кислота, гліцин.
Існують три основні способи отримання амінокислот: екстракція з білкових гідролізатів рослинної сировини, хімічний синтез, мікробний синтез. Суттєва перевага мікробного синтезу амінокислот перед хімічним методом полягає в отриманні певних ізомерів (L-форм).
Мікроорганізм здатні накопичувати амінокислоти у процесі росту. Проте продуцентів, які здійснюють економічно вигідний синтез амінокислот, не так багато. Як правило, використовують ауксотрофні мутанти, які завдяки відсутності ряду ферментних систем, здатні до над- синтезу одного з метаболітів. Амінокислоти максимально накопичуються в середовищі наприкінці експоненційної фази росту культури.
Найпоширенішими продуцентами амінокислот вважають грампозитивні, неспороутворювальні палички родів Corinebacterium, Micrococcus, Arthrobacter, Brevibacterium.
Вітаміни, провітаміни, коферменти. Шляхом мікробного синтезу отримують вітаміни В12, В2, С, ергостерин. Мікробний синтез вітамінів має велике практичне значення, незважаючи на переваги хімічних методів.
Вітамін В12 використовують у медицині та тваринництві. Як продуценти застосовують різні мікроорганізми: Propionibacterium reudenreichii, термофільні метаногенні бактерії, актиноміцети.
Рибофлавін (В2). Продуцентами рибофлавіну у природі є вищі рослини, дріжджі, міцеліальні гриби, бактерії. Більшість мікроорганізмів утворює вільний рибофлавін та його коферментні форми - ФМН та ФАД. Найбільш активні продуценти - цвільові гриби Aspergillus niger, Eremotecium ashbyii.
Ергостерин - вихідний продукт виробництва жиророзчинного вітаміну D2. Джерелом ергостерину є фітопланктон, бурі та зелені водорості, дріжджі та цвілеві гриби. У дріжджів ергостерин становить 6090 % від інших стеринів. Вміст його у клітині може сягати від 0,2 до 10 % від сухої біомаси дріжджів.
У промисловості ергостерин отримують, використовуючи дріжджі Saccharomyces serevisiae, Saccharomyces carlsbergensis, гриби родів Aspergillus, Penicillium. Культивування проводять при високій температурі та інтенсивній аерації в середовищі, яке містить надлишок вуглецю порівняно з азотом. Отримують як очищений кристалічний вітамін D2, так і концентрат, який являє собою висушену та опромінену біомасу дріжджів. При дії рентгенівського опромінення рівень ергостерину збільшується у 2-3 рази за рахунок стимуляції ліпідного обміну.
Вітамін С використовується в медицині, для стабілізації вина, пива, масла, морозива та інших продуктів. Із семи послідовних стадій синтезу вітаміну лише одна здійснюється за допомогою бактерій Gluconobacter oxydans - трансформація Д-сорбіту в L-сорбозу. Бактерії вирощують на середовищах з 20 % сорбіту та дріжджовим екстрактом. При глибинному культивуванні вихід сорбози становить 98 % за 20-40 год. Після завершення циклу сорбозу вилучають хімічним шляхом.