ИММУНОЛОГИЯ - Ройт А. - Мир 2000
Глава 22. Вторичная иммунологическая недостаточность
СПИД
Возбудителем СПИДа является вирус иммунодефицита человека (ВИЧ), который передается половым путем, при гемотрансфузии или при введении препаратов крови, а также от больной матери ребенку в перинатальный период. Существуют два основных варианта вируса - ВИЧ-1 и ВИЧ-2, причем последний эндемичен для Западной Африки и, по-видимому, менее патогенен.
Более 80% инфицированных ВИЧ людей проживают в развивающихся странах, где в 80% случаев вирус передается половым путем (70% гетеро- и 10% гомосексуальных контактов). По прогнозам Всемирной организации здравоохранения (ВОЗ), к 2000 году общее число ВИЧ-инфицированных лиц на планете составит 30 млн. (из которых 99% будут жителями развивающихся стран), а число погибших от СПИДа достигнет 2 млн. в год.
Вирус
ВИЧ относится к вирусам, содержащим двухцепочечную РНК; диаметр его частицы составляет 100-120 нм (рис. 22.4). Основные гены ВИЧ — это gag (кодирует сердцевинный белок), pol (ген полимеразы/обратной транскриптазы) и env (кодирует белок оболочки вируса). Кроме того, несколько дополнительных генов служат для регуляции синтеза вирусных белков. Рецептором для ВИЧ является антиген CD4, который присутствует на Т-лимфоцитах CD4+и клетках моноцитарно-макрофагального ряда. С молекулой CD4 связывается вирусный гликопротеин gp120; в процессах последующего слияния вируса с клеткой и его интернализации, опосредуемых гликопротеином gp41, участвуют хемокиновые корецепторы.
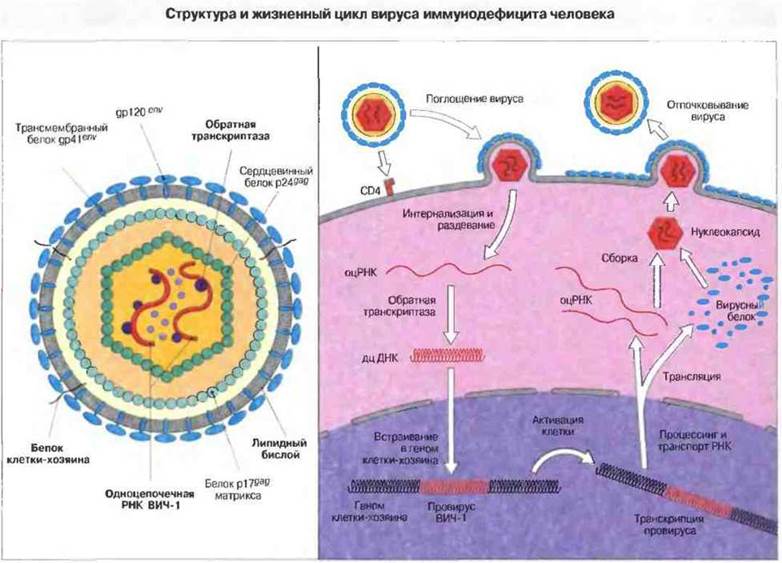
Рис. 22.4. После раздевания вириона вирусная одноцепочечная РНК (оцРНК) транскрибируется с участием обратной транскриптазы в двухцепочечную ДНК (дцДНК). При участии вирусного фермента интегразы эта ДНК встраивается в геном клетки-хозяина как провирус ВИЧ. Активация клетки ведет к транскрипции ДНК с образованием вирусной мРНК и последующему синтезу белков, формирующих структуру вирусной частицы. После сборки вирусные частицы высвобождаются путем отпочковывания от клетки; затем происходит дальнейшее формирование их структуры (оно включает расщепление крупного сердцевинного белка-предшественника на небольшие белковые компоненты при участии вирусных протеаз) с образованием зрелых вирионов.
Расстройства иммунных функций
Спектр этих расстройств весьма широк и включает нарушения активации клеток иммунной системы в результате прямого действия ВИЧ, а также истощение и дисфункцию субпопуляции Т-клеток CD4+, развивающиеся со временем и составляющие основную причину возникновения иммунодефицита. Каким образом вирус убивает клетки-мишени, еще не совсем ясно. Для объяснения предложены разные механизмы, в частности накопление РНК и неинтегрированной ДНК в цитоплазме и внутриклеточное связывание CD4 с gp120. Инфицированные клетки могут соединяться с неинфицированными в результате взаимодействия gp120-CD4, при этом образуются гигантские многоядерные клетки и синцитий. Связываясь с поверхностью неинфицированных Т-клеток CD4+, gp120 делает их также чувствительными к антителозависимой клеточной цитотоксической активности (АЗКЦ); инфицированные клетки могут уничтожаться gp120-специфическими цитотоксическими Т-лимфоцитами. Белки ВИЧ способны действовать как суперантигены, вызывая выраженную экспансию пула иммунокомлетентных клеток с его последующим истощением. Кроме того, ВИЧ может индуцировать апоптоз Т-клеток и вызывать повреждение клеточной мембраны и лизис при отпочковывании вирусных частиц с поверхности клетки.
Нарушения иммунных функций под влиянием ВИЧ состоят в истощении субпопуляции Т-клеток CD4+и угнетении их реакций на антигены, митогены, аллоантигены и антитела анти - CD3 с параллельным снижением продукции ИЛ-2 и другими изменениями продукции цитокинов. В результате этих нарушений утрачиваются способность цитотоксических Т-клеток к ВИЧ-специфичному ответу и некоторые антигенпрезентирующие клеточные функции. При этом возрастает число активированных и ареактивных Т-клеток CD8+, повышается содержание β2-микроглобулина и неоптерина в сыворотке, происходит поликлональная В-клеточная активация с появлением В-лимфоцитов, невосприимчивых к действию Т-независимых В-клеточных активаторов, возрастает образование аутоантител и иммунных комплексов.
Результаты модельных опытов по определению реакции вируса и Т-клеток CD4+, содержащихся в плазме крови, на антивирусную терапию показали, что среднее время полужизни вируса и инфицированных клеток в циркуляции составляет менее 2 сут. Ежедневно из инфицированных клеток высвобождаются 109-1010 вирусных частиц и сходное число новых клеток подвергается инфицированию и погибает.
Клиническое течение заболевания
Первичная ВИЧ-инфекция может сопровождаться кратковременными расстройствами, напоминающими инфекционный мононуклеоз, с недомоганием, мышечными болями, припухлостью лимфатических узлов, фарингитом и сыпью. Происходит временное уменьшение числа периферических Т-клеток CD4+, повышение содержания Т-лимфоцитов CD8+и содержания ВИЧ в плазме крови (рис. 22.5). С помощью иммуноферментного метола в период от 2 до 6 нед после инфицирования удается обнаружить антитела к сердцевинному и оболочечному белкам вируса. Хроническая инфекция не сопровождается клиническими проявлениями, однако примерно 33% больных имеют увеличенные лимфатические узлы. У половины инфицированных в течение 9-10 лет развивается СПИД.
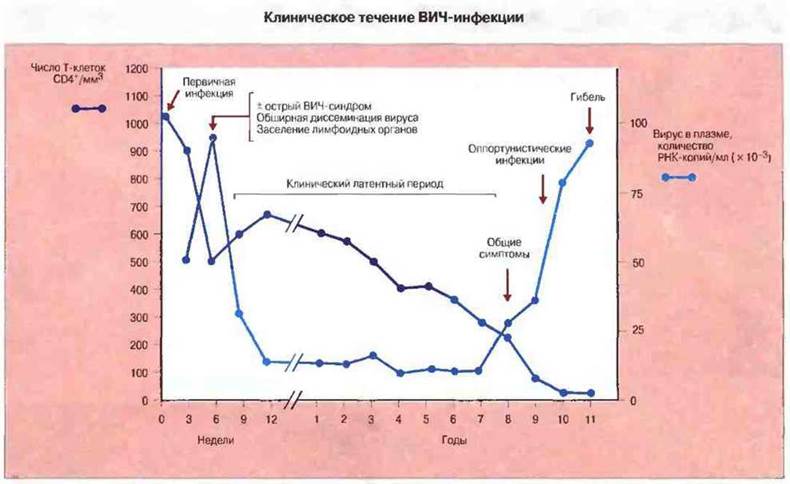
Рис. 22.5. Типичное течение ВИЧ-инфекции. (Рисунок любезно предоставлен д-ром A.S. Fauci: из работы Pantaleo G., Graziosic. 1993. N. Engl. J. Med. 328: 327-35, изменено с разрешения.)
На поздних стадиях заболевания отмечаются неспецифические симптомы общего характера: лихорадка, ночная потливость, диарея и потеря веса наряду с «минорными» явлениями, главным образом со стороны слизистых оболочек и кожи; например, у больных может возникать кандидоз ротовой полости (молочница), опоясывающий лишай, герпетические поражения (вирус простого герпеса) аноректальной области и различные кожные инфекции. Часто эти расстройства служат предвестниками развития тяжелых оппортунистических инфекций и опухолей, которое и представляет собой собственно СПИД. К этому времени число Т-клеток СD4+ обычно становится меньше 200/мкл (рис. 22.5).
Наиболее часто встречающимся видом новообразований при СПИДе является саркома Капоши многоочаговая опухоль эндотелиального происхождения (рис. 22.6). Широко распространяясь, опухоль поражает кожу, слизистые оболочки, внутренние органы (кишечник и легкие) и лимфатические узлы. С развитием опухоли ассоциирована инфекция, возбудителем которой является вирус герпеса человека 8, HHV8 (human herpes virus 8) Описано также возникновение у больных СПИДом В-клеточных лимфом, поражающих головной мозг, кишечник и костный мозг.
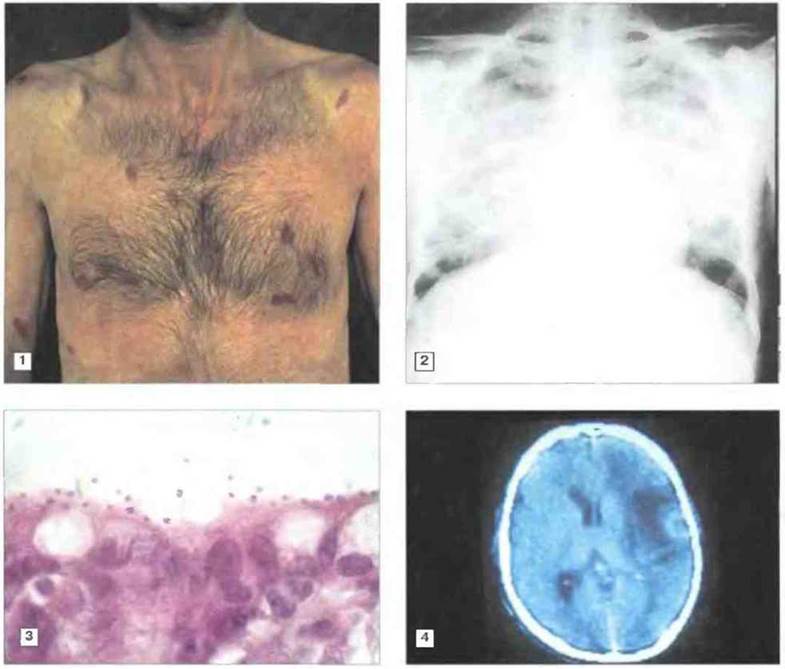
Рис. 22.6. Патологические проявления, характерные для СПИДа. 1. Множественные очаги саркомы Капоши на поверхности груди и живота. 2. Рентгенограмма грудной клетки больного пневмонией, вызванной Pneumocystis carinii. Видно двустороннее интерстициальное затемнение. 3. Небольшой биоптат кишечника больного диареей, вызванной Cryptosporidium. На поверхности слизистой оболочки видны промежуточные формы криптоспоридий (небольшие розовые пятна). 4. Сканограмма, полученная с помощью компьютерной томографии головы больного церебральным токсоплазмозом. Клинически расстройство проявлялось в судорогах и слабости левых руки и ноги. Инъекция контрастирующего вещества выявила в правом полушарии кольцевидный очаг поражения с отеком вокруг него (темная зона).
Оппортунистические инфекции развиваются большей частью в результате реактивации микробов, присутствующих в организме в латентном состоянии, и в некоторых случаях вследствие инфицирования микроорганизмами из внешней среды, с которыми человек постоянно контактирует. Эти инфекции трудно диагностировать, и лечение часто лишь подавляет их проявления, не приводя к полному выздоровлению. Для них характерно возникновение рецидивов, что делает необходимым проведение постоянной супрессивной или поддерживающей терапии; при атом применяются лекарственные препараты, опасные из-за своих побочных эффектов.
Главными объектами поражения при СПИДе являются три системы; дыхательная, пищеварительная и нервная. Обычная оппортунистическая инфекция при СПИДе — пневмония, и чаше всего ее вызывает Pneumocystis carinii (рис. 22.6). Однако возбудителями заболеваний легких могут быть и другие бактерии, включая Mycobacterium tuberculosis, а также фибы. Причиной расстройства глотания обычно является кандидат (молочница), и, кроме того, возможны язвенные поражения пищевода, вызываемые цитомегаловирусом. У больных с потерей веса, страдающих диареей, чаше всего могут быть выделены патогенные простейшие (Cryptosporidium и микроспориями) (рис. 22.6), однако обнаруживаются также и энтеробактерии — Salmonella и Campylobacter.
Неврологические осложнения СПИДа обусловлены либо прямым действием на нервную систему ВИЧ и возбудителей оппортунистических инфекций, либо развитием лимфомы. Связанная со СПИДом деменция, первоначально диагностируемая у 10-20% больных с другими проявлениями СПИДа, теперь возникает реже благодаря применению более эффективных методов антивирусной терапии. Встречаются также заболевания спинного мозга и периферических нервов. Токсоплазмоз (протозойная инфекция) вызывает образование кист в головном мозге и расстройства неврологических функций (рис. 22.6). Гриб Cryptococcus neoformans может вызывать менингит. Ряд поражений нервной системы возникает под влиянием других инфекционных агентов: цитомегаловирус вызывает воспаление сетчатки, головного и спинного мозга и спинномозговых корешков, вирус полиомы (JC-вирус), который инфицирует олигодендроциты в головном мозге, — возникновение быстро прогрессирующего летального демиелинизирующего заболевания — лейкоэнцефалопатии.
Противовирусная терапия
В 1987 г. для лечения ВИЧ-инфекции был предложен зидовудин (AZT), первый из полученных нуклеозидных аналогов - ингибиторов обратной транскриптазы (НИОТ). С того времени были достигнуты значительные успехи в разработке и применении других НИОТ, а также ненуклеозидных ингибиторов обратной транскриптазы (ННИОТ) и ингибиторов протеаз (см. рис. 22.4).
Монотерапия зидовудином на поздних стадиях заболевания снижает смертность в ближайшие сроки после начала лечения и задерживает прогрессирование болезни. Будучи применен в ранний период инфекции, этот препарат дает слабый и преходящий клинический эффект и не повышает выживаемость. В связи с этим были применены комбинации двух или большего числа терапевтических агентов в расчете на их аддитивный или синергичный эффект, а также с целью задержать развитие лекарственной резистентности; такую задержку может обеспечивать снижение частоты мутаций RT-гена или же возникновение обратных мутаций, которые могут приводить к утрате резистентности или делать вирус менее компетентным. Комбинация двух НИОТ снижала скорость прогрессирования СПИДа и смертность от него примерно на 40% в интервале от 1 до 3 лет по сравнению с монотерапией. Оказалось также клинически эффективным сочетанное применение НИОТ и ингибиторов протеаз. Использование других комбинаций, в состав которых входят и НИОТ, и ННИОТ, и ингибиторы протеаз, дает многообещающий противовирусный эффект вместе с резким кратковременным увеличением числа Т-клеток CD4+- дополнительный фактор, улучшающий клиническое течение заболевания.
Остается неясным вопрос об оптимальном сроке начала терапии, однако большинство врачей считает, что лечение нужно начинать тогда, когда при повторном определении содержания CD4+-клеток их число оказывается сниженным до 200-400/мл, а также во всех случаях, когда у больных возникают симптомы заболевания. Ориентиром может также быть уровень вирусной РНК в сыворотке крови. Необходимо указать, что даже монотераиин относится к дорогостоящим способам лечения, и это создает трудности для лечения больных СПИДом в развивающихся странах. Поскольку в настоящее время не имеется средств, излечивающих СПИД полностью, как нет и вакцины против этой инфекции, главным оружием в борьбе со СПИДом может быть профилактика, т. е. пропаганда здорового образа жизни и контроль за распространением инфекции.
Вопросы для размышления
■ Почему антимитотические лекарственные препараты должны обладать иммуносупрессивными свойствами?
■ Какой эффект, по вашему мнению, должно давать комбинированное применение циклоспорина и рапамицина: неаддитивный, аддитивный или синергичный?
■ Представьте, что вы являетесь главой округа в одной из развивающихся стран с ограниченными бюджетными средствами. Какие мероприятия по снижению заболеваемости инфекционнымиболезнями вы стали бы финансировать в первую очередь?
■ Каковы последствия быстрого мутирования РНК-вирусов, например ВИЧ?
■ Предположим, что можно трансфицировать клетки антисмысловым нуклеозидом, включающимся в мРНК регуляторных белков ВИЧ. Какие клетки вы избрали бы в качестве мишенитрансфекции, чтобы получить максимальный терапевтический эффект для данного больного?
■ Какие элементы питания, назначаемые для приема в умеренно избыточном количестве, могут усиливать иммунитет?
■ Каковы наиболее характерные изменения иммунной системы при белково-калорической недостаточности?
■ Представьте, что вы лечите тяжелобольных и стариков; какая диета улучшит их состояние и снизит тяжесть инфекции?
ДОПОЛНИТЕЛЬНАЯ ЛИТЕРАТУРА
Chandra R.K. (ed). 1992. Nutrition and Immunology. St John's NF, Canada ARTS Biomedical.
Chandra R.K. 1996 Nutrition, immunity and infection.
Proc. Natl. Acad. Sci USA 93: 14304-307.
Chandra R.K. 1997. Graying of the immune system,
Can nutrient supplements improve immunity in the elderly? JAMA 277: 1898-99.
Gershwin M.E., Beach R.S. Hurley L.S. 1984. Nutrition and Immunity. New York: Academic Press.