ИММУНОЛОГИЯ - Ройт А. - Мир 2000
Глава 25. Гиперчувствительность - тип III
ОТЛОЖЕНИЕ КОМПЛЕКСОВ В ТКАНЯХ
Иммунные комплексы могут длительное время оставаться в крови. Однако сама по себе их персистенции здесь обычно неопасна; неприятности начинаются лишь при отложении комплексов в тканях.
В связи с этим возникают два вопроса:
✵ с чем связано отложение комплексов и
✵ почему комплексы при разных заболеваниях обнаруживают сродство к разным тканям?
Наиболее важным фактором отложения иммунных комплексов в тканях служит, вероятно, увеличение сосудистой проницаемости
Эксперименты на животных показывают, что такие инертные вещества, как коллоидный уголь, после введения вазоактивных соединений (например, гистамина или серотонина) откладываются в стенках сосудов. После введения агентов, вызывающих выброс вазоактивных аминов (включая гистамин) из тучных клеток, аналогичным образом откладываются и циркулирующие иммунные комплексы. Предварительное введение антигистаминных препаратов блокирует этот эффект.
При исследовании экспериментальной болезни иммунных комплексов у кроликов установлено, что длительное введение антагонистов вазоактивных аминов, таких как хлорфенирамин и метисергид, значительно уменьшает отложение иммунных комплексов (рис. 25.17). Еще большее значение (для целей профилактики) имеет тот факт, что у молодых мышей NZB/NZW, которым вводили метисергид, повреждения почек были выражены слабее, чем у контрольных животных (рис. 25.18).
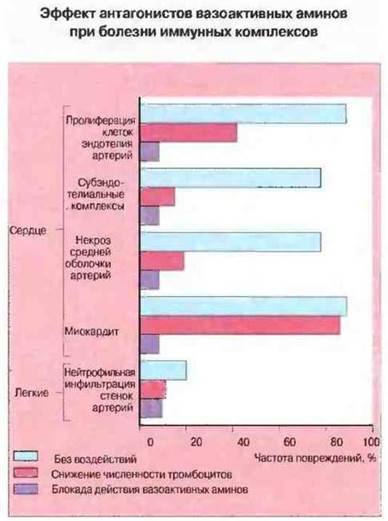
Рис. 25.17. У кроликов вызывали сывороточную болезнь однократным введением бычьего сывороточного альбумина. Опыты проводили на трех группах животных: 1) контрольных, 2) со сниженным количеством тромбоцитов и 3) получавших препараты, блокирующие действие вазоактивных аминов. Регистрировали частоту характерных для сывороточной болезни изменений в сердце и легких. Введение лекарственных средств значительно ослабляло проявления болезни за счет снижения сосудистой проницаемости и уменьшения благодаря этому отложения иммунных комплексов.
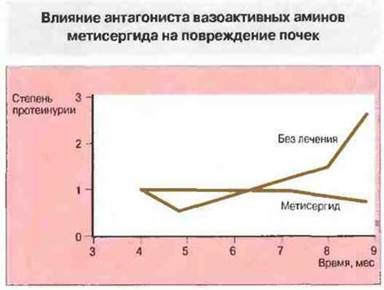
Рис. 25.18. Повреждение почек (оцениваемое по степени протеинурии) регистрировали у мышей NZB/NZW в течение 5 мес. У животных, не получавших лечения, развивалась тяжелая протеинурия, тогда как у мышей, получавших метисергид, этого не наблюдалось. Метисергид блокирует образование вазоактивного амина 5-гидрокситриптамина (серотонина) и тем самым тормозит различные воспалительные реакции, например отложение комплексов, нейтрофильную инфильтрацию сосудистых стенок и пролиферацию клеток эндотелия, вызывающие патологию почечных клубочков.
Повышение сосудистой проницаемости может иметь многочисленные последствия, значение которых зависит от характера заболевания и вида животных. Это затрудняет интерпретацию отдельных данных, получаемых на экспериментальных моделях. В целом, однако, и комплемент, и тучные клетки, и базофилы, и тромбоциты могут считаться потенциальными продуцентами вазоактивных аминов.
Отложение иммунных комплексов наиболее вероятно в тех структурах, где имеется высокое артериальное давление и турбулентный ток крови
Многие макромолекулы откладываются в капиллярах почечных клубочков, где кровяное давление примерно в четыре раза выше, чем в других капиллярах (рис. 25.19). Если у кроликов с помощью частичного сужения почечной артерии или перевязки мочеточника снизить давление в клубочках, отложение макромолекул также уменьшается. Если же путем индукции экспериментальной гипертензии повысить давление в клубочках, то увеличивается и отложение в них иммунных комплексов, как это показано на модели сывороточной болезни. Наиболее тяжелые повреждения возникают в тех участках, где имеется турбулентный ток крови, например в местах изгиба или бифуркации артерий, а также в таких «сосудистых фильтрах», как хориоидное сплетение и цилиарное тело глаза.
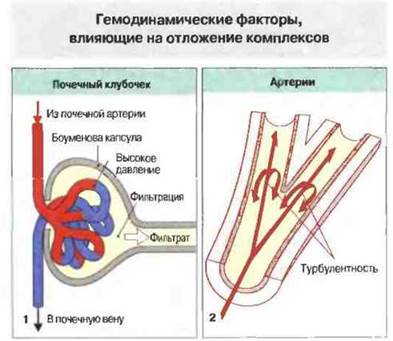
Рис. 25.19. К факторам, влияющим на отложение комплексов, относятся фильтрация и высокое давление крови; оба эти фактора действуют при образовании ультрафильтрата в почечных клубочках (1). Турбулентный ток крови в местах изгиба или бифуркации артерий (2) также способствует отложению иммунных комплексов.
Отложение комплексов в определенных тканях может быть связано с аффинностью к ним антигенов
Местным высоким давлением крови можно объяснить более частое отложение иммунных комплексов в определенных органах, но это не объясняет, почему при разных заболеваниях комплексы откладываются в разных органах. При СКВ основным органом-мишенью являются почки, тогда как при ревматоидном артрите, несмотря на наличие комплексов в крови, почки обычно не страдают, а основной мишенью оказываются суставы.
Возможно, органная специфичность поражения определяется содержащимся в комплексе антигеном, причем существует экспериментальная модель, убедительно подтверждающая такое предположение. Введение мышам эндотоксина приводит к повреждению клеток и высвобождению ДНК, которая связывается с базальной мембраной капилляров интактных почечных клубочков. В результате происходит поликлональная активация В-клеток и образуются антитела к ДНК, которые взаимодействуют с ДНК, фиксированной в ткани, вызывая местное формирование иммунных комплексов (рис. 25.20). Продукция ревматоидного фактора — IgM-антител к IgG - создаст возможность дальнейшего образования иммунных комплексов in situ. Не исключено, что будут найдены антигены со сродством к специфическим органам и при других заболеваниях.
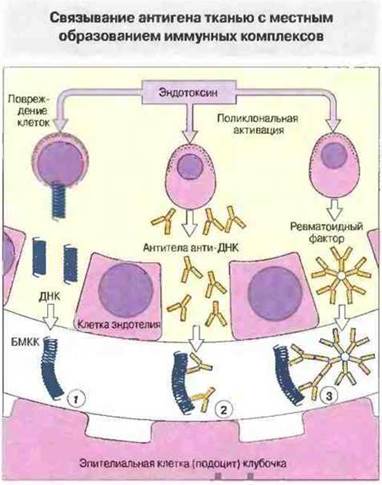
Рис. 25.20. Введенный мышам эндотоксин увеличивает сосудистую проницаемость и повреждает клетки, приводя к высвобождению ДНК, которая затем откладывается (1) на коллагене базальной мембраны клубочкового капилляра (БМКК). Эндотоксин может вызывать также поликлональную активацию В-клеток, часть которых продуцирует аутоантитела, такие как анти-ДНК и анти-IgG (последние известны как ревматоидные факторы, РФ). Антитела анти-ДНК связываются с отложениями ДНК, образуя местные иммунные комплексы (2). РФ обладают низкой аффинностью к мономерному IgG, но с высокой авидностью связываются с уже образовавшимся комплексом ДНК/анти-ДНК (3). Таким образом, in situ происходит дальнейшее формирование иммунного комплекса.
Важное значение в ряде случаев может иметь заряд антигена и антитела. Например, положительно заряженные антигены и антитела должны с большей вероятностью откладываться на отрицательно заряженной базальной мембране клубочков. На судьбу комплексов, содержащих гликопротеиновые антигены, влияет и степень их гликозилирования, поскольку некоторые механизмы клиренса (например, с участием маннан-связывающего белка) активируются при взаимодействии с молекулами сахаров.
При ряде заболеваний в органе-мишени образуются и антитела, и антигены. Это наиболее выражено при ревматоидном артрите — ревматоидный фактор IgG анти-IgG продуцируется в этом случае плазматическими клетками синовиальной оболочки; затем эти антитела взаимодействуют друг с другом (аутоассоциация), вызывая тем самим воспалительную реакцию.
Место отложения иммунных комплексов отчасти зависит от их размеров
Примером этого служат почки. Мелкие иммунные комплексы способны проходить сквозь базальную мембрану клубочкового капилляра и достигать ее эпителиальной стороны; для крупных комплексов мембрана непроницаема и они обычно накапливаются между эндотелием и базальной мембраной, в мезангии (рис. 25.21). Размеры иммунных комплексов зависят от валентности антигена, а также от титра и аффинности антител.
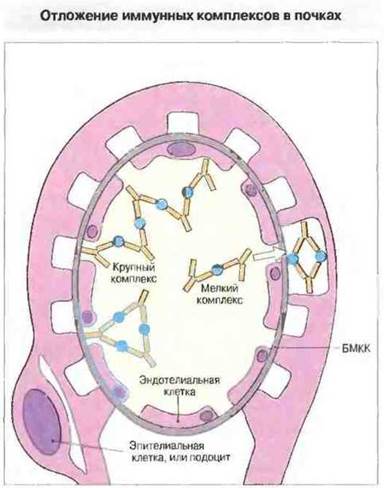
Рис. 25.21. Место отложения комплексов в почках зависит от размеров комплексов, присутствующих в крови. Крупные комплексы откладываются на базальной мембране клубочковых капилляров (БМКК), тогда как мелкие проходят через нее на эпителиальную сторону.
Отложение иммунных комплексов зависит от класса входящих в них иммуноглобулинов
Существуют заметные возрастные и половые различия между классами и подклассами антител анти-ДНК, образующихся при СКВ. Так, у мышей NZB/NZW по мере их взросления происходит переключение с преимущественного синтеза IgM на продукцию IgG2a. У самок это происходит раньше, чем у самцов, и совпадает с началом поражения почек, что свидетельствует о значении класса антител для отложения комплексов в ткани (рис. 25.22).
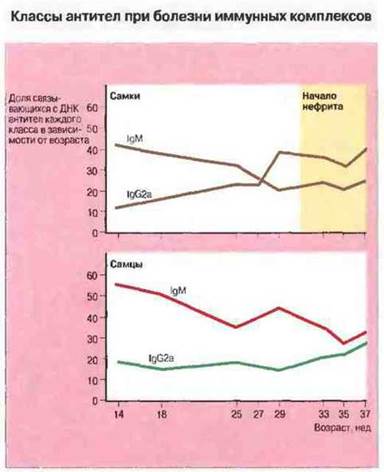
Рис. 25.22. У мышей NZB/NZW болезнь иммунных комплексов развивается спонтанно и проявляется вслед за переключением класса антител с IgM на IgG2a, которое происходит в раннем возрасте. На графике показано соотношение IgM- и IgG2а-изотипов антител анти-ДНК у самок и самцов. И переключение классов антител, и смертельное поражение почек раньше возникает у самок мышей этой линии.