ИММУНОЛОГИЯ - Ройт А. - Мир 2000
Глава 28. Аутоиммунные процессы и аутоиммунные заболевания
ПАТОГЕНЕЗ
Аутоиммунные процессы часто приводят к развитию болезни. Обнаружение аутоантител при том или ином заболевании указывает на три возможности:
✵ аутоантитела служат причиной патологического процесса;
✵ аутоантитела образуются вследствие повреждения тканей, вызванного тем или иным патологическим процессом;
✵ существует некий третий фактор, который лежит в основе и повреждения ткани, и появления аутоантител.
Иногда аутоантитела действительно появляются вследствие повреждения ткани (вторая возможность). Например, у лиц, перенесших инфаркт миокарда, в сыворотке могут присутствовать аутоантитела к антигенам сердечной мышцы. Однако простая травма, приводящая к высвобождению аутоантигенов, редко индуцирует образование аутоантител. В большинстве случаев при заболеваниях, сопровождающихся продукцией аутоантител, реализуется первая возможность, т. е. аутоиммунный процесс является причиной тканевых повреждений.
В патогенетической роли аутоиммунных процессов можно убедиться путем экспериментального моделирования
Примеры индуцированных аутоиммунных процессов. Самый простой способ проверки того, служит ли причиной заболевания аутоиммунный процесс, — это попытки воспроизведения данного заболевания у экспериментальных животных путем намеренной индукции у них аутоиммунных процессов. Для этого животным вводят аутоантигены (собственные антигены) в полном адъюванте Фрейнда (см. гл. 17), и это действительно вызывает органоспецифическое поражение некоторых органов. Введение тиреоглобулина, например, может вызвать воспалительное поражение щитовидной железы, а введение основного белка миелиновой оболочки развитие энцефаломиелита. После введения тиреоглобулина у животных не только появляются антитиреоидные аутоантитела, но и происходит инфильтрация щитовидной железы мононуклеарными клетками с нарушением структуры органа (рис. 28.8). Хотя такие изменения никоим образом нельзя считать тождественными тиреоидиту Хасимото, все же они в целом сходны с теми, какие наблюдаются при этом заболевании у человека.
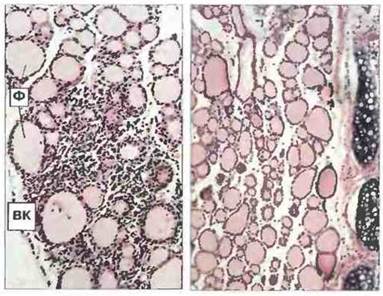
Рис. 28.8. Гистологическая картина экспериментального аутоаллергического тиреоидита. На срезе щитовидной железы животного, которому вводили тиреоглобулин (слева), видна деструкция фолликулов и выраженная инфильтрация мононуклеарными воспалительными клетками (ВК). Часть фолликулов (Ф) остается интактной, но в других имеются начальные признаки разрушения. Справа - контрольный срез, на котором видны нормальные тиреоидные фолликулы, заполненные коллоидом. Окраска гематоксилином-эозином, х 200.
Возможность экспериментальной индукции аутоиммунного заболевания зависит от линии животных. Например, подверженность крыс и мышей энцефаломиелиту в результате введения основного белка миелиновой оболочки связана с небольшим числом определенных генных локусов, главным образом в области генов МНС класса II. Аутоаллергический энцефаломиелиту животных восприимчивых линий можно вызвать также введением Т-клеток, специфичных к основному белку миелиновой оболочки. Такие Т-хелперные (Тх) клетки принадлежат к субпопуляции CD4/Tх1, причем введение реципиентам антител к CD4 непосредственно перед ожидаемым началом болезни предотвращает ее возникновение, блокируя взаимодействие CD4 на Тх-клетках с молекулами МНС класса II на антигенпрезентируюших клетках (АПК) (см. гл. 10). Результаты опытов указывают на значение реет риктированных по молекулам МНС класса II аутореактивных Тх-клеток в развитии таких заболеваний и подчеркивают важнейшую роль МНС.
Примеры спонтанных аутоиммунных процессов. Изучение спонтанных аутоиммунных заболеваний у животных позволяет получить много важных сведений. Одним из классических объектов таких исследований служат куры линии OS (рис. 28.9), у которых спонтанно появляются антитиреоидные аутоантитела, а щитовидная железа подвергается прогрессивной деструкции вследствие хронического воспаления. В сыворотке этих птиц присутствуют аутоантитела к тиреоглобулину. Кроме того, сыворотка примерно 15 % кур линии OS взаимодействует и с тканью желудка (поджелудка) здоровых кур. Эти результаты весьма напоминают полученные в аналогичном тесте с сывороткой больных пернициозной анемией, у которых присутствуют аутоантитела, реагирующие с париетальными клетками желудка.

Рис. 28.9. Куры линии OS. У кур этой линии спонтанно развивается аутоиммунный тиреоидит, напоминающий болезнь Хасимото. Такие птицы (справа) гораздо мельче контрольных кур того же возраста; кроме того, у них наблюдаются и другие симптомы гипотиреоза, такие как непереносимость холода (взъерошенные перья), кожные нарушения (длинные шелковистые перья), плохая носкость, жировые отложения под кожей и в брюшной области (отсюда и название линии - Obese strain), повышение уровня липидов в сыворотке и т. д. Все эти симптомы можно предотвратить добавлением к корму цыплят тироксина. (Фото любезно предоставлено проф. G. Wick.)
Таким образом, заболевание у кур линии OS сходно с аутоиммунным заболеванием щитовидной железы у человека не только по характеру нарушений в самой железе и появлению аутоантител к различным компонентам тиреоидной ткани, но и по сочетанию с аутоантителами к тканям желудка. Поэтому существенно важно, что на таких птицах установлена выраженная зависимость исхода заболевания от иммунологического статуса организма. Например, если вскоре после вылупления удалить у цыпленка фабрициеву сумку (где происходит созревание В-клеток), тяжесть тиреоилита значительно уменьшается. Следовательно, в патогенезе заболевания принимают участие В-клетки, которые либо продуцируют антитела, либо презентируют антигены патогенным Т-лимфоцитам. С другой стороны, удаление тимуса у цыплят приводит к более тяжелому течению тиреоилита, что свидетельствует о сдерживающей роли тимуса при данном заболевании (рис. 28.10). Парадоксально, но разрушение всей популяции Т-клеток у взрослых кур путем введения больших количеств антисыворотки к Т-клеткам полностью блокирует как продукцию аутоантител, так и поражение щитовидной железы. Таким образом, Т-клеткам при этом заболевании принадлежит, по-видимому, центральная роль в опосредовании и регуляции патологического процесса.
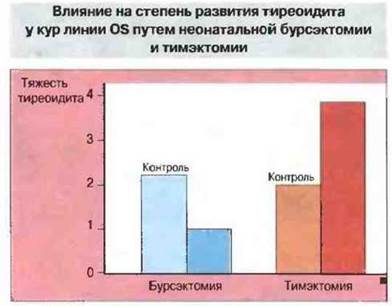
Рис. 28.10. Тяжесть тиреоидита оценивали по выраженности лимфоидной инфильтрации. Удаление фабрициевой сумки в неонатальном возрасте уменьшало тяжесть тиреоидита, что свидетельствует о важной роли антител в его патогенезе. Удаление тимуса в тот же период приводило к более тяжелому течению болезни, из чего можно сделать вывод о сдерживающей роли супрессорных Т-клеток в развитии тиреоидита.
У человека аутоантитела могут непосредственно оказывать патогенное действие
Исследования на человеке для изучения аутоиммунных заболеваний, естественно, гораздо более сложная задача, чем опыты на животных. Тем не менее уже получено множество данных, указывающих на значение аутоантител в патогенезе таких заболеваний и у человека. Рассмотрим основные примеры.
Тиреотоксикоз. Причиной ряда патологических состояний может быть действие аутоантител к гормональным рецепторам, имитирующих функцию обычных гормонов, впервые присутствие подобных антирецепторных антител было установлено при тиреотоксикозе (рис. 28.11). Поскольку антитела класса IgG у больной тиреотоксикозом матери проходят через плаценту, феномен неонатального тиреотоксикоза можно изучать как своего рода природную «модель» пассивного переноса антител. Имеются многочисленные описания случаев гиперактивности щитовидной железы у детей, родившихся от больных тиреотоксикозом матерей; через несколько недель, по мере распада полученных от матери антител, ребенок выздоравливает.
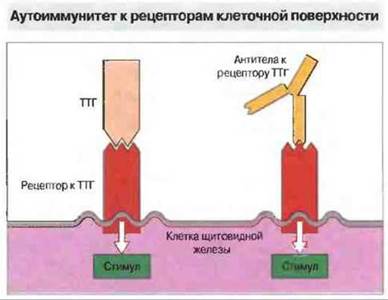
Рис. 28.11. При связывании тиреотропного гормона (ТТГ) с рецептором происходит активация клетки щитовидной железы (слева). Антитела к рецептору ТТГ, присутствующие в сыворотке больных тиреотоксикозом (болезнь Грейвса, или базедова болезнь), взаимодействуют с рецептором аналогичным образом, передавая тем самым тиреоидной клетке такой же стимул (справа), что приводит к гиперпродукции тиреоидных гормонов.
Злокачественная миастения. Аналогичный феномен отмечен у матерей, страдающих злокачественной миастенией — заболеванием, при котором антитела к рецепторам ацетилхолина попадают через плаценту в плод и вызывают временную мышечную слабость у новорожденных.
Другие рецепторные болезни. Несколько реже встречаются случаи с присутствием аутоантител к рецепторам инсулина и β-адренергическим рецепторам: антитела второго вида часто обнаруживаются у больных бронхиальной астмой. Сыворотка больных с синдромом Ламберта-Итона содержит антитела к пресинаптическим кальциевым каналам, и введение ее мышам вызывает у животных нейромышечные нарушения. При синдроме Гийена-Барре в сыворотке присутствуют аутоантитела к натриевым канатам.
Мужское бесплодие. Еще одним примером аутоиммунных заболеваний служат редкие случаи мужского бесплодия, в которых именно антитела к сперматозоидам обусловливают их склеивание в сперме головками или хвостами (рис. 28.12).
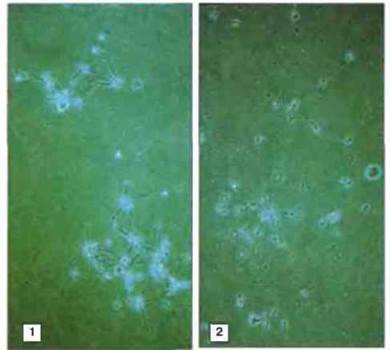
Рис. 28.12. Агглютинация сперматозоидов. Аутоантитела к сперматозоидам вызывают их склеивание головками (1) или хвостами (2).
Пернициозная анемия. При этом заболевании аутоантитела препятствуют нормальному всасыванию витамина В12. Чтобы произошло всасывание, молекула витамина В12 должна предварительно связаться с белком, носящим название внутреннего фактора; в виде комплекса с белком витамин транспортируется через слизистую оболочку стенки кишечника. Ранние исследования пассивного транспорта показали, что сыворотка больных пернициозной анемией препятствует всасыванию витамина у здоровых лиц, если поступает в желудок вместе с комплексом внутренний фактор-витамин В12. В дальнейшем было установлено, что блокируют всасывание витамина присутствующие в сыворотке антитела к внутреннему фактору. К настоящему времени известно, что у больных пернициозной анемией эти антитела секретируются в желудочную полость плазматическими клетками слизистой желудка (рис. 28.13).
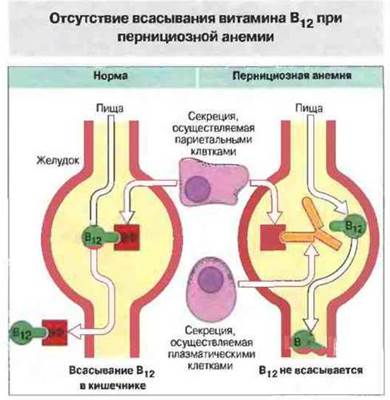
Рис. 28.13. В норме витамин В12, содержащийся в пище, всасывается в тонком кишечнике в виде комплекса с внутренним фактором (ВФ), который синтезируют париетальные клетки слизистой желудка. При пернициозной анемии местно синтезируемые аутоантитела к внутреннему фактору связываются с ним, препятствуя осуществлению его функции в качестве переносчика витамина В12.
Синдром Гудпасчера. При синдроме Гудпасчера происходит связывание антител с базальной мембраной капилляров почечных клубочков in vivo (см. рис. 25.3). Для доказательства пазогенного действия этих антител был проведен опыте их пассивным переносом. Антитела, элюированные из почки умершего больного с синдромом Гудпасчера, вводили приматам, чьи почечные антигены настолько сходны с человеческими, что введенные антитела взаимодействуют с базальной мембраной клубочковых капилляров. Обезьяны, которым вводили эти антитела, погибали от гломерулонефрита.
Заболевания крови. Появление аутоантител к эритроцитам и тромбоцитам обусловливает развитие соответственно аутоиммунной гемолитической анемии и идиопатической тромбоцитопенической пурпуры. Причиной еще одного заболевания кропи — первичного антифосфолипидного синдрома, для которого характерны рецидивирующая тромбоэмболия и предрасположенность к выкидышам, служит взаимодействие аутоантител с комплексом кардиолипин-β2-гликопротеин 1.
Патогенное действие при системных аутоиммунных заболеваниях оказывают иммунные комплексы
При СКВ причиной реакций гиперчувствительности III типа, описанных в гл. 25, служат, как установлено, иммунные комплексы, которые состоят из ДНК и антител и откладываются в почках, коже, суставах и сосудистых сплетениях. У лиц с генетическими дефектами в системе активации комплемента по классическому пути выведение иммунных комплексов из крови резко замедлено, и этим обусловлена особая предрасположенность к развитию СКВ.
Существуют и экспериментальные модели СКВ. Так, у гибридных мышей, полученных при скрещивании линий новозеландская черная и новозеландская белая, спонтанно развивается СКВ с проявлениями в виде гломерулонефрита и образования антител к ДНК. Подавление иммунных реакций у этих животных (например, введением антител к CD4) облегчает симптомы заболевания и увеличивает продолжительность жизни, что служит дополнительным доказательством причинной роли аутоиммунных процессов (рис. 28.14).

Рис. 28.14. Для мышей линии новозеландская черная (New Zeland Black, NZB) характерно спонтанное развитие аутоиммунной гемолитической анемии. У гибридов этих животных с мышами линии новозеландская белая (New Zeland White, NZW) появляются аутоантитела к ДНК и обусловленный отложением иммунных комплексов гломерулонефрит, аналогичный тому, который наблюдается у больных СКВ. Применение иммуносупрессии с использованием моноклональных антител к CD4 (маркеру Тх-клеток) значительно уменьшает тяжесть гломерулонефрита и снижает титр антител к двухцепочечной ДНК у животных 8-месячного возраста. Судя по этому, причина болезни связана с аутоиммунными процессами (поданным Wofsy et al. 1985. J. Exp. Med. 161:378.)
Эрозия хрящей и костей при ревматоидном артрите обусловлена действием макрофагов и фибробластов, стимулированных цитокинами (их продуцируют активированные Т-клетки) и иммунными комплексами, образующимися в результате сильной иммунологической реакции в синовиальной ткани. К образованию комплексов может приводить связывание между собой молекул ревматоидных факторов класса IgG, специфичных к Fcy-фра! ментам; этот процесс облегчается в случае отсутствия в обеих N-cвязанных олигосахаридных цепях Fc-фрагмента концевого остатка галактозы. Наличие агалакто-гликоформы IgG в составе иммунных комплексов может способствовать развитию воспалительных процессов, в результате того что она реагирует с маннозосвязывающим белком и ФНО.