Настольная книга учителя химии 10 класс - поурочные разработки
СПОСОБЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ АЛЬДЕГИДОВ И КЕТОНОВ - КИСЛОРОДОСОДЕРЖАЩИЕ СОЕДИНЕНИЯ
Цели урока. Обобщить знания учащихся о свойствах альдегидов и кетонов. Рассмотреть другие способы их получения. Познакомить учащихся с важнейшими представителями этих классов органических соединений и их применением.
Оборудование: растворы NaOH, НСl, формалин, ацетон, ацетат натрия, реактив Люголя; демонстрационные образцы аптечных препаратов (уротропин, кальцекс, лизоформ, формидрон), прибор для получения газов, пробирки.
I. Способы получения альдегидов и кетонов
Получение альдегидов и кетонов — это благодатный материал для повторения и закрепления знаний, поскольку большинство способов учащимся уже известны, поэтому эту часть урока лучше провести в форме беседы с элементами самостоятельной работы.
1. Окисление или дегидрирование спиртов.
Исторически первым способом получения карбонильных соединений было окисление спиртов. Учитель спрашивает: «Каково должно быть строение спирта, чтобы при его окислении образовался альдегид?». Формулировка вопроса часто ставит ребят в тупик, но либо самостоятельно, либо с помощью учителя они находят правильный ответ: спирт должен быть первичным. Соответственно, вторичные спирты окисляются до кетонов. В качестве первого задания учитель просит написать уравнение реакции окисления конкретного спирта: например, 2-метилпропанола.
Как правило, более сложными для выполнения оказываются обратные задачи. Не следует забывать их при изучении любого класса соединений.
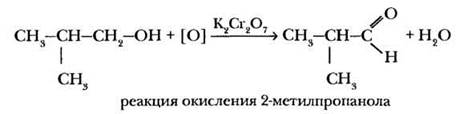
1-ый уровень. При окислении некоторого спирта образовался 2,3-диметилбутаналь. Определите формулу исходного спирта и назовите его.
Начинать рассуждение нужно с анализа правой части уравнения. Для этого в первую очередь необходимо составить формулу продукта реакции.
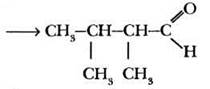
В данной реакции углеродный скелет молекулы не претерпевает никаких изменений. Окисление спирта — это отщепление двух атомов водорода. Поэтому «восстановить» исходную молекулу можно, мысленно присоединив по карбонильной группе молекулу водорода:
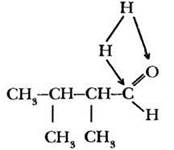
При этом не забыть разорвать π-связь, т. е. двойную связь превратить в одинарную:
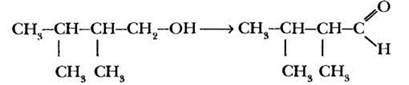
Осталось добавить в левую часть реагент, в правую — побочный продукт реакции, указать условия ее проведения (окислитель).
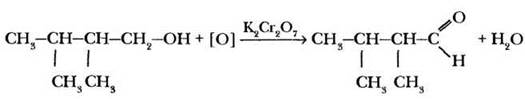
2-й уровень. 4-Метилпентанон-2 (метилизобутилкетон) используется в качестве растворителя сополимеров винилхлорида, эпоксидных смол, а также компонента типографских и художественных красок. Предложите способ получения этого кетона окислением соответствующего спирта.
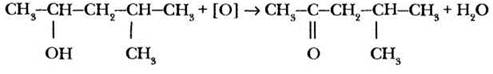
2. Гидратация алкинов.
Учащиеся вспоминают, в каких условиях ацетиленовые углеводороды присоединяют молекулу воды. В профильном классе не лишним будет упомянуть правило Марковникова для гидратации гомологов этина и правило Эльтекова. В общеобразовательном классе учитель ограничивается закреплением знания реакции гидратации ацетилена. В профильном классе задание можно усложнить.
2-й уровень. В производстве ацетилена пиролизом метана побочным продуктом реакции является пропин. Какое вещество получают гидратацией этого углеводорода в условиях реакции Кучерова?
3. Пиролиз карбоновых кислот и их солей.
Еще средневековые алхимики заметили, что при нагревании свинцового сахара (ацетата свинца (СН3СОО)2Рb) выделялась некая «квинтэссенция», названная «уксусным спиртом». В конце XVIII в. в Англии образующуюся жидкость стали применять в осветительных лампах и назвали «ламповой кислотой». Элементный состав таинственного соединения был установлен в 1831 г. Ю. Либихом и Ж. Дюма, а А. Уильямсон придал ему молекулярную формулу C3H6O. Примерно в то же время появилось название ацетон, что в переводе с латинского acetum означает уксус. Согласитесь, что не все обращали внимание на то, что слова «ацетат» и «ацетон» однокоренные. После установления структуры ацетона пиролиз кальциевых и бариевых солей карбоновых кислот стал одним из способов получения кетонов:
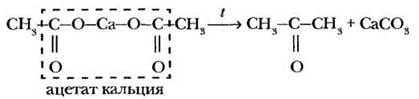
В 1856 г. итальянский химик Рафаэль Пириа обнаружил, что при нагревании смеси формиата кальция и соли какой-либо другой одноосновной кислоты в качестве основного продукта реакции получается альдегид:
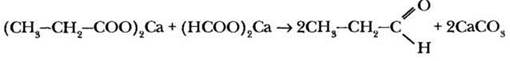
Более полувека спустя усилиями французского химика П. Сабатье данный метод был усовершенствован. Вместо солей в реакции использовались сами кислоты, пары которых пропускали над нагретым катализатором — оксидом титана (IV):
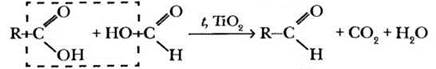
Продемонстрировать получение карбонильных соединений пиролизом солей карбоновых кислот можно на следующем опыте. В пробирку с газоотводной трубкой помещают 2 г ацетата натрия (реактив представляет собой кристаллогидрат CH3COONa · 3Н2O). Пробирку наклонно закрепляют в лапку штатива, снабжают пробкой с газоотводной трубкой, опущенной в пробирку-приемник, охлаждаемую водой со льдом (рис. 27).
Ацетат натрия в пробирке нагревают газовой горелкой. Вначале соль растворяется в собственной кристаллизационной воде, по мере ее выкипания твердеет, затем плавится и закипает. Через некоторое время в приемнике собирается некоторое количество жидкости, представляющей собой водный раствор ацетона и уксусной кислоты. В эту пробирку добавляют 2 мл воды, 0,5 мл 10%-ного раствора щелочи, 4-5 капель реактива Люголя и слегка нагревают. Проба отчетливо показывает наличие ацетона. В пробирку с твердым остатком после нагревания (дождаться полного охлаждения!) добавляют соляную кислоту. Интенсивное вспенивание указывает на образование в ней карбоната натрия.
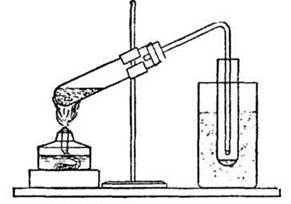
Рис. 27. Установка для демонстрации пиролиза ацетата натрия
II. Отдельные представители альдегидов и кетонов
Формальдегид. В настоящее время метаналь получают каталитическим дегидрированием метанола или окислением метана.
В учебнике упоминается очень интересное соединение — уротропин. Впервые оно было получено А. М. Бутлеровым в 50-х гг. XIX в. при действии на формальдегид аммиаком. Молекулярная формула вещества (CHS)6N4 определила его химическое название — гексаметилен-тетрамин. Структура вещества здесь приводится только для учителя:
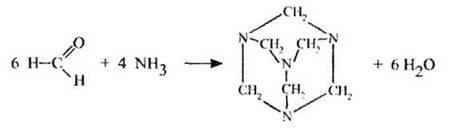
При нагревании в присутствии кислот уротропин вновь разлагается на аммиак и формальдегид. Это его свойство позволяет использовать уротропин в медицине в качестве антисептического средства. В организме человека он медленно гидролизуется, выделяющийся формальдегид уничтожает болезнетворные микроорганизмы. На том же свойстве основано применение препарата кальцекс, представляющего собой комплекс уротропина с хлоридом кальция.
Большое количество формальдегида используется для производства феноло-формальдегидных смол. Их смешивают с различными наполнителями и изготавливают пластмассы, называемые фенопластами. При растворении фенолоформальдегидных смол в ацетоне или спирте получают лаки.
При взаимодействии формальдегида с карбамидом (мочевиной) (NH2)2CO получают карбамидную смолу, а из нее — аминопласты. Из этой пластмассы изготавливают электротехнические изделия (выключатели, розетки), материалы для отделки мебели и интерьеров, древесно-стружечные плиты, искусственный мрамор, тепло- и звукоизоляционные пористые материалы.
Большое количество формальдегида используется в органическом синтезе для производства лекарственных веществ, красителей.
Широко применяется 40%-ный водный раствор формальдегида — формалин. Его использование связано со способностью свертывать белок. Так, например, в кожевенном производстве в результате дубильного действия формалина кожа твердеет и не подвергается гниению. На том же свойстве основано применение формалина для хранения биологических препаратов. Формалин используется для дезинфекции и протравливания семян.
Ацетальдегид. Основным способом получения уксусного альдегида в настоящее время является каталитическое окисление этилена, которое упоминалось при изучении алкенов. Катализатором процесса служит смесь хлоридов меди (II) и палладия (II).
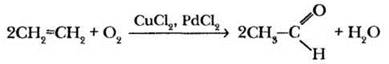
Уксусный альдегид находит широкое применение в органическом синтезе, в частности в производстве уксусной кислоты, полимерных материалов.
Акролеин. Важнейшим непредельным альдегидом является пропеналь или акролеин. В настоящее время его получают каталитическим окислением пропена кислородом воздуха в присутствии соединений висмута.
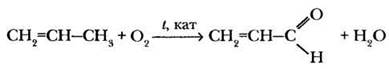
Акролеин, как непредельное соединение, сочетает свойства алкена и альдегида. Он вступает в реакции конденсации по карбонильной группе, а также легко полимеризуется по двойной связи. Первое свойство используется в органическом синтезе для получения гетероциклических соединений, многие из которых используются для получения лекарственных веществ, второе — при получении сополимеров акролеина с другими мономерами. Подобно формальдегиду, акролеин обладает дубильным действием.
Бензальдегид. Первым представителем гомологического ряда ароматических альдегидов является бензойный альдегид или бензальдегид. Это вещество содержится в природе во многих эфирных маслах, придавая им запах горького миндаля. Это свойство и обусловливает применение синтетического бензальдегида в пищевой промышленности и парфюмерии.
В промышленности бензальдегид получают каталитическим окислением толуола или взаимодействием бензола с оксидом углерода (П) в присутствии катализатора Фриделя-Крафтса.
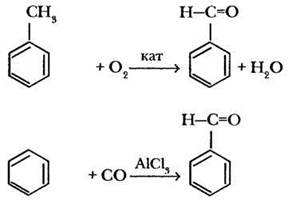
Для преподавателей, предпочитающих тестирование иным формам контроля и проверки знаний, предлагаем задания к данному уроку именно в такой форме.
1-й уровень
1. Общая формула предельных альдегидов
![]()
2. Альдегиды получают окислением спиртов
а) первичны.
б) вторичны.
в) третичных
г) непредельных
3. Для получения уксусного альдегида по реакции Кучерова следует взять
а) бутин-1
б) бутин-2
в) пропин
г) этин
4. Формальдегид нельзя получить
а) каталитическим дегидрированием метанола
б) дегидратацией метанола
в) окислением метанола
г) каталитическим окислением метана
5. К непредельным альдегидам относится
а) бензальдеги.
б) ацетальдегид
в) акролеи.
г) формальдегид
6. Тривиальное название альдегида с неразветвленной цепочкой из семи углеродных атомов — энантовый альдегид. Его международное название
а) гексаналь
б) гептаналь;
в) октаналь;
г) пентаналь
7. Формалин — это
а) иное название формальдегида
б) водный раствор формальдегида
в) продукт окисления формальдегида
г) продукт восстановления формальдегида
2-й уровень
1. Бутанон-2 можно получить
а) окислением бутанола-1
б) восстановлением бутаналя
в) дегидратацией бутанола-2
г) окислением бутанола-2
2. Один и тот же продукт получается гидратацией
а) ацетилена и этилена
б) бутина-1 и бутина-2
в) гексина-1 и гексина-2
г) пропина и бутина-2
3. Синтез изомасляного альдегида осуществляют окислением
а) бутанола-.
б) бутанола-2
в) 2-метилпропанола-.
г) 2-метил бутанола-1
4. Нагреванием смеси ацетата и формиата кальция можно получить
а) метаналь
б) этаналь
в) пропаналь
г) бутаналь
5. Отличить акролеин от пропионового альдегида можно с помощью
а) бромной воды
б) аммиачного раствора оксида серебра
в) аммиачного раствора гидроксида меди (II)
г) нагретой медной проволоки
6. Межклассовыми изомерами являются
а) этаналь и пропанон-.
б) пропанол-1 и пропаналь
в) пропеналь и пропанал.
г) бутен-3-ол-1 и бутаналь
7. Кротоновой конденсацией бензальдегида с ацетальдегидом получают коричный альдегид — вещество с запахом корицы, используемое в парфюмерии и пищевой промышленности. Его формула