Универсальные поурочные разработки по Физике 8 класс к учебнику А. В. Перышкина
Решение задач - Урок 4 - Изменение агрегатных состояний вещества
Цели: закрепить знания учащихся по теме «Изменение агрегатных состояний вещества»; сформировать навыки расчета количества теплоты при изменении агрегатного Состояния вещества и сгорании топлива.
Ход урока
I. Проверка знаний
Первые 10-15 минут урока можно отвести на письменную проверочную работу по теме «Теплота сгорания топлива». Учитель заранее готовит карточки с разноуровневыми заданиями.
Уровень 1
1. Какая физическая величина показывает, сколько энергии выделяется при сжигании 1 кг топлива? Какой буквой ее обозначают?
2. В каком случае можно получить большее количество теплоты: сжигая 1 кг торфа или 1 кг антрацита?
Уровень 2
1. Какая масса каменного угля была сожжена в печи, если при этом выделилось 60 МДж теплоты?
2. Сколько энергии выделится при полном сгорании керосина объемом 5 л?
Уровень 3
1. Удельная теплота сгорания каменного угля примерно в два раза больше, чем удельная теплота сгорания торфа. Что это значит?
2. На сколько градусов Цельсия нагреются 3 кг воды, если вся теплота, выделившаяся при полном сгорании 10 г спирта, пошла на ее нагревание?
3. Почему рачительный хозяин предпочитает покупать березовые дрова, а не осиновые? Цена дров одинаковая.
Уровень 4
1. На спиртовке нагрели 175 г воды от 15 °С до 75 °С. Начальная масса спиртовки со спиртом была равна 163 г, а по окончании нагревания - 157 г. Найдите КПД нагревательной установки.
2. Каково отношение масс спирта и бензина в смеси, если удельная теплота сгорания этой смеси 40 МДж/кг?
II. Решение задач
Далее весь урок должен быть полностью посвящен подготовке к контрольной работе. Так как определенный тип задач на расчет количества теплоты, выделяемого при сгорании топлива, был отработан недостаточно полно, это необходимо учесть.
Структура урока должна быть такой, чтобы ученики могли в полной мере представить полный набор задач по данному разделу. Очень важно при этом сформировать целостное восприятие изученной темы.
Несколько типичных по теме задач следует решить у доски.
Задача 1
Определите, какое количество теплоты необходимо для превращения 200 г льда при температуре -10 °С в воду с температурой 20 °С.
Дано:

Решение:
По таблицам находим значения сл, св, λ, tпл.
Общее количество теплоты состоит из трех частей: Q = Q1 + Q2 + Q3, где
1. ![]() - количество теплоты для нагревания льда до температуры плавления.
- количество теплоты для нагревания льда до температуры плавления.
2. ![]() - количество теплоты, которое идет на плавление льда.
- количество теплоты, которое идет на плавление льда.
3. ![]() - количество теплоты, которое идет на нагревание воды.
- количество теплоты, которое идет на нагревание воды.
Тогда: ![]()
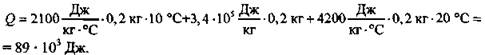
(Ответ: Q = 89 · 103 Дж.)
Задача 2
В воду массой 400 г и температурой 10 °С впустили 10 г водяного пара с температурой 100 °С. Определите, какая температура установится в сосуде.
Дано:
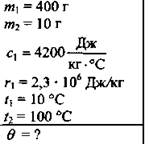
Решение:
В основе решения задачи лежит уравнение теплового баланса: Qотл = Qпол.
Предположим, что в сосуде вода нагреется до температуры смеси Θ. Тогда: Qотл = Q1 + Q2, где Q1 = r · m2 - количество теплоты, отданное паром при конденсации.
![]()
Количество теплоты, полученное холодной водой, будет равно: ![]()
Итак.
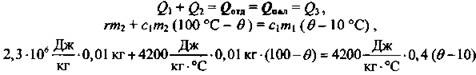
Откуда: 4,4 · 104
(Ответ: Θ = 25,8 °С.)
Задача 3
Кусок льда массой 8 кг имеет температуру 0 °С. Его начинают плавить, сжигая керосин. Что будет в сосуде, когда сгорит 100 г керосина?
Дано:
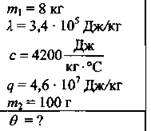
Решение:
Предположим, что количества теплоты, которая выделится при сгорании топлива, хватит и на плавление льда, и на нагревание воды до температуры Θ.
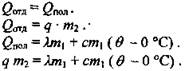
Откуда:
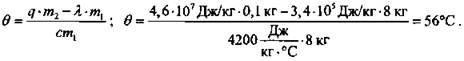
(Ответ: В сосуде будет находиться вода при температуре Θ = 56 °С.)
Далее для самостоятельного решения можно предложить выполнить две-три несложных задачи.
Задача 4
В сосуд с водой массой 2 кг и температурой 60 °С положили кусочек льда массой 50 г и температурой 0 °С. Какая температура установится в сосуде? (Ответ: Θ = 56 °С.)
Задача 5
Сколько бензина нужно сжечь, чтобы 200 кг воды нагреть на 30 °С? (Ответ: m = 0,55 кг.)
Задача 6
Какое количество горячей воды с температурой 80 °С нужно налить в холодную воду массой 20 кг и температурой 10 °С, чтобы установилась температура смеси 30 °С? (Ответ: m = 8 кг.)
Домашнее задание
1. Повторить материал по теме «Изменение агрегатных состояний вещества».
2. Задачи и упражнения (учебник, с. 126) № 187,188.
3. Сборник задач В. И. Лукашика, Е. В. Ивановой, № 1043-1045.