Биохимические основы жизнедеятельности организма человека - Волков Н.И., Несен Э.Н. 2000
Биохимические основы жизнедеятельности организма человека
Обмен энергии в организме
Биологическое окисление основной путь энергообразования в клетках организма
Процесс биологического окисления питательных веществ в организме привлекает внимание ученых уже более 200 лет. Связано это с тем, что биологическое окисление веществ в тканях организма, как и процесс горения, сопряжено с освобождением энергии.
Существенный вклад в развитие этой проблемы внесли А.В. Энгельгардт (1930) и В.А. Белицер (1941), которые установили взаимосвязь (сопряжение) процесса окисления с фосфорилированием АДФ. Ими показано, что энергия, выделяющаяся при окислении питательных веществ, не только рассеивается в виде тепла, но и накапливается в молекулах АТФ.
В настоящее время процессы биологического окисления и образования АТФ в клетках организма хорошо изучены благодаря работам таких известных исследователей, как О. Варбург, Г. Кребс, П. Митчелл, А. Ленинджер, В.П. Скулачев и многие другие.
Процессы биологического окисления. При обмене веществ в организме человека протекают окислительно-восстановительные реакции. Процесс окисления любого вещества связан с отдачей электронов окисляемым веществом (донором электронов), а процесс восстановления — с присоединением электронов к какому-то веществу (акцептору электронов). Рассмотрим процесс окисления-восстановления на примере прямой реакции окисления водорода атомарным кислородом (в неживой природе — это реакция горения):
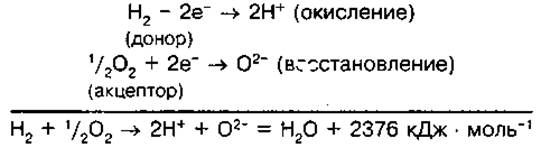
В ходе этой реакции высокоэнергетические электроны молекулы водорода переходят на низкоэнергетическую орбиту атома кислорода и теряют часть энергии. Процесс непосредственного взаимодействия водорода с кислородом сопровождается быстрым высвобождением энергии в виде теплового взрыва. В живых организмах в целях сохранения целостности клетки выделение энергии происходит постепенно.
Процесс биологического окисления питательного вещества — субстрата (S) в клетках организма протекает с участием специфических ферментов и переносчиков водорода (А) согласно следующей схеме:
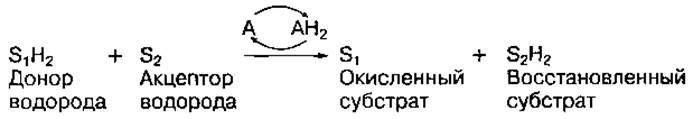
Конечным акцептором водорода в реакциях биологического окисления в клетках организма человека могут быть органические вещества и кислород вдыхаемого воздуха. Процессы биологического окисления питательных веществ в клетках, протекаемые с участием кислорода воздуха, называются тканевым дыханием.
Типы реакций биологического окисления. Выделяют аэробные и анаэробные реакции биологического окисления веществ. Если акцептором водорода является кислород — это аэробный, или дыхательный тип окисления. Протекает он с участием ферментов оксидаз:
![]()
Если акцептором водорода является не кислород, а какое-либо органическое вещество (например, S2), то такой тип окисления является анаэробным. В анаэробных реакциях участвуют ферменты дегидрогеназы:
![]()
Кроме этих реакций в клетках протекают окислительно-восстановительные реакции с изменением валентности атомов железа, как это имеет место при передаче водорода на кислород в системе дыхательной цепи митохондрий:
![]()
Взаимосвязь процессов биологического окисления и образования АТФ. Освобождаемая в реакциях биологического окисления энергия может рассеиваться в виде тепла или улавливаться в процессе синтеза макроэргических соединений. Поэтому выделяют свободное и сопряженное окисление.
Свободное окисление не взаимосвязано с переходом энергии биологического окисления в энергию макроэргических соединений. Выделяющаяся энергия рассеивается в виде тепла. Этот вид энергообразования в клетках важен для теплорегуляции и детоксикации вредных продуктов обмена веществ. Наблюдается он при отдельных видах мышечной деятельности и интенсивной разминки.
Сопряженное окисление связано с переходом свободной энергии, выделяющейся в процессе биологического окисления, в доступную для использования форму энергии — макроэргические связи АТФ или другие виды энергии, например ионный градиент. Различают такие виды сопряженного окисления, как субстратное фосфорилирование и окислительное фосфорилирование.
Субстратное фосфорилирование — это синтез АТФ за счет переноса высокоэнергетического ортофосфата (Н3РO4) от окисляемого субстрата на АДФ. Такое фосфорилирование происходит в основном в мышцах при анаэробном окислении глюкозы с участием высокоспецифических ферментов. Примером может служить окисление 2-фосфоглицериновой кислоты в процессе превращения ее в пировиноградную кислоту. Механизм образования АТФ в этой реакции связан с внутримолекулярным окислением 2-фосфоглицериновой кислоты и превращением ее в макроэргическое соединение — фосфоэнолпировиноградную кислоту:
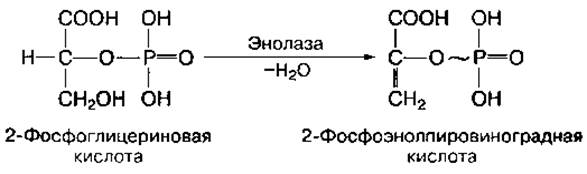
Фосфоэнолпировиноградная кислота благодаря ферменту пируваткиназе способна передавать высокоэнергетический фосфат на АДФ с образованием АТФ и пировиноградной кислоты:
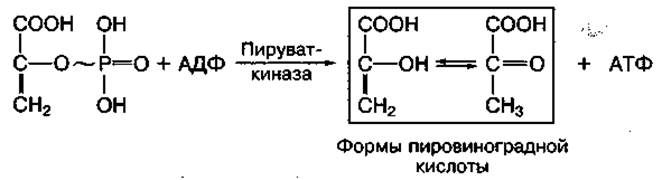
За счет реакций субстратного фосфорилирования образуется сравнительно небольшое количество АТФ в клетке.
Окислительное фосфорилирование — это синтез АТФ за счет энергии, которая выделяется при переносе электронов по дыхательной цепи от окисляемых питательных веществ к атомарному кислороду. Окислительное фосфорилирование является основным механизмом образования АТФ в аэробных условиях.
Субстратное фосфорилирование и окислительное фосфорилирование характеризуются разной степенью сопряженности между реакциями, протекающими с освобождением и накоплением энергии. При субстратном фосфорилировании окисление тесно связано с образованием первичного макроэргического соединения. При окислительном фосфорилировании окисление в дыхательной цепи непосредственно не связано с синтезом АТФ и первоначально используется для образования протонного потенциала, который в дальнейшем приводит к синтезу АТФ. Энергия протонного потенциала может затрачиваться и на другие виды работы, поэтому образование АТФ не является единственным и обязательным следствием окисления.
Ферменты и коферменты реакций биологического окисления, их участие в метаболизме клеток. Окислительно-восстановительные реакции в организме катализируются специфическими ферментами из класса оксидоредуктаз. Реакции окисления, связанные с отщеплением водорода от окисляемого субстрата (дегидрогенизация), катализируются ферментами дегидрогеназами, а реакции присоединения водорода к кислороду — ферментами оксидазами. Дегидрогеназы содержат в своем активном центре небелковую часть (кофермент), которая осуществляет функцию переносчика водорода. Основными переносчиками водорода являются никотинамидные и флавиновые коферменты.
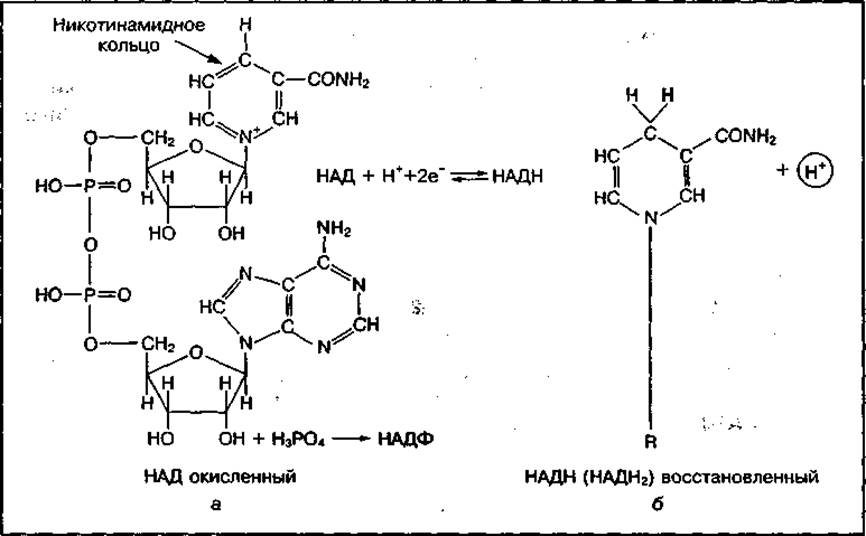
Рис. 15 Строение НАД и НАДФ (а), процесс их восстановления (б)
К никотинамидным конферментам относятся НАД (никотинамидадениндинуклеотид) и НАДФ (никотинамидадениндинуклеотидфосфат). Они непрочно связаны с белковой частью фермента и могут легко переходить к другим ферментам.
В организме имеется большое количество НАД-зависимых ферментов, которые не только участвуют в реакциях энергообразования, но и катализируют другие реакции, например реакции биосинтеза веществ. Достаточно изученным НАД-зависимым ферментом является лактатдегидрогеназа, которая катализирует обратимую реакцию окисления пировиноградной кислоты в молочную. От активности этого фермента зависит скорость аэробного и анаэробного окисления глюкозы в мышцах.
Переносчики водорода НАД и НАДФ состоят из двух мононуклеотидов, связанных между собой остатками фосфорной кислоты. Активная их часть представлена амидом никотиновой кислоты (витамин РР). Никотинамидное кольцо НАД способно забирать один протон Н+ и два электрона (2е-) от окисляемого субстрата (S1) и переходить из окисленной формы в восстановленную (рис. 15).
Участие НАД в окислении веществ можно представить схематически:
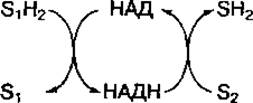
Восстановленная форма НАДН легко перемещается в клетке и может отдавать водород на другие вещества — субстраты (S2). При этом протон другого атома водорода (Н+) остается в водной среде. Поэтому восстановленную форму переносчика НАД обозначают как НАДН или НАДН2.
Молекула НАДФ в отличие от НАД содержит дополнительный остаток фосфорной кислоты, присоединенный к углеводному компоненту одного из нуклеотидов (см. рис. 15). Кофермент НАДФ способен присоединять водород, переходя в восстановленную форму (НАДФН2), и выполнять роль переносчика водорода; НАДФН2 входит в состав ферментов, которые катализируют анаболические реакции в обмене веществ (анаболизм), в то время как НАД является коферментом катаболизма углеводов, жиров и аминокислот. Следовательно, НАД и НАДФ регулируют разнонаправленные метаболические процессы. Изменением количества этих коферментов в клетке можно направленно влиять на процессы энергообразования и восстановительного синтеза веществ в организме.
К флавиновым коферментам относятся ФМН (флавинмононуклеотид) и ФАД (флавинадениндинуклеотид); ФМН и ФАД являются простетической группой ферментов, т. е. прочно связаны с их белковой частью. Они не могут свободно переходить от фермента к ферменту.
Переносчики ФМН и ФАД представляют собой сложные соединения, активной частью которых является изоаллоксазиновое кольцо рибофлавина (витамина В2). К атомам азота этого кольца могут присоединяться два атома водорода либо два протона (2Н+) и два электрона (2е-), при этом коферменты переходят из окисленной формы в восстановленную: ФАД → ФАДН2 (рис. 16).
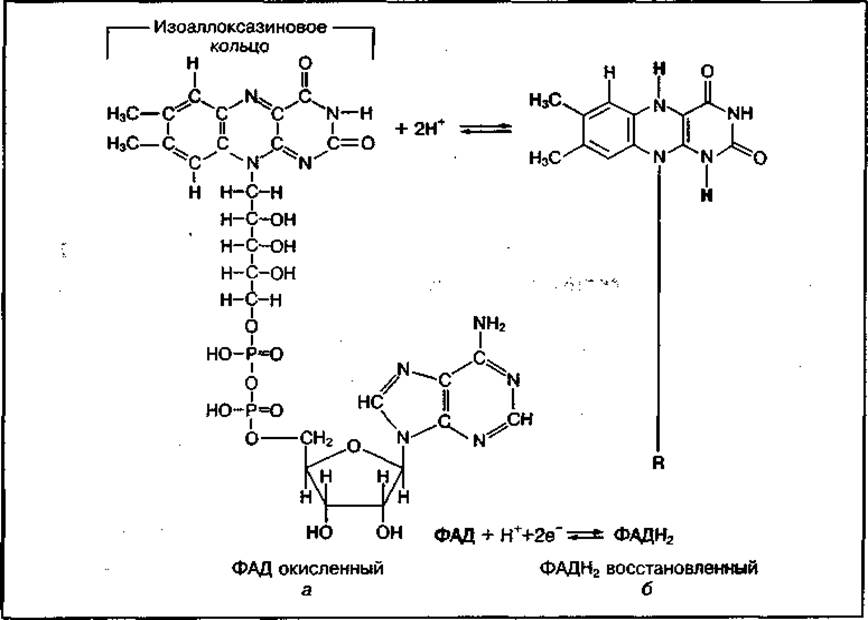
Рис. 16 Строение ФАД (а) и процесс его восстановления (б)
Флавиновые коферменты участвуют в окислении янтарной кислоты и некоторых продуктов обмена жирных кислот; ФМН — один из переносчиков водорода в дыхательной цепи митохондрий.