Биохимические основы жизнедеятельности организма человека - Волков Н.И., Несен Э.Н. 2000
Биохимические основы жизнедеятельности организма человека
Гормоны - регуляторы обмена веществ
Биологическая роль гормонов
Гормоны гипофиза
Гипофиз — нижний придаток головного мозга — является так называемой центральной эндокринной железой, которая взаимодействует с гипоталамусом и обеспечивает взаимосвязь нервной и эндокринной систем. Гормоны гипофиза координируют функции других желез внутренней секреции (см. рис. 49). Гипофиз имеет переднюю (аденогипофиз), среднюю (промежуточную) и заднюю (нейрогипофиз) доли.
Передняя доля гипофиза секретирует гормоны белковой природы, которые называются тройными. К ним относятся соматотропный (СТТ), или гормон роста (ГР), тиреотропный (ТТГ), адренокортикотропный (АКТТ), гонадотропный (ГТ), пролактин (ПЛ), липотропный (ЛТГ) гормоны.
Соматотропный гормон стимулирует рост и развитие тела, увеличивает рост трубчатых костей в длину, усиливает синтез белка, нуклеиновых кислот и гликогена, т. е. проявляет анаболическое действие. Кроме того, он способствует мобилизации жиров из жировой ткани, усиливает их окисление, а также транспорт аминокислот через мембраны. Этот гормон уменьшает скорость окисления углеводов в тканях, что способствует повышению ее уровня в крови. Недостаток соматотропного гормона в раннем возрасте приводит к карликовости без нарушения умственного развития, а избыток — к гигантизму. Если избыток гормона проявляется в юношеском возрасте, то могут несимметрично увеличиваться конечности и подбородок. Возникает заболевание акромегалия. В настоящее время получен синтетический гормон роста, идентичный человеческому, что позволяет успешно лечить больных с нарушением секреции этого гормона; СТГ — единственный гормон, который имеет видовую специфичность действия.
Тиреотропный гормон активирует функцию щитовидной железы, увеличивает число и размеры ее клеток.
Адренокортикотропный гормон поддерживает структуру коры надпочечников и усиливает образование в них гормонов. При отсутствии этого гормона кора надпочечников атрофируется. Повышение уровня АКТТ в крови, например при стрессе, вызывает стимуляцию синтеза кортикостероидов, которые играют важную роль в адаптации организма к стрессовым воздействиям.
Гонадотропные гормоны, которые включают фолликулостимулирующий (ФСГ) и лютеинизирующий (ЛГ) гормоны, регулируют функцию половых желез (гонад) — семенников и яичников. Так, ФСГ стимулирует развитие фолликулов в яичниках женщин и семенных канальцев у мужчин; ЛГ участвует в образовании желтого тела у женщин и клеток Лейдинга, которые вырабатывают тестостерон у мужчин. Следовательно, гонадотропные гормоны, влияя на выработку тестостерона, усиливают анаболические процессы. Пониженная секреция этих гормонов приводит к атрофии половых желез.
Лактотропный гормон (пролактин) контролирует развитие молочных желез и выработку в них молока, а также образование лютеинизирующего гормона, который влияет на развитие гонад.
Липотропный гормон стимулирует расщепление жиров в жировой ткани и их использование в процессах энергообразования.
Средняя доля гипофиза секретирует меланостимулирующий гормон — меланотропин (МТ), который влияет на пигментацию кожи, адаптацию глаз к темноте и функцию щитовидной железы.
Задняя доля гипофиза содержит два гормона — окситоцин и вазопрессин (антидиуретический гормон). Окситоцин стимулирует сокращение гладких мышц матки и функцию молочных желез. Вазопрессин повышает кровяное давление и регулирует ресорбцию воды почками, уменьшая количество суточной мочи. При недостаточности этого гормона количество суточной мочи резко увеличивается (до 25 л ∙ сут-1) и развивается заболевание несахарный диабет. Следовательно, этот гормон играет важную роль в регуляции содержания воды в организме, поддержании физиологического объема крови.
Гормоны щитовидной железы
Щитовидная железа состоит из двух долей, расположенных на передней стороне трахеи ниже гортани (рис. 53). В ней синтезируются три важных тиреоидных гормона: тироксин (Т4), трийодтиронин (Т3) и кальцитонин.
Тироксин и трийодтиронин являются производными аминокислоты — тирозина. Их молекулы содержат четыре (Т4) или три (Т3) атома йода. Эти гормоны регулируют обмен углеводов, жиров и белков, стимулируют процессы энергообразования, так как активируют мобилизацию и окисление углеводов и жиров, усиливая основной обмен на 60—100 %. Это приводит к повышению температуры тела. Кроме того, они активируют биосинтез белка, что стимулирует процессы роста и развития организма, особенно в молодом возрасте.
При снижении секреторной функции щитовидной железы (гипотиреоз) в раннем возрасте наблюдается задержка процессов роста и полового созревания, а также умственного развития (кретинизм). Если такое нарушение возникает во взрослом организме, то на 30—40 % снижается основной обмен вследствие изменения белкового обмена. В подкожной клетчатке накапливается вода и возникает отек — микседема. Причиной гипотиреоза может быть недостаток йода в пище и воде. В этом случае щитовидная железа разрастается и возникает заболевание эндемический зоб.
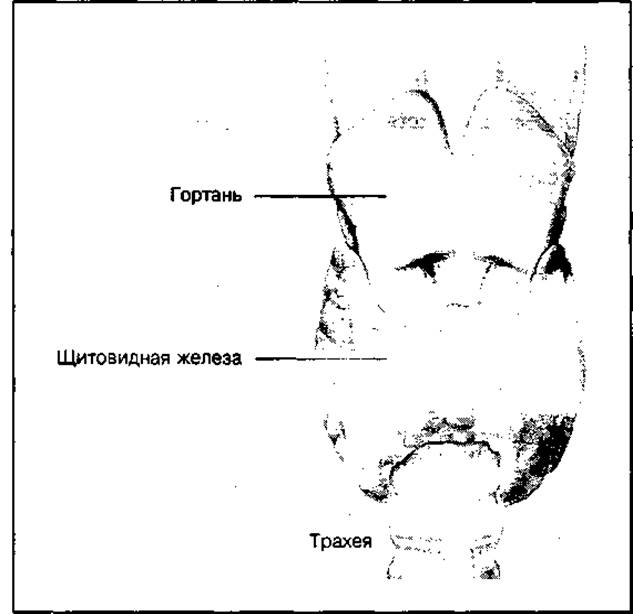
Рис. 53 Расположение щитовидной железы
Кальцитонин является полипептидом, состоящим из 32 аминокислотных остатков. Он снижает уровень кальция и фосфора в крови и усиливает поступление их в костную ткань, в противоположность гормону паращитовидной железы, который повышает содержание кальция в крови за счет усиления выхода его из костей и поступления из кишечника, как и витамин D (см. главу 7).
Гормоны поджелулочной железы
Поджелудочная железа обладает экзо- и эндокринной функцией. Эндокринную функцию выполняют островки Лангерганса, в которых синтезируются полипептидные гормоны — инсулин, глюкагон и соматостатин. Островки Лангерганса включают три типа гормонсинтезирующих клеток: альфа-, бета- и дельта-клетки (рис. 54).
Инсулин синтезируется бета-клетками, регулирует обмен углеводов, жиров и белков. Действие на углеводный обмен связано с тем, что инсулин усиливает транспорт глюкозы из крови в скелетные мышцы, сердечную мышцу и жировую ткань за счет повышения проницаемости клеточных мембран этих тканей и стимулирует синтез гликогена в печени и мышцах. Таким образом инсулин снижает уровень глюкозы в крови, т. е. проявляет гипогликемический эффект. Инсулин стимулирует также синтез и депонирование жира в жировой ткани, проникновение аминокислот в клетки и синтез из них белка. Следовательно, инсулин способствует запасанию питательных веществ, т. е. проявляет анаболическое действие.
Главным стимулом для секреции инсулина служит повышение концентрации глюкозы в крови. Такое же влияние оказывают и аминокислоты. При недостаточной секреции инсулина развивается сахарный диабет, для которого характерно высокое содержание глюкозы в крови (гипергликемия) и присутствие ее в моче (глюкозурия). Ткани в качестве источника энергии начинают использовать жиры, что, в конечном итоге, приводит к диабетической коме и летальному исходу. Введение больным сахарным диабетом инсулина частично нормализует метаболические процессы и сохраняет им жизнь.
Глюкагон синтезируется альфа-клетками островковой ткани поджелудочной железы. Его действие противоположно действию инсулина. Глюкагон стимулирует расщепление гликогена в печени и таким образом повышает содержание глюкозы в крови, а также способствует образованию глюкозы в печени из аминокислот и жиров при истощении запасов гликогена, активирует распад жиров (липолиз) в жировой ткани. Следовательно, действие его направлено на мобилизацию энергетических запасов организма при увеличении энергетических потребностей.
Фактором, регулирующим выделение глюкагона поджелудочной железой, как и инсулина, является уровень глюкозы в крови. В противоположность инсулину, секреция глюкагона увеличивается при снижении этого уровня и уменьшается при его нормализации. Оба гормона регулируют постоянство глюкозы в крови (рис. 55).
Соматостатин секретируется дельта-клетками поджелудочной железы, а также гипофизом (см. рис. 48). Он подавляет выход инсулина и глюкагона из их секреторных клеток.
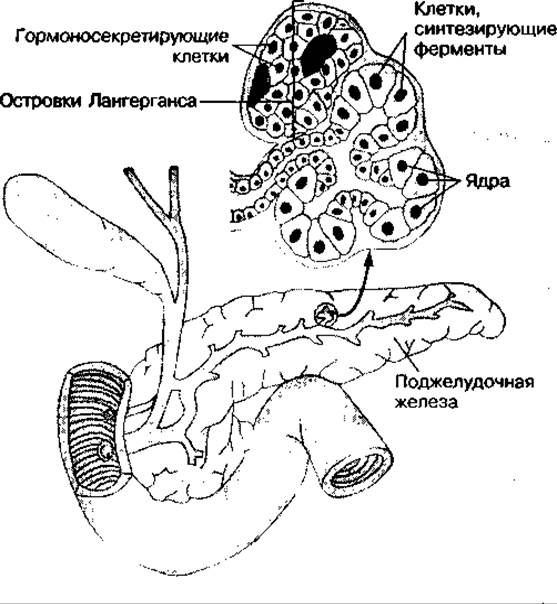
Рис. 54 Гормоно- секретирующие клетки (островки Лангерганса) поджелудочной железы
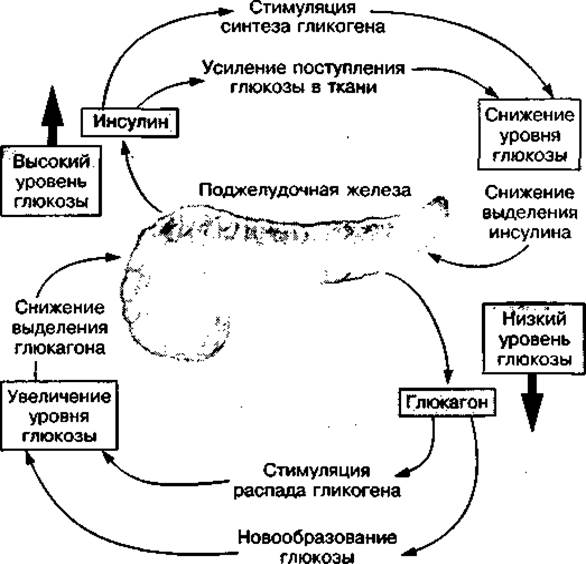
Рис. 55 Совместная регуляция постоянства концентрации глюкозы крови инсулином и глюкагоном
Гормоны над почечников
Надпочечники расположены на верхних полюсах передней части почек. Каждый надпочечник имеет два слоя: наружный — корковый и внутренний — мозговой (рис. 56). В них синтезируются разные гормоны со специфическими биологическими функциями. Кора надпочечников синтезирует около 40 стероидных гормонов, которые называются кортикостероидами. Основными являются три группы: глюкокортикостероиды, минералокортикостероиды и гонадокортикоиды.
Глюкокортикостероиды (глюкокортикоиды) включают кортизол (гидрокортизон) и кортикостерон. Эти гормоны усиливают синтез глюкозы в печени из веществ неуглеводной природы (аминокислот, жирных кислот) и предотвращают резкое снижение глюкозы в крови, например при голодании, физических нагрузках. В мышцах, коже, жировой ткани они усиливают процессы распада белков и жиров, которые используются как энергетические вещества. Такое действие глюкокортикоидов играет важную роль в адаптации организма к различным стрессовым факторам — холода, голода, страха, интенсивных физических нагрузок, так как они мобилизуют запасные питательные вещества (жиры, белки) из периферических тканей и предотвращают истощение запасов гликогена в печени. В печени также происходит синтез новых белков, в том числе адаптогенных ферментов, необходимых для стимуляции адаптационных процессов.
Минералокортикостероиды представлены в основном альдостероном, который регулирует обмен минеральных веществ (натрия и калия) и воды.
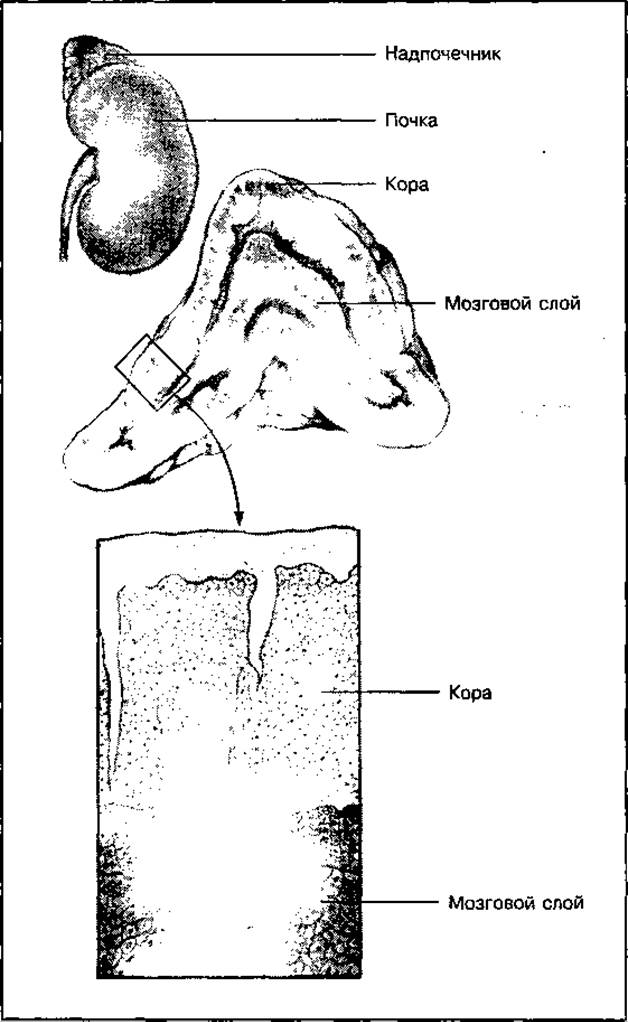
Рис. 56 Локализация надпочечников и двух его слоев — коры и мозгового слоя
Он задерживает в организме натрий и воду, а выводит калий, контролируя объем плазмы крови, а также баланс натрия и калия в клетках. Секреция альдостерона увеличивается при уменьшении объема плазмы. При недостатке минералокортикоидов происходит обезвоживание организма, что отрицательно влияет на функциональное состояние.
Гонадокортикостероиды — это в основном мужские половые гормоны (андрогены), в незначительном количестве — женские (эстрогены). Они контролируют те же функции, что и гормоны половых желез, но менее выраженно.
Мозговой слой надпочечников синтезирует два гормона — адреналин и норадреналин. Они называются катехоламинами. Оба гормона, как отмечалось выше, синтезируются из аминокислоты тирозина под воздействием нервных импульсов. Норадреналин синтезируется также в нервных окончаниях симпатической нервной системы и является ее нейропередатчиком (медиатором). Оба гормона играют важную роль в приспособительных реакциях организма, особенно в условиях стресса.
Адреналин и норадреналин стимулируют мобилизацию энергетических запасов организма, усиливают распад гликогена в печени, способствуют повышению содержания глюкозы в крови. Данные гормоны усиливают также распад гликогена в скелетных мышцах, окисление глюкозы в процессе гликогенолиза, распад резервных жиров в жировой ткани. Наряду с мобилизацией энергетических ресурсов они вызывают сужение мелких артерий, но способствуют расширению венечных сосудов сердца и скелетных мышц, улучшая тем самым кровоснабжение этих тканей и их функции.
Американский физиолог У. Кеннон назвал адреналин «гормоном страха, борьбы или бегства». Под воздействием стрессового фактора увеличивается выброс катехоламинов в кровь, что, кроме рассмотренных эффектов, стимулирует образование гормонов гипофиза (АКТГ) и коры надпочечников. Последние обеспечивают формирование адаптивных изменений в организме, способствующих повышению устойчивости его к действию стресс-фактора (см. главу 13).
Гормоны половых желез
Половые гормоны синтезируются в основном в половых железах (гонадах): семенниках — у мужчин и яичниках — у женщин. Незначительное количество половых гормонов образуется также в коре надпочечников и плаценте.
В мужских половых железах синтезируются стероидные гормоны — андрогены, основным представителем которых является тестостерон. Он начинает вырабатываться в клетках Лейдинга в период полового созревания (в 12—14 лет) под действием лютеинизирующего гормона гипофиза. Тестостерон проявляет андрогенное и анаболическое действие. Андрогенное действие тестостерона связано с формированием вторичных половых признаков (тембр голоса, мужская конституция тела и т. п.) и регуляцией репродуктивной функции. Андрогены также ускоряют закрытие зон роста костей. Анаболическое действие тестостерона связано с влиянием его на обмен белка. Этот гормон и другие андрогены усиливают синтез белка в печени, почках и, особенно, в скелетных мышцах. Поэтому андрогены и их синтетические аналоги используются в клинике и спорте для ускорения восстановления организма после болезни или напряженной мышечной деятельности, а также для наращивания мышечной массы. Индукция синтеза белка, в том числе ферментов, приводит к усилению процессов энергообразования. Тем не менее применение гормональных анаболиков в практике спорта для повышения физических возможностей спортсмена запрещено Международным олимпийским комитетом. Стероидные анаболики отнесены к группе допинговых средств, поскольку отрицательно влияют на здоровье спортсменов.
В женских половых железах синтезируются стероидные гормоны эстрогены. Основными представителями эстрогенов являются эстрадиол и прогестерон. Эстрогены регулируют менструальный цикл и детородную функцию организма, развитие вторичных половых признаков, стимулируют синтез белка в матке, особенно во время беременности, а также в сердце и печени, оказывая анаболическое действие. Они усиливают также катаболические реакции в скелетных мышцах.
Прогестероны синтезируются клетками желтого тела и регулируют функцию матки во второй половине менструального цикла. Они стимулируют процессы, обеспечивающие наступление и сохранение беременности, тормозят выработку эстрогенов. Под влиянием прогестерона (совместно с эстрогенами) матка увеличивается, в результате чего оплодотворенная яйцеклетка прикрепляется к ее стенке и развивается плод. Прогестероны способствуют росту молочных желез. Отсутствие их во-время беременности приводит к гибели плода.