Биологическая химия - Березов Т. Т., Коровкин Б. Ф. 1998
Обмен простых белков
Всасывание продуктов распада белков
Превращения аминокислот под действием микрофлоры кишечника
Известно, что микроорганизмы кишечника для своего роста также нуждаются в доставке с пищей определенных аминокислот. Микрофлора кишечника располагает набором ферментных систем, отличных от соответствующих ферментов животных тканей и катализирующих самые разнообразные превращения пищевых аминокислот. В кишечнике создаются оптимальные условия для образования ядовитых продуктов распада аминокислот: фенола, индола, крезола, скатола, сероводорода, метилмеркаптана, а также нетоксичных для организма соединений: спиртов, аминов, жирных кислот, кетокислот, оксикислот и др.
Все эти превращения аминокислот, вызванные деятельностью микроорганизмов кишечника, получили общее название «гниение белков в кишечнике». Так, в процессе распада серосодержащих аминокислот (цистин, цистеин, метионин) в кишечнике образуются сероводород H2S и метилмеркаптан CH3SH. Диаминокислоты — орнитин и лизин — подвергаются процессу декарбоксилирования с образованием аминов — путресцина и кадаверина.
Из ароматических аминокислот: фенилаланин, тирозин и триптофан — при аналогичном бактериальном декарбоксилировании образуются соответствующие амины: фенилэтиламин, параоксифенилэтиламин (или тирамин) и индолилэтиламин (триптамин). Кроме того, микробные ферменты кишечника вызывают постепенное разрушение боковых цепей циклических аминокислот, в частности тирозина и триптофана, с образованием ядовитых продуктов обмена — соответственно крезола и фенола, скатола и индола.
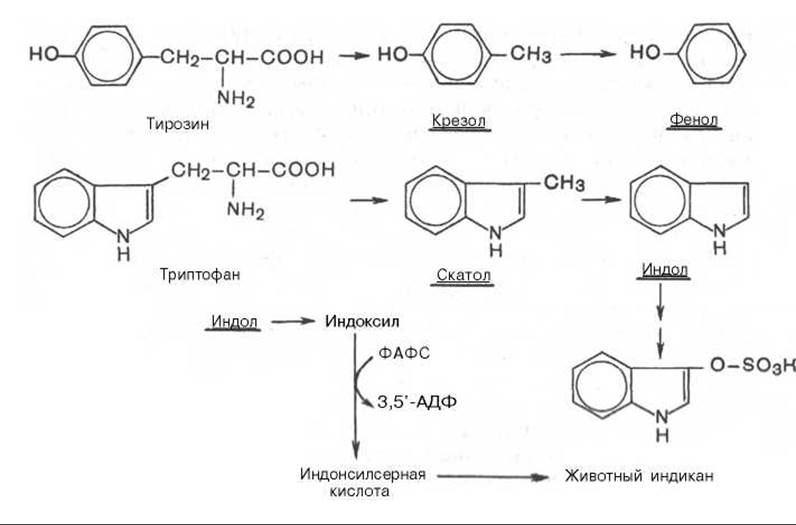
После всасывания эти продукты через воротную вену попадают в печень, где подвергаются обезвреживанию путем химического связывания с серной или глюкуроновой кислотой с образованием нетоксичных, так называемых парных, кислот (например, фенолсерная кислота или скатоксилсерная кислота). Последние выделяются с мочой. Механизм обезвреживания этих продуктов изучен детально. В печени содержатся специфические ферменты — арилсульфотрансфераза и УДФ-глюкоронилтрансфераза, катализирующие соответственно перенос остатка серной кислоты из ее связанной формы — 3'-фосфоаденозин-5'-фосфосульфата (ФАФС) и остатка глюкуроновой кислоты также из ее связанной формы — уридил-дифосфоглюкуроновой кислоты (УДФГК) на любой из указанных продуктов.
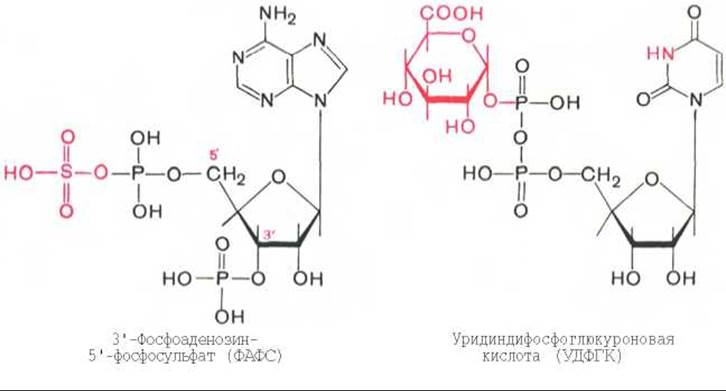
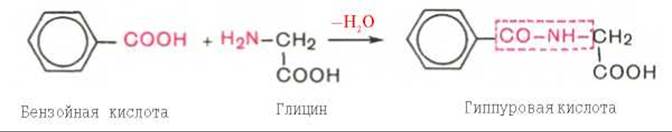
Индол (как и скатол) предварительно подвергается окислению в индоксил (соответственно скатоксил), который взаимодействует непосредственно в ферментативной реакции с ФАФС или с УДФГК. Так, индол связывается в виде эфиросерной кислоты. Калиевая соль этой кислоты получила название животного индикана, который выводится с мочой (см. главу 18). По количеству индикана в моче человека можно судить не только о скорости процесса гниения белков в кишечнике, но и о функциональном состоянии печени. О функции печени и ее роли в обезвреживании токсичных продуктов часто также судят по скорости образования и выделения гиппуровой кислоты с мочой после приема бензойной кислоты (см. главу 16).
Таким образом, организм человека и животных обладает рядом защитных механизмов синтеза, биологическая роль которых заключается в обезвреживании токсичных веществ, поступающих в организм извне или образующихся в кишечнике из пищевых продуктов в результате жизнедеятельности микроорганизмов.