Биологическая химия - Березов Т. Т., Коровкин Б. Ф. 1998
Обмен простых белков
Обезвреживание аммиака в организме
В организме человека подвергается распаду около 70 г аминокислот в сутки, при этом в результате реакций дезаминирования и окисления биогенных аминов освобождается большое количество аммиака, являющегося высокотоксичным соединением. Поэтому концентрация аммиака в организме должна сохраняться на низком уровне. Действительно, уровень аммиака в крови в норме не превышает 60 мкмоль/л (это почти в 100 раз меньше концентрации глюкозы в крови). В опытах на кроликах показано, что концентрация аммиака 3 ммоль/л является летальной. Таким образом, аммиак должен подвергаться связыванию в тканях с образованием нетоксичных соединений, легко выделяющихся с мочой.
Один из путей связывания и обезвреживания аммиака в организме, в частности в мозге, сетчатке, почках, печени и мышцах, — это биосинтез глутамина (и, возможно, аспарагина). Глутамин и аспарагин выделяются с мочой в небольшом количестве. Было высказано предположение, что они выполняют скорее транспортную функцию переноса аммиака в нетоксичной форме. Ниже приводится химическая реакция синтеза глутамина, катализируемого глутаминсинтетазой*.
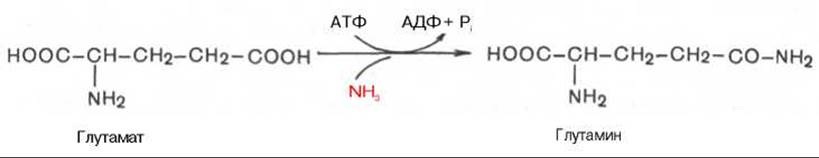
Механизм этой синтетазной реакции, подробно изученный А. Майстером, включает ряд стадий. Синтез глутамина в присутствии глутаминсинтетазы может быть представлен в следующем виде:
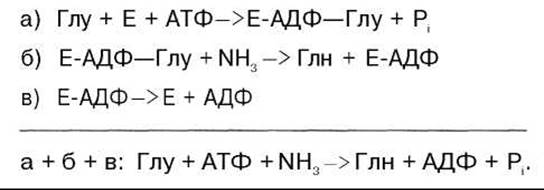
Биосинтез аспарагина протекает несколько отлично и зависит от природы ферментов и донора аммиака. Так, у микроорганизмов и в животных тканях открыта специфическая аммиакзависимая аспарагинсинтетаза, которая катализирует синтез аспарагина в две стадии:
а) Асп + Е + АТФ -> Е-аспартил~АМФ + PPi;
б) Е-аспартил~АМФ + NH3 -> Асн + Е + АМФ.
В животных тканях содержится, кроме того, глутаминзависимая аспарагинсинтетаза, которая для синтеза во второй стадии использует амидную группу глутамина:
б) Е-аспартил~АМФ + Глн -> Асн + Е + АМФ + Глу.
Суммарная ферментативная реакция синтеза аспарагина может быть представлена в следующем виде:
Асп + АТФ + NH3 (или Глн) —> Асн + АМФ + РРi + (Глу).
* Конечные продукты обмена глутамина (гистидин, глюкозо-6-фосфат, АМФ, цАМФ и др.), как и Гли, и Ала, оказались аллостерическими ингибиторами глутаминсинтетазы. Фермент подвергается также ковалентной модификации путем аденилирования-деаденилирования (остаток Тир), и тогда он оказывается более чувствительным к аллостерическим ингибиторам. Суммарный тормозящий эффект превышает действие одного какого-либо ингибитора. Этот тип регуляции известен как согласованное ингибирование.
Видно, что энергетически синтез аспарагина обходится организму дороже, поскольку образовавшийся РРі далее распадается на ортофосфат.
Часть аммиака легко связывается с а-кетоглутаровой кислотой благодаря обратимости глутаматдегидрогеназной реакции. Если учесть связывание одной молекулы аммиака при синтезе глутамина, то нетрудно видеть, что в организме имеется хорошо функционирующая система, связывающая две молекулы аммиака:
![]()
Глутамин, кроме того, используется почками в качестве резервного источника аммиака (образуется из глутамина под действием глутаминазы), необходимого для нейтрализации кислых продуктов обмена при ацидозе и защищающего тем самым организм от потери с мочой используемых для этих целей ионов Na+.