БИОХИМИЯ - Основные регуляторы и биологические жидкости человеческого организма - 2016 год
3. НУКЛЕИНОВЫЕ КИСЛОТЫ
3.7. Практическая часть. Определение химического состава нуклеопротеидов
Цель работы - научиться определять химический состав гидролизата нуклеопротеидов.
Нуклеопротеиды представляют собой сложные белки, содержащие в качестве простетической группы нуклеиновые кислоты. Из нуклеопротеидов состоит основная масса клеточного ядра, поэтому данные белки могут быть выделены из тканей, богатых ядерным веществом (щитовидной железы, семенников, сперматозоидов и др.).
Являясь структурными элементами органелл клетки (ядра и цитоплазмы) и выполняя важнейшие специфические функции в живом организме, нуклеопротеиды играют важную биологическую роль. Деление клеток, биосинтез белков, передача наследственной информации тесно связаны с нуклеопротеидами, в частности с входящими в их состав нуклеиновыми кислотами (ДНК и РНК).
Нуклеиновые кислоты - это высокомолекулярные соединения, построенные из большого числа нуклеопротеидов, которые состоят из гетероциклического основания (пуринового и пиримидинового) и углеводной компоненты (рибозы или 2 - дезоксирибозы), а также фосфорной кислоты.
3.7.1. Изучение состава нуклеопротеидов
При проведении частичного гидролиза нуклеопротеиды распадаются на составные части: белки, преимущественно основного характера (протамины и гистоны), и нуклеиновые кислоты.
Более полный гидролиз приводит к распаду белков и нуклеиновых кислот:
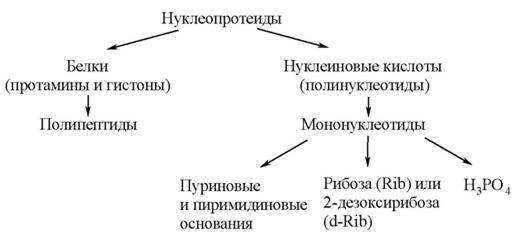
Исследование химического состава нуклеопротеидов проводят на примере дрожжей, которые подвергают гидролизу с последующим изучением его продуктов (полипептидов, пуриновых оснований, углеводных компонентов и фосфорной кислоты).
Гидролиз осуществляют следующим образом. В круглодонную колбу объемом 100 мл помещают 1 г свежих или 0,2 г сухих пекарских дрожжей, приливают 20 мл 10 % раствора серной кислоты (Н2SO4) и 20 мл дистиллированной воды. Колбу закрывают пробкой с воздушным холодильником, закрепляют с небольшим наклоном и кипятят под тягой 1 час. Охлаждают, доводят объем до первоначального дистиллированной водой, отфильтровывают через складчатый фильтр. С фильтратом проводят указанные ниже реакции.
3.7.1.1. Реакции на полипептиды
Опыт 1. Биуретовая реакция на полипептиды
К 5 каплям гидролизата дрожжей добавляют 10 капель 10 % раствора гидроокиси натрия (NаОН) и 1 - 2 капли 5 % раствора сульфата меди (II) - СиSO4 до появления сине-фиолетовой или красно-фиолетовой окраски раствора.
В отчете следует отметить наблюдения, сделать вывод о наличии в нуклеопротеиде полипептидов.
3.7.1.2. Реакции на пуриновые основания
Опыт 2. Серебряная проба на пуриновые основания
Метод основан на способности пуриновых оснований образовывать с аммиачным раствором нитрата серебра (АgNO3) осадок серебряных солей пуриновых оснований (аденина, гуанина), окрашенных в светло-коричневый цвет:
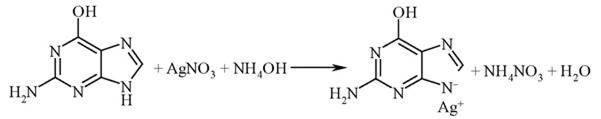
В пробирку вносят 10 капель гидролизата дрожжей, добавляют по каплям концентрированный раствор аммиака (NН4ОН) до щелочной реакции по универсальной индикаторной бумаге (1 - 10 капель) и 10 капель аммиачного раствора нитрата серебра (АgNO3), который готовят добавлением концентрированного раствора аммиака к 2 - 3 % раствору нитрата серебра до растворения осадка. Через 3-5 минут образуется рыхлый бурый осадок серебряных соединений пуриновых оснований.
В отчете следует указать свои наблюдения и сделать вывод о наличии пуриновых оснований в нуклеопротеидах. Какие пуриновые основания в них могут содержаться?
3.7.1.3. Качественные реакции на пентозы
Опыт 3. Дифениламиновая проба (реакция Дише)
Метод основан на способности дезоксирибозы ДНК образовывать в реакции с дифениламином соединения синего цвета при нагревании в среде, содержащей смесь ледяной уксусной кислоты и концентрированной серной кислоты. С рибозой РНК аналогичная реакция дает зеленое окрашивание.
Для приготовления дифениламинового реактива 1 г дифениланилина растворяют в 100 мл ледяной уксусной кислоты (СН3СO2Н) и к полученному раствору добавляют 2,75 мл концентрированной серной кислоты (Н2SO4).
К 10 каплям гидролизата нуклеопротеидов дрожжей приливают 0,5 - 1 мл дифениламинового реактива. Содержимое пробирки перемешивают и нагревают на водяной бане в течение 15 - 20 минут. Отмечают характерное окрашивание раствора.
В отчете следует указать свои наблюдения и сделать вывод о наличии в нуклеопротеидах пентоз. Какие пентозы в них могут содержаться?
Опыт 4. Проба Троммера
Эта проба, как и две последующие, основана на способности рибозы и 2-дезоксирибозы, имеющих свободный гликозидный гидроксил, восстанавливать в щелочной среде окисные формы металлов (Сu, Fе, Вi) до закисных, а закисные - до свободного состояния. Сахара же в этих условиях дают различные продукты окисления.
Основана проба Троммера на указанных ниже реакциях.
1. При добавлении водного раствора гидроксида натрия (NаОН) к раствору сульфата меди (II) - СuSO4 образуется осадок гидроксида меди (II) - Сu(ОН)2 синего цвета:
![]()
2. При нагревании в присутствии восстанавливающих сахаров (рибозы, 2-дезоксирибозы) гидроксид меди (II) - Сu(ОН)2 восстанавливается до гидроксида меди (I) - СuОН (желтый осадок), затем до Сu2O - оксида меди (I), и в конечном результате образуется кирпично-красный осадок.
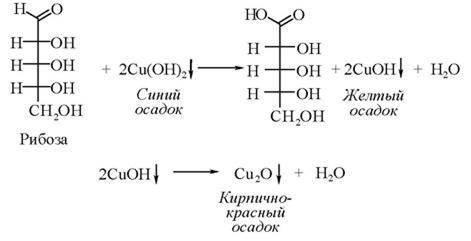
Избыток сульфата меди (II) - СuSO4 мешает реакции, так как ведет к образованию большого количества Сu(ОН)2 - гидроксида меди (II), который при нагревании распадается с образованием черного осадка СuО - оксида меди:
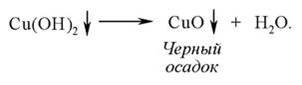
К 5 каплям гидролизата дрожжей добавляют 5 капель 30 % раствора гидроксида натрия (NаОН) и несколько капель 7 % раствора сульфата меди (II) - СuSO4 до появления неисчезающей мути Сu(OН)2 - гидроксида меди (II). При нагревании до кипения выпадает желтый осадок гидроксида меди (I) - СuОН ИЛИ кирппчно- красный осадок оксида меди (I) - Сu2O.
В отчете следует записать свои наблюдения, сделать вывод о наличии в нуклеопротеидах пентоз и об их восстанавливающих свойствах и указать, какой особенностью строения обусловлены эти свойства (при затруднении см. в части 1 данного пособия раздел 3).
Опыт 5. Проба Феллинга
Проба Феллинга является модификацией пробы Троммера. В ней используется реактив Феллинга, для приготовления которого в пробирке смешивают 5 капель 7 % раствора сульфата меди (II) - СUSO4 И 5 капель раствора сегнетовой соли (345 г KNaC4H4O6 • 4Н2O - тетрагидрата двойной натриевой-калиевой соли винной кислоты растворяют в дистиллированной воде), добавляют 140 г гидроксида натрия (NаОН) и доводят водой в мерной колбе до 1 л.
К реактиву Феллинга добавляют 5 - 7 капель гидролизата дрожжей, перемешивают и нагревают до кипения. Наблюдают выпадение окрашенного осадка.
В отчете следует указать цвет осадка, как изменяется окраска раствора, сделать вывод о наличии в нуклеопротеидах пентоз.
Опыт 6. Реакция Толленса
В отличие от двух предыдущих реакций реакция Толленса является специфичной для пентоз. Она обусловлена взаимодействием флороглюцина с фурфуролом, образующимся из пентозы при нагревании с соляной кислотой (НСI). При этом получается продукт конденсации красного цвета.
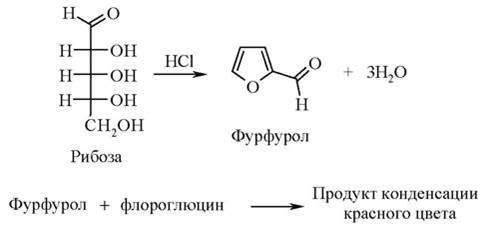
В пробирку вносят 5 - 7 капель гидролизата дрожжей, 2 - 3 капли 0,5 % раствора флороглюцина в концентрированной соляной кислоте (НСI) и кипятят в течение 1 минуты. Наблюдают за изменением окраски раствора.
В отчете следует отметить, как изменяется окраска раствора, сделать вывод о наличии в нуклеопротеидах пентоз.
Опыт 7. Реакция Молиша
В пробирку вносят 10 капель гидролизата дрожжей, добавляют 3 капли 1 % раствора тимола, затем по стенке пробирки (осторожно!) добавляют 20 капель концентрированной соляной кислоты (НСI) и кипятят в течение 1 минуты. Наблюдают за изменением окраски раствора.
В отчете следует отметить, как изменяется окраска раствора, сделать вывод о наличии в нуклеопротеидах пентоз.
3.7.1.4. Качественные реакции на фосфорную кислоту
Опыт 8. Молибденовая проба на фосфорную кислоту
Для приготовления молибденового реактива в 100 мл дистиллированной воды растворяют 7,5 г молибдата аммония - (NН4)2МоO4 и добавляют 100 мл 32 % раствора азотной кислоты (НNО3) плотностью 1,2 г/см3.
В пробирку вносят 5 капель гидролизата дрожжей, добавляют 10-20 капель молибденового реактива и кипятят в течение нескольких минут. При охлаждении пробирки под струей холодной воды выпадает кристаллический осадок фосфорной соли молибдата аммония лимонно-желтого цвета:
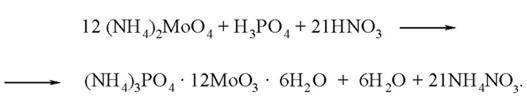
3.7.1.5. Качественные реакции на лекарственные препараты нуклеотидной природы
В качестве лекарственного препарата нуклеотидной природы используют раствор аденозинтрифосфата (АТФ, средства улучшающего метаболизм и энергообеспечение тканей).
Опыт 9. Обнаружение рибозы в аденозинтрифосфате
Метод основан на обнаружении рибозы с помощью дифенил - аминовой реакции.
В пробирку вносят 5 капель раствора аденозинтрифосфата натрия, прибавляют 10 капель дифениламинового реактива и нагревают 10 минут на кипящей водяной бане.
В отчете отмечают результат реакции, делают вывод о присутствии рибозы в структуре аденозинтрифосфата.
3.7.2. Практическое значение работы
Реакции на компоненты нуклеиновых кислот могут применяться для их идентификации и количественного анализа в биохимических исследованиях, а в фармации - для контроля качества препаратов нуклеотидной природы.