БИОХИМИЯ - В. В. Емельянов - 2016
РАЗДЕЛ 1. ФЕРМЕНТЫ
1.1. Общая характеристика ферментов
Ферменты - это специфические белки, которые действуют как катализаторы в биологических системах.
Являясь веществами белковой природы, ферменты обладают всеми свойствами белков:
- имеют несколько уровней организации макромолекул, подтвержденных данными рентгеноструктурного анализа;
- подобно растворимым белкам, образуют коллоидные растворы;
- дают положительные цветные реакции на белки;
- являются амфотерными соединениями;
- склонны к денатурации под влиянием тех же факторов: температуры, изменений рН, действия солей тяжелых металлов, физических факторов (ультразвука, ионизирующего излучения и т. д.):
- ферменты, как и белки, при гидролизе распадаются до аминокислот.
В отличие от других белков, ферменты обладают каталитической активностью. При этом, обладая свойствами, присущими неорганическим катализаторам, они существенно отличаются от них рядом свойств (табл. 1).
Таблица 1. Сходства и различия каталитического действия ферментов и неорганических катализаторов
Сходства |
Различия |
Ускоряют только термодинамически возможные реакции |
Действуют в мягких условиях (t = 36-37 °С) |
В случае обратимых реакций ускоряют и прямую и обратную реакции |
Эффективность действия зависит от рН |
Чувствительны к активаторам и ингибиторам |
Термолабильность |
Действуют в малых количествах |
Высокая специфичность |
Действие ферментов в организме регулируется |
|
Широкий диапазон каталитического действия |
|
Высокая эффективность действия |
Учение о ферментах выделено в самостоятельную науку - энзимологию. Термин «энзим» (от греч. еn zyme - в дрожжах) так же, как и «фермент» (от лат. fer- mentum - закваска), означает процесс, связанный с выделением газов, брожением.
1.2. Локализация ферментов в организме
Ферменты по локализации и функциональности делят на три группы:
I - общие ферменты (универсальные);
II - органоспецифические;
III — органеллоспецифические.
Общие ферменты обнаруживаются практически во всех клетках, обеспечивают жизнедеятельность клетки, катализируя реакции биосинтеза белка, нуклеиновых кислот, образование биомембран и основных клеточных органелл, энергообмен. Общие ферменты разных тканей и органов, тем не менее, отличаются по активности.
Ферменты, свойственные только или преимущественно определенному органу или ткани, называются органоспецифическими. В печени - это аргиназа, урокиназа, гистидаза, y-глутамилтрансфераза, аланинаминотрансфераза, сорбитолдегидрогеназа. Органоспецифическим ферментом почек и костной ткани является щелочная фосфатаза, предстательной железы - кислая фосфатаза, поджелудочной - α-амилаза и липаза.
Внутри клетки ферменты распределены также неравномерно. Одни ферменты находятся в коллоидно-растворенном состоянии в цитозоле, другие вмонтированы в клеточные органеллы (структурированное состояние). Разным органеллам клетки присущ специфический набор ферментов, которые определяют их функции:
- клеточная мембрана: щелочная фосфатаза, аденилатциклаза, К+-Na+-АТФ-аза;
- цитоплазма: ферменты гликолиза, пентозного цикла;
- микросомы: ферменты, обеспечивающие гидроксилирование;
- рибосомы: ферменты, обеспечивающие синтез белка;
- лизосомы: гидролитические ферменты;
- митохондрии: ферменты цикла трикарбоновых кислот и окислительного фосфорилирования;
- ядро клетки: ферменты, обеспечивающие синтез РНК и ДНК;
- ядрышко: ДНК-зависимая РНК-полимераза.
В клетке существуют отсеки (компартменты), которые, отличаясь набором ферментов, отличаются и метаболизмом (компартментализация метаболизма).
Определение в плазме или сыворотке крови активности органо- или органеллоспецифических ферментов широко используется в клинической диагностике. Увеличение активности ферментов в плазме (сыворотке) крови связано прежде всего с цитолизом (т. е. повышением проницаемости биомембран или некрозом клетки) и выходом ферментов в кровяное русло. При этом активность ферментов в поврежденном органе уменьшается, а в плазме или сыворотке крови возрастает.
1.3. Строение ферментов
В природе существуют как простые, так и сложные ферменты. Первые целиком представлены полипептидными цепями и при гидролизе распадаются исключительно на аминокислоты. Большинство природных ферментов относятся к сложным белкам, содержащим, помимо полипептидных цепей, какой-либо небелковый компонент - кофермент или кофактор. В литературе существуют различные трактовки этих терминов. Мы придерживаемся точки зрения, согласно которой кофермент - небелковая часть сложного фермента, являющаяся органическим веществом, кофактор - неорганическим.
Кофакторами чаще всего служат ионы металлов: железа, меди, цинка и др. Кофакторы необходимы для проявления каталитической активности многих ферментов.
Многие коферменты являются производными водорастворимых витаминов (табл. 2).
Таблица 2. Коферменты, производные витаминов
Витамины |
Коферменты |
РР (никотиновая кислота) |
НАД+, НАДФ |
В2 (рибофлавин) |
ФАД, ФМН |
В6 (пиридоксаль) |
Пиридоксальфосфат |
В1 (тиамин) |
Тиаминпирофосфат |
В9 (фолиевая кислота) |
Тетрагидрофолиевая кислота |
В12 (цианокобаламин) |
Кобаламины |
Можно выделить три группы коферментов:
- принимающие участие в окислительно-восстановительных реакциях: (НАД+/ НАДН2, НАДФ+/НАДФН2, ФАД/ФАДН2, KoQ);
- принимающие участие в переносе атомных групп: пиридоксальфосфат (перенос аминогрупп), биотин (перенос диоксида углерода), тетрагидрофолиевая кислота (перенос метильных и других одноуглеродных групп);
- принимающие участие в реакциях синтеза, изомеризации и расщепления: тиаминпирофосфат (декарбоксилирование кетокислот), коэнзим А (для активации жирных кислот).
Некоторые коферменты (ФМН, ФАД, пиридоксальфосфат) стабильно связаны с ферментом, и их можно рассматривать как часть активного центра. Другие коферменты (НАД+, НАДФ+, КоА) в условиях живой клетки связываются с активным центром только в момент реакции. В этом они сходны с субстратами ферментов. Если в ходе реакции кофермент претерпевает химические изменения, прямо противоположные происходящим в субстрате, то такие коферменты можно рассматривать как второй субстрат или косубстрат. Более того, иногда именно превращения кофермента имеют физиологическое значение, например, образование НАДН2 в ЦТК и его окисление в дыхательной цепи.
1.3.1. Активный центр ферментов
Ферменты характеризуются наличием специфических центров катализа. Активный центр - это часть молекулы фермента, которая специфически взаимодействует с субстратом и принимает непосредственное участие в катализе. Активный центр, как правило, находится не на поверхности молекулы фермента, а в узком гидрофобном углублении (нише), что благоприятствует созданию высокой концентрации субстрата (рис. 1). Активные центры ферментов формируются на уровне третичной структуры. Любые воздействия, приводящие к денатурации, т. е. нарушению третичной структуры, приводят к разрушению структуры активного центра и, соответственно, к потере ферментом каталитических свойств.
Рис. 1. Активный центр фермента (схема по Малеру и Кордесу): темные полосы - участки полипептидной цепи фермента; R - аминокислотные остатки и их порядковые
номера (с N-конца)
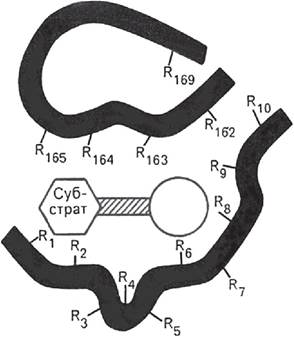
В активном центре условно можно выделить два участка: субстратсвязывающий участок (контактная площадка), который обеспечивает специфическое комплементарное связывание субстрата, и собственно каталитический центр, непосредственно вступающий в химическое взаимодействие с субстратом. В активный центр фермента часто входит участок для связывания кофактора.
Большинство субстратов соединяется с активным центром в нескольких точках. Благодаря этому молекула субстрата связывается с активным центром единственно возможным способом, что обеспечивает избирательность дальнейших химических превращений.
1.3.2. Аллостерические центры ферментов
У группы регуляторных ферментов помимо активного центра, в молекуле фермента может присутствовать также аллостерический центр или центры (от греч. allos - другой и stems - пространственный, структурный), которые находятся за пределами активного центра. К аллостерическому центру могут присоединяться молекулы модуляторов (активаторов или ингибиторов), регулирующие активность ферментов. Присоединение модулятора к аллостерическому центру изменяет конформацию молекулы фермента и, соответственно, конфигурацию активного центра, вызывая повышение или снижение активности фермента (рис. 2).
Рис. 2. Схематическое изображение аллостерического фермента, состоящего из двух протомеров: S - субстрат; М1 - модификатор, связывающийся в активном центре; М2 - эффектор, связывающийся в аллостерическом центре
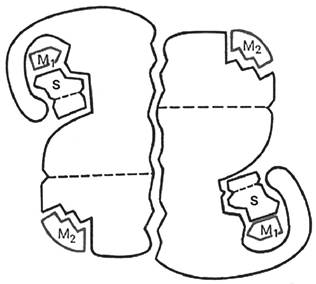
Аллостерические центры известны далеко не у каждого фермента. Обычно они присущи ферментам, обладающим четвертичной структурой, которые легче поддаются весомым конформационным перестройкам. У фермента может быть несколько разных аллостерических центров. Благодаря их избирательности, активность фермента по-разному меняется под действием различных модуляторов.
1.4. Изоферменты
Изоферменты - это множественные формы фермента, катализирующие одни и те же реакции, но отличающиеся по физическим и химическим свойствам (сродство к субстрату, скорость катализируемой реакции, электрофоретическая подвижность, различная чувствительность к ингибиторам и активаторам, термостабильность, оптимум рН).
В качестве примера можно рассмотреть лактатдегидрогеназу (ЛДГ) - фермент, катализирующий обратимую реакцию:
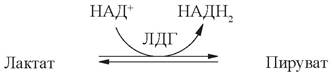
Этот фермент существует в виде 5 изоформ, каждая из которых состоит из 4 протомеров (субъединиц) двух типов (М и Н). Изоферменты ЛДГ различаются на уровне четвертичной структуры: ЛДГ1 - 4Н; ЛДГ2 - 3Н1М; ЛДГ3 - 2Н2М; ЛДГ4 - 1Н3М; ЛДГ5 - 4М. Полипептидные цепи Н- и М-типа имеют одинаковую молекулярную массу, но в составе первых преобладают дикарбоновые аминокислоты, последних - диаминокислоты, поэтому они несут разный заряд и могут быть разделены методом электрофореза. Обозначение изоформ принято в соответствии с их подвижностью к аноду (рис. 3).
Рис. 3. Распределение и относительные количества изоферментов ЛДГ в различных органах. Экстракты нанесены на линию, отмеченную надписью «Старт». При заданных условиях опыта (рН) 4 изофермента ЛДГ движутся к аноду, а один (ЛДГ5) - к катоду

В процессе индивидуального развития организма происходит изменение содержания изоформ в той или иной ткани. У зародыша преобладают ЛДГ4 и ЛДГ5. После рождения происходит изменение содержания изоформ в некоторых тканях. В миокарде, надпочечниках, где доминирует аэробный обмен, преобладают ЛДГ1 и ЛДГ2. В тканях, где сохранился анаэробный обмен, преобладают ЛДГ4 и ЛДГ5 (скелетная мускулатура, печень).
Существование изоформ повышает адаптационную возможность тканей, органов и организма в целом к меняющимся условиям. Определение изоферментного спектра плазмы крови ЛДГ имеет клинико-диагностическое значение для дифференциальной диагностики: при инфаркте миокарда преобладают ЛДГ1 и ЛДГ2, а при заболеваниях печени - ЛДГ4и ЛДГ5.
1.5. Специфичность ферментов
В отличие от неорганических катализаторов ферменты характеризуются специфичностью действия. Специфичность действия фермента определяется структурой активного центра.
Фермент может обладать чрезвычайно высокой избирательностью по отношению к субстрату. Например, фермент уреаза распознает только одно вещество - мочевину, катализируя ее расщепление до СО2 и аммиака:

Если фермент катализирует превращение определенного единственного субстрата, такая специфичность называется абсолютной субстратной специфичностью. Однако встречается она редко.
Обычно субстратная специфичность бывает относительной (групповой). Это означает, что фермент способен ускорять однотипную реакцию у группы сходных по строению веществ. Например, алкогольдегидрогеназа катализирует окисление не только этанола, но и других алифатических спиртов:
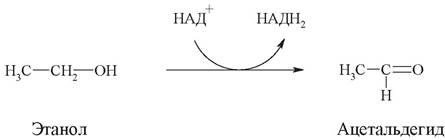
К числу ферментов с групповой специфичностью относятся пищеварительные ферменты. Так, пепсин, относящийся к протеазам, расщепляет пептидные связи в белках как животного, так и растительного происхождения, отличающихся по аминокислотному составу. Основным местом действия пепсина является пептидная связь -СО-NH-. Липазы, расщепляющие сложноэфирные связи, катализируют гидролиз жиров на глицерин и жирные кислоты, но не действуют на пептидные связи.
Стереохимическая специфичность обусловлена существованием оптически изомерных L- и D-форм или геометрических изомеров химических веществ. Например, фермент фумараза катализирует превращение фумаровой кислоты (трансизомер), но не действует на малеиновую кислоту (цис-изомер):
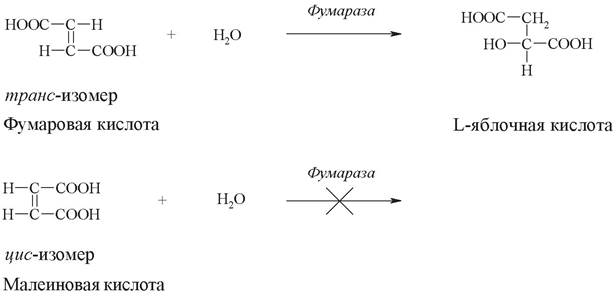
Большинство ферментов, участвующих в превращениях аминокислот, действуют лишь на Z-изомеры, а ферменты, катализирующие превращения углеводов - на D-изомеры углеводов.
Таким образом, благодаря специфичности действия, ферменты обеспечивают протекание с высокой скоростью лишь определенных реакций из огромного разнообразия возможных превращений в микропространстве клеток и целостном организме, регулируя тем самым интенсивность обмена веществ.
1.6. Механизм действия ферментов
Любая ферментативная реакция включает несколько промежуточных этапов (рис. 4):
Рис. 4. Основные этапы ферментативного катализа
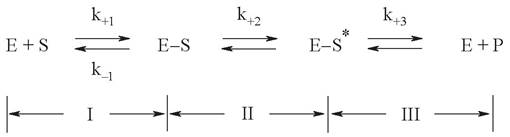
Этап I - сорбция субстрата (S) субстратсвязывающим участком активного центра фермента (Е) с образованием ферментсубстратного комплекса (E-S). Этот этап реализуется за счет образования слабых невалентных взаимодействий, поэтому полностью обратим. Конформационные изменения в процессе сорбции усиливают пространственное соответствие активного центра и субстрата.
Этап II - ковалентное преобразование субстрата в составе ферментсубстратного комплекса, в результате чего появляется комплекс с химически измененным субстратом (E-S*). В этом этапе участвует собственно каталитический центр, который обеспечивает разрыв одних и формирование других химических связей.
Поэтому данный этап необратим, за исключением собственно обратимых реакций. Необходимость ковалентных превращений делает этап II самой медленной стадией, лимитирующей скорость всего ферментативного процесса.
Этап III - десорбция готового продукта реакции (Р) из комплекса E-S*, которая сопровождается освобождением фермента в его исходном виде. Этот этап, как и этап II, является необратимым (за исключением катализа обратимых реакций).
1.7. Основы кинетики ферментативных реакций
Кинетика изучает влияние различных факторов на скорость реакции. Общие принципы кинетики химических реакций применимы и к ферментативным реакциям. Скорость ферментативной реакции измеряют по убыли субстрата или приросту продукта реакции за единицу времени. Принято измерять начальную скорость реакции, чтобы свести к минимуму влияние таких факторов, как уменьшение концентрации субстрата, обратимость реакции, образование продуктов, тормозящих реакцию. В качестве единиц скорости реакции используют моль/с или мкмоль/мин.
Интервал времени, в течение которого скорость реакции равна начальной скорости или близка к ней, соответствует прямолинейному участку графика зависимости скорости реакции от времени (рис. 5).
Рис. 5. Зависимость скорости ферментативной реакции от времени. Начальная скорость (v0) увеличивается пропорционально концентрации фермента (Е)
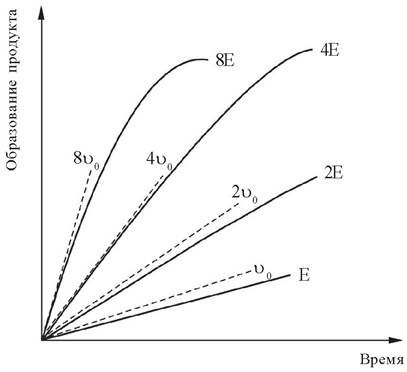
Эксперименты in vitro позволяют исследовать ферментативную реакцию, варьируя тот или иной параметр при соблюдении постоянства остальных.
1.7.1. Зависимость скорости реакции от концентрации фермента
Зависимость скорости реакции от концентрации фермента изучают, варьируя количество фермента при достаточно высокой концентрации субстрата. В этих условиях скорость реакции в интервале времени, соответствующем начальной скорости реакции, прямо пропорциональна концентрации фермента в реакционной смеси (рис. 6).
Рис. 6. Зависимость скорости ферментативной реакции от концентрации фермента [E] при достаточно высокой концентрации субстрата
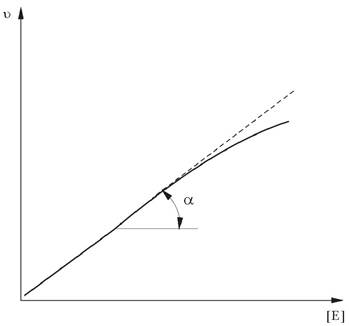
Разделив скорость реакции, измеренную на линейном участке, на концентрацию фермента в реакционной смеси, получают параметр - активность фермента. Активность фермента - это скорость ферментативной реакции, отнесенная к концентрации фермента. По сути, это - тангенс угла наклона линейного участка к оси абсцисс. Ферменты могут находиться в разном функциональном состоянии, поэтому параметры «активность фермента» и «количество фермента» могут не совпадать. Активность фермента характеризует не количество, а эффективность фермента.
Для оценки количества фермента Международная система единиц (СИ) рекомендует единицу «катал». Катал - это такое количество фермента, которое преобразует 1 моль субстрата за 1 с.
Для биологических объектов данная единица измерения чрезмерно велика, поэтому используют единицу нанокатал. Обычно применяют более удобную международную единицу (МЕ). МЕ - это количество фермента, которое преобразует 1 мкмоль субстрата за 1 мин.
1.7.2. Влияние концентрации субстрата на скорость реакции
Влияние концентрации субстрата можно исследовать путем измерения скорости реакции в серии проб с постоянной концентрацией фермента, но возрастающей концентрацией субстрата.
График зависимости скорости ферментативной реакции (v) от концентрации субстрата при фиксированной концентрации фермента представляет собой гиперболу (рис. 7).
Рис. 7. Зависимость скорости реакции ферментативной реакции от концентрации субстрата при постоянной концентрации фермента
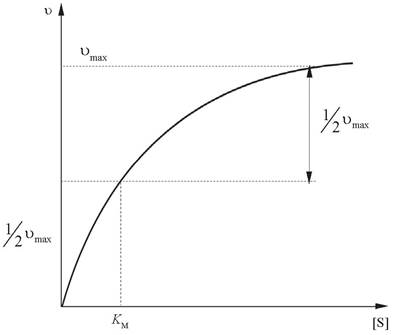
Вначале скорость реакции прямо пропорциональна концентрации субстрата, при ее дальнейшем увеличении скорость реакции постепенно достигает максимального значения. Это означает, что все связывающие участки фермента заняты (насыщены). Скорость реакции на этом участке не зависит от концентрации субстрата. Такую кривую называют кривой субстратного насыщения.
Уравнение, описывающее кривую субстратного насыщения, было предложено Михаэлисом и Ментен и носит их имена (уравнение Михаэлиса - Ментен):
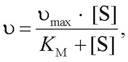
где [S] - концентрация субстрата;
Ʋ - скорость реакции при данной концентрации субстрата;
КМ - константа Михаэлиса.
Ʋmax и КМ - главные кинетические константы, характеризующие фермент в его реакции с данным субстратом.
Легко рассчитать, если Ʋ = 1/2 Ʋmax, то КМ = [S], т. е. КМ - это концентрация субстрата, при которой скорость реакции составляет 1/2 Ʋmax. Константу Михаэлиса можно вычислить по графику. Отрезок на абсциссе, соответствующий скорости, равной половине максимальной, представляет собой КМ.
Ʋmax - максимальная скорость данной ферментативной реакции, т. е. предельное значение, к которому стремится скорость реакции при бесконечно большом увеличении концентрации субстрата.
С целью упрощения определения величины vmax и КМ уравнение Михаэлиса - Ментен можно линеаризовать:
1/Ʋ = Км + [S]/ Ʋmax • [S]
1/Ʋ = KM/ Ʋmax • [S] + 1/ Ʋmax.
1/Ʋ = KM/ Ʋmax - 1/[S] + 1/ Ʋmax - уравнение Лайнуивера - Берка.
Уравнение, описывающее график Лайнуивера - Берка, - это уравнение прямой линии y = kx + b, где 1/Ʋmax - это отрезок, отсекаемый прямой на оси ординат; KM/Ʋmax - тангенс угла наклона прямой; пересечение прямой с осью абсцисс дает величину 1/KM (рис. 8). График Лайнуивера - Берка позволяет определить КМ по относительно небольшому числу точек. Этот график также используют при оценке действия ингибиторов.
Рис. 8. График Лайнуивера - Берка
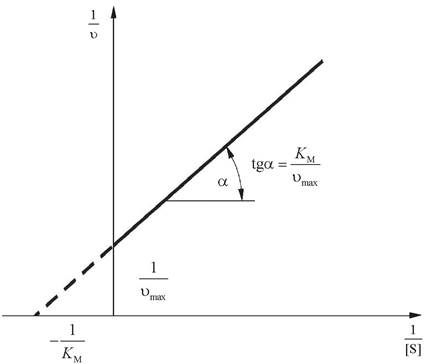
Значения КМ изменяются в широких пределах: от 10-6 моль/л для очень активных ферментов до 10-2 моль/л для малоактивных ферментов. Оценки КМ имеют практическое значение. При концентрациях субстрата, в 100 раз превышающих KM, фермент будет работать практически с максимальной эффективностью, поэтому Ʋmax будет отражать количество присутствующего активного фермента. Это обстоятельство используют для оценки содержания фермента в препарате. Кроме того, КМ является характеристикой фермента.
1.7.3. Зависимость скорости ферментативной реакции от температуры
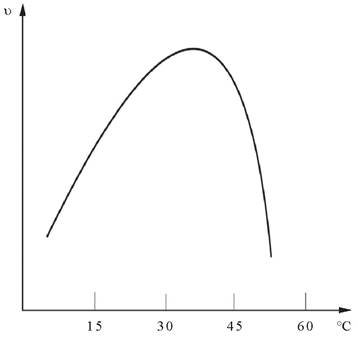
Ферменты, вещества белковой природы, проявляют максимальную активность в ограниченном температурном интервале (рис. 9). При температурах до 40-50 °С скорость реакции увеличивается согласно теории химической кинетики, т. е. в соответствии с правилом Вант-Гоффа возрастает примерно в 2 раза. При более высоких температурах тепловая денатурация приводит к уменьшению количества активного фермента и в конечном итоге - к полному прекращению ферментативной реакции. Термолабильность отличает ферменты от неорганических катализаторов.
Рис. 9. Зависимость скорости ферментативной реакции (Ʋ) от температуры среды
1.7.4. Зависимость скорости ферментативной реакции от рН
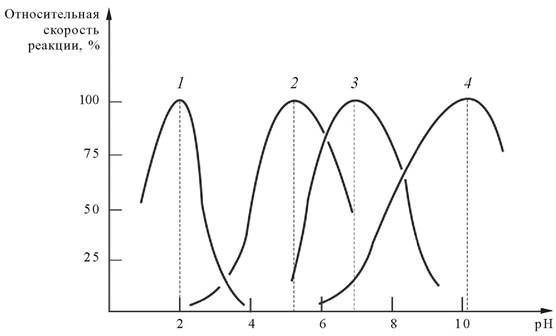
Оптимум рН действия большинства ферментов лежит в пределах физиологических значений 6,0-8,0. Пепсин активен при рН 1,5 — 2,0, что соответствует кислотности желудочного сока. Аргиназа, специфический фермент печени, активен при 10,0. Влияние рН среды на скорость ферментативной реакции связывают с состоянием и степенью ионизации ионогенных групп в молекуле фермента и субстрата (рис. 10). Этот фактор определяет конформацию белка, состояние активного центра и субстрата, формирование фермент-субстратного комплекса, собственно процесс катализа.
Рис. 10. Влияние рН среды на скорость ферментативной реакции: 1 - пепсин; 2 - лизоцим; 3 - амилаза слюны; 4 - аргиназа
1.8. Ингибирование активности ферментов
Важной особенностью ферментов является их инактивация под влиянием определенных ингибиторов. Ингибиторы - это вещества, вызывающие частичное или полное торможение ферментативных реакций. Ингибирование ферментативной активности может быть необратимым или обратимым, конкурентным или неконкурентным.
Необратимое ингибирование - это стойкая инактивация фермента, возникающая в результате ковалентного связывания молекулы ингибитора в активном центре или в другом особом центре, изменяющем конформацию фермента. Диссоциация столь устойчивых комплексов с регенерацией свободного фермента практически исключена. Для преодоления последствий такого ингибирования организм должен синтезировать новые молекулы фермента.
Обратимое ингибирование характеризуется равновесным комплексообразованием ингибитора с ферментом за счет нековалентных связей, вследствие чего такие комплексы способны к диссоциации с восстановлением активности фермента.
Классификация ингибиторов на конкурентные и неконкурентные основана на том, что ослабляется (конкурентное ингибирование) или не ослабляется (неконкурентное ингибирование) их действие при повышении концентрации субстрата.
Конкурентные ингибиторы - это, как правило, вещества, структура которых сходна со структурой субстрата. Данное обстоятельство позволяет им связываться в том же активном центре, что и субстрат, препятствуя взаимодействию фермента с субстратом уже на стадии связывания. После связывания ингибитор может быть превращен в некий продукт или остается в активном центре, пока не произойдет диссоциация.
Обратимое конкурентное ингибирование можно представить в виде схемы:
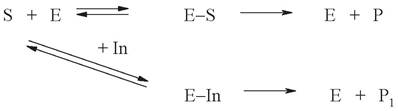
Степень ингибирования фермента определяется соотношением концентраций субстрата и ингибитора. Классическим примером подобного типа ингибирования является торможение активности фермента сукцинатдегидрогеназы малонатом, который вытесняет сукцинат из субстратного участка и препятствует его превращению в фумарат.
При необратимом ингибировании имеет место ковалентное связывание ингибитора в активном центре. Примером необратимого ингибирования может служить инактивация фермента триозофосфатизомеразы трихлорацетолфосфатом. Этот ингибитор является структурным аналогом субстрата - диоксиацетонфосфата и необратимо присоединяется к остатку глутаминовой кислоты в активном центре.
1.9. Классификация и номенклатура ферментов
Современные классификация и номенклатура ферментов были разработаны Комиссией по ферментам Международного биохимического союза, учрежденной в 1956 г., и утверждены на V Международном биохимическом конгрессе в 1961 г. в Москве (табл. 3). Эта классификация и номенклатура действуют и поныне, пополняясь вновь открываемыми ферментами.
Таблица 3. Международная классификация ферментов
№ п/п |
Класс |
Тип катализируемой реакции |
1 |
Оксидоредуктазы |
Окисление - восстановление (перенос электронов и протонов) |
2 |
Трансферазы |
Межмолекулярный перенос групп атомов, отличных от атомов водорода |
3 |
Гидролазы |
Гидролиз различных связей (с участием молекулы воды) |
4 |
Лиазы |
Расщепление связей углерода с кислородом, азотом, серой или другим углеродом без участия молекул воды |
5 |
Изомеразы |
Внутримолекулярный перенос групп с образованием изомерных форм |
6 |
Лигазы (синтетазы) |
Соединение двух молекул и образование связей С-С, С-О, С-S и С-N, сопряженное с разрывом макроэргической связи (АТФ или его аналогов) |
Согласно действующей классификации все ферменты разделены на шесть классов по типу катализируемой реакции (см. табл. 3). Каждый фермент имеет свой шифр.
Ввиду многообразия ферментов, входящих в каждый класс, они делятся на подклассы, а те в свою очередь - на подподклассы.
Согласно номенклатуре, наименование фермента должно состоять из названия его субстрата и обозначения типа катализируемой реакции, которое заканчивается окончанием -аза. Если в реакции участвуют два субстрата, то приводятся названия обоих (разделенны двоеточием). Отсюда - громоздкость систематических наименований. Поэтому было решено «узаконить» употребление и многих рабочих названий, которые гораздо короче и удобнее:
1. Оксидоредуктазы - ферменты, катализирующие окислительно-восстановительные реакции. Для ферментов этого класса характерны следующие особенности:
- они формируют окислительно-восстановительные системы;
- катализируют реакции, связанные с высвобождением энергии;
- являются сложными ферментами, в качестве коферментов действуют НАД, ФАД, гем, KoQ.
Научное (систематическое) название: название донора электронов: название акцептора электронов и название класса.
Рабочее название: где возможно, используется термин дегидрогеназа или редуктаза. Если акцептором электронов является кислород - оксидаза.
Пример:

Научное название фермента: L-лактат: НАД+-оксидоредуктаза.
Рабочее название: лактатдегидрогеназа.
2. Трансферазы - класс ферментов, катализирующих реакции переноса атомных групп или молекулярных остатков от одного субстрата к другому. В зависимости от типа переносимой группы выделяют подклассы:
- фосфотрансферазы (-РО3Н2);
- аминотрансферазы (-NH2);
- метилтрансферазы (-СН3);
- ацилтрансферазы![]() и др.
и др.
Научное название фермента: донор переносимой группы: акцептор группы: название группы и название класса.
Рабочее название: донор группы + трансфераза или акцептор: группа + трансфераза.
Пример:
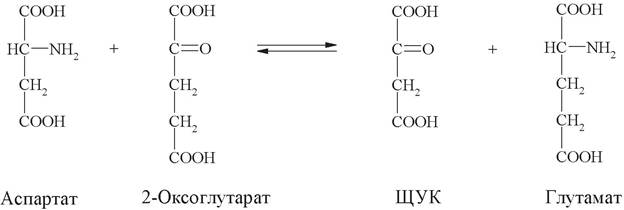
Научное название фермента: аспартат: 2-оксоглутаратаминотрансфераза. Рабочее название: аспартатаминотрансфераза.
3. Гидролазы - ускоряют реакции гидролитического расщепления. Подкласс указывает на природу расщепляемой связи:
- эстеразы (расщепляют сложноэфирную связь);
- гликозидазы (расщепляют гликозидную связь);
- пептидазы (гидролизуют пептидную связь).
Научное название фермента: название субстрата: отщепляемая группа + название класса.
Рабочее название: название субстрата с окончанием -аза.
Пример:
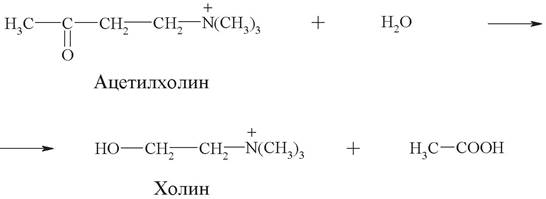
Научное название фермента: ацетилхолин-ацетилгидролаза.
Рабочее название: ацетилхолинэстераза.
4. Лиазы. К классу лиаз относят ферменты, катализирующие разрыв связей С-О, С-С, С-N и др., а также обратимые реакции отщепления различных групп от субстратов негидролитическим путем. Эти реакции сопровождаются образованием двойной связи или присоединением групп к месту разрыва двойной связи.
Научное название фермента: название субстрата: отщепляемая группа + название класса.
Рабочее название: название субстрата + класс.
Пример:
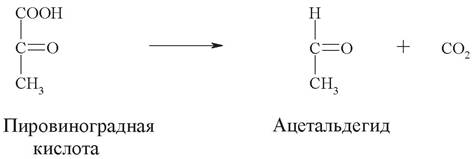
Научное название: пируваткарбоксилиаза.
Рабочее название: пируватдекарбоксилаза.
5. Изомеразы. К данному классу относят ферменты, катализирующие взаимопревращения изомеров. Исходя из типа катализируемой реакции, выделяют пять подклассов:
- рацемазы и эпимеразы (катализируют взаимопревращение оптических изомеров);
- цис-транс-изомеразы (катализируют взаимопревращение геометрических изомеров);
- внутримолекулярные оксидоредуктазы;
- внутримолекулярные трансферазы (мутазы);
- внутримолекулярные лиазы.
6. Лигазы (синтетазы). К классу лигаз относят ферменты, катализирующие синтез органических веществ из двух исходных молекул с использованием энергии распада АТФ (или другого нуклеозидтрифосфата). Систематическое название их составляют по форме «X : Y лигаза», где X и Y обозначают исходные вещества. В качестве примера можно назвать Z-глутамат: аммиак лигазу (рекомендуемое сокращенное название «глутаминсинтетаза»), при участии которой из глутаминовой кислоты и аммиака в присутствии АТФ синтезируется глутамин.
Вопросы для проверки усвоения материала
1. Ферменты: определение, значение в живых системах. Строение ферментов: активный центр, аллостерический центр, их функции.
2. Коферменты и кофакторы, химическая природа и функции. Роль витаминов в проявлении каталитической активности ферментов. Сравнительная характеристика ферментов и небиологических катализаторов.
3. Механизм ферментативного катализа.
4. Международная классификация и номенклатура ферментов: принцип построения, шифры ферментов. Характеристика классов ферментов (оксидоредуктазы, трансферазы, гидролазы, лиазы, изомеразы, лигазы).
5. Регуляция активности ферментов. Зависимость скорости ферментативной реакции от концентрации фермента, субстрата, температуры и рН среды. Уравнения
Михаэлиса - Ментен и Лайнуивера - Берка, константа Михаэлиса, кривая субстратного насыщения. Конкурентные и аллостерические модуляторы.
6. Локализация ферментов в клетке. Ферменты клеточных органелл (ядро, митохондрии, рибосомы, лизосомы, аппарат Гольджи, эндоплазматическая сеть, цитоскелет, клеточный центр).
Письменное домашнее задание
Обязательное
1. Составьте структурную формулу трипептида H2N-Val-Cys-Asp-COOH и определите, в какой области рН находится его изоэлектрическая точка.
2. При формировании третичной структуры гормона инсулина оказываются пространственно сближенными следующие фрагменты полипептидной цепи:
Leu-Val-Cys-Gly-Glu-Arg, Leu-Glu-Asn-Tyr-Cys-Asp.
Какие типы связей между боковыми радикалами аминокислот могут при этом образоваться?
3. На схеме представлено 5 химических реакций, протекающих в организме, в которых принимают участие аспарагиновая кислота (аспартат) и аспарагин.
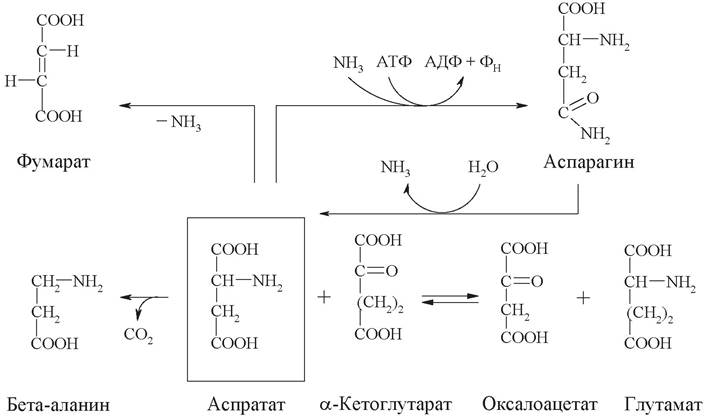
Запишите уравнения реакций, укажите классы катализирующих их ферментов и дайте название каждому ферменту по систематической номенклатуре.
4. Фермент дипептидаза из слизистой оболочки тонкой кишки катализирует реакцию гидролиза дипептида глицилглицина. В следующей таблице представлена зависимость скорости ферментативной реакции от концентрации субстрата в отсутствие и в присутствии модулятора - трасилола:
Концентрация субстрата, ммоль/л |
Скорость реакции, ммоль/с |
|
В отсутствие трасилола |
В присутствии трасилола |
|
0,1 |
0,33 |
0,06 |
0,5 |
1,00 |
0,28 |
1,0 |
1,33 |
0,50 |
2,0 |
1,6 |
0,80 |
4,0 |
1,78 |
1,14 |
8,0 |
1,88 |
1,45 |
Задание:
а) напишите уравнение реакции гидролиза дипептида;
б) постройте график зависимости скорости реакции от концентрации субстрата в обоих случаях в координатах Михаэлиса - Ментен и Лайнуивера - Берка;
в) определите максимальную скорость реакции и константу Михаэлиса;
г) какой вид модуляции активности фермента имеет место в данном случае?
д) с каким участком молекулы фермента связывается модулятор?
Дополнительное
1. На схеме представлено 5 химических реакций, протекающих в организме, в которых принимают участие глутаминовая кислота и глутамин.
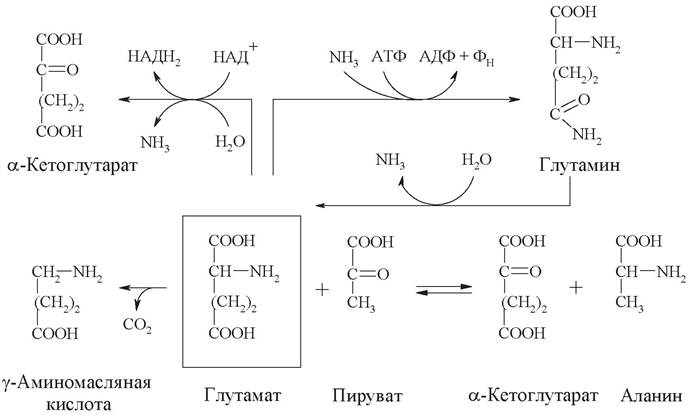
Запишите уравнения реакций, укажите классы катализирующих их ферментов и дайте название каждому ферменту по систематической номенклатуре.
2. Фермент фосфофруктокиназа катализирует реакцию превращения фрукто- зо-6-фосфата во фруктозо-1,6-дифосфат. В таблице представлена зависимость скорости ферментативной реакции от концентрации фруктозо-6-фосфата в отсутствие и в присутствии модулятора - цитрата (лимонной кислоты):
Концентрация фруктозо-6-фосфата, мкмоль/л |
Скорость реакции, мкмоль/с |
|
В отсутствие цитрата |
В присутствии цитрата |
|
0,5 |
1,7 |
0,7 |
1,0 |
2,5 |
1,0 |
5,0 |
4,2 |
1,7 |
10,0 |
4,5 |
1,8 |
15,0 |
4,7 |
1,9 |
20,0 |
4,8 |
1,9 |
Задание:
а) постройте график зависимости скорости реакции от концентрации субстрата в обоих случаях в координатах Михаэлиса - Ментен и Лайнуивера - Берка;
б) определите максимальную скорость реакции и константу Михаэлиса;
в) какой вид модуляции активности фермента имеет место в данном случае?
г) с каким участком молекулы фермента связывается модулятор?
Типовой вариант тестового контроля по теме «Ферменты»
Инструкция: при отсутствии дополнительных указаний в вопросе теста выберите один верный вариант ответа.
1. Выберите название фермента, катализирующего следующую реакцию:
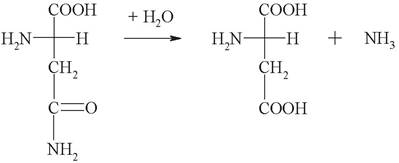
а) аспарагин: аммиак лигаза;
б) аспарагинаминотрансфераза;
в) аспарагин: аммиак лиаза;
г) аспарагин: Н2О оксидоредуктаза;
д) аспарагин: аммиак гидролаза.
2. Фермент липаза катализирует гидролиз триглицеридов в жировой ткани. Под действием другого фермента - протеинкиназы - к молекуле липазы присоединяются фосфатные группы, что увеличивает активность липазы. Как называется такой тип регуляции активности фермента:
а) конкурентный;
б) аллостерический;
в) ковалентная модификация;
г) индукция-репрессия.
3. Выберите общее свойство ферментов и небиологических катализаторов:
а) активность регулируется активаторами и ингибиторами;
б) действуют только при низких температурах;
в) способны ускорять реакции до 1017 раз;
г) обладают высокой специфичностью к субстрату;
д) снижают энергетический барьер реакции.
4. Какую роль играют водорастворимые витамины в ферментативном катализе:
а) являются простыми ферментами;
б) являются сложными ферментами;
в) служат предшественниками коферментов;
г) служат аллостерическими центрами ферментов;
д) являются конкурентными ингибиторами ферментов.
5. В каких клеточных органеллах содержатся ферменты, отвечающие за репликацию и репарацию ДНК:
а) эндоплазматическая сеть;
б) ядро;
в) рибосомы;
г) аппарат Гольджи;
д) лизосомы.
6. Какая характеристика фермента остается неизменной при денатурации:
а) растворимость в воде;
б) биологическая активность;
в) константа Михаэлиса;
г) первичная структура;
д) вязкость раствора.
7. С активным центром фермента, содержащим серин, глутаминовую кислоту и валин, наиболее вероятно будет взаимодействовать:
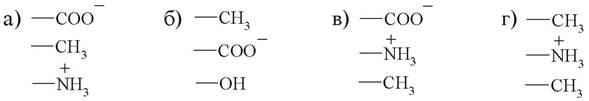
8. Какой ученый предложил теорию, согласно которой в процессе ферментативного катализа происходит взаимное приспособление фермента и субстрата по геометрическому и электронному строению:
а) Э. Фишер;
б) Л. Михаэлис;
в) М. Ментен;
г) Д. Кошланд;
д) Э. Корниш-Боуден.
9. Вставьте пропущенные слова (3 ответа) в предложение: «Обратимый конкурентный ингибитор структурно подобен ..., присоединяется к ... центру фермента и вытесняется из него избытком ...»
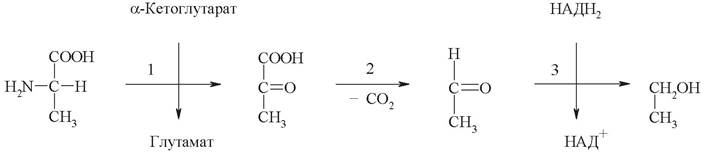
10. Напишите названия и номера классов ферментов (6 ответов), катализирующих реакции 1, 2 и 3: