БИОХИМИЯ - В. В. Емельянов - 2016
РАЗДЕЛ 2. БИОЛОГИЧЕСКОЕ ОКИСЛЕНИЕ
2.1. Этапы энергетического обмена
Неотъемлемым свойством живого является обмен веществ (метаболизм) - совокупность разнообразных биохимических процессов, в результате которых поступающие питательные вещества усваиваются, происходит освобождение энергии и синтез необходимых организму соединений. Метаболизм состоит из двух частей: анаболизма (синтеза сложных веществ из более простых с затратой энергии) и катаболизма (распада более сложных веществ до более простых с выделением энергии). Анаболизм и катаболизм неразрывно связаны между собой: анаболизм поставляет катаболизму вещество, катаболизм поставляет анаболизму энергию. Однако в условиях постоянной температуры передача энергии в виде тепла от одного химического процесса другому невозможна. Поэтому в живых системах имеет место передача энергии посредством особых макроэргических соединений, обладающих значительным запасом энергии. Универсальным макроэргическим соединением во всех клетках служит аденозинтрифосфорная кислота (аденозинтрифосфат, АТФ).
Нередко катаболизм образно называют «горением», говорят, что питательные вещества «сгорают». Аналогия между горением и катаболизмом весьма условна. В обоих случаях мы имеем химическое превращение (окисление) органических веществ в СО2 и Н2О в присутствии кислорода. Однако горение - процесс молниеносный, нерегулируемый и неэффективный (вся энергия рассеивается в виде тепла). Напротив, при катаболизме энергия органических веществ выделяется порциями на различных его этапах, достаточно эффективно запасается при синтезе АТФ, а процесс регулируется потребностью клетки в энергии. Установлено, что КПД системы синтеза АТФ в клетке составляет 40-45 %. Баланс между синтезом и расходом АТФ строго соблюдается, поэтому количество АТФ, присутствующее в клетке в каждый момент времени, невелико. Зато масса АТФ, образующаяся и расходующаяся за сутки в организме взрослого человека, сопоставима с массой его тела!
Рассмотрим подробнее «бюджет» метаболизма: в чем заключается суть процессов синтеза АТФ и на какие нужды клетки его расходуют. Известно два способа синтеза АТФ: аэробный (окислительное фосфорилирование) и анаэробный (субстратное фофорилирование). Анаэробный катаболизм представляет собой неполное окисление органических веществ, характерен только для углеводов (гликолиз), сопровождается образованием молочной кислоты и малым энергетическим выходом - 2 молекулы АТФ на 1 молекулу глюкозы. В физиологических условиях анаэробный катаболизм дает не более 10 % всей АТФ в клетке. Исключением из этого общего правила являются скелетные мышцы: в белых мышечных волокнах основное количество АТФ синтезируется анаэробным путем. Кроме того, гликолиз становится единственно возможным путем продукции АТФ в любой клетке при дефиците кислорода - гипоксии. Однако анаэробный катаболизм в большинстве случаев не способен длительно поддерживать жизнедеятельность клеток. Так, хорошо известно, что самые чувствительные к гипоксии клетки - нейроны коры больших полушарий головного мозга - могут прожить без кислорода не более 5 мин.
Большинство клеток получают свыше 90 % необходимой АТФ за счет аэробного катаболизма. Это высокоэффективный биохимический процесс полного окисления органических веществ (углеводов, липидов и белков) до неорганических соединений СО2 и Н2О в присутствии кислорода. Аэробное окисление 1 молекулы глюкозы дает возможность синтезировать 38 молекул АТФ, похожие значения дает окисление аминокислот, а полное окисление липидов поставляет клетке сотни молекул АТФ на 1 молекулу вещества. Большинство клеток могут использовать все три класса питательных веществ как источник энергии. Тем не менее, в их использовании наблюдается очередность: углеводы служат первым энергетическим «топливом», при исчерпании запасов которых клетки переходят на катаболизм липидов. Белки подвергаются катаболизму в последнюю очередь, в экстремальных ситуациях, например, при длительном голодании.
Весь синтезируемый фонд АТФ клетки расходуют на совершение различных видов полезной работы. Во-первых, это химическая работа - реакции анаболизма, по определению требующие затраты АТФ. Сюда относятся все биосинтезы в клетках, в особенности самые «дорогостоящие» - синтезы биополимеров (белков, ДНК и РНК, полисахаридов) и липидов. Во-вторых, это механическая работа - процессы перемещения клеток и их органелл в пространстве, в том числе и мышечное сокращение. Наконец, это осмотическая работа - процессы активного транспорта веществ через биологические мембраны, направленные на создание разности концентраций этих веществ внутри клетки и во внеклеточной жидкости. Если в роли таких веществ выступают зараженные частицы - ионы К+, Na+, Ca2+, Cl-, то формируется не только разность концентраций, но и разность потенциалов. В этом случае говорят о совершении электрической работы. Однако следует помнить, что КПД всех этих видов работы существенно ниже 100 %. Оставшаяся доля энергии АТФ переходит в тепло. В этом заключается еще одна важная функция всех процессов распада АТФ - функция теплопродукции.
В энергетическом обмене принято различать следующие основные этапы.
Подготовительный этап. Включает в себя реакции гидролиза в желудочно-кишечном тракте питательных веществ до их мономеров: белков - до аминокислот, полисахаридов - до моносахаридов (в основном глюкозы), липидов - до жирных кислот и глицерина. Данный этап необходим, чтобы сделать питательные вещества доступными для каждой клетки, поскольку крупные молекулы не подвергаются всасыванию в кровь.
Промежуточный обмен. Включает многочисленные биохимические реакции аминокислот, глюкозы, жирных кислот и глицерина, направленные на их превращение в ограниченный круг «малых» молекул - пировиноградной кислоты, ацетилкоэнзима А и ряда других. Промежуточный обмен не требует затраты кислорода и протекает с синтезом небольшого количества АТФ в реакциях субстратного фосфорилирования.
Терминальный (заключительный) этап. Происходит полное окисление продуктов промежуточного обмена до неорганических веществ. Этот этап протекает в митохондриях клеток, где происходит потребление кислорода и образование СО2 и Н2О, и в ходе окислительного фосфорилирования синтезируется основное количество АТФ.
2.2. Цикл Кребса
Цикл Кребса (цикл трикарбоновых кислот, ЦТК) является процессом окисления ацетилкоэнзима А - универсального продукта катаболизма углеводов, липидов и белков. ЦТК протекает в митохондриях с участием 8 ферментов, которые локализованы в матриксе в свободном состоянии или на внутренней поверхности внутренней мембраны.
Основной функцией ЦТК является образование восстановленных коферментов НАДН2 и ФАДН2, которые поставляют протоны в дыхательную цепь. Кроме того, субстраты ЦТК могут использоваться для глюконеогенеза, переаминирования, синтеза гема, жирных кислот. Таким образом, ЦТК интегрирует все виды обмена веществ.
2.2.1. Реакции ЦТК
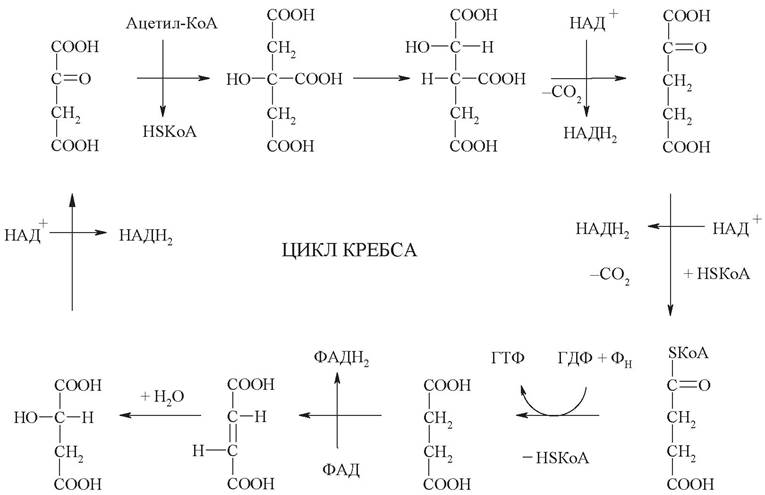
1. Цитратсинтаза катализирует превращение оксалоацетата и ацетилкоэнзима А в лимонную кислоту (цитрат):
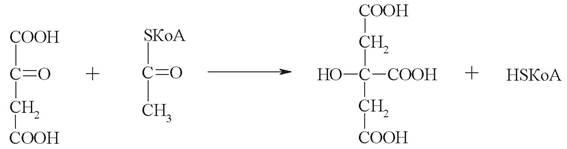
2. Аконитаза превращает цитрат в изолимонную кислоту (изоцитрат). Сначала происходит дегидратация цитрата с образованием промежуточного продукта - цис-аконитовой кислоты (цис-аконитата). Данное соединение не выходит из активного центра фермента, поэтому его формулу принято обозначать в квадратных скобках. Завершает реакцию присоединение воды по двойной связи с образованием изоцитрата:
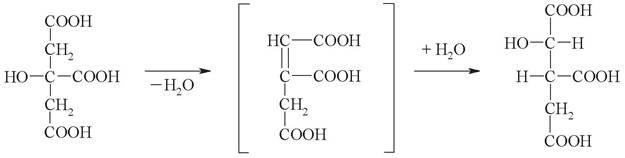
3. Изоцитратдегидрогеназа декарбоксилирующая катализирует окислительное декарбоксилирование изоцитрата. Сначала гидроксильная группа изоцитрата окисляется до кетоновой, образуется щавелевоянтарная кислота (оксалосукцинат). Затем оксалосукцинат теряет карбоксильную группу в виде СО2, образуется α-кетоглутарат:
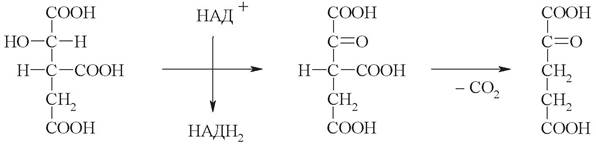
4. Следующая стадия ЦТК - окислительное декарбоксилирование α-кетоглутарата. Она катализируется а-кетоглутаратдегидрогеназным комплексом, состоящим из 3 ферментов и 5 коферментов: тиаминдифосфата, кофермента А, липоамида, НАД+, ФАД. Продукт реакции - сукцинилкоэнзим А - макроэргическое соединение:
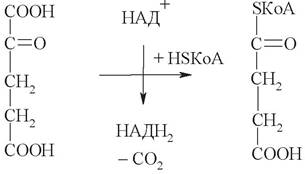
5. Синтез янтарной кислоты (сукцината) ферментом сукцинилкоэнзим А синтетазой. Энергия макроэргической тиоэфирной связи в молекуле сукцинилкоэнзима А затрачивается на синтез молекулы ГТФ из ГДФ и фосфата - это единственная в ЦТК реакция субстратного фосфорилирования:
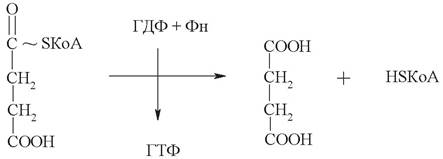
6. Сукцинатдегидрогеназа, флавопротеин внутренней мембраны митохондрии, катализирует окисление сукцината до фумаровой кислоты (фумарата):
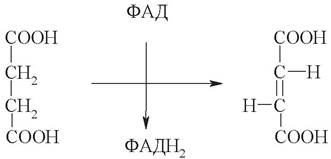
7. Фумараза стереоспецифично присоединяет воду по двойной связи фумарата с образованием L-яблочной кислоты (L-малата):
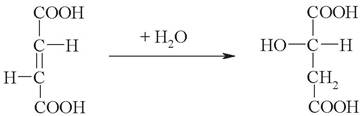
8. Малатдегидрогеназа замыкает ЦТК окислением гидроксильной группы L-малата с образованием оксалоацетата, который затем реагирует с новой молекулой ацетилкоэнзима А, и цикл повторяется вновь:
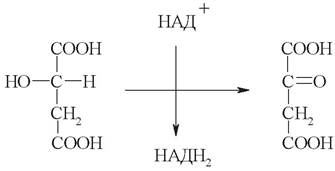
Общая схема реакций ЦТК представлена на рис. 11.
Рис. 11. Общая схема реакций цикла Кребса
2.2.2. Энергетический баланс одного оборота ЦТК
В 4 окислительно-восстановительных реакциях ЦТК образуются 3 НАДН2 и 1 ФАДН2, которые направляются далее в дыхательную цепь окислительного фосфорилирования. В процессе окислительного фосфорилирования в дыхательной цепи из 1 НАДН2 образуется 3 АТФ, из 1 ФАДН2 - 2 АТФ. Из 1 ГТФ, образующегося в ЦТК за счет субстратного фосфорилирования, синтезируется 1 АТФ. Таким образом, за 1 оборот ЦТК синтезируется 12 АТФ.
2.3. Тканевое дыхание и окислительное фосфорилирование
Заключительным этапом энергетического обмена служат протекающие в митохондриях тканевое дыхание и окислительное фосфорилирование. Тканевое дыхание - потребление кислорода в дыхательной цепи митохондрий с энергетической целью. Функцию тканевого дыхания выполняет комплекс ферментов, локализованных на внутренней мембране митохондрий. Окислительное фосфорилирование - синтез АТФ на внутренней мембране митохондрий в присутствии кислорода. Процесс окислительного фосфорилирования катализируется ферментом АТФ-синтазой. Краткая характеристика структуры компонентов, необходимых для синтеза АТФ в митохондриях, представлена в табл. 4. Перейдем к рассмотрению механизма их работы.
Компоненты дыхательной цепи располагаются в мембране в порядке повышения их сродства к электрону (ё). Таким образом, е перемещается по дыхательной цепи от веществ с низким сродством к ë к веществам с более высоким сродством к ё. Окисление НАДН2 происходит следующим образом:
а) пара ё и протонов (Н+) переносятся с НАДН2 на флавопротеин - НАДН-дегидрогеназу, которая направляет пару Н+ в межмембранное пространство, а пару ё - на железосерные центры (FeS-центры) дыхательной цепи.
б) убихинон принимает пару ё от железосерных центров и пару Н+ из матрикса, превращаясь в восстановленный убихинон, затем переносит пару Н+ в межмембранное пространство, а пару ё - на цитохром b566.
Таблица 4. Компоненты системы синтеза АТФ в митохондриях
№ п/п |
Компонент |
Локализация |
Особенности структуры |
Функции |
|
1 |
Субстраты и ферменты БО |
НАД-зависимые - в матриксе, ФАД-зависимые - во внутренней мембране |
НАД-зависимые субстраты: изоцитрат, α-кетоглутарат, малат, пируват, глутамат, β-оксиацилКоА. ФАД-зависимые субстраты, сукцинат, ацилКоА, α-глицеролфосфат |
Восстановление НАД+ и ФАД, поставщики Н+в дыхательную цепь |
|
2 |
Дыхательная цепь |
НАДН-дегидрогеназа |
Внутренняя мембрана |
Флавопротеин; кофермент - ФМН; FeS-центр |
Перенос ё и Н+ с НАДН2 |
Убихинон (коэнзим Q10) |
Внутренняя мембрана |
Производное хинона + радикал из 10 изопреновых звеньев |
Перенос ё и Н+ с ФАДН2 |
||
Цитохромы b566 —> b582 —> c1 —> c — > a —> a3 |
Внутренняя мембрана |
Гемопротеины; кофермент - гем, у цитохромоксидазы - дополнительно атом Сu |
Перенос ё на конечный акцептор - кислород |
||
3 |
АТФ-синтаза |
Внутренняя мембрана и матрикс |
F0 - субъединица в мембране; F1- субъединица обращена в матрикс |
Транспорт Н+ из межмембранного пространства в матрикс и фосфорилирование АДФ |
|
4 |
Транслоказа адениловых нуклеотидов |
Внутренняя мембрана |
Белок-антипортер |
Перенос АТФ из матрикса в межмембранное пространство в обмен на АДФ |
|
5 |
Переносчик фосфата |
Внутренняя мембрана |
Белок-антипортер |
Перенос фосфата из межмембранного пространства в матрикс в обмен на ОН- |
|
в) ё от цитохрома b566 передаются на цитохром b582, а затем на убихинон, принимающий пару Н+ из матрикса и превращающийся в восстановленный убихинон. Затем восстановленный убихинон вновь передает пару Н+ в межмембранное пространство, а ё направляет на железосерный центр.
г) с этого момента дыхательная цепь осуществляет транспорт только ё, транспорт Н+ в матрикс завершен. Электроны, полученные от железосерного центра, транспортируются по системе цитохромов с1, с, а и а3 на конечный акцептор - кислород.
д) цитохромы а и а3 тесно связаны друг с другом и получили общее название цитохромоксидаза, поскольку они непосредственно контактируют с молекулярным кислородом. В состав цитохромоксидазы входит не только гемовое железо, но и медь. В активном центре цитохромоксидазы происходит реакция
4е + 4Н+ + О2 —> 2Н2О.
Таким образом, в дыхательной цепи митохондрий осуществляется четырехэлектронное восстановление кислорода с образованием «метаболической воды».
В случае окисления ФАДН2 последовательность событий та же, но начинается с пункта (б): убихинон принимает пару ё и Н+ непосредственно от ФАДН2.
Установлено, что разность окислительно-восстановительных потенциалов между первым (НАДН2) и последним (кислородом) компонентом дыхательной цепи составляет около 1,14 В, что создает запас энергии около 220 кДж, достаточный для синтеза 3 молекул АТФ. Поэтому вся дыхательная цепь условно может быть поделена на 3 участка, разность окислительно-восстановительных потенциалов в которых достаточна для синтеза 1 молекулы АТФ - 3 пункта сопряжения дыхания и фосфорилирования: 1-й - между НАДН2 и НАДН-дегидрогеназой, 2-й - между цитохромами b582 и с, 3-й - между цитохромами а и а3. Таким образом, окисление 1 молекулы НАДН2 в дыхательной цепи дает возможность синтезировать 3 молекулы АТФ, а 1 молекулы ФАДН2 - только 2 молекулы АТФ.
2.3.1. Хемиосмотическая теория
Для объяснения механизма окислительного фосфорилирования в 1961 г. П. Митчеллом была предложена хемиосмотическая теория. В обобщенном виде суть хемиосмотической теории можно представить следующим образом: внутренняя мембрана митохондрий разделяет потоки е и Н+ - первые транспортируются вдоль мембраны, вторые - поперек, при этом создается трансмембранный электрохимический потенциал, обусловленный разностью зарядов и концентраций протонов в матриксе и межмембранном пространстве митохондрий. Энергия этого электрохимического потенциала используется АТФ-синтазой для синтеза АТФ из АДФ и фосфата, т. е. для фосфорилирования. Согласно концепции, П. Митчелла тканевое дыхание и окислительное фосфорилирование сопряжены, а сопрягающим звеном между ними служит электрохимический потенциал: дыхание создает его, а фосфорилирование расходует.
При переносе Н+ из матрикса в межмембранное пространство на внутренней мембране создается осмотический градиент протонов (химический потенциал)
∆рН = 60 мВ (при ∆рН = 1) (в матриксе рН выше, чем в межмембранном пространстве). Так как каждый Н+ несет положительный заряд, на внутренней мембране также появляется разность электрических потенциалов ∆V= 160 мВ, внутренняя сторона мембраны заряжается отрицательно, внешняя - положительно. В сумме осмотический градиент протонов и разность потенциалов образуют электрохимический потенциал, который составляет около 220 мВ.
Энергия образовавшегося на внутренней мембране митохондрий электрохимического потенциала может использоваться для фосфорилирования АДФ в АТФ, транспорта веществ через мембрану митохондрий и теплопродукции.
Сведения о структуре и функциях компонентов дыхательной цепи и АТФ-син- тазы обобщены в табл. 4.
2.3.2. Механизм окислительного фосфорилирования
Процесс фосфорилирования осуществляется АТФ-синтазой (Н+-АТФ-аза), которая потребляет 40-45 % свободной энергии, выделившейся при окислении. АТФ-синтаза представляет собой интегральный белок, состоящий из двух субъединиц - F0 и F1. Субъединица F0 - канал в мембране, предназначенный для транспорта протонов из межмембранного пространства в матрикс. Субъединица F1 - каталитическая - именно она катализирует реакцию синтеза АТФ из АДФ и фосфата. Когда значение трансмембранного потенциала достигает критической величины 200-250 мВ, Н+ устремляются из межмембранного пространства в матрикс по открывшемуся каналу. Выделяющаяся в результате этого энергия расходуется ферментом на образование макроэргической связи АТФ из АДФ и фосфата - окислительное фосфорилирование. При каждом переносе Н+ через канал F0 энергия электрохимического потенциала расходуется на поворот стержня субъединицы F1, в результате чего изменяется конформация фермента, облегчается связывание АДФ и фосфата.
2.4. Регуляция энергетического обмена
Цикл Кребса, тканевое дыхание и окислительное фосфорилирование функционируют в клетке согласованно. Главный принцип их согласованной регуляции: синтез АТФ должен отвечать потребностям клетки в нем. Когда в клетке активно происходит потребление АТФ, накапливается АДФ. Именно АДФ является главным стимулятором всех этапов энергетического обмена. Зависимость скорости дыхания клеток от концентрации АДФ получила название дыхательный контроль.
Дыхательный контроль осуществляется с участием 4 регуляторных ферментов ЦТК: цитратсинтазы, изоцитратдегидрогеназы, α-кетоглутаратдегидрогеназного комплекса и малатдегидрогеназы. Эти ферменты ЦТК ингибируются НАДН2 и АТФ, которые являются продуктами ЦТК и окислительного фосфорилирования. НАД+ и АДФ активируют эти ферменты ЦТК. Кроме того, скорость окислительного фосфорилирования напрямую лимитируется доступностью АДФ, который поступает в матрикс в обмен на АТФ.
Энергетический обмен находится также и под гормональным контролем. Инсулин через ряд промежуточных посредников активирует ЦТК на уровне α-кетоглутаратдегидрогеназного комплекса, а также активирует окислительное декарбоксилирование пирувата, поставляющего ацетилкоэнзим А циклу Кребса, и гликолиз, продуцирующий пируват. Хорошо известно, что при дефиците инсулина, который развивается при сахарном диабете, эти аэробные процессы ингибированы, а пируват превращается в лактат. Стимулируют энергетический обмен в клетке гормоны щитовидной железы - тироксин и трийодтиронин. Под действием тиреоидных гормонов активируется перенос АДФ в матрикс митохондрии, ускоряются тканевое дыхание и синтез АТФ, а также увеличивается теплопродукция.
2.5. Другие пути использования кислорода
Известны также пути использования кислорода с пластическими целями. Реакции микросомального окисления, активно протекающие в печени и надпочечниках, приводят к внедрению кислорода в окисляемый субстрат. Эндогенными субстратами микросомального окисления являются холестерин, стероидные гормоны, ненасыщенные жирные кислоты. Велико значение этого процесса для обезвреживания ксенобиотиков (чужеродных организму соединений).
Небольшое количество кислорода в клетках превращается в активные формы - свободные радикалы и их предшественники, способные нарушать структуру липидов, белков, нуклеиновых кислот. Для защиты от подобного повреждения в клетках имеется антиоксидантная система, включающая ряд ферментов (каталаза, супероксиддисмутаза, глутатионпероксидаза, глутатионредуктаза) и низкомолекулярных органических веществ, в том числе витаминов А, С, Е, липоевой кислоты и глутатиона.
Сравнительная характеристика различных путей использования кислорода в клетке представлена в табл. 5.
Вопросы для проверки усвоения материала
1. Понятие об обмене энергии в живых системах, биоэнергетике и биологическом окислении. Макроэргические связи и макроэргические соединения, их виды и значение. АТФ как универсальный энергоноситель. Пути генерации и использования АТФ в клетке, сравнительная характеристика окислительного и субстратного фосфорилирования.
2. Этапы утилизации энергии питательных веществ: подготовительный, промежуточный обмен и митохондриальный, сущность и значение. Образование и экскреция СО2 и Н2О - конечных продуктов метаболизма.
3. Цикл трикарбоновых кислот (цикл Кребса): сущность и биологическое значение. Реакции цикла Кребса: субстраты, ферменты, коферменты. Регуляция цикла Кребса.
Таблица 5. Пути использования кислорода в реакциях биологического окисления
Путь |
% от потребляемого O2 |
Химическая сущность |
Локализация в клетке |
Ферментные системы |
Биологическое значение |
Оксидазный |
90 |
O2 + 4ё + 4Н+ —> 2Н2O |
Внутренняямембрана митохондрий |
Дыхательная цепь. Поставщики Н+ - НАД+- и ФАД-зависимые дегидрогеназы ЦТК, β-окисления и др. |
Энергетическое |
Монооксигеназный |
8 |
SH2 + О2 + НАД(Ф)Н2 —> SH-OH + НАД(Ф)+ + Н2O |
Наружнаямембрана митохондрий,мембрана гладкой ЭПС, аппаратаГольджи, ядра,плазмолемма |
Флавопротеин, цитохромы Р450 и b5. Поставщики НАДФН2 - пентозофосфатный путь, цитозольные малат- и изоцитратдегидрогеназа |
1. Синтез эндогенных веществ (желчных кислот, стероидных гормонов, аминокислот, катехоламинов, витаминов А и D5). 2. Катаболизм эндогенных субстратов (билирубин, стероидные гормоны) и ксенобиотиков (лекарства и яды) |
Диоксигеназный |
2 |
SH2 + O2 —> HO-S-OH или S + O2 —>O=S=O |
|||
Свободно радикальный |
<1 |
S + АФК —> S-O-O- и т. д. |
Повсеместно |
Неферментативные цепные свободнорадикальные реакции |
1. Обновление мембран, фагоцитоз, синтез эйкозаноидов, процессы апоптоза. 2. Повреждение мембран, белков, ДНК, процессы некроза, воспаления, канцерогенеза |
4. Дыхательная цепь митохондрий: строение и функции, свойства компонентов, биологическое значение. Строение и функции АТФ-синтетазы. Механизм сопряжения тканевого дыхания (ТД) и окислительного фосфорилирования (ОФ) - хемиосмо- тическая теория Митчелла. Разобщение ТД и ОФ: сущность и биологическое значение.
5. Моно- и диоксигеназные реакции (микросомальное окисление). Роль мик- росомального окисления в обезвреживании ксенобиотиков. Свободнорадикальный путь использования кислорода: активные формы кислорода, их биологическое значение. Антиоксидантная защита клетки: ферментативные и неферментативные механизмы, их значение.
Письменное домашнее задание
Обязательное
1. Катаболизм этанола в организме протекает в печени преимущественно по следующей схеме:
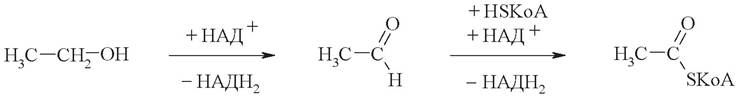
и завершается окислением ацетил-КоА в цикле Кребса.
Рассчитайте энергетический баланс (количество молекул АТФ) полного окисления этанола до СО2 и Н2О. Какие вещества (ферменты, коферменты, субстраты) необходимы для полноценного катаболизма этанола?
2. Из клеток миокарда выделили митохондрии и инкубировали в среде с достаточным содержанием кислорода и субстратов биологического окисления. В ходе эксперимента в суспензию добавляли различные вещества, обладающие известным действием на процессы тканевого дыхания и окислительного фосфорилирования: АДФ, ингибитор дыхательной цепи, разобщитель дыхания и фосфорилирования. На следующем рисунке представлены графики потребления кислорода и образования АТФ в данной системе до введения модуляторов (участок А) и после него (участок В):
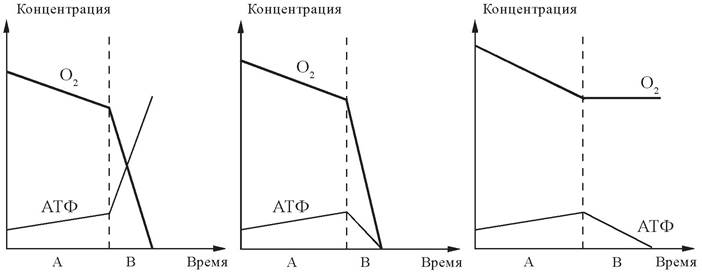
Какие из приведенных модуляторов могли обусловить наблюдаемые закономерности в каждом случае? Ответ обоснуйте.
3. Нафталин - токсичное соединение. При поступлении в организм через желудочно-кишечный тракт нафталин накапливается в печени, где обезвреживается по следующей схеме:
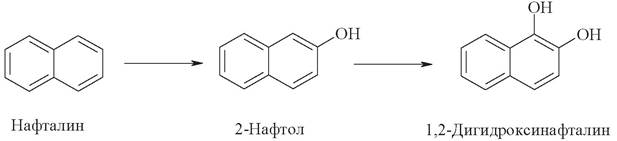
Какой путь потребления кислорода имеет место в данном случае? Укажите на схеме ферменты и коферменты каждой стадии. Какое биологическое значение имеет изменение растворимости в воде метаболитов по сравнению с нафталином?
4. В условиях нормальной работы митохондрий кислород восстанавливается до воды по следующей схеме: О2 + 4ё + 4Н+ —> Н2О, однако небольшое его количество превращается в супероксидный анион-радикал: О2 + ё —> О2-. Каково положительное и отрицательное значение этого процесса? Какие механизмы имеются в клетке для инактивации данного соединения? Предположите, при каких условиях митохондрии будут продуцировать большие количества супероксида?
Дополнительное
1. Ацетилсалициловая кислота (аспирин) широко применяется как противовоспалительное, жаропонижающее и обезболивающее средство. В желудочнокишечном тракте ацетилсалициловая кислота гидролизуется на уксусную и салициловую кислоты, последняя метаболизируется в печени по следующей схеме:
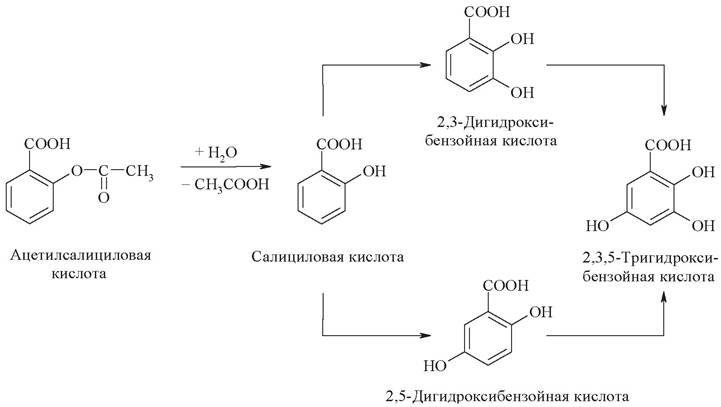
Определите, какой путь потребления кислорода имеет место в данном случае. Укажите на схеме ферменты и коферменты каждой стадии. Как изменяется растворимость метаболитов в воде по сравнению с салициловой кислотой? Какое биологическое значение имеет это явление?
2. К культуре клеток был добавлен фосфолипид, меченый радиоактивным 14С по линоленовой кислоте. Введенная метка была быстро обнаружена в плазматической мембране клеток. Однако после ультрафиолетового облучения культуры содержание метки в мембранах снизилось в 2 раза. Опыт повторили, предварительно добавив к культуре витамин Е. В этих условиях содержание метки снизилось только на 10 %. В чем причина выявленных различий?
Типовой вариант тестового контроля по теме «Биологическое окисление»
Инструкция: при отсутствии дополнительных указаний в вопросе теста выберите один верный вариант ответа.
1. Выберите название фермента, катализирующего следующую реакцию цикла Кребса:
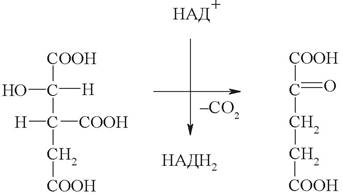
а) фумараза;
б) изоцитратдегидрогеназа;
в) малатдегидрогеназа;
г) сукцинатдегидрогеназа;
д) цитратсинтаза.
2. Что из перечисленного происходит на митохондриальном этапе энергетического обмена:
а) окислительное фосфорилирование;
б) дегидрирование карбоновых кислот в цикле Кребса;
в) разрушение ацетилкоэнзима А до СО2;
г) восстановление кислорода до воды;
д) все перечисленное.
3. Как изменяется потребление кислорода и синтез АТФ митохондриями при воздействии на них цианидов - ингибиторов дыхания:
а) потребление кислорода увеличивается, синтез АТФ увеличивается;
б) потребление кислорода увеличивается, синтез АТФ уменьшается;
в) потребление кислорода уменьшается, синтез АТФ увеличивается;
г) потребление кислорода уменьшается, синтез АТФ уменьшается.
4. Какую функцию в клетке выполняет витамин Е:
а) необходим для протекания цикла Кребса;
б) участвует в реакциях субстратного фосфорилирования;
в) переносит электроны и протоны в дыхательной цепи митохондрий;
г) является главным жирорастворимым антиоксидантом;
д) является разобщителем дыхания и фосфорилирования.
5. Какой кофермент необходим для работы цитохрома Р450:
а) НАДН2;
б) НАДФН2;
в) аскорбиновая кислота;
г) липоевая кислота;
д) тиаминпирофосфат.
6. Какова энергетическая эффективность окисления в дыхательной цепи коферментов НАДН2 и ФАДН2:
а) НАДН2 и ФАДН2 - по 3 АТФ;
б) НАДН2 и ФАДН2 - по 2 АТФ;
в) НАДН2 - 3 АТФ, ФАДН2 - 2 АТФ;
г) НАДН2 - 2 АТФ, ФАДН2 - 3 АТФ.
7. Укажите роль глутатиона (G-SH) в антиоксидантной системе клетки:
а) является коферментом глутатионпероксидазы;
б) является коферментом глутатионредуктазы;
в) обезвреживает супероксидный анион-радикал;
г) является главным жирорастворимым антиоксидантом;
д) все перечисленное.
8. Выберите характеристику микросомального окисления ксенобиотиков:
а) расходуется кислород, липофильные вещества становятся гидрофильными;
б) расходуется кислород, гидрофильные вещества становятся липофильными;
в) кислород не расходуется, липофильные вещества становятся гидрофильными;
г) кислород не расходуется, гидрофильные вещества становятся липофильными.
9. Вставьте пропущенные слова (3 ответа) в предложение: «Движение ... по дыхательной цепи митохондрий создает запас энергии для перемещения ... через мембрану, энергия мембранного потенциала тратится на синтез ...»
10. Напишите названия и номера классов ферментов (6 ответов), катализирующих реакции 1, 2 и 3: