БИОХИМИЯ УЧЕБНИК ДЛЯ ВУЗОВ - Е. С. Северина - 2004
РАЗДЕЛ 8. ОБМЕН ЛИПИДОВ
VIII. Обмен и функции фосфолипидов
Метаболизм фосфолипидов тесно связан со многими процессами в организме: образованием и разрушением мембранных структур клеток, формированием ЛП, мицелл жёлчи, образованием в альвеолах лёгких поверхностного слоя, предотвращающего слипание альвеол во время выдоха. Нарушения обмена фосфолипидов — причина многих заболеваний, в частности, респираторного дистресс-синдрома новорождённых, жирового гепатоза, наследственных заболеваний, связанных с накоплением гликолипидов, — лизосомных болезней. При лизосомных болезнях снижается активность гидролаз, локализованных в лизосомах и участвующих в расщеплении гликолипидов.
А. Обмен глицерофосолипидов
Синтез фосфатидилхолинов, фосфатидилэтаноламинов и фосфатидилсеринов
Начальные этапы синтеза глицерофосфолипидов и жиров происходят одинаково до образования фосфатидной кислоты. Фосфатидная кислота может синтезироваться двумя разными путями: через глицеральдегид-3-фосфат и через дигидроксиацетонфосфат (рис. 8-57).
Рис. 8-57. Схема синтеза глицерофосфолипидов. R1 — радикал насыщенной жирной кислоты; R2 — радикал полиеновой жирной кислоты; SАМ — S-аденозилметионин.
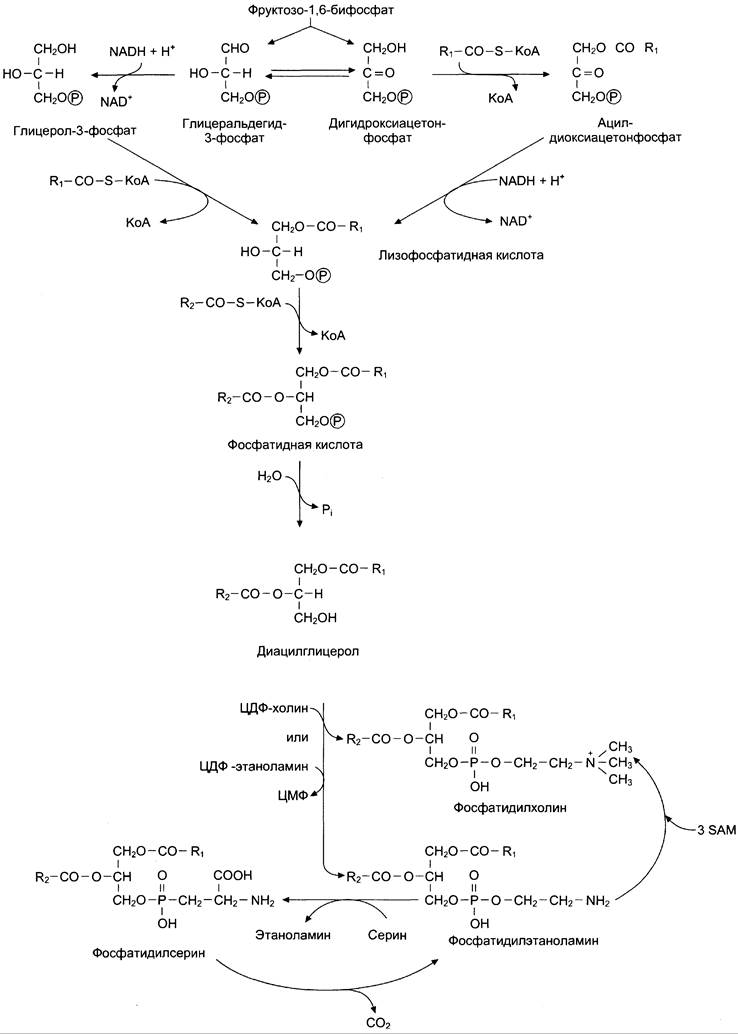
На следующем этапе фосфатидаза отщепляет от фосфатидной кислоты фосфатный остаток, в результате чего образуется диацилглицерол. Дальнейшие превращения диацилглицерола также могут идти разными путями. Один из вариантов — образование активной формы «полярной головки» фосфолипида: холин, серин или этаноламин превращаются в ЦЦФ-холин, ЦДФ- серин (рис. 8-58) или ЦЦФ-этаноламин.
Рис. 8-58. Синтез ЦДФ-холина. «Полярная головка» фосфатидилхолина превращается за счёт энергии АТФ в активную форму — фосфохолин, который затем присоединяется к ЦТФ с одновременным удалением РРi, что сдвигает равновесие реакции вправо. Образовавшийся ЦДФ-холин — донор холина для синтеза молекул фосфатидилхолинов. ЦДФ-холин — цитидилдифосфохолин; ЦМФ — цитидилмонофосфат; Р — остаток фосфорной кислоты.
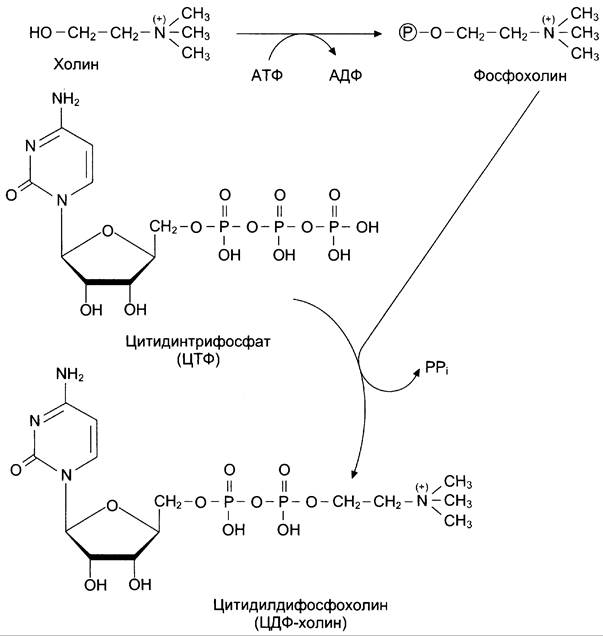
Далее диацилглицерол взаимодействует с ЦДФ- производными, при этом выделяется ЦМФ, и образуется соответствующий фосфолипид, например, фосфатидилхолин. Между глицерофосфоли- пидами возможны различные взаимопревращения. Фосфатидилхолин может образовываться и другим путём: из фосфатидилэтаноламина, получая последовательно 3 метальные группы от SAM. Фосфатидилсерин может превращаться в фосфатид илэтаноламин путём декарбоксилирования. Фосфатидилэтаноламин может превращаться в фосфатидилсерин путём обмена этаноламина на серин.
Дипальмитоилфосфатидилхолин — основной компонент сурфактанта лёгких
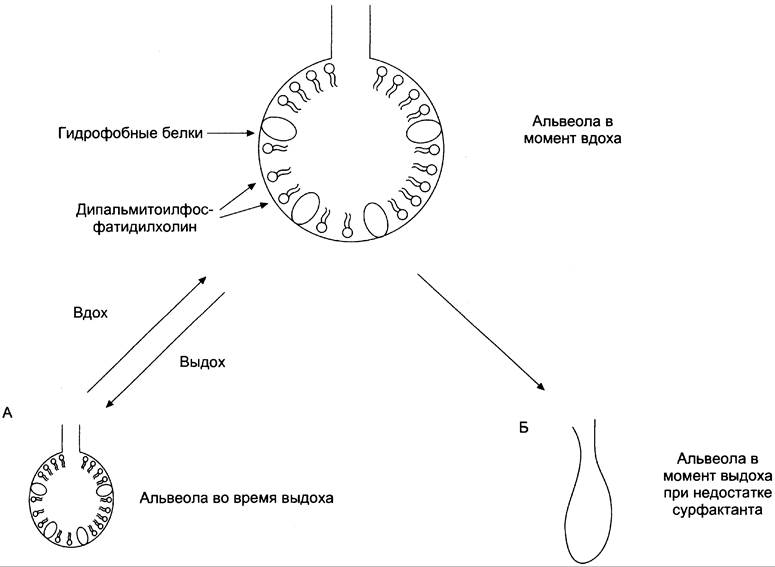
Сурфактант — внеклеточный липидный слой с небольшим количеством гидрофобных белков, выстилающий поверхность лёгочных альвеол и предотвращающий слипание стенок альвеол во время выдоха (рис. 8-59). Основной компонент сурфактанта — дипальмитоилфосфатидилхолин, составляющий до 80% от всех фосфолипидов, входящих в состав сурфактанта. Кроме того, в сурфактант входят гидрофобные белки, общее количество которых не превышает 10 — 20%.
Рис. 8-59. Влияние сурфактанта на функцию альвеол. А — сурфактант уменьшает поверхностное натяжение жидкости, выстилающей поверхность альвеол, и предотвращает слипание стенок альвеол во время выдоха. Меньшее давление воздуха необходимо, чтобы наполнить альвеолы воздухом; Б — в отсутствие сурфактанта или при его недостаточном образовании (у недоношенных детей) стенки альвеол во время выдоха спадаются, и требуется давление воздуха в 10 раз большее, чтобы наполнить альвеолы.
Синтез дипальмитоилфосфатидилхолина (лецитина) в пневмоцитах II типа происходит в процессе эмбрионального развития и резко увеличивается в период от 32 до 36 нед беременности.
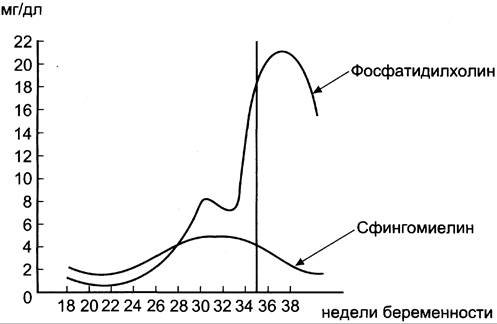
Важным показателем нормального формирования сурфактанта служит соотношение фосфа- тидилхолин/сфингомиелин >4 (рис. 8-60). Это соотношение можно определять, исследуя состав амниотической жидкости. Недостаточное формирование сурфактанта у недоношенных детей после рождения приводит к развитию респираторного дистресс-синдрома — основной причины смерти у этой группы новорождённых. Соотношение фосфатидилхолин/сфингомиелин <2 указывает на высокий риск развития респираторного дистресс-синдрома. В случае необходимости лечение беременных кортикостероидами стимулирует синтез сурфактанта в лёгких плода и уменьшает риск развития респираторного дистресс-синдрома.
Рис. 8-60. Изменение соотношения фосфатидилхолин/сфингомиелин в амниотической жидкости в различные периоды беременности. На 35-й неделе беременности концентрация фосфатидилхолина увеличивается по отношению к сфингомиелину в 4 раза, что характеризует нормальное развитие лёгких.
Синтез фосфатидилинозитола и кардиолипина
Другой путь превращений диацилглицерола, при котором образуется активная форма — ЦДФ- диацилглицерол приводит к образованию фосфатидилинозитола и кардиолипина (см. схему ниже).
Фосфатидилинозитол далее может фосфорилироваться с образованием фосфатидилинозитол- 4,5-бисфосфата, фосфолипида, располагающегося в наружной мембране клеток и участвующего в передаче гормональных сигналов внутрь клетки (см. раздел 5). Кардиолипин находится, главным образом, во внутренней мембране митохондрий и в небольшом количестве в сурфактанте лёгких.
Катаболизм глицерофосфолипидов
Различные типы фосфолипаз, локализованных в клеточных мембранах или в лизосомах, катализируют гидролиз глицерофосфолипидов (см. раздел 5). Гидролиз некоторых глицерофосфолипидов под действием фосфолипаз имеет значение не только как путь катаболизма, но и как путь образования вторичных посредников или предшественников в синтезе биологически активных веществ — эйкозаноидов. Кроме того, фосфолипазы А1 и А2 участвуют в изменении состава жирных кислот в глицерофосфолипидах, например, при синтезе в эмбриональном периоде развития дипальмитоилфосфатидилхолина — компонента сурфактанта.
Б. Функции и обмен сфинголипидов
Сфинголипиды — производные церамида, образующегося в результате соединения аминоспирта сфингозина и жирной кислоты. В группу сфинголипидов входят сфингомиелины и гликосфинголипиды (см. табл. 8-4, рис. 8-61).
Сфингомиелины находятся в мембранах клеток различных тканей, но наибольшее их количество содержится в нервной ткани. Сфингомиелины миелиновых оболочек содержат в основном жирные кислоты с длинной цепью: лигноцериновую (24:0) и нервоновую (24:1) кислоты, а сфингомиелин серого вещества мозга содержит преимущественно стеариновую кислоту.
Гликосфинголипиды — гликолипиды, в состав которых входят церамид и один или несколько остатков углеводов, и сиаловая (N-ацетилнейраминовая) кислота (см. рис. 8-5, 8-8, 8-61).
Схема
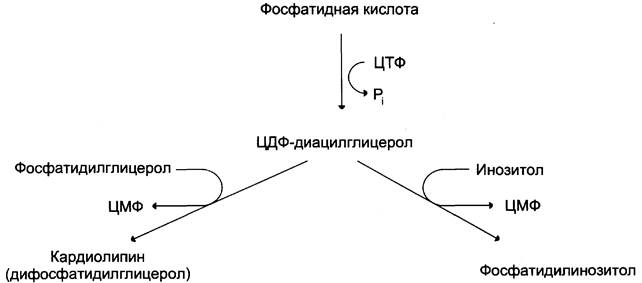
Рис. 8-61. Структуры гликосфинголипидов. А — общая схема строения гликосфинголипидов; Б — структура радикалов, связанных с церамидом, и названия отдельных гликосфинголипидов. Обозначения: цер — церамид; глк — глюкоза; гал — галактоза; гал-Nац — N-ацетилгалактозамин; N-АНК — N-ацетилнейраминовая кислота.

Гликосфинголипиды локализованы в плазматических мембранах клеток таким образом, что углеводная часть молекулы располагается на поверхности клеток и часто обладает антигенными свойствами. Эта часть молекул обеспечивает взаимное узнавание клеток и их взаимодействие. Интересно, что углеводная часть структуры антигенов на поверхности эритроцитов (по системе AB0) может быть связана как с церамидом, так и с белками. В последнем случае структура антигена является не гликолипидом, а гликопротеином.
Некоторые ганглиозиды — рецепторы бактериальных токсинов. Например, GMl, находящийся на поверхности клеток кишечного эпителия, является местом прикрепления холерного токсина — белка, секретируемого возбудителями холеры.
Функции гликосфинголипидов можно суммировать следующим образом:
Взаимодействие между:
✵ клетками;
✵ клетками и межклеточным матриксом;
✵ клетками и микробами.
Модуляция:
✵ активности протеинкиназ;
✵ активности рецептора фактора роста;
✵ антипролиферативного действия (апоптоза, клеточного цикла).
Обеспечение:
✵ структурной жёсткости мембран;
✵ конформации белков мембран.
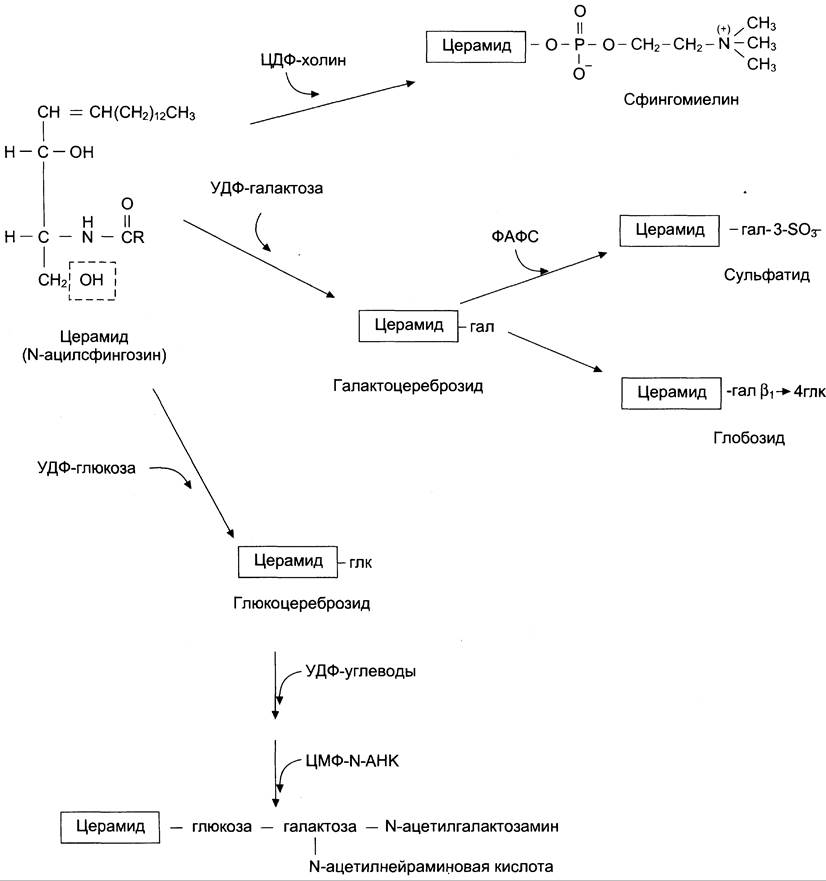
Синтез церамида и его производных. Синтез сфинголипидов начинается с образования церамида. Серин конденсируется с пальмитоил-КоА. Продукт их взаимодействия сначала восстанавливается коферментом NАDРH, затем к аминогруппе дигидросфингозина амидной связью присоединяется жирная кислота, содержащая, как правило, 24 атома углерода. После окисленияFАD-зависимой дегидрогеназой образуется церамид. Церамид служит предшественником в синтезе большой группы сфинголипидов: сфингомиелинов, не содержащих углеводов, и гликосфинголипидов (рис. 8-62). Последующие реакции синтеза катализируются специфическими трансферазами, набор которых отличается в разных тканях. Соединение фосфорилхолина с церамидом сфингомиелинсинтазой приводит к образованию сфингомиелина. Присоединение углеводных компонентов катализируется специфическими гликозилтрансферазами. Донорами углеводных компонентов служат активированные сахара: УДФ-галактоза и УДФ-глюкоза. Галактоцереброзид — главный липид миелиновых оболочек; глюкоцереброзид входит в состав мембран многих клеток и служит предшественником в синтезе более сложных гликолипидов или продуктом на пути их катаболизма.
Рис. 8-62. Синтез сфинголипидов из церамида. Обозначения: гал — галактоза; глк — глюкоза; гал — Nац-N-ацетилгалактозамин; N-АНК — N-ацетилнейраминовая кислота; УДФ-галактоза, УДФ-глюкоза — активные формы углеводов, присоединяемые специфическими гликозилтрансферазами; ЦМФ-N-АНК — активная форма N-ацетилнейраминовой кислоты; ФАФС — фосфоаденозилфосфосульфат — активная форма серной кислоты. Фосфохолин или углеводы присоединяются по месту гидроксиметильной группы церамида (выделена пунктиром). Каждый остаток углевода присоединяется специфической гликозилтрансферазой в цистернах шероховатого ЭР и аппарате Гольджи.
Катаболизм сфингомиелина и его нарушения.
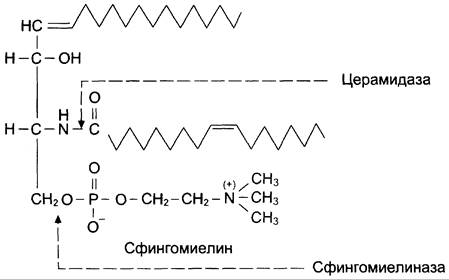
В лизосомах находятся ферменты, способные гидролизовать любые компоненты клеток. Эти ферменты называют кислыми гидролазами, так как они активны в кислой среде. Значение pH = 5, оптимальное для работы ферментов, создаётся протонным насосом, который, используя энергию АТФ, накачивает ионы водорода в лизосомы. Катаболизм сфингомиелинов и гликолипидов происходит в лизосомах. В распаде сфингомиелинов участвуют 2 фермента — сфингомиелиназа, отщепляющая фосфорилхолин, и церамидаза, продуктами действия которой являются сфингозин и жирная кислота (рис. 8-63).
Рис. 8-63. Гидропиз сфингомиелина.
Генетический дефект сфингомиелиназы — причина болезни Ниманна—Пика. Дети с таким дефектом погибают в раннем возрасте. Симптомы заболевания: увеличение печени и селезёнки (гепатоспленомегалия), в лизосомах которых накапливается сфингомиелин; умственная отсталость. Генетический дефект другого фермента (церамидазы) приводит к развитию болезни Фарбера, симптомами которой также являются гепато- и спленомегалия, а также поражение суставов (болезненность, отёчность).
Катаболизм гликосфинголипидов. Катаболизм гликосфинголипидов начинается с перемещения их с поверхности клетки в цитоплазму по механизму эндоцитоза. В результате молекулы, расположенные на поверхности мембран, оказываются в эндоцитозных везикулах в цитоплазме и сливаются с лизосомами. В лизосомах находятся все ферменты, необходимые для гидролиза сложных молекул гликосфинголипидов: α- и β-галактозидазы, β-глюкозидазы, нейраминидаза (сиалидаза) и церамидаза. В результате последовательных реакций гидролиза сложные молекулы гликосфинголипидов распадаются до мономеров: глюкозы, галактозы, жирной кислоты, сфингозина и других метаболитов.
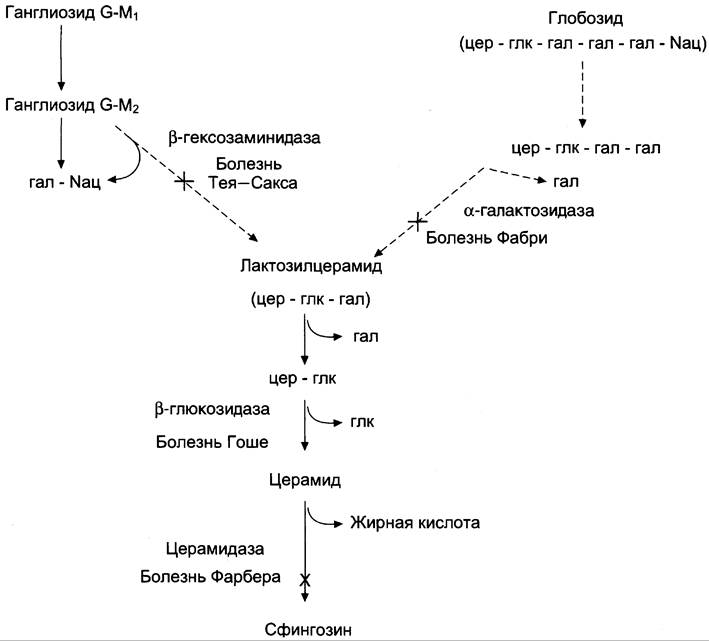
Генетические дефекты лизосомных ферментов катаболизма гликосфинголипидов. В норме синтез и катаболизм гликосфинголипидов сбалансированы таким образом, что количество этих компонентов в мембранах постоянно. Если имеется генетический дефект какого-либо лизосомного фермента, участвующего в катаболизме гликосфинголипида, то в лизосомах накапливается недеполимеризованный субстрат, так называемые «остаточные тельца», размеры лизосом увеличиваются, их мембрана может разрушаться, ферменты выходят в цитозоль, и функции клеток нарушаются. Генетические заболевания вследствие дефекта какого-либо из ферментов катаболизма гликосфинголипидов называют сфинголипидозами, или лизосомными болезнями. Эти заболевания редки, но среди некоторых популяций людей их частота очень высока. Так, болезнь Гоше вследствие дефекта фермента β-глюкозидазы (рис. 8-64) у евреев встречается с частотой 166:100 000, болезнь Тея-Сакса (дефект фермента β-гексозаминидазы) — с частотой 33:100 000. Сфинголипидозы обычно приводят к смерти в раннем возрасте, так как происходит поражение клеток нервной ткани, где сконцентрированы гликосфинголипиды. Однако при болезнях Гоше и Фабри больные живут относительно долго.
Рис. 8-64. Катаболизм гликосфинголипидов. На схеме указаны ферменты, генетические дефекты которых являются причиной наследственных заболеваний — сфинголипидозов.