Підручник - БІОЛОГІЧНА ХІМІЯ - Губський Ю.І. - 2000
Розділ I. БІОМОЛЕКУЛИ ТА КЛІТИННІ СТРУКТУРИ
ГЛАВА 4. ВУГЛЕВОДИ ТА ЇХ ПОХІДНІ
4.3. ГЕТЕРОПОЛІСАХАРИДИ. ПРОТЕОГШКАНИ. ГШКОПРОТЕЇНИ
Гетерополісахариди
Гетерополісахариди — полімери, побудовані з великої кількості різних моносахаридних одиниць та їх похідних. У біохімії та фізіології людини і тварин найбільше значення мають гетерополісахариди глікозамінглікани.
Глікозамінглікани — гетерополісахариди, побудовані з дисахаридних залишків, які повторюються. Моносахаридними компонентами дисахаридних залишків глікозамінгліканів є найчастіше гексуронові кислоти (глюкуронова або іноді ідуронова тощо) та N-ацетилпохідні гексозамінів (глюкозаміну, галактозаміну).
До глікозамінгліканів належать численні тваринні біополімери, що складають міжклітинний матрикс сполучної тканини, який заповнює простір між окремими клітинами. Застаріла назва цих сполук — мукополісахариди — вказує, що сполуки даного класу були вперше виділені з муцину — компоненту слизів, що є змазуючою речовиною, яка виконує функцію фізіологічного мастила. Найбільш вивченими глікозамінгліканами є гіалуронова кислота, хондроїтинсульфати, дерматансульфати, кератансульфати, гепарансульфати, які входять до складу шкіри, сухожиль, хрящів суглобів, забезпечуючи механічну міцність та пружність органів, еластичність їх сполучень. Глікозамінглікан гепарин є природним антикоагулянтом.
Глікозамінглікани є поліаніонними молекулами. Щонайменше один із моносахаридних компонентів у молекулах глікозамінгліканів несе кислотне угруповання — карбоксильну або сульфатну групу, що забезпечує їх високу гідрофільність, тобто здатність утримувати в біологічних тканинах значну кількість води.
Усі глікозамінглікани виконують свої біохімічні та фізіологічні функції, будучи зв’язаними з білками. Ковалентні комплекси глікозамінгліканів сполучної тканини (гіалуронової кислоти, хондроїтинсульфатів тощо) з білками отримали назву протеогліканів, що є представниками мішаних біополімерів (глікокон’югатів).
Таблиця 4.1. Структурні компоненти глікозамінгліканів
Глікозамінглікан |
Склад дисахаридноїодиниці |
Гіалуронова кислота |
D-глюкуронат + N-ацетилглюкозамін |
Хондро їтинсульфати |
D-глюкуронат + N-ацетилгалактозамінсульфат |
Дерматансульфати |
D-ідуронат + N-ацетилгалактозамінсульфат (або D-глюкуронат) |
Кератансульфати |
D-галактоза + N-ацетилглюкозамінсульфат |
Гепарансульфати та Гепарин |
D-глюкуронат + N-ацетилглюкозамінсульфат (або D-ідуронат) |
Гіалуронова кислота — лінійний гетерополісахарид, у якому D-глюкуронова кислота та К-ацетил-D-глюкозамін сполучені між собою β-1,3-глікозидним зв’язком; окремі дисахаридні фрагменти об’єднані β-1,4-глікозидними зв’язками:
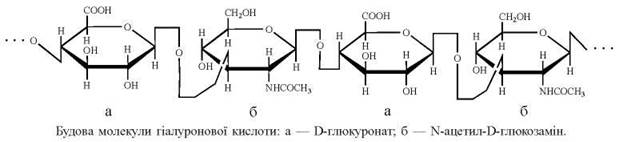
Гіалуронова кислота має найбільшу молекулярну масу з усіх глікозамінгліканів — 105-107. Велика кількість груп — СОО- формує значний негативний заряд молекули, сприяє утриманню води та катіонів Na+. Гіалуронова кислота наявна в пухкій сполучній тканині, синовіальній рідині суглобів, скловидному тілі ока.
Хондроїтинсульфати — глікозамінглікани, що у складі відповідних протео- гліканів (див. нижче) є важливими структурними компонентами хрящової тканини. Молекулярна маса хондроїтинсульфатів — 10-60 кД. Дисахаридні фрагменти складаються із глюкуронової кислоти та сульфатованого N-ацетилгалактозаміну, сполучених β-1,3-глікозидним зв’язком. Група —SOO-присутня в 4-му або 6-му положеннях залишку N-ацетилгалактозаміну (хондроїтин-4- та хондроїтин-6-сульфати, відповідно):
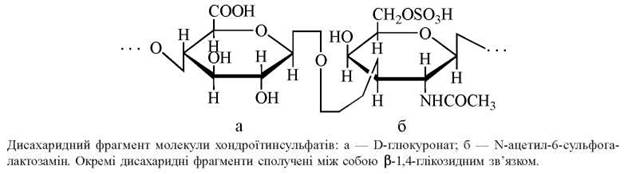
Кератансульфати — глікозамінглікани, сульфатовані в 6-му положенні залишку N-ацетилглюкозаміну. Подібно до хондроїтинсульфатів, кератансульфати сполучені з білками у формі протеогліканів. Розрізняють кератансульфат I — глікозамінглікан рогівки ока та кератансульфат II — компонент кісткової тканини.
Гепарансульфати — глікозамінглікани, присутні на зовнішніх поверхнях тваринних клітин. Уроновими кислотами у складі дисахаридних одиниць гепарансульфатів є глюкуронова та ідуронова кислоти, що сполучені β-1,4-глікозидними зв’язками із сульфатованими N-ацетилглюкозамінними залишками.
Гепарин — глікозамінглікан, який синтезується тучними клітинами сполучної тканини і виконує функцію антикоагулянта за рахунок активації інгібуючої дії антитромбіну III, що протидіє внутрішньосудинному згортанню крові.
Подібно до гепарансульфатів, ланцюги гепарину мають дисахаридні одиниці, до складу яких входить ідуронова та глюкуронова кислоти (ідуронова кислота переважає у гепарині на відміну від гепарансульфатів, складаючи до 90 % загального вмісту уронових кислот), зв’язані за типом β(1→4) з N- або O-сульфатованими залишками глюкозаміну та N-ацетилглюкозаміну:
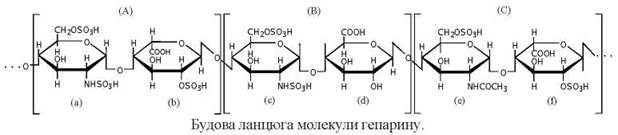
Подані три дисахаридні фрагменти (А), (В) та (С) (в квадратних дужках), до складу яких входять:
(A) О- та N-сульфатований ілюкозамін (а), сполучений із сульфатованою ідуроновою кислотою (b);
(B) O- та N-сульфатований глюкозамін (c), сполучений із глюкуроновою кислотою (d);
(C) О-сульфатований N-ацетилглюкозамін (е), сполучений із сульфатованою ідуроновою кислотою (f).
Гепарин та гепарансульфати мають спільного попередника у вигляді несульфатованоого полісахаридного ланцюга гепаринового протеоглікану. Модифікація полісахариду в складі протеоглікану включає в себе дію епімерази, яка перетворює частину залишків глюкуронової кислоти в ідуронову, та реакції O- і N-сульфування.
Протеоглікани
Протеоглікани — гібридні молекули (глікокон’югати), у складі яких білки ковалентно зв’язані з полісахаридами глікозамінгліканами. У складі протеогліканів на частку білків припадає 5-10 % маси молекули і на частку вуглеводної частини — 90-95 %.
Полісахаридні ланцюги сполучені з поліпептидним фрагментом молекул протеоглікану, утворюючи:
1) О-глікозидні зв’язки між гідроксильними групами моносахаридів та OH-групами серину або треоніну;
2) N-глікозиламінові зв’язки між ацетильною групою N-ацетилглюкозамінів та амідним азотом аспарагіну поліпептиду.
Типова молекула протеоглікану складається із центрального, серцевинного поліпептидного ланцюга — кору(core — серцевина, ядро; англ.), з боків якого приєднані молекули глікозамінгліканів.
Завдяки електростатичному відштовхуванню окремих поліаніонних ланцюгів полісахаридів загальна структура протеоглікану нагадує в цілому щіточку або ялинку.
За умов взаємодії в міжклітинному матриксі сполучної тканини протеогліканів із молекулами гіалуронової кислоти утворюються складні структурні комплекси з гіалуроновою кислотою посередині та бічними ланцюгами протеогліканів («ялинка з ялинок»). Встановлено, що з однією молекулою гіалуронової кислоти може сполучатися до 150 молекул сульфатованих протеогліканів (рис. 4.1).
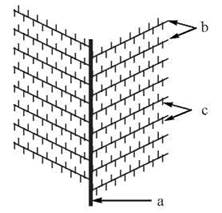
Рис. 4.1. Схема будови протеогліканового агрегату, що складається з молекули гіалуронової кислоти (а), серцевинних («корових») поліпептидів (b) та глікозамінгліканів (с).
Протеоглікани, сполучені з гіалуроновю кислотою, утворюють гелеподібний матрикс — «основну речовину» сполучної тканини, яка протидіє дифузії чужорідних молекул та мікроорганізмів усередину тканин. Будучи полівалентними аніонами, глікозамінгліканові компоненти протеогліканів зв’язують значну кількість екстрацелюлярного Na+ та, відповідно, Н2О, що зумовлює механізм участі тканинних протеогліканів у регуляції водно-сольового обміну.
Глікопротеїни
Глікопротеїни — гібридні молекули, що є складними білками, з поліпептидною основою яких ковалентно зв’язані олігосахаридні (гліканові) ланцюги.
Глікопротеїни є численною групою білків із різноманітними функціями. В цілому можна зазначити, що глікопротеїнами є більшість позаклітинних білків. Це структурні білки біомембран та екстрацелюлярного матриксу, зокрема сполучної тканини (колаген, еластин, муцини, слизові секрети, білки кісткового матриксу); білки крові, в тому числі фактори згортальної системи, транспортери вітамінів, гормонів, мінеральних елементів; гормони (хоріонічний гонадотропін, тиреотропін); білки імунної системи (імуноглобуліни, інтерферони, компоненти системи комплементу); ферменти (протеази, нуклеази, глікозидази) тощо.
Глікопротеїни та близькі до них за будовою гліколіпіди створюють поверхневоклітинний глікокалікс, компоненти якого беруть участь у міжклітинній взаємодії, регуляції клітинного поділу та її порушеннях при злоякісному рості. Глікопротеїни клітинної поверхні реалізують функцію взаємного розпізнавання клітин, що має особливе значення в процесах імунітету: полісахариди клітинної мембрани є антигенами, відносно яких розвиваються реакції клітинного імунітету, зокрема при трансплантації органів та тканин.
Вміст вуглеводного компоненту в більшості глікопротеїнів невеликий, але іноді складає до 50-80 % маси молекули. Кількість вуглеводних ланцюгів у складі окремих молекул глікопротеїнів змінюється від одного до кількох десятків. У свою чергу, кожен олігосахаридний ланцюг глікопротеїнів містить від 1 до 15 монозних залишків. Ці ланцюги можуть бути лінійними або розгалуженими.
Найчастіше у вуглеводному фрагменті глікопротеїнів організму людини зустрічаються такі цукри, як галактоза (Gal), глюкоза (Glc), маноза (Man), фукоза (Fuc), N-ацетилгалактозамін (GalNAc), N-ацетилглюкозамін (GlcNAc), N-ацетилнейрамінова (сіалова) кислота (NeuAc).
Подібно до протеогліканів, у молекулах глікопротеїнів олігосахаридні ланцюги зв’язані з поліпептидною частиною молекули за рахунок:
1) O-глікозидного зв’язку між цукром та OH-групою серину або треоніну;
2) N-глікозидного зв’язку між цукром та амідною групою аспарагіну.
Представниками О-зв’язаних глікопротеїнів є муцини (слизові білки) і деякі білки крові та біомембран. У складі цих глікопротеїнів цукром, що безпосередньо зв’язаний з Ser або Thr пептидного ланцюга, є GalNAc.
N-зв’язані глікопротеїни мають як олігосахаридний фрагмент, що безпосередньо зв’язаний з NH-групою аспарагіну, пентасахарид (Man)3(GlcNAc)2, з яким сполучені різні за будовою зовнішні олігосахаридні фрагменти. Ці зовнішні розгалужені олігосахаридні ланцюги нагадують молекулярні «антени», що відіграють головну роль у взаємодії клітин між собою та з іншими білковими і полісахаридними структурами.
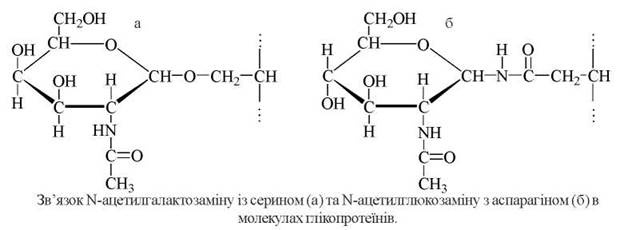
Приклади будови O- та N-зв’язаних олігосахаридних компонентів глікопротеїнів: