СТРУКТУРА И СВОЙСТВА БИОМОЛЕКУЛ - А. Е. Земляков - 2017
16. ЛИПИДЫ: ЛИПИДНЫЕ КОМПЛЕКСЫ И БИОЛОГИЧЕСКИЕ МЕМБРАНЫ
❖ Мицеллы - простейшие агрегаты, образуемые липидами в объемной фазе растворителя. В зависимости от полярности растворителя реализуются мицеллы обычного типа, либо "обращенные" мицеллы.
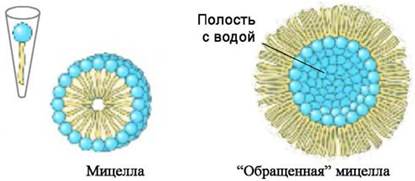
В воде легко создают мицеллы липиды, имеющие объемную и/или заряженную полярную часть и относительно небольшие углеводородные цепи, например, ганглиозиды или диоктаноилфосфатидилхолин. Одной из движущих сил процесса образования мицелл является стремление системы уменьшить гидрофильно-гидрофобные взаимодействия.
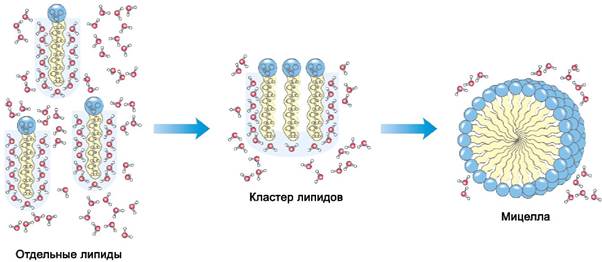
Важное свойство мицелл - способность солюбилизировать (растворять в себе) вещества, которые без мицелл в данной среде нерастворимы. Так мицеллы обычного типа могут включать жирорастворимые вещества, например, витамин А.
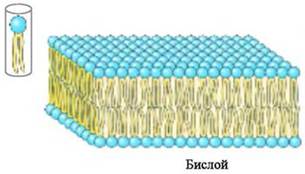
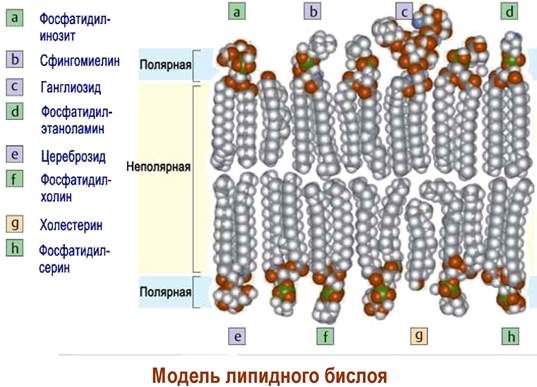
❖ Липидные бислои. Не образующие мицеллы липиды в объемной фазе воды агрегатизируются в бимолекулярный слой толщиной 4-5 нм. При этом полярные головки липидов контактируют с водой, а гидрофобные углеводородные «хвосты» образуют малополярный слой. Бислои наиболее характерны для липидов, у которых сравнимы площади сечения полярных и неполярных частей, например, для фосфолипидов.
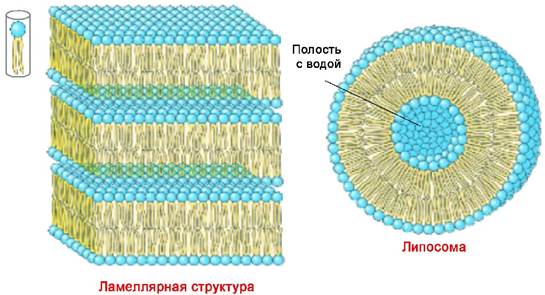
При низком содержании воды (до 40%) система гомогенна и имеет слоистое (ламеллярное) строение. При увеличении водной фазы образуются замкнутые моно или полиламеллярные структуры - липосомы. Липосомы аналогично мицеллам способны включать в себя различные биологически активные вещества и обеспечивать специальную доставку в клетки.
❖ Молекулярная организация биологических мембран. Еще в первой половине ХХ века было установлено, что биологические мембраны представляют собой комплекс белков и липидов. Было предложен ряд вариантов взаимного распределения этих компонентов в мембране, но они опровергались экспериментальными данными.
В 1972 г. американские исследователи С. Сингер и Г. Николсон предложили «жидкостно-мозаичную» модель биомембран, которая с определенными дополнениями считается в настоящее время общепринятой. По этой модели основу липидной мембраны составляют фосфолипиды и стерины, образующие биомолекулярный слой.

В состав фосфолипидов входят остатки предельных и непредельных карбоновых кислот. Ненасыщенные углеводородные цепи менее плотно прилегают друг к другу, тем самым уменьшается гидрофобное взаимодействие между отдельными фосфолипидными молекулами и, соответственно, увеличивается подвижность липидов.
В липидный бислой погружены белки, часть которых находятся на поверхности мембраны (периферические белки), а другие - интегральные белки, пронизывают липидный слой.
Интегральные белки имеют большие гидрофобные участки и поэтому сильно связаны с липидным окружением. Гидрофильные аминокислоты в основном формируют поверхность, контактирующую с водным окружением.
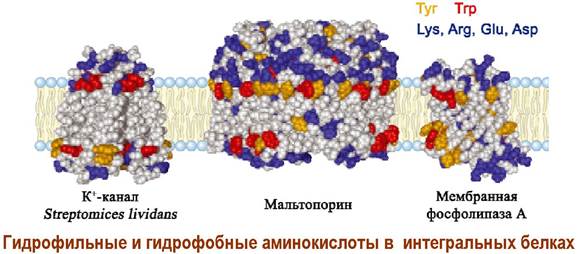
Взаимодействие белков с липидным окружением, включая стерины и гликолипиды, формирует участки липидной мембраны с меньшей подвижностью - микродомены, которые как льдины плавают по «липидному морю» биомембраны.

Таблица 12. Главные компоненты мембран различных организмов
Мембраны клеток |
Белки (%) |
Фосфолипиды (%) |
Стерины (%) |
Другие липиды |
Миелиновая оболочка человека |
30 |
30 |
19 |
Гликолипиды |
Печень мышей |
45 |
27 |
25 |
|
Лист кукурузы |
47 |
26 |
7 |
Гликолипиды |
Дрожжи |
52 |
7 |
4 |
Триглицериды, эфиры стеринов |
E. coli |
75 |
25 |
Многие из интегральных белков выполняют функцию рецепторов или ионных каналов. Ряд мембранных белков обладает свойствами ферментов. Интегральные белки обычно гликозилированы. Олигосахаридные цепи таких гликопротеинов в совокупности с гликолипидами образуют углеводный слой (гликокаликс) на поверхности клетки, например, олигосахаридные детерминанты на поверхности эритроцитов.
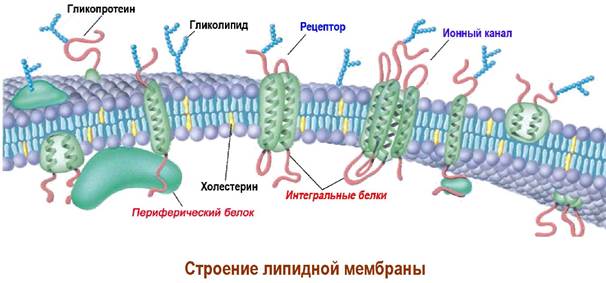
В одних участках молекулы липидов легко вращаются вокруг собственной оси и передвигаются по плоскости липидного слоя - латеральная диффузия, а в других липидные компоненты находятся в сильно упорядоченном состоянии.
Ряд белков способны перемещаться по поверхности мембраны, тогда как другие находятся в фиксированном положении за счет взаимодействий с цитоскелетом или внутренними органами клетки. Биологические свойства мембранных белков проявляются обычно именно в комплексе с биомембраной.
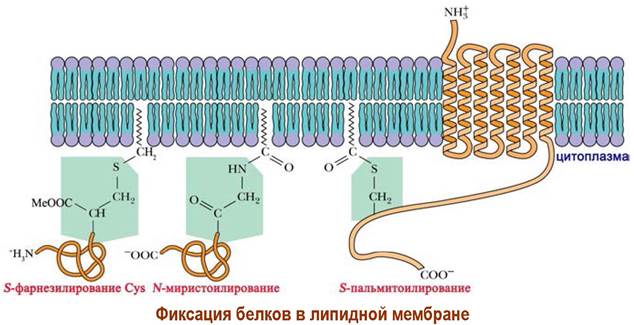
Для белков реализуется абсолютная асимметрия расположения на био-мембране. Они всегда ориентированы строго определенным образом. Этому способствует как, рассмотренное выше взаимодействие гидрофобных аминокислот с липидным слоем, так и дополнительная фиксация посредством введения в белок липофильных молекул. Углеводородные «хвосты» таких структур внедряются в липидный бислой и выступают в качестве «липидных якорей».
Для липидов также наблюдается асимметрия на внутреннем и внешнем слоях мембраны - т. е. одни и те же липиды находятся в различных концентрациях.
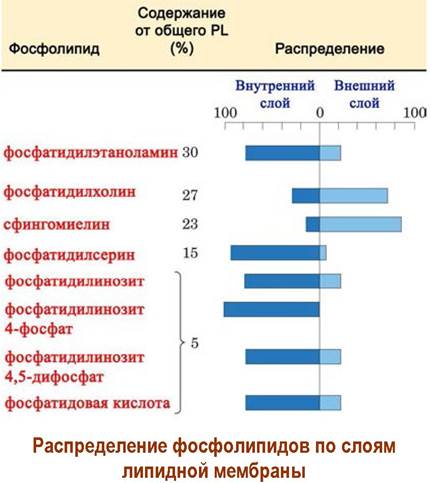
Такая асимметрия липидов существует, несмотря на то, что в реальных мембранах облегченно происходит «флип-флоп» - перескок липида с внешнего слоя во внутренний и наоборот.
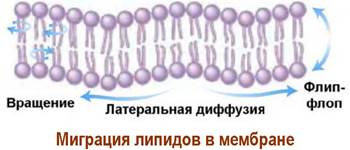
Процессу «флип-флопа» способствуют специальные мембранные белки - флипазы, облегчающие энергетически невыгодный перенос полярной головки липида через гидрофобный слой.
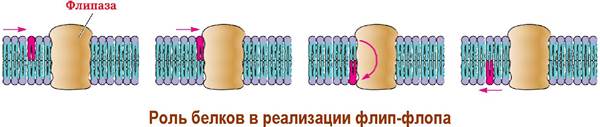
❖ Клеточная стенка микобактерий. У каждого вида клеток поверхность имеет свои особенности. Известно, что бактерии туберкулеза чрезвычайно устойчивы к действию антисептических препаратов, в т. ч. кислот, щелочей, окислителей. Во много это связано с организацией клеточной стенки микобактерий. Липид-белковая мембрана этого рода бактерий покрыта сеткой пептидогликана, к которому по остаткам мурамовой килоты (приблизительно по одному из десяти) присоединены фосфодиэфирной связью (линкер) цепи арабиногалактана. В этом полисахариде галактановый кор связан с арабинофуранозными цепями, содержащими блоки миколевых кислот.
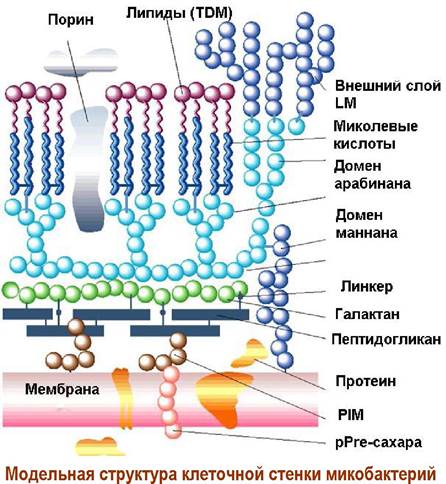
С другой стороны, за счет внедренных в биомембрану липидных «якорей» фосфатидилинозита, связанного с остатком маннозы (PIM), на ней удерживаются цепи липоарабиноманнана (LAM). В качестве липидных «якорей» также участвуют молекулы полипренильных (pPre) производных сахаров. Таким образом, на поверхности клетки формируется мощная углеводная оболочка, которая дополняется капсулярным слоем полисахаридов (глюканы, маннаны).
Высоколипофильные остатки миколевых кислот в свою очередь способны за счет гидрофобных взаимодействий удерживать поверхностные гликолипиды, в т. ч. TDM, а также гидрофобные белки. Так формируется второй липидный слой, отличающийся по строению от фосфолипидного бислоя.
❖ Транспорт через мембраны. Одна из главных функций биомембран - осуществлять избирательный транспорт различных веществ, в том числе ионов. Практически для всех соединений, кроме молекул воды и еще некоторых низкомолекулярных продуктов, свободный транспорт (простая диффузия) через мембрану невозможен. На поверхности клеток существуют специальные структуры - белки-каналы, по которым осуществляется специализированный транспорт веществ. Ранее были рассмотрены ионнотропные рецепторы - ионные-каналы.
Еще одним примером протеинов, участвующих в мембранном транспорте, являются аквапорины. Эти интегральные мембранные белки обеспечивают прохождение в клетку молекул воды, но не пропускают крупные молекулы, а также ионы. Ряд аквапоринов реализуют также транспорт молекул аммиака, углекислого газа, глицерина.
За открытие авапоринов американский профессор П. Агре в 2003 г. удостоен Нобелевской премии по химии.


На модельных мембранах хорошо изучен транспорт ионов с помощью специальных соединений: ионофоров и антибиотиков- каналообразователей.
✵ Ионофоры - специфические молекулы или их ансамбли, которые образуют комплекс с ионами на одной стороне мембраны, в виде такого комплекса переносят их через липидный слой и затем высвобождают ионы. Такие вещества иначе называют «переносчиками».
Наиболее известный «переносчик» - циклический пептид валиномицин. Его структура содержит три блока, состоящих из D- и L-валина и двух гидроксикислот - L-молочной (Lac) и D-2-гидрокси-3-метилбутановой (Hmb).
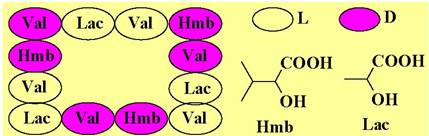
Размеры внутренней полости соответствуют радиусу ионов калия, который координируется атомами кислорода карбонильных групп сложноэфирных связей. При этом наблюдается высокая селективность по отношению к катиону. Прочность комплекса с ионом калия многократно выше, чем с ионом натрия.
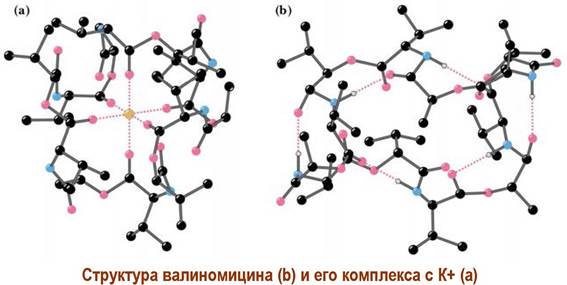
В неполярной среде за счет шести внутримолекулярных водородных связей (С=О…Н-К) молекула принимает конформацию объемной буквы S. При координировании с ионом калия конформация молекулы изменяется, экранируя внутренний ион. В таком виде молекула легко преодолевает липидный слой. В полярной водной фазе молекула принимает «открытую» форму, высвобождая ион К+.
✵ Антибиотики-каналообразователи. Ряд пептидных антибиотиков, например, грамицидин А, способны образовывать в бислойной мембране канал, через который могут проходить ионы. Структурно грамицидин А представляет собой линейный пентадекапептид с закрытыми N- и С-концами.
Возможно два типа построения канала: две молекулы образуют антипараллельную двойную спираль, что было показано на моделях в органических растворителях, или две молекулы грамицидина А образуют спираль, стыкуясь «голова к голове». Последний вариант реализуется в липидных мембранах.
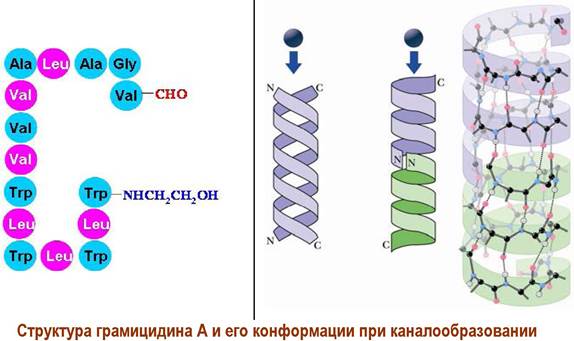
В клетках каналы образуются как сложные комплексы из молекул антибиотиков-каналообразователей и стеринов. Такие каналы проницаемы не только для воды, ионов, но даже для небольших нейтральных молекул типа глюкозы.
Контрольные задания
Тест 5 (вариант)
1. Напишите структурную формулу аденозин-5'-трифосфата.
2. Напишите структурную формулу олеиновой кислоты.
3. Определите название данного соединения и к какой группе липидов оно относится.
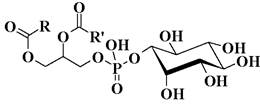
I. N-олеилсфингозин; II. N-линолеилсфингозин; III. нервон; IV. глобозид; V. холестерилпальмитат; VI. эргостерилпальмитат; VII. фосфатид илхолин; VIII. фосфатидилсерин; IX. фосфатидилинозит; Х. церамидфосфохолин; XI. 1-О-пальмитоил-sn-глицерин; XII. 3-О-пальмитоил-sn-глицерин
А. глицеролипиды; Б. воски; В. стерины; Г. фосфолипиды; Д. сульфолипиды; Е. гликолипиды; Ж. сфинголипиды.
4. Составьте смысловые пары:
А. кодон; Б. экзон; В. интрон; Г. промотор; Д. терминатор.
I. участок ДНК, с которого начинается транскрипция; II. участок ДНК, на котором останавливается транскрипция; III. участок ДНК из трех нуклеотидов; IV. участок гена, кодирующий синтез белка; V. некодирующие участки ДНК.
5. Расставьте буквенные индексы названий веществ и процессов в соответствии с позициями в схеме транскрипции:
А. терминатор; Б. промотор; В. фактор; Г. мРНК; Д. ДНК; Е. ATP, GTP, CTP, TTP; Ж. ATP, GTP, CTP, UTP; З. транскриптаза.
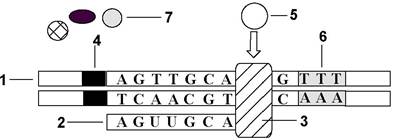
6. Найдите название представленных соединений
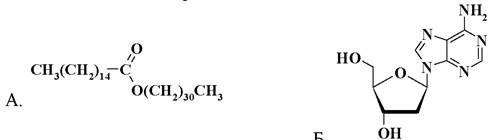
1. мирицилпальмитат; 2. холестерин; 3. стигмастерин; 4. эргостерин; 5. сфингозин; 6. тимидин; 7. риботимидин; 8. уридин; 9. псевдоуридин; 10. дезоксицитидин; 11. дезоксиаденозин; 12. дезоксигуанозин.