Биотехнология - Ю.О. Сазыкин 2006
Частная биотехнология
Лекарственные препараты, получаемые в фармацевтической промышленности биотехнологическими методами
Пробиотики
Пробиотики — живые организмы и/или вещества микробного или иного происхождения, оказывающие при естественном способе введения благоприятные эффекты на физиологические функции, а также на биохимические и поведенческие реакции организма хозяина, оптимизируя его микробиологический статус.
Симбионт — участник симбиоза — совместного проживания организмов разных видов в одной и той же экологической нише. Симбиоз многоклеточных организмов с одноклеточными — древнейшее явление в эволюции. Оно возникло в тот момент, когда появились многоклеточные организмы. Известно, что в соответствии с научными представлениями жизнь на Земле возникла около 3-4 млрд лет назад в силу естественных причин. При этом первыми живыми существами были микроорганизмы. По некоторым данным их эволюция продолжалась около миллиарда лет. Именно за это время сформировалось все многообразие биохимических реакций, которые лежат в основе центрального метаболизма всех живых существ.
Многоклеточные организмы возникли на основе одноклеточных в мировом океане (в одной и той же экологической нише) и симбиоз многоклеточных организмов с одноклеточными наблюдался с самого начала их возникновения. Известно, что в процессе эволюции у многоклеточных организмов сформировались механизмы, обеспечивающие переменчивость внутренней среды, и типы взаимодействия многоклеточных организмов с одноклеточными. На сегодня известны следующие формы симбиоза:
✵ мутуализм — взаимовыгодный симбиоз;
✵ паразитизм — один из партнеров получает одностороннюю выгоду за счет другого;
✵ комменсализм — один из партнеров получает одностороннюю выгоду, не нанося при этом никакого ущерба другому организму;
✵ нейтрализм — партнеры не оказывают заметного влияния один на другого.
Все эти формы наблюдаются при рассмотрении симбиоза одноклеточных микроорганизмов с многоклеточными. Когда говорят конкретно о симбиозе человека с микроорганизмами, имеют в виду, что кожные покровы, слизистые оболочки и полости человеческого тела, сообщающиеся с внешней средой, заселены огромным количеством микроорганизмов — симбионтов.
Примеры: желудочно-кишечный тракт (ЖКТ) — от полости рта до прямой кишки; органы дыхания — от носоглотки до альвеол; толстый кишечник.
Особенно много микроорганизмов в толстом кишечнике, где насчитывается до 20 родов и более 100 видов микроорганизмов, обладающих огромной метаболической активностью. По этой активности микроорганизмы толстого кишечника сравнивают иногда с печенью, где метаболическая активность считается наивысшей. Естественно, что микроорганизмы толстого кишечника существенно влияют на физиологию человека (рис. 18). Микрофлора толстого кишечника участвует в процессе переваривания пищи — попадающие туда белки, углеводы и другие компоненты пищи расщепляются ферментами, продуцируемыми микроорганизмами-симбионтами. Они также способны продуцировать так называемые целлюлазы — комплекс ферментов, который позволяет расщеплять клетчатку. Для человека эта функция симбионтной микрофлоры играет небольшую роль, у некоторых же организмов (травоядных и жвачных животных) усвоение клетчатки осуществляется только благодаря микроорганизмам-симбионтам. Микроорганизмы толстого кишечника могут осуществлять гидролиз (способствовать усвоению) других компонентов пищи. В частности, молочнокислые бактерии расщепляют лактозу до молочной кислоты. Микроорганизмы-симбионты способны также расщеплять некоторые другие попадающие с пищей соединения. Например, они могут восстанавливать нитраты до нитритов и затем катализировать их. Нитриты могут обладать мутагенными и аутогенными (онкогенными) свойствами, поэтому, нейтрализуя их, микроорганизмы предотвращают воздействие этих потенциально активных аутогенных (онкогенных) факторов на организм человека. Но следует отметить, что некоторые микроорганизмы-симбионты могут активировать некоторые проканцерогенные вещества.
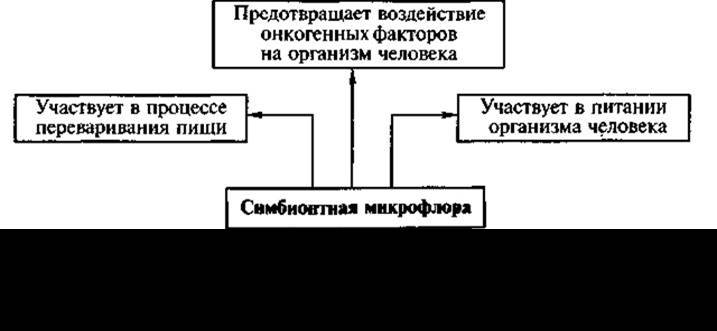
Рис. 18. Функции симбионтной микрофлоры
Микроорганизмы-симбионты обеспечивают организм человека некоторыми питательными веществами, например витаминами (К, группы В, в меньшей степени каротиноидами и другими жирорастворимыми витаминами). Кроме витаминов они способны продуцировать органические кислоты (молочную, уксусную, янтарную, муравьиную), которые всасываются и усваиваются макроорганизмом. Некоторые из этих микроорганизмов могут продуцировать незаменимые аминокислоты, в частности лизин, триптофан, треонин. Одновременно микроорганизмы симбионты обеспечивают утилизацию микроэлементов, образуя комплексы, которые более эффективно всасываются стенками кишечника, что особенно важно, когда этих микроэлементов в пище оказывается недостаточно.
Симбионтная микрофлора является также стимулятором неспецифического иммунитета (антигенным стимулятором) и обеспечивает неспецифическую резистентность макроорганизма.
И последнее: заселив ЖКТ (резидентная микрофлора), микроорганизмы-симбионты препятствуют поселению здесь посторонних микроорганизмов, в том числе и патогенных. В окружающей среде существует огромное количество микроорганизмов, которые нашли бы в кишечнике человека благоприятные условия для своего развития (это и обилие питательных веществ, и постоянная температура, и влажность). Однако патогенные микроорганизмы (гнилостные, а также продуцирующие разные токсины и токсические соединения, например, Clastridium butulinum) не размножаются в кишечнике человека. Почему же этого не происходит? Потому что экологическая ниша занята микроорганизмами-симбионтами, препятствующими поселению в ней посторонней микрофлоры.
Функции симбионтной микрофлоры в основном были установлены в течение прошлого века. Главную роль сыграли эксперименты на стерильных животных (гнотобионтах). Гнотобиология — область биологии, которая занимается изучением стерильных животных, в организм которых вводят тот или иной микроорганизм, а затем исследуют влияние микрофлоры на жизнедеятельность организма животных и птиц. Например, для получения стерильного цыпленка куриное яйцо тщательно обрабатывают антисептиками, убивая все микроорганизмы на поверхности и в порах скорлупы, и помещают его в термостат. Через 21 день вылупляется цыпленок, которого помещают в стерильную камеру, куда подается стерильный воздух; кормят стерильной пищей и поят стерильной водой.
Стерильных животных также можно получать кесаревым сечением, например, беременной свинье делают кесарево сечение; затем половину числа поросят помещают в стерильные условия, а остальных — в обычные и сравнивают. На основании подобных опытов было установлено:
✵ стерильные животные живут несколько дольше, чем нестерильные. В начале прошлого века И. И. Мечников выдвинул гипотезу, что одна из причин старения — отравление организма человека гнилостной микрофлорой, обитающей в толстом кишечнике. Идея И. И. Мечникова о том, что существуют гнилостные микроорганизмы, с которыми можно бороться с помощью других микроорганизмов, которые подавляют рост первых, получила свое дальнейшее развитие и на ее основе были созданы препараты пробиотиков;
✵ эти животные нуждаются в большом количестве питательных веществ, витаминов, органических кислот, хуже усваивают некоторые органические соединения;
✵ они чрезвычайно чувствительны к любой слабовирулентной и даже условно-патогенной инфекции. Попавшие в стерильную среду условно-патогенные бактерии сразу же заселяют ЖКТ и, не находя там никакой конкуренции, проникают в кровоток, вызывая инфекцию и быструю гибель животного. Это связано с отсутствием у таких животных реакций неспецифического иммунитета, которые индуцируются симбионтной микрофлорой.
Какие же микроорганизмы-симбионты обитают в ЖКТ? Классификация их постоянно меняется, поэтому рассмотрим основные группы микроорганизмов, присутствующих в ЖКТ.
Первая группа — бифидобактерии (Bifidobacterium bifidum, longum, infantis, breve) и молочнокислые бактерии (Lactobacillus acidophilus, plantarum) — грамположительные, анаэробные микроорганизмы (строгие анаэробы), обычно лишенные каталазы, неспорообразующие. Это самая многочисленная группа микроорганизмов-симбионтов. В процессе метаболизма они продуцируют молочную кислоту (иногда только ее) и другие органические кислоты (уксусную И Т.Д.).
В кишечном содержимом ребенка, находящимся на грудном вскармливании, бифидобактерии составляют до 99 % всех микробных популяций. Их титр доходит до 1011 — 1012 в 1 г кишечного содержимого. Это сметанообразная масса, из которой состоят экскременты ребенка, находящегося на грудном вскармливании. С началом прикорма к содержимому кишечника ребенка присоединяются другие микроорганизмы. Среди них важная роль принадлежит лактобактериям или молочнокислым бактериям. Количество лактобацилл у здоровых людей в 1 г кишечного содержимого колеблется, составляя (5 — 50) ∙ 109.
Большинство из вышеперечисленных бактерий относится к совершенно безвредным микроорганизмам. Они ни при каких условиях не вызывают патологические процессы. Существует вид Lactobacillus plantamm — растительная палочка (млечный сок на срезах растений), которая также присутствует в кишечнике человека. Этот микроорганизм не относится к совершенно безвредным лактобактериям. У людей с различными видами иммунодефицита (СПИД, аутоиммунные заболевания и т.д.) Lactobacillus plantarum находят даже на клапанах сердца при эндокардитах.
Следующий род молочнокислых бактерий кишечника — энтерококки, которые сравнительно недавно были выделены из рода Streptococcus. Существуют два важнейших вида энтерококков: Enterococcus faecium и Enterococcus faecalis. Среди последнею вида культур часто встречаются штаммы, которые могут вызывать патологические процессы.
Вторая группа бактерий — условно-патогенные и гнилостные бактерии (в принципе, это одни и те же микроорганизмы, и это деление носит условный характер). Условно-патогенные (следует из названия) бактерии при определенных условиях могут вызывать патологические процессы. Эти бактерии постоянно присутствуют в организме человека и поражают его, когда он либо ослаблен, либо в том случае, когда численность условно-патогенных бактерий возрастает до очень высоких значений. В последнем случае они вызывают вялотекущие воспалительные процессы в ЖКТ (энтероколиты и дизентероподобные заболевания). Также они могут заселять и нетипичные для них области, например протоки поджелудочной железы и желчного пузыря, а также сам желчный пузырь, вызывая там патологические процессы (в нормальном состоянии в этих областях микроорганизмов-симбионтов нет — они стерильны).
Наконец, у ослабленных людей условно-патогенные микроорганизмы могут поступать в кровь и вызывать очаговые воспалительные процессы (эндокардиты, артриты, гнойничковые заболевания — вплоть до сепсиса). Важнейшая по значению группа (не по численности) — семейство энтеробактерий — кишечная группа микроорганизмов. К ней относятся как явные патогены, например некоторые виды сальмонелл — возбудители таких инфекционных заболеваний, как тиф, паратиф (Sallmonella typhi и Sallnionelia paratyphi) и дизентерия (Shigellae), так и большое количество условно-патогенных бактерий. К числу последних относятся: кишечная палочка, протеи, сальмонеллы, стафилококки и др.
Второй по численности род микроорганизмов обитателей кишечника (после бифидобактерий) — бактероиды. Это неотрицательные микроорганизмы, строгие анаэробы. Их титр в одном грамме кишечного содержимого составляет 1010—1011. Среди этих микроорганизмов есть и муколитические штаммы, выполняющие полезные функции, однако у ослабленных людей эти штаммы могут вызывать патологические процессы.
Следующая группа — кластридии (Clastridium). Эти микроорганизмы выполняют важную экстралитическую функцию (именно кластридии продуцируют экстралитические ферменты); одновременно при определенных условиях они могут вызывать и патологические процессы, например при попадании в брюшную полость. К кластридиям также относятся и некоторые патогены (возбудители газовой гангрены, столбняка, ботулизма).
В кишечнике (так же как и в других полостях организма) встречаются дрожжи рода Candida (условно-патогенные микроорганизмы, которые при избыточном размножении вызывают молочницу). При применении антибиотиков широкого спектра действия резидентная микрофлора кишечника уничтожается, а так как эти антибиотики не действуют на дрожжи рода Candida, то естественно, что в отсутствие конкуренции эти микроорганизмы избыточно размножаются.
Итак, важнейшая роль среди этих двух основных групп микроорганизмов принадлежит бифидо- и молочнокислым бактериям, которые благодаря своей антагонистической активности по отношению к условно-патогенным бактериям подавляют жизнедеятельность последних. При этом они полностью контролируют численность условно-патогенных и гнилостных бактерий и поддерживают ее на уровне, безопасном для физиологии человека.
Симбионтная микрофлора делится на пристеночную и внутриполостную. Пристеночные бактерии размножаются на поверхности эпителия, а внутриполостные прикрепляются к твердым остаткам пищи, так как многим видам бактерий для того, чтобы они размножались (делились), нужно прикрепиться к какому-нибудь твердому субстрату.
К внутриполостным относятся энтеробактерии и некоторые штаммы бифидо- и лактобактерий.
Антагонистическая активность бифидо- и молочнокислых бактерий по отношению к условно-патогенной микрофлоре (бактериостатическое и бактерицидное действия) проявляется в виде факторов ее подавления:
✵ образования молочной и других органических кислот (муравьиная кислота), токсичных для условно-патогенных и гнилостных микроорганизмов. Одновременно эти кислоты снижают pH кишечного содержимого (закисляя его), что также неблагоприятно сказывается на жизнедеятельности последних;
✵ образования пероксидных соединений, при расщеплении которых выделяется атомарный кислород, подавляющий клетки условно-патогенной микрофлоры;
✵ образования антибиотикоподобных веществ (бактериоцинов: ацидофилина, колицинов и др.), подавляющих метаболизм условно-патогенных и гнилостных бактерий, взаимодействуя с клеточной мембраной и вызывая лизис клеток;
✵ способности прикрепляться к эпителию кишечника, образуя на его поверхности плотную биопленку (за счет интенсивного размножения), что является препятствием для фиксации патогенных микроорганизмов;
✵ изменения окислительно-восстановительного потенциала среды, что создает неблагоприятные условия для размножения условно-патогенных и гнилостных микроорганизмов.
Совокупность этих факторов в целом подавляет избыточное развитие условно-патогенной и гнилостной микрофлоры. Состояние микроэкологической системы толстого кишечника, когда молочнокислые бактерии превалируют в численности над условно-патогенными и гнилостными бактериями, называется эубиозом или эубактериозом. И наоборот, состояние, при котором численность бифидо- и молочнокислых бактерий снижается, а гнилостных и условно-патогенных соответственно возрастает, называется дисбактериозом. Избыточное размножение гнилостных микроорганизмов будет вызывать интоксикацию макроорганизма, включая порочный круг явлений, когда у ослабленного человека возникают и развиваются дополнительные инфекции. Более того, при этом условно-патогенные микроорганизмы способны сами вызывать развитие дисбактериоза.
Какие причины ведут к развитию дисбактериоза? Одна из них — попадание в организм человека группы веществ с антибактериальной активностью. Среди таких веществ первое место принадлежит антибиотикам. Конечно, антибиотики, как раньше, так и сейчас, играют колоссальную роль в терапии больных с инфекциями разного рода, спасении сотен миллионов жизней, но у них имеется негативный эффект: они не выбирают между мутуалистическими штаммами (молочнокислые бактерии), патогенными и условно-патогенными микроорганизмами. Антибиотики широкого спектра действия подавляют всю микрофлору ЖКТ, в том числе и молочнокислые бактерии. Их подавление ведет к тому, что по завершении лечения условно-патогенные бактерии и гнилостные микроорганизмы начинают доминировать над молочнокислыми бактериями. Дело в том, что в клетках гнилостных и условно-патогенных бактерий чаще встречаются плазмиды, определяющие устойчивость к тем или иным антибиотикам, которые передаются от клетки к клетке. В результате популяция условно-патогенных и гнилостных микроорганизмов становится устойчивой к действию тех или иных антибиотиков.
Кроме антибиотиков в организм человека с пищей попадают вещества, которые вводят в пищу специально для предотвращения ее порчи гнилостными микроорганизмами. Это так называемые консерванты, которые сами по себе обладают антибактериальной активностью. В пище могут содержаться и антибиотики, которые применяют в животноводстве и птицеводстве для лечения заболевших животных и птиц, а также для стимулирования их роста и развития. Пища (особенно растительная) может содержать гербициды и пестициды, обладающие антибактериальной активностью.
Развитию дисбактериоза способствует изменение гормонального статуса макроорганизма (во время полового созревания, беременности, при половом угасании). Физиологическое состояние макроорганизма влияет на жизнедеятельность, размножение и поддержание симбионтной (в частности, пристеночной) микрофлоры. С возрастом количество пристеночной микрофлоры (молочнокислых бактерий) уменьшается, происходит изменение гормонального статуса. При этом возможно очень быстрое слущивание пристеночной микрофлоры — слизистая обнажается и становится доступной для условно-патогенных и гнилостных микроорганизмов.
Оказывается, что если человек испытал сильный стресс, то у него на следующий день может появиться диарея и связано это с изменением гормонального статуса под влиянием стресса. А если этот стресс хронический, то тем самым создаются условия для развития дисбактериоза.
Препараты пробиотиков предназначены для профилактики и лечения дисбактериоза. В России производят в основном моновалентные препараты: бифидумбактерин (на основе Bifidobacterium bifidum), апилак (на основе Lactobacillus acidophillus), колибактерин (на основе кишечной палочки Е. coli М-17), лактобактерин (на основе Lactobacillus plantarum, fermentum). Комплексные препараты, например бификол (Bifidobacterium и Е. coli М-17). За рубежом — поливалентные (комплексные) препараты: симбиофтор (Enterococcus faecium + Е. coli), бификор (Bifidobacterium longum + Enterococcus faeclium), примадофилюс (содержит комплекс микроорганизмов симбионтов) и другие — энтерод (на основе дрожжей), гастрофарм (Lactobacillus bulgarius не является симбионтом и поэтому действует какое-то короткое время). Существуют препараты, которые содержат живые клетки микроорганизмов симбионтов, но при этом не являются пробиотиками, например бактисуптил (на основе культуры Bacillus cereus, мутантного штамма 1Р 5832).
Особенно широко применяют пробиотики в клинике детских болезней (при острой дизентерии, сальмонеллезе, эшерихиозе, вирусных диареях, диатезе и др.). Известно, что в детском организме еще не сформировалась м икроэкологическая система ЖКТ, поэтому у детей часто наблюдаются диспепсия и диарея. В этом случае применение препаратов пробиотиков оказывается очень эффективным. Изучение длительного применения препаратов пробиотиков в детских коллективах показало, что дети, систематически получавшие данные препараты и кисломолочные продукты, содержащие пробиотические штаммы, реже болеют не только кишечными инфекциями, но и ОРЗ, лучше растут и развиваются, легче переносят любые детские инфекции. Препараты пробиотиков также применяют в комплексном лечении кишечных инфекций (при колитах; бактериальных кольпитах, вызванных стафилококком и кишечной палочкой; энтероколитах на фоне нарушения микрофлоры с дефицитом или полным отсутствием бифидофлоры и др.).
По завершении лечения антибиотиками необходимо обязательно провести лечение пробиотиками для восстановления нормальной микрофлоры. Пробиотики назначают также ослабленным людям при соматических заболеваниях. Нередко возникает порочный круг, когда сама ослабленность является причиной дисбактериоза, а он в свою очередь усугубляет течение соматического заболевания. Препараты пробиотиков назначают и лицам преклонного возраста, так как у них в связи с изменением гормонального статуса уменьшается количество бифидо- и лактобактерий. Поэтому для нормализации микрофлоры нужно периодически (а в преклонном возрасте — постоянно) потреблять диетические пищевые продукты наряду с препаратами пробиотиков. Например, ацидофилин, который получают на основе ацидофильной закваски, бифидумбактерин.
Какова технология процесса получения таких препаратов? Во-первых, необходимо иметь штаммы микроорганизма симбионта. Их выделяют из кишечного содержимого здоровых детей и взрослых, например штамм Enterococcus faecium был выделен из кишечника ребенка. Во-вторых, выделенные штаммы обязательно надо идентифицировать. Дело в том, что для получения пробиотиков разрешены штаммы только определенных видов микроорганизмов. Эти штаммы должны обладать следующими свойствами:
✵ эффективной антагонистической активностью, обеспечиваемой в свою очередь синтезом органических кислот, которые штамм должен активно продуцировать. При выделении штаммов бифидобактерий важным антагонистическим началом продуктов метаболизма являются муравьиная и молочная кислоты. Желательно также, чтобы эти штаммы продуцировали пероксиды и антибиотикоподобные вещества;
✵ эффективной способностью прикрепляться к эпителию кишечника, если речь идет о пристеночных микроорганизмах;
✵ не гидролизовать кишечную слизь, которая обладает протективным действием. Некоторые микроорганизмы продуцируют мукополисахариды, которые разрушают (гидролизуют) эту слизь;
✵ не повреждать клетки кишечного эпителия (холециты).
Отобранные штаммы обязательно проверяют на патогенность
и токсичность in vitro на культуре клеток холецитов, на чувствительных животных. Побочные эффекты у пробиотиков не должны проявляться даже при их избыточных дозах. Для проверки препарат вводят в организм чувствительных животных в больших количествах, иногда до нескольких граммов на килограмм веса.
Штаммы должны быть технологичны, т.е. хорошо расти и размножаться на искусственных питательных средах. Их обрабатывают методом лиофилизации: замораживают до низких температур и затем высушивают при низком давлении. Соответственно, отобранные штаммы должны быть криорезистентны и выдерживать процедуру высушивания.
Удовлетворяющие всем этим требованиям штаммы поступают в контрольный институт, откуда их передают в фармацевтическое производство с соответствующими документами, в которых отражены их характеристики. В заводских лабораториях штаммы высеивают на искусственные питательные среды, проверяют их соответствие паспортным данным (род, вид, биологические свойства). И только после этого используют для получения препаратов пробиотиков. В условиях промышленного производства эти штаммы рассеивают и получают отдельные колонии, которые затем пересевают на агаризованные или жидкие питательные среды (например, молочнокислые бактерии хорошо растут в обезжиренном молоке).
И бифидобактерии, и лактобациллы, и энтерококки — это ауксотрофы, т. е. для своего роста они нуждаются в ряде питательных веществ и микроэлементов, не могут сами синтезировать аминокислоты, пуриновые и пиримидиновые основания, витамины: их должна содержать питательная среда. Для культивирования этих бактерий используют такое сырье, которое разрешено к применению в пищевой промышленности, так как препарат, выращенный на этих средах, впоследствии используется для внутреннего применения.
Источником аминокислот обычно служит белок молока (казеин), который гидролизуют с помощью ферментов (трипсина и пепсина) и получают, соответственно, триптол или пептол. Как источник витаминов, а также пиримидиновых и пуриновых оснований используют дрожжевой экстракт, который получают из дрожжей рода Saccharomyces (пивных либо пекарских). В качестве микроэлементов используют соли магния, марганца, цинка, которые добавляют в питательную среду для культивирования молочнокислых бактерий. Источником энергии, как правило, служит лактоза или глюкоза.
Обычно молочнокислые бактерии культивируют от 8 до 16 ч (довольно короткая ферментация). Собирают штаммы в той фазе роста, при которой выживание клеток культуры будет наиболее длительным, что в свою очередь, при дальнейшем получении препарата, обеспечивает его длительное хранение. Все это определяется экспериментальным путем и часто является ноу-хау фирмы-производителя. Как правило, выбирают конец логарифмической фазы или начало стационарной, в зависимости от культуры (штамма). По завершении процесса культивирования получают бактериальную суспензию, содержащую в 1 мл 109 и более клеток. Эти клетки собирают, используя поточные центрифуги или сепараторы, в которых образуется похожая на сметану с кремовым оттенком масса со специфическим запахом кислого молока (напоминает прессованные дрожжи). Раствор криопротекторов (вещества белковой природы — обезжиренное молоко или желатин; углеводы — лактоза, сахароза) добавляют в проточную массу и получают густую суспензию клеток, которую разливают в ампулы. Затем их замораживают в жидком азоте и подвергают лиофильной сушке. Сухая масса приобретает пузырчатый вид. Ее измельчают и определяют титр, в соответствии с которым вносят во флаконы (стеклянные, пластмассовые) или смешивают с культурой другого штамма. В последнем случае получают несколько видов микроорганизмов симбионтов.
Форма выпуска — флаконы (бифидумбактерин) или ампулы (бификол, содержащий бифидобактерии и кишечную палочку), или капсулы (индийский препарат «Нутролин В», содержащий штаммы лактобацилл), или пакетики (бифидумбактерин фирмы «Партнер», Россия).